Частота, причины и диагностика аномальных маточных кровотечений
Аномальные маточные кровотечения (АМК) являются распространенным заболеванием, оказывающим влияние на 20–30% женщин репродуктивного возраста.
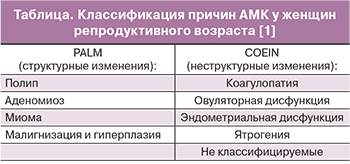 Классификация причин АМК (PALM–COEIN) [1] представлена в таблице.
Классификация причин АМК (PALM–COEIN) [1] представлена в таблице.
В России в настоящее время принята традиционная тактика при маточном кровотечении любой степени тяжести: госпитализация в стационар и выскабливание матки. В прошлом столетии при отсутствии методов ультразвукового сканирования тактика была оправдана, так как при выскабливании матки было возможно обнаружить миоматозные узлы, деформирующие полость матки, гиперплазию эндометрия и другие патологические процессы. В настоящее время в соответствии с рекомендациями по лечению АМК диагностика основывается на данных ультразвукового сканирования. Также необходим контроль общего анализа крови (гемоглобин, количество эритроцитов, при необходимости ферритина и железа в сыворотке крови).
Ряд авторов отмечают, что можно использовать выскабливание матки как хирургический гемостаз, но при последующих менструациях объем кровопотери сохраняется или увеличивается [2]. Выскабливание матки у женщин репродуктивного возраста может привести к повреждению базального слоя эндометрия и, как следствие, к неблагоприятным исходам беременности: выкидышам, невынашиванию, плацентарной недостаточности и задержке роста плода, преждевременным родам [3].
Из структурных или органических причин наиболее распространенным заболеванием, проявляющимся кровотечением, является миома матки (30%) и полипы (10%). Эти больным показано оперативное лечение и удаление новообразований.
Проспективное исследование 292 женщин в возрасте 31,2±1,5 года (M±m), жительниц Краснодарского края с миомой матки показало, что основными жалобами, побуждающими пациентку обратиться за медицинской помощью были кровотечение – у 201 (68,8%) и астенический синдром у 192 (45,5%). У всех женщин отмечались обильные менструальные и межменструальные кровотечения. Количество узлов на одну женщину варьировало от 2 до 12, в среднем – 5,4±0,3. Анемия легкой степени тяжести была выявлена у 79 (27,1%) женщин, анемия средней степени тяжести – у 79 (27,1%) женщин [4].
Значительно реже имеет место злокачественное новообразование эндометрия. У всех женщин с АМК после 45 лет целесообразна гистероскопия, прицельная биопсия эндометрия с последующим патоморфологическим его исследованием [5].
Лечение аномальных маточных кровотечений
С целью как остановки АМК, так и регуляции менструального цикла применяют различные лекарственные средства.
Нестероидные противовоспалительные средства (НПВС) имеют высокую эффективность (кровопотеря на фоне приема НПВС снижается в среднем на 58%). Но препараты имеют неоптимальный профиль безопасности, особенно при длительном использовании [6, 7]. Способность НПВС купировать маточные кровотечения обусловлена подавлением активности фермента циклооксигеназы и, как следствие, снижением синтеза простациклина, препятствующего агрегации тромбоцитов.
Транексамовая кислота (синтетическое производное лизина) – действенное и достаточно безопасное средство, снижающее кровопотерю в среднем на 58%. В соответствии с инструкцией по применению препарата: при профузном маточном кровотечении препарат назначают по 1–1,5 г 3–4 раза в сутки в течение 3 дней. При кровотечении на фоне болезни Виллебранда или других коагулопатиях курс применения может быть увеличен до 10 дней. Показано положительное влияние транексамовой кислоты на качество жизни и сексуальных отношений [8, 9].
Левоноргестрел-высвобождающая внутриматочная система (ВМС-ЛНГ), уменьшает менструальную кровопотерю на 74–97% [10]. В течение первого месяца при использовании ВМС-ЛНГ длительность кровотечений может увеличиваться, о чем необходимо предупреждать пациенток. Нередко после введения ВМС-ЛНГ мажущие кровянистые выделения осложняют жизнь женщины в течение 1–1,5 лет, психологически это ограничивает врачей в применении данного метода. В подростковом и раннем репродуктивном возрасте ВМС-ЛНГ не используют, поскольку механизм действия метода связан с атрофией эндометрия.
Широкое распространение с целью уменьшения кровопотери из матки имеют комбинированные оральные контрацептивы (КОК). Эффективность КОК составляет 43%. Кровотечение при использовании КОК обычно прекращается уже в течение 24 ч (так называемый гормональный гемостаз). Действие КОК связано с подавлением пролиферации эндометрия и опосредованным сокращением количества теряемой крови [6]. При дальнейшем применении для профилактики повторных кровотечений необходимо учитывать приверженность к лечению конкретной пациентки. Согласно результатам последних исследований при назначении КОК женщины часто были не полностью удовлетворены их применением: 69% сообщили хотя бы об одном нежелательном эффекте препарата. Среди женщин, у которых возникали побочные эффекты, 65% сообщили, что были вынуждены отказаться от дальнейшего использования КОК из-за побочных эффектов [7].
Гестагены в циклическом режиме в лютеиновую фазу для лечения обильных менструаций малоэффективны, однако они хорошо регулируют менструальный цикл [7]. Прием медроксипрогестерона ацетата (10 мг/сут) или норэтистерона ацетата (2,5–5 мг/сут) в циклическом режиме с 16-го по 25-й день обеспечивает предсказуемый профиль кровотечений. Применение дидрогестерона в дозе 20 мг/сут с 11-го по 25-й день менструального цикла способствует нормализации цикла у большинства больных и снижению длительности и интенсивности кровотечений [8].
Агонисты гонадотропин-рилизинг-гормона (аГнРГ) неэффективны в терапии обильных менструаций. Их применяют только по определенным показаниям в качестве терапии второй линии [7]. Эти средства полностью блокируют работу гипоталамо-гипофизарно-яичниковой оси, вызывают аменорею у 89% пациенток, что сопровождается выраженными побочными явлениями: сухостью влагалища, приливами, потливостью, а при длительном использовании (6 мес и более) – остеопенией. Механизм действия аГнРГ связан с уменьшением количества гонадотропиновых рецепторов в гипофизе с супрессией выброса гонадотропинов и последующим снижением уровня эстрадиола до состояния гипогонадизма.
Несмотря на распространенность применения КОК, у курящих женщин и женщин с ожирением имеются ограничения по их назначению в связи с риском венозных тромбозов. Распространенность ожирения и ассоциированных с ним заболеваний сопоставима с масштабами эпидемии. В России четверть (25,6%) детей и подростков имеет излишнюю массу тела и ожирение [9]. Ожирение у женщин, проживающих в РФ, также встречается с частотой 24–25% (ВОЗ, 2015). Большинство исследователей указывают на олигоменорею как на наиболее распространенную форму нарушений менструального цикла у женщин с ожирением [10], на фоне чего при длительно существующей ановуляции развиваются пролиферативные процессы эндометрия [11]. Данные исследовательской группы (Д.О. Санта-Мария Фернандес и соавт., 2015) показали, что при гистологическом исследовании эндометрия у женщин с ожирением и олиго/аменореей в возрасте 20–29 лет выявлена простая железистая гиперплазия, и у 25% пациенток она имеет рецидивирующий характер [12]. E.R. Pomp и соавт. (2007) показали, что у женщин с ожирением, использовавших КОК, риск тромбозов увеличивался значительно (OR 23,78, 95% ДИ 13,35–42,34), по сравнению с женщинами с нормальным индексом массы тела. Совместный эффект носительства мутаций фактора V (Leiden) и ожирения привел к увеличению риска тромбозов (OR 7,86, 95% ДИ 4,70–13,15). У женщин с носительством полиморфизма гена протромбина 20210A это было связано с кратным повышенным риском (OR 6,58, 95% ДИ 2,31–18,69). Ожирение повышает риск венозных тромбозов, особенно у женщин, использующих оральные контрацептивы [13]. Риск венозных тромбозов у курящих женщин, применяющих КОК в возрасте 35–44 года, значительно высокий и составляет 1 на 5,2 тыс. женщин в год [14]. Это в 6,4 раза чаще, чем у некурящих женщин в этом же возрасте, использующих КОК. Поэтому применение КОК с целью остановки кровотечения и нормализации менструального цикла ограничено. Это свидетельствует о том, что необходимы другие методы регуляции менструального цикла. Альтернативой может быть применение препаратов прогестерона, не действующих на систему гемостаза, в частности дидрогестерона [15].
Дидрогестерон – метаболически нейтральный препарат и, будучи производным прогестерона, обладает благоприятным метаболическим профилем в связи с отсутствием у него андрогенной, глюкокортикоидной и минералокортикоидной активностей, ответственных за усугубление инсулинорезистентности и дислипидемических расстройств на фоне приема прогестагенов, производных 19-норстероидов. Кроме того, еще одно преимущество дидрогестерона – отсутствие антигонадотропного влияния и подавления овуляции при приеме в дозе, обеспечивающей адекватную секреторную трансформацию эндометрия. Возможно, стабилизация массы тела при назначении прогестагенов в циклическом режиме у пациенток с ожирением происходит за счет разрыва порочного круга негативных метаболических эффектов, развивающихся в отсутствие прогестерона при ановуляции.
Риск развития рака эндометрия в течение жизни составляет примерно 3%. Рак эндометрия – это гормонозависимое заболевание, тесно связанное с гиперэстрогенемией. Одной из основных причин возникновения дисбаланса эстрогена/прогестерона является ожирение. Ожирение связано с гормональными расстройствами, а также с дисрегуляцией активности инсулиноподобного фактора роста, которые в совокупности приводят к гиперплазии эндометрия и, возможно, аденокарциноме эндометрия. С целью коррекции гормональных нарушений у женщин с ожирением целесообразно назначение прогестерона [16]. Принимая во внимание данные о том, что препараты прогестерона в большей степени нормализуют регуляцию менструального цикла, а не влияют на степень кровопотери, рекомендации по совместному применению дидрогестерона и транексамовой кислоты во II фазе менструального цикла в течение 3–4 менструальных циклов выглядят убедительно. Транексамовая кислота по 2–4,5 г в сутки в течение 4–7 дней (II фаза менструального цикла) уменьшает кровопотерю на 34–59% [17] и дидрогестрон по 20 мг с 11-го по 25-й или с 14-го по 28-й день менструального цикла позволяет его нормализовать и уменьшить кровопотерю [8].
Заключение
АМК – актуальная проблема в современной гинекологии, требующая дифференцированного подхода к выбору терапии. В связи с ограничением применения КОК (риск венозных тромбозов) у курящих женщин и/или женщин с ожирением показаны альтернативные методы терапии. У данного контингента женщин целесообразно сочетанное применение дидрогестерона и транексамовой кислоты во II фазу менструального цикла в течение 3–4 менструальных циклов. Дальнейшее использование дидрогестерона рекомендовано в период снижения массы тела. Это является профилактикой гиперпластических процессов в эндометрии, в том числе рака эндометрия. Отсутствие влияния дидрогестерона на липидный профиль, регуляция менструального цикла позволяет рекомендовать этот препарат для курящих женщин, женщин с ожирением и АМК.



