Введение
На настоящем этапе развития медицины инструментальные исследования кишечника являются ведущими в диагностике заболеваний дистальных отделов желудочно-кишечного тракта (ЖКТ). Одним из обязательных предварительных этапов исследования является подготовка кишечника, или кишечный лаваж (КЛ). Термин «лаваж» (от французского «le lavage» – промывание, орошение) широко применяется в медицине (желудочный, кишечный, бронхиальный и др.), означая промывание какого-либо полого органа с диагностической и лечебной целью. Адекватной подготовке кишечника к инструментальному исследованию в настоящее время уделяется особое внимание, поскольку недостаточное интестинальное очищение существенно затрудняет визуализацию и может приводить к пропуску патологических признаков, удлинению инструментальной процедуры и развитию осложнений [1].
Научные предпосылки и эволюция методов очищения кишечника
Обоснование данного метода восходит к трудам врачевателей древности. Так, известный средневековый персидский ученый и врач Абу Али Хусейн ибн Абдаллах ибн Сина (Авиценна) в фундаментальном труде «Канон врачебной науки» утверждал: «Скопление излишков есть материальная причина всех болезней, старения и преждевременной смерти. Очищение от излишков – есть путь здоровья и долголетия» [2], – и предлагал использовать очищение ЖКТ путем применения слабительных средств при широком спектре заболеваний внутренних органов, в т.ч. сопровождающихся интоксикацией и копростазом, как с профилактической, так и с лечебной целью.
Исторические более ранние работы, посвященные КЛ, касаются подготовки кишечника к радиологическим исследованиям, в т.ч. ирригоскопии, и хирургическим манипуляциям [3, 4]. В трудах отечественных ученых конца XX – начала XXI вв. метод КЛ получил научное обоснование и нашел широкое применение в терапии токсикозов различного генеза [5, 6]. Однако триумф метода КЛ определило развитие эндоскопической техники и, соответственно, инструментального исследования толстой кишки.
Способы подготовки кишечника к инструментальным исследованиям прошли достаточно длительный эволюционный путь. Первоначальные методы, заключавшиеся, по общему правилу, в назначении за сутки до исследования внутрь 30 г касторового масла с последующей постановкой вечером того же и утром следующего дня 1–2 очистительных клизм, не обеспечивали должной визуализации слизистой оболочки. Гидромеханических способы, включавшие помимо диетических ограничений и дачи слабительных в значительных дозах постановку сифонных клизм, характеризовались высокой трудоемкостью и требовали специальных условий, оборудования и обученного медицинского персонала. Мероприятия переходного периода подразумевали пероральный лаваж кишечника значительным объемом (7–12 л) 0,9%-ного раствора натрия хлорида или иного сбалансированного электролитного раствора либо прерывистое орошение прямой кишки большим (20–22 л) количеством жидкости в сочетании с солевыми слабительными. Данные способы характеризовались значительной длительностью (до 48–72 часов), плохой субъективной переносимостью пациентами и могли вызывать клинически значимые нарушения водно-электролитного обмена и декомпенсацию недостаточности кровообращения, что ограничивало их применение при широком круге заболеваний сердечно-сосудистой, дыхательной, пищеварительной и мочевыделительной систем.
Оставляла желать лучшего и эффективность подготовки кишечника к исследованиям. В работе Belsey J. et al. [7] было показано, что более 20% колоноскопий завершались преждевременно, не достигyed этапа интубации слепой кишки. D.K. Rex показал, что 20–40% пациентов, подвергнутых инструментальным исследованиям, имели некачественную подготовку кишечника [8]. В значительном числе случаев это было обусловлено большим объемом предписанного к приему внутрь раствора (4 л) и плохими вкусовыми качествами препарата, снижавшими приверженность выполнению рекомендаций пациентами [9, 10]. Deepak P. et.al. [11], проанализировав опыт колоноскопий с недостаточным уровнем подготовки, отметили снижение частоты выявления аденом и полипов до 50%. Последствиями вынужденного повторного назначения колоноскопии являются усугубление физических и психологических страданий пациента, ассоциированных с данной процедурой, увеличение сроков установления диагноза, повышение стоимости диагностики и риска осложнений эндоскопической процедуры.
Микробиологические последствия очищения кишечника также представляются весьма значимыми. КЛ оказывает быстрое и существенное влияние на микробиоту толстой кишки. Так, в работе J. Jalanka et al. [12] показано, что в результате очищения кишечника общая микробная нагрузка толстой кишки уменьшается более чем в 30 раз, при этом преимущества в пролиферации получают Proteobacteria, Fusobacteria и Dorea formicigenerans. При этом отмечено, что двухэтапная подготовка кишечника («сплит-режим») оказывает менее выраженное влияние на микробный пейзаж кишки, чем одномоментный прием всего объема слабительного. Относительно сроков восстановления микрофлоры после КЛ литературные данные противоречивы. Так, некоторые авторы [12] утверждают, что оно происходит в течение 2 недель, тогда как другие [13] сообщают, что и через месяц после процедуры у пациентов наблюдается значимое уменьшение уровня лактобактерий с пролиферацией представителей семейств Enterobacteriaceae, Rikenellaceae, Eubacteriaceae и Streptococcaceae.
В результате длительного эмпирического накопления знаний и научного осмысления проблемы сформулированы требования к идеальному методу интестинальной подготовки к инструментальным исследованиям. Он должен обеспечивать быстрое, прогнозируемое, надежное и полное опорожнение кишечника от каловых масс и компонентов лаважного промывного раствора, не усугублять тяжесть заболевания кишечника, не оказывать неблагоприятного местного (на слизистую оболочку кишечника и микробиоту ЖКТ) и системного действия, в т.ч. в отношении сердечно-сосудистой, мочевыделительной систем и водно-электролитного обмена, хорошо переноситься пациентами, выполняться ими самостоятельно либо с минимальным привлечением медицинского персонала, не требовать специальных условий и оборудования, обеспечивать индивидуальный выбор схемы подготовки с учетом коморбидности пациента и планируемого времени манипуляции на кишечнике, обеспечивать информативность процедуры (не искажать параметры эндоскопического изображения [цвет, очертания, отражение], в т. ч. при применении витальных красителей и использовании современных режимов работы эндоскопического оборудования), не оказывать повреждающего действия на эндоскоп, быть фармакоэкономически приемлемым [14]. Схемы подготовки кишечника к инструментальным исследованиям по мере исторического развития постепенно приближаются к выполнению данных требований.
Современные зарубежные рекомендации [15] полагают адекватной такую подготовку, при которой остаточное содержимое кишечника не препятствует выявлению образований размером >5 мм. Для оценки результатов подготовки кишечника к инструментальным исследованиям используются различные шкалы. Исторически одной из первых попыток объективно оценить состояние подготовки кишечника стала предложенная в 1994 г. шкала Aronchick [16], основанная на рекомендациях Американского общества гастроинтестинальной эндоскопии и Американской гастроэнтерологической ассоциации. Она позволяла стратифицировать подготовку кишечника от отличной до неадекватной на основании учета количества жидкости, полутвердого и твердого кишечного содержимого в просвете кишечника, а также площади (в процентах) доступной визуализации поверхности кишки. Критики шкалы отмечали сложность и субъективизм количественных параметров, а также отсутствие дифференцировки оценки по отделам кишечника. Эти недостатки попытались преодолеть при разработке шкал Ottawa Bowel Preparation Scale (OBPS, 2004), Boston Bowel Preparation Scale (BBPS, 2009), Harefield Cleansing Scale (НCS, 2012) и Chicago Bowel Preparation Scale (CBPS, 2013) [15, 17–19]. Шкалы отличаются количеством баллов, вектором оценки (по возрастанию/убыванию), характером подразделения толстой кишки на сегменты. При оценке по шкале CBPS важное значение имеет фактор отмывания. Оценка очищения кишечника по шкале Harefield завершается присвоением степени от A (наилучшее очищение) до D (неудовлетворительное очищение). Шкалы НCS и BBPS обеспечивают рандомизированную оценку качества подготовки кишечника при применении различных препаратов и широко используются при проведении клинических исследований. Всем предложенным шкалам присущи свои преимущества и недостатки [14]. Существуют систематические обзоры по сопоставлению различных шкал в отношении информативности [20]. Достаточно простой и тщательно валидизированной считается Бостонская шкала подготовки кишечника (BBPS) [21]. В соответствии с ней толстая кишка подразделяется на три сегмента (правый, включающий слепую и восходящую ободочную кишку; поперечный, включающий поперечную ободочную кишку, печеночный и селезеночный изгибы; и левый, включающий нисходящую ободочную, сигмовидную и прямую кишку), при этом каждый сегмент оценивается в баллах (табл. 1) и результаты суммируются, интерпретируясь в пределах от 0 до 9 баллов, где 0 соответствует неудовлетворительной подготовке, 9 – полному очищению кишечника.
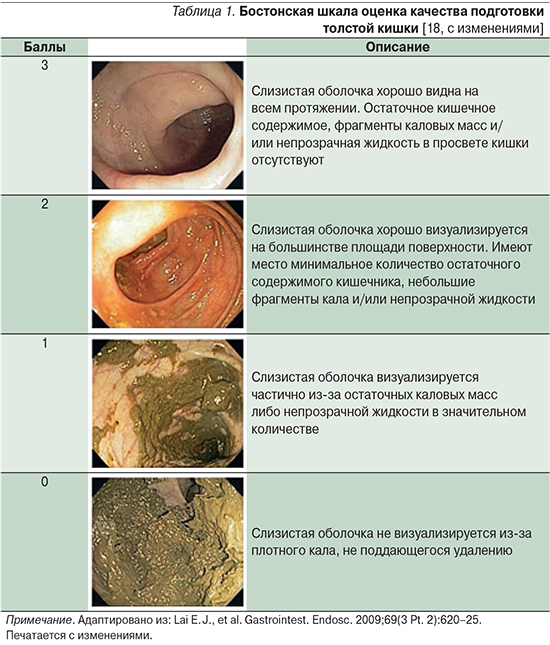
В качестве более достоверной и надежной альтернативы некоторыми авторами рассматривается шкала CBPS, однако предложенный алгоритм оценки представляется более сложным для ординарного эндоскописта и менее применимым в рутинной клинической практике, а ряд приведенных в статье [22] данных не демонстрирует клинически и статистически значимых различий между сравниваемыми Бостонской и Чикагской шкалами.
Организационно схемы подготовки кишечника к инструментальным исследованиям сочетают в себе диетические рекомендации и антеградный пероральный КЛ с использованием фармакологических слабительных средств.
Диетические рекомендации
Важнейшей в плане реализации диетических ограничений является т.н. бесшлаковая диета. Она подразумевает прием в течение 1–5 дней, предшествовавших колоноскопии, прозрачной жидкости и пищи с пониженным содержанием балластных веществ, в первую очередь пищевых волокон или грубой клетчатки. Разрешены к употреблению, в частности, продукты и блюда из риса и очищенной муки высшего сорта, супы мясные на нежирном бульоне без овощей; паровые котлеты и тефтели из нежирной говядины, телятины; кура в отварном виде, также в виде котлет, фрикаделек; куриное яйцо; отварная рыба нежирных сортов: хек, судак, минтай, треска, пикша и пр.; ряд молочных продуктов: нежирный творог, натуральный йогурт, нежирный кефир; отварной/печеный картофель (без кожуры); желе, сахар, мед; прозрачные некрепкие напитки (чай, компоты, кисели, соки без мякоти, ягод и зерен). Следует избегать употребления продуктов, содержащих цельные и измельченные зерна, орехи, мак и пр. Не используются в пищу ржаной хлеб, бобовые (горох, фасоль, чечевица), свежие/сушеные овощи и фрукты, ягоды, особенно с мелкими косточками, зелень (белокочанная капуста, салат, лук, укроп, петрушка, кинза), молочные супы, жирные и жилистые сорта птицы (утка, гусь), мясо (свинина, баранина) и рыба (форель, лосось, сельдь и пр.), колбасы, сосиски, сардельки, копчености, консервы, соленья, морские водоросли, ряд молочных продуктов (йогурт с наполнителями, сметана, сливки, мороженое), острые приправы (горчица, перец, лук, чеснок), алкогольные и газированные напитки. В день, предшестовавший колоноскопии, желателен изолированный прием прозрачных жидкостей (мясной бульон, чай, фруктовые соки без мякоти, негазированная минеральная и питьевая вода).
Существуют различные точки зрения на временной рубеж, после которого перед колоноскопией недопустимо пероральное употребление пищи и жидкости. В случае проведения эндоскопии в состоянии сохраненного сознания пациента, согласно Проекту рекомендаций эндоскопического общества РФ [14], непосредственно перед началом исследования допустим прием сладких жидкостей (чай или кофе с медом, кисель), которые не помешают исследованию, но улучшат самочувствие пациента и позволят легче перенести колоноскопию. При выполнении исследования под наркозом прием жидкостей за 2 часа до манипуляции запрещается. Мотивировано это отсутствием у пациента в состоянии общей анестезии кашлевого рефлекса и тем самым повышенной вероятностью регургитационных осложнений, вплоть до рефлекторного бронхоспазма и аспирационной пневмонии. В реальной клинической практике в соответствии с требованиями анестезиологов этот период увеличивается до 6–8 часов.
Информированное согласие
В качестве обязательного компонента процедуры очищения кишечника в настоящее время рассматривается получение информированного согласия, представляющее собой процесс разрешения пациентом и добровольного принятия к исполнению предложенного врачом медицинского вмешательства. Показано, что разъяснение пациенту смысла и особенностей процедуры в наглядной и доступной форме, в т.ч. с помощью образовательных буклетов, не только улучшает качество подготовки, но и повышает частоту успешного проведения колоноскопии, в частности, по показателю интубации слепой кишки [23].
Медикаментозные средства
Слабительные препараты или лаксативы, используемые в целях КЛ, могут быть классифицированы по происхождению (табл. 2) [24] и механизму действия (табл. 3).
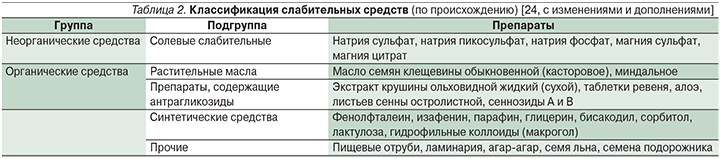
Традиционно в целях подготовки кишечника к колоноскопии применяются такие препараты, как касторовое масло, магния сульфат, маннитол, лактулоза (Дюфалак, Лактусан, Прелакс), натрия пикосульфат (Пикопреп), натрия фосфат (Флит Фосфо-Сода), препараты на основе макроголя (Фортранс, Лавакол, Эндофальк, Мовипреп). За рубежом, кроме того, используются средства Suprep (натрия сульфат, калия сульфат, магния сульфат), Suclear (натрия сульфат, калия сульфат, магния сульфат, ПЭГ 3350), Prepopik (натрия пикосульфат, магния сульфат, ангидрид лимонной кислоты), Generic (магния цитрат), Osmoprep (натрия фосфат моно- и двуосновной). Каждый из них имеет свои достоинства и недостатки.

Касторовое масло к настоящему времени сохранило преимущественно историческое значение в линейке средств подготовки к колоноскопии, однако в страте малообеспеченных граждан ввиду низкой стоимости продолжает оставаться востребованным. Механизм действия: при приеме внутрь препарат расщепляется липазой в тонкой кишке с образованием рицинолевой кислоты, которая вызывает раздражение рецепторов кишечника (на всем его протяжении) и рефлекторное усиление кишечной перистальтики. Слабительный эффект наступает обычно через 5–6 часов. К побочным эффектам относят абдоминальные боли, тошноту, рвоту, выраженную диарею, токомиметический эффект, нарушение электролитного обмена, судороги. Касторовое масло способно вызывать обострение хронических заболеваний печени, желчевыводящих путей и поджелудочной железы, что ограничивает его применение соответствующими категориями больных.
Соли магния при приеме внутрь характеризуются наличием гиперосмолярного солевого слабительного эффекта, обеспечивающего развитие осмотической диареи. Наиболее распространенный магния сульфат помимо послабляющего обладает противосудорожным, антиаритмическим, вазодилатирующим, гипотензивным, спазмолитическим, седативным, желчегонным, токолитическим фармакологическим действиями. Механизм слабительного эффекта реализуется за счет затруднения всасывания (не более 20%) препарата в кишечнике, что способствует повышению в ЖКТ осмотического давления, внутрипросветному выходу по градиенту концентрации и задержке жидкости в просвете кишечника, что способствует усилению перистальтики. Кроме того, препарат стимулирует высвобождение холецистокинина, вызывающего интралюминальную задержку жидкости и электролитов и ускорение тонко- и толстокишечного транзита. Дефекация обычно отсрочена и развивается через 4–6 часов после приема препарата. Абсорбированная его часть выводится почками, при этом усиливается диурез, скорость почечной экскреции пропорциональна концентрации в плазме и величине клубочковой фильтрации. Способ применения (в качестве слабительного): внутрь, натощак, взрослым – по 20–25 г в 200 мл воды. Поскольку магния сульфат при поступлении в системную циркуляцию выводится исключительно почками, препарат должен с исключительной осторожностью использоваться при нефропатиях и хронической почечной недостаточности. Противопоказания: хроническая почечная недостаточность тяжелой степени, гиперчувствительность, гипермагниемия, аппендицит, ректальное кровотечение, кишечная непроходимость, дегидратация, беременность, лактация, детский возраст (до 18 лет). Применение препарата ограничено при острых воспалительных заболеваниях ЖКТ, нарушениях проводимости, поражении миокарда, хронической почечной недостаточности. Побочные эффекты (при приеме внутрь) многочисленны: тошнота, рвота, диарея, обострение воспалительных заболеваний ЖКТ, нарушение электролитного баланса (повышенная утомляемость, астения, спутанность сознания, аритмия, судороги), метеоризм, абдоминальная боль спастического характера, жажда, признаки и симптомы гипермагниемии (особенно при почечной недостаточности).
В ранних схемах КЛ с достаточно высокой эффективностью использовался в качестве подготовки к т.н. ректальной пульсирующей ирригации («per rectal pulsed irrigation») [25], заключавшейся в 30-минутном введении теплой воды через задний проход непосредственно перед эндоскопией. К недостаткам метода относятся его трудо- и времязатратность, инвазивность и потребность в помощи квалифицированного медицинского персонала. В современных рекомендациях в качестве самостоятельного cредства очищения кишечника он не представлен, периодическое назначение обусловлено главным образом экономическими причинами. В качестве компонента гидромеханического ретроградного лаважа в начале 1990-х гг. изучалась возможность использования магния цитрат [25], однако широкого применения данный способ не нашел.
Маннитол. В качестве слабительного средства имеет исключительно историческое значение, в гастроэнтерологии в настоящее время применяется исключительно при проведении гидро-МРТ кишечника. Использовался в ранних рецептурах, но его применение было оставлено ввиду бактериальной ферментации препарата представителями микробиоты кишечника с образованием водорода и метана. Описаны случаи объемного взрыва кишечного содержимого при проведении эндоскопической полипэктомии в условиях использования диатермокоагулятора [26, 27].
Натрия фосфат представляет собой низкообъемный гиперосмолярный раствор, содержащий в 100 мл 48 г моноосновной и 18 г двуосновной соли. Действие препарата реализуется посредством увеличения за счет осмотических процессов задержки воды в просвете кишечника с последующим усилением его перистальтики. В день, предшестовавший колоноскопии, содержимое одного флакона (45 мл), растворенное в 120 мл кипяченой воды, принимают внутрь дважды в день с 10–12-часовым промежутком. Между приемами препарата употребляют внутрь прозрачную жидкость в объеме от 240 мл до максимально переносимого количества. Применение препарата ограничено возможными значимыми изменениями водно-электролитного баланса. Помимо дозозависимой абсорбции ионов натрия и фосфатов возможно развитие эксикоза и/или дисэлектролитемии (гипокальциемия, гипокалиемия, ацидоз), а также повреждение слизистой оболочки кишечника на макро- и микроуровнях, вплоть до формирования афтоидных эрозий, что может приводить к гипердиагностике воспалительных заболеваний кишечника. Согласно Европейскому консенсусу [28], натрия фосфат не рекомендуется для очистки кишечника ввиду потенциальной нефротоксичности и других нежелательных явлений, однако его использование возможно пациентами, для которых препараты на основе полиэтиленгликоля или натрия пикосульфата неэффективны или плохо переносятся. Фосфатная нефропатия чаще развивается у пациентов со скомпрометированной функцией почек, дегидратацией, гиперкальциемией либо гипертензией при использовании ингибиторов АПФ, блокаторов рецепторов ангиотензина, является дозо- и возрастзависимой. Следует отметить, что, согласно отечественной инструкции по медицинскому применению, исключительными показаниями к применению метода являются подготовка кишечника к инструментальным исследованиям либо оперативному вмешательству на кишечнике. Применение препарата противопоказано при гиперчувствительности к его компонентам, наличии кишечной непроходимости, мегаколона, острых воспалительных заболеваниях кишечника, почечной либо сердечной недостаточности, выраженных проявлениях абдоминального болевого и диспепсического синдромов, а также в возрасте до 15 лет.
Лактулоза. Механизм непосредственно слабительного действия препарата обусловлен двумя основными компонентами: гиперосмолярностью сиропа, обеспечивающей увеличение объема кишечного содержимого, и снижением pH кишечного содержимого вследствие метаболизации лактулозы кишечной микрофлорой до короткоцепочечных жирных кислот (молочной, уксусной, масляной, пропионовой), что приводит к стимуляции перистальтики кишечника и его опорожнению. Среди показаний к применению препарата подготовка кишечника к инструментальным исследованиям не значится, однако фактически он достаточно часто используется с этими целями «off label». Противопоказания: повышенная чувствительность к активному компоненту или фруктозе, галактозе, лактозе; галактоземия; непроходимость кишечника. С осторожностью следует использовать при нарушениях углеводного обмена. Наиболее частым побочным эффектом применения лактулозы является развитие метеоризма [29], требующее параллельного назначения пеногасителя (симетикона).
Натрия пикосульфат является основным действующим веществом единственного представленного на рынке препарата Пикопреп, в состав которого также входят лимонная кислота и оксид магния. Натрия пикосульфат, превращающийся в кишечнике в активный бис-(п-гидроксифенил)-пиридил-2-метан, оказывает стимулирующее действие на слизистую оболочку толстой кишки. Магния цитрат, образующийся при взаимодействии лимонной кислоты и оксида магния, вызывает осмотическое слабительное действие. Активные компоненты обладают местным действием и фактически не всасываются. Выпускается в форме порошка, который растворяют в 150 мл кипяченой воды, принимают внутрь дважды с интервалом не менее 6 часов с обязательным условием дополнительного приема внутрь прозрачной жидкости суммарным объемом от 2 л. Препарат разрешен к применению взрослыми и детьми начиная с возраста 1 год. Некоторые исследователи заявляют о сопоставимой эффективности препаратов натрия пикосульфата с лаксативами на основе макроголя [1].
Макрогол. Высокомолекулярный полимер на основе полиэтиленгликоля (ПЭГ) с молекулярным весом 3350 либо 4000 Da. Оказывает осмотическое действие, удерживая молекулы воды принимаемого раствора в просвете кишки. Увеличенный объем кишечного содержимого усиливает перистальтику кишечника. В результате ускоряется продвижение размягченных каловых масс по толстой кишке. Действие продукта начинается через 1–1,5 часа и длится 2–5 часов. Практически не абсорбируется в кишечнике, не проникает в системное кровообращение, не метаболизируется.
Способы применения лаксативов
В 1980 г. Davis et al. [30] обосновали целесообразность применения осмотически сбалансированного коллоидно-электролитного лаважного раствора на основе макроголя (ПЭГ), при этом последний обеспечивает собственно осмотическое слабительное действие, а солевая составляющая – изотоничность и изоосмотичность, предотвращая транскишечный транспорт воды и электролитов. Стандартный 4-литровый режим дозирования препарата в день перед процедурой стал «золотым стандартом» при подготовке к манипуляциям на кишечнике. Однако некоторые органолептические характеристики (соленый вкус, неприятный сульфатный запах) оригинального препарата (Фортранс), значительный объем потребляемой жидкости и вследствие этих причин низкая приверженность пациентов соблюдению рекомендаций сподвигли исследователей на дальнейшее совершенствование средств КЛ в направлении уменьшения объемных характеристик потребляемого раствора, оптимизации режима и времени его приема, солевого состава, улучшения вкусовых качеств.
Второе поколение современных препаратов на основе ПЭГ (Эндофальк) обеспечивает минимизацию потребности в солевых компонентах за счет уменьшения молекулярной массы ПЭГ с 4000 до 3350 Да, не содержит сульфатов, характеризуется улучшенными органолептическими свойствами за счет включения ароматизирующих компонентов.
Препараты на основе ПЭГ признаны основными консенсусами мира в качестве средства выбора для подготовки к колоноскопии, а также видеокапсульной эндоскопии [14, 15, 28]. Однако некоторые исследователи [31] оспаривают это утверждение в пользу натрия пикосульфата. Согласно Европейскому консенсусу по подготовке кишечника к фиброколоноскопии и видеокапсульной эндоскопии [28, 32], базирующихся на применении ПЭГ, способы подготовки кишечника рекомендуются в качестве средств первой линии для обеих процедур. Стандартным для «полнообъемной» схемы подготовки является прием внутрь 4 л раствора в день накануне колоноскопии, по 250 мл каждые 15 минут до полного очищения кишечника, контролируемого по состоянию промывных вод, либо до полного потребления 4 л раствора. ПЭГ более безопасен (в т.ч. в отношении высвобождения водорода), более эффективен и лучше переносится, чем схемы на основе маннитола.
Присутствующие на отечественном фармацевтическом рынке препараты (Фортранс, Мовипреп, Лавакол, Эндофальк) отличаются главным образом формой выпуска, а также составом и дозировкой вспомогательных компонентов. Так, препарат Фортранс помимо ПЭГ содержит натрия хлорид, калия хлорид, натрия гидрокарбонат, натрия сульфат безводный, натрия сахаринат. Мовипреп, помимо макрогола с молекулярной массой 3350 Да, включает натрия сульфат, натрия хлорид, калия хлорид, ацесульфам калия, ароматизатор лимонный, аскорбиновую кислоту, натрия аскорбат. Лавакол, препарат отечественного производства, кроме ПЭГ, содержит хлориды натрия и калия, а также сульфат и гиброкарбонат натрия. Имеет относительно малую разовую дозу (12 г на саше), что облегчает его дозирование. Бессульфатная форма макрогола (Эндофальк) обладает улучшенными по сравнению с традиционными препаратами ПЭГ вкусовыми характеристиками при сопоставимой эффективности и безопасности [29].
Несмотря на все преимущества препаратов на основе ПЭГ, до 20% пациентов не в состоянии завершить подготовку по причине их неприятных вкусовых качеств и значительного объема раствора. Последнее устраняется т.н. раздельным (в «сплит-режиме») приемом препарата, подразумевающим использование 3 л раствора в день накануне исследования и 1 л в ранние утренние часы дня процедуры. Значимым оказался и временной интервал между приемом препарата и колоноскопией. Так, потребление раствора ПЭГ в сроки до 5 часов перед процедурой привело к более качественному очищению кишечника, чем таковое в сроки более 19 часов до процедуры. Дополнительные исследования продемонстрировали преимущества сплит-схемы перед одноэтапным приемом в отношении как безопасности, так и эффективности процедуры.
В литературе активно обсуждается вопрос предикторов неадекватной подготовки кишечника к эндоскопии. По данным Американского общества гастроинтестинальной эндоскопии [15], к таковым относятся предшествовавший эпизод неадекватной подготовки кишечника к фиброколоноскопии; неанглоязычные пациенты; наличие страховки Medicaid; отсутствие семьи; пребывание на стационарном лечении; полипрагмазия (в т.ч. употребление опиатов); ожирение; пожилой возраст; мужской пол; сопутствующая патология (сахарный дипбет, острое нарушение мозгового кровообращения, деменция, болезнь Паркинсона); низкая комплаентность. Следует отметить, что в ряде случаев недостаточное очищение кишечника может определяться индивидуальными особенностями физиологии ЖКТ пациента, а потому считается неуправляемым фактором риска.
Перспективы развития метода кишечного лаважа
С учетом вышеизложенного среди перспективных направлений совершенствования методики КЛ можно выделить следующие:
1. Повышение информированности пациента относительно предстоящей процедуры и методики подготовки к ней, минимизация вероятности ошибки в приеме лаважного раствора, несоблюдения инструкции по медицинскому применению препарата, что достигается методами разъяснения, в т ч. визуализации, а в ряде случаев – и суггессии [33].
2. Оптимизация схемы применения препарата [9, 10, 34]. Наиболее перспективной в этом отношении признано использование раздельного метода подготовки кишечника, при этом конкретные временные и объемные параметры метода являются объектом пристального научного изучения исследователями [8, 15, 35, 36]. Посредством сплит-режима достигается уменьшение объема вводимого за непродолжительное время препарата, снижение выраженности побочных явления, повышение комплаентности пациентов и обеспечивается минимизация вторичного внутрипросветного загрязнения кишечника, развивающегося на фоне продолжающейся секреции желудка, тонкой и толстой кишки [36]. Особое внимание уделяется т.н. низкообъемным (<3 л) схемам подготовки [37].
3. Включение в состав комбинации компонентов, обеспечивающих высокое качество очищения кишечника с минимальной вероятностью развития побочных явлений. Данное направление реализуется посредством исключения из прописей органолептически неблагоприятных компонентов, в частности натрия сульфата. При наличии запоров и успешном использовании пациентом лаксативов для их коррекции предлагается продолжить их прием, зачастую в увеличенной дозировке [29].
4. Использование средств симптоматической терапии, направленной на профилактику и/или купирование осложнений и побочных явлений от назначения очищающего раствора и таким образом обеспечивающих повышение приверженности пациента выполнению врачебных рекомендаций [38].
К ним можно отнести охлаждение раствора для перорального применения, использование различных вкусовых добавок [29], предварительное применение бисакодила, магния цитрата. Профилактический прием прокинетиков [39] (метоклопрамида итоприда гидрохлорид, мозаприда цитрат), не оказывая существенного прямого влияния на степень очищения кишечника, способствует повышению переносимости процедуры посредством минимизации проявлений желудочной диспепсии и вследствие этого повышению комплаентности пациентов [38]. Кроме того, в качестве дополнения при подготовке к колоноскопии широко применяют симетикон. Препарат помогает уменьшить флатуленцию, ассоциированную с манипуляцией, а также используется в качестве пеногасителя в просвете кишечника, что улучшает визуализацию слизистой оболочки. Широко используется комбинация данных подходов [14, 28, 29], реализуемая с учетом требований доказательной медицины и индивидуальных особенностей пациентов [40].
5. Изыскание возможностей расширения режима двигательной активности пациента при подготовке к исследованию [41].
6. Поиск новых средств КЛ.
Сотрудники СЗГМУ им. И.И. Мечникова [29] разработали алгоритм подготовки к колоноскопии, обеспечивающий оптимальный эффект очищения кишечника с учетом опыта предыдущих колоноскопий, возможности приема значительного объема жидкости внутрь, массы тела пациента и наличия у него запоров, а также характера стула в день колоноскопии. При этом конечными модифицируемыми факторами являются объем лаважного раствора, этапность схемы приема, а также факт дополнительного применения и дозировка бисакодила либо натрия пикосульфата.
Поиск способов потенцирования лаважного эффекта ПЭГ продолжается и по сию пору. Памятуя о том, что новое – это хорошо забытое старое, исследователи пытаются совместить т.н. современные и традиционные слабительные для повышения эффективноси процедуры подготовки кишечника. Так, в публикации Х. Tian et al. (2018) [42] заявлено о проведении рандомизированного двойного слепого проспективного сравнительного исследования по изучению эффективности и безопасности подготовки кишечника к колоноскопии в 3 режимах: касторовое масло (30 мл)+аскорбиновая кислота (5 г)+ПЭГ (1 л); касторовое масла (30 мл)+2 л ПЭГ; 3 л ПЭГ. Результаты планируется опубликовать в ближайшее время.
Собственный авторский опыт [43, 44] применения средств КЛ согласуется с известными данными литературы, при этом отмечено, что использование современных осмотических слабительных средства на основе ПЭГ даже при снижении комплаентности сопровождается удовлетворительной подготовкой кишечника к инструментальному исследованию при невысокой частоте и выраженности нежелательных явлений, однако может сопровождаться изменениями со стороны микроэлементного состава крови, в частности содержания сывороточного железа.
Заключение
Таким образом, полноценная качественная и безопасная подготовка кишечника к колоноскопии является неотъемлемым элементом инструментальной процедуры, в значительной степени определяющим успех диагностического исследования. Несмотря на имеющиеся трудности, в настоящее время мировым медицинским сообществом выработан достаточно четкий алгоритм действий для достижения оптимального результата. Соединение организационных, диетических и медикаментозных мероприятий обеспечивает успех исследования. Современные методы антеградного КЛ обеспечивают высокую эффективность подготовки кишечника к инструментальным исследованиям при удовлетворительной безопасности процедуры. Оптимальными средствами медикаментозного очищения кишечника продолжают оставаться осмотические слабительные препараты на основе ПЭГ. К методам повышения их эффективности и безопасности относятся индивидуализированный подход, двухэтапная подготовка, применение комбинаций слабительных средств, использование по показаниям средств симптоматической терапии.



