Инфекции нижних дыхательных путей (НДП) занимают одно из ведущих мест в структуре патологии органов дыхания, что связано с высокими показателями заболеваемости, распространенности, в ряде случаев – летальности. Данная патология остается тяжелым социально-экономическим бременем как для пациентов, так и для общества, оказывая значительную нагрузку на бюджеты здравоохранения различных уровней.
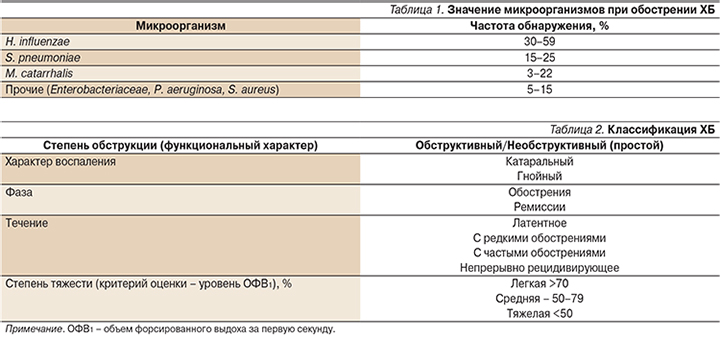
НДП представлены анатомо-функциональными структурами респираторной системы, располагающимися ниже уровня гортани (трахея, бронхи, бронхиолы, альвеолы). Инфекционное поражение каждого из этих отделов дыхательных путей характеризуется соответствующими этиологическими особенностями, клиническими проявлениями, течением, прогнозом, подходами к лечению. Основные нозологические формы, при которых инфекция становится ведущим или основным этиологическим фактором поражения НДП, – это острые и хронические бронхиты, пневмонии. При острых бронхитах ведущим этиологическим фактором является вирусная инфекция, не требующая назначения антибактериальных препаратов [1, 10]. Под хроническим бронхитом (ХБ) понимают хроническое воспалительное заболевание бронхов, характеризующееся морфологической перестройкой их слизистой оболочки, сопровождающееся гиперсекрецией слизи, нарушением очистительной функции бронхов, что проявляется постоянным или периодически возникающим кашлем и выделением мокроты. По рекомендациям Всемирной организации здравоохранения, бронхит может считаться хроническим при отхождении мокроты в течение периода не менее 3 месяцев в году на протяжении более 2 лет [5, 9]. Среди населения России заболеваемость ХБ, рассчитанная на основе данных по обращаемости больных за медицинской помощью, составляет 10–20% [2]. Факторами, приводящими к развитию ХБ, могут быть курение, длительное воздействие неблагоприятных экологических, профессиональных и бытовых факторов, частые вирусные инфекции, дефицит α1-антитрипсина. В подавляющем числе (75–80%) случаев обострение ХБ обусловлено присоединением вторичной бактериальной инфекции, которая определяет дальнейшее течение и прогрессирование заболевания [2, 6]. При легком обострении доминирующее значение имеют такие возбудители, как Haemophilus influenzae (нетипируемые и некапсулированные формы), Streptococcus pneumoniae, Moraxella catarrhalis. При более тяжелых обострениях (выраженная дыхательная недостаточность, декомпенсация сопутствующей патологии и др.), нередко требующих госпитализации в отделения интенсивной терапии, удельный вес названных микроорганизмов снижается и увеличивается доля грамотрицательных бактерий, в частности различных видов Enterobacteriaceae и в тяжелых ситуациях P. aeruginosa (табл. 1) [1, 3].
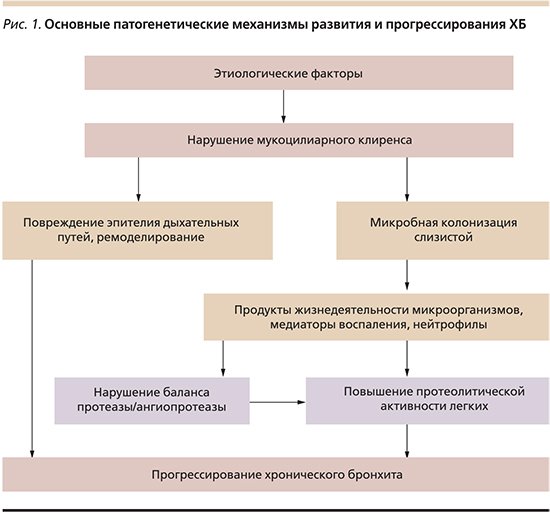
Различные этиологические факторы повреждают систему местной защиты дыхательных путей на различных уровнях (включая нарушение мукоцилиарного клиренса, клеточного и гуморального звеньев иммунитета). При этом создаются условия для микробной колонизации слизистой оболочки бронхов, развивается воспалительная реакция с высвобождением ряда медиаторов и притоком нейтрофилов, что стимулирует продукцию слизи и оказывает дальнейшее повреждающее действие на эпителиальные клетки (рис. 1) [6].
Классификация ХБ представлена в табл. 2 [8].
Классическими признаками, характеризующими обострение ХБ, являются следующие критерии, предложенные N.R. Anthonisen и соавт. [11]: появление или усиление одышки; увеличение объема отделяемой мокроты и усиление гнойности мокроты. Наличие всех трех вышеуказанных критериев описывается как I тип, двух из них – как II, одного – как III тип обострения заболевания [1–3]. Схема поэтапного ведения пациентов с ХБ представлена на рис. 2 [6].
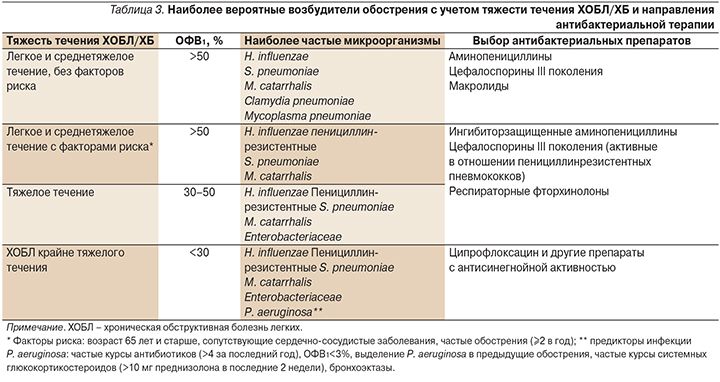
Лечение ХБ должно быть направлено на устранение симптомов обострения заболевания, снижение скорости прогрессирования диффузного повреждения бронхов, уменьшение частоты обострений, удлинение ремиссии, повышение качества жизни [5, 6]. Для лечения ХБ используются такие препараты, как противомикробные и муколитические лекарственные средства (ЛС), бронходилататоры и иммуномодуляторы. При обострении ХБ, вызванном бактериальной инфекцией, основным методом лечения остается эмпирическая антибактериальная терапия. При выборе ЛС необходимо учитывать тяжесть обострения, тип обострения, активность ЛС в отношении наиболее часто встречающихся возбудителей с учетом возможной антибиотикорезистентности, оптимальные фармакокинетические свойства (высокая биодоступность, способность к проникновению в мокроту и слизь, длительность действия), спектр возможных нежелательных побочных эффектов, качество препарата и удобство приема, способствующее высокому комплайнсу пациента [6]. Антибактериальные препараты показаны пациентам с I типом обострения ХБ, т.к. в данном случае наиболее вероятна инфекционная природа обострения. Также основанием для назначения антибактериальной терапии является II тип обострения ХБ (при наличии гнойной мокроты) и тяжелое обострение заболевания, требующее госпитализации [2]. Для лечения ХБ в период обострения возможно применение макролидов, пенициллинов, тетрациклинов, фторхинолонов, цефалоспоринов [6]. Алгоритм антибиотикотерапии при обострении ХБ в зависимости от типа и тяжести обострения представлен на рис 3 и в табл. 3 [2, 3].
Одним из препаратов, соответствующих вышеуказанным критериям, является представитель цефалоспоринов III поколения – цефдиторен пивоксил. Прежде всего он отличается наиболее «сбалансированным» спектром активности среди пероральных цефалоспоринов. Так, в отличие от цефалексина, цефуроксима, цефиксима и цефтибутена цефдиторен высокоактивен в отношении всех основных «типичных» бактериальных возбудителей внебольничных респираторных инфекций: S. pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, H. influenzae, Moraxella сatarrhalis, и представителей семейства Enterobacteriaceae [4]. Важным отличием цефдиторена от других цефалоспоринов III поколения для перорального приема (цефиксим, цефтибутен) является также его высокая бактерицидная активность в отношении пенициллинрезистентных пневмококков благодаря его сродству с пенициллин-связывающими белками. По выраженности бактерицидного эффекта через 24 часа цефдиторен превосходит другие пероральные β-лактамы, включая амоксициллин/клавуланат, цефуроксим, цефиксим, цефподоксим, и не уступает респираторным фторхинолонам [7]. Еще одним преимуществом цефдиторена, особенно актуальным в наше время, является его устойчивость к гидролизу большинства β-лактамаз грамотрицательных бактерий. Препарат также обладает хорошими фармакокинетическими характеристиками, а именно: высокой биодоступностью, способностью создавать надежные бактерицидные концентрации в очаге поражения. Кроме этого препарат не метаболизируется в печени и обладает хорошим профилем переносимости и безопасности [4, 7]. Клиническая и микробиологическая эффективность цефдиторена подтверждена в ряде рандомизированных клинических исследований [4, 12–14]. Рекомендуемые режим дозирования при обострении хронического бронхита – по 200 мг каждые 12 часа в течение 5 дней. Нужно отметить, что цефдиторен может применяться не только для стартовой пероральной терапии в амбулаторных условиях, но и как препарат для ступенчатой терапии внебольничных инфекций у госпитализированных пациентов, являясь в данном случае единственным адекватным пероральным β-лактамом для перехода с терапии парентеральными цефалоспоринами III поколения [4].

В заключение можно сказать, что грамотно проведенная антибиотикотерапия будет не только купировать симптомы обострения ХБ, но и способствовать увеличению длительности периода между обострениями и, соответственно, повышению качества жизни больного.



