По данным Клинических рекомендаций Европейской ассоциации урологов (ЕАУ) 2022 г., «хроническая тазовая боль (ХТБ) определяется как постоянная или персистирующая боль, которая ощущается* в структурах, связанных с тазом, у мужчин или женщин. Она часто сопровождается негативными когнитивными, поведенческими, сексуальными и эмоциональными реакциями, а также симптомами, свидетельствующими о нарушении функции нижних мочевых путей, сексуальной сферы, кишечника или гинекологических функций».
При наличии ноцицептивной боли, которая со временем становится хронической/персистирующей, она должна быть непрерывной или рецидивировать в течение не менее 3 месяцев (в соответствии с МКБ-11). При циклической боли допустимо использовать период времени более 6 месяцев.
При неострой боли и признаках центральной сенсибилизации боль можно расценивать как хроническую, вне зависимости от длительности. Синдромы ХТБ можно разделить на состояния с хорошо описанной патологией (например, инфекция или рак) и состояния без явной патологии. Для описания первой группы предлагается использовать термин «тазовая боль, связанная со специфическими заболеваниями», а для описания второй группы – «синдром хронической тазовой боли» [1]. «В новой классификации МКБ-11 эти группы получили новые названия: первая будет называться хронической вторичной тазовой болью, вторая – хронической первичной тазовой болью». Последующая классификация относится только к синдрому хронической первичной тазовой боли. Синдром хронической первичной тазовой боли (СХПТБ) является хронической тазовой болью, при которой не доказано наличие инфекции или другой локальной патологии, которая могла бы обусловливать боль. Он часто сопровождается негативными когнитивными, поведенческими, сексуальными и эмоциональными реакциями, а также симптомами, свидетельствующими о нарушении функции нижних мочевых путей, сексуальной сферы, кишечника или гинекологических функций. СХПТБ относится к ХТБ.
В соответствии с данными Международной ассоциации тазовой боли выделено 6 облигатных для данного заболевания признаков: 1) длительность болевого синдрома ≥6 месяцев; 2) низкая эффективность терапии; 3) несоответствие выраженности боли по ощущениям пациента выраженности повреждения ткани; 4) наличие признаков депрессивного расстройства; 5) прогрессирующее ограничение физической активности; 6) наличие поведенческих расстройств [2, 3].
Хроническими болями в тазу страдают по разным данным от 7 до 24% населения земли; существует более ста заболеваний, в клинической картине которых основным симптомом является хроническая тазовая боль [4, 5]. Выделяют гинекологические, урологические, желудочно-кишечные, сосудистые, скелетно-мышечные, неврологические, психологические причины ХТБ [5, 6].
Согласно Клиническим рекомендациям Европейской ассоциации урологов 2022 г., в пункте 3.2.5.8. описывается «сопутствующая патология при синдромах тазовой боли», в том числе и повреждение нерва. Спинальная патология и любая другая патология по ходу пораженного нерва могут вызывать нейропатическую боль в зоне его иннервации. Кроме того, повреждение нерва могут вызывать неопластические заболевания, инфекция и травма, хирургический разрез и послеоперационный рубец [7].
«Срамной нерв может поражаться на следующих уровнях: 1) грушевидная мышца. Например, в рамках синдрома грушевидной мышцы: в ряде случаев нерв проходит через мышцу и может ею сдавливаться; в других случаях проблема связана с гипертрофией или спазмом мышцы; 2) крестцово-остистые и крестцово-бугорковые связки (около 42% случаев); 3) в канале Алькока, медиальнее внутренней запирательной мышцы, в ее фасции (до 26%); 4) на нескольких уровнях (в 17% случаев); 5) зона повреждения определяет локализацию ощущаемой боли и характер сопутствующих симптомов (чем дистальнее повреждение, тем реже вовлекается анальная область)» [1, 8].
Механизм развития туннельных форм пудендоневропатии (ПНП) связан с анатомическими особенностями расположения полового нерва. Он формируется из S2, S3, S4 спинномозговых нервов и является одной из коротких ветвей крестцового сплетения [8].
Исследование, посвященное нейрогенному (неврогенному, нейропатическому, невропатическому) варианту хронической тазовой боли, проведено Neill M.E. [9].
По Sсhmidt R.A. (1991), одна из основных причин нейрогенной тазовой боли – компрессия или натяжение n. pudendus [10].
По МКБ-10 пудендальная нейропатия (невропатия) относится к G58.8 Другие уточненные виды мононейропатий. Согласно МКБ-11, в отдельную рубрику вынесена нейропатическая боль – MG30.5 Хроническая нейропатическая боль, принципы лечения которой основываются на патофизиологических механизмах, с разделением на: MG30.50 Хроническая центральная нейропатическая боль и MG30.51 Хроническая периферическая нейропатическая боль [11].
В клинической картине туннельных ПНП главным симптомом является боль (пудендальная невралгия). Она оценивается согласно Нантским диагностическим критериям ПНП (2006) [12, 13].
Основные (обязательные) критерии: 1) Боль в зоне иннервации полового нерва: от ануса до пениса/клитора. 2) Боль ощущается преимущественно в положении сидя. 3) Боль не вызывает ночных пробуждений. 4) Боль с отсутствием объективного сенсорного нарушения. 5) Боль купируется блокадой полового нерва.
Дополнительные диагностические критерии: 1) Боль жгучая, стреляющая, колющая, может сопровождаться онемением. 2) Аллодиния или гиперпатия. 3) Ощущение инородного тела в прямой кишке или влагалище (а также в уретре, мочевом пузыре) – симпаталгия. 4) Обострение боли в течение дня. 5) Боль преимущественно односторонняя. 6) Боль провоцируется дефекацией. 7) Резкая пальпаторная болезненность седалищной ости. 8) Результаты нейрофизиологических исследований.
Компрессия в половом канале (синдром пудендального канала – СПК, синдром канала Алкока, синдром велосипедиста, промежностная невралгия) является наиболее описанным в литературе тунельных синдромов полового нерва. СПК часто сочетается с компрессией половой артерии.
Beco J. выделяет три домена диагностики СПК [14]. Три основных симптома СПК: 1. Перинеодиния, прокталгия, вульводиния (скроталгия – боль в мошонке); 2. Анальная инконтиненция – недержание кала; 3. Уринарная инконтиненция – недержание мочи [15].
Прицельно для изучения СХПТБ мы ограничили коридор нашей сферы деятельности понятием «хроническая нейрогенная тазовая боль при нейропатии полового нерва», подразумевая, что другие органические причины тазовой боли не выявлены или они не могут являться источником хронической боли, но имеются инструментальные признаки нарушения периферической иннервации мышц тазового дна и клинические проявления дисфункции органов малого таза – анальная инконтиненция, затруднение эвакуации кишечного содержимого и мочи и/или болевой синдром (а также эректильная/эякуляторная дисфункция).
С помощью функциональных нейрофизиологических методов исследования (стимуляционная электронейромиография с электродом Св. Марка) мы имеем возможность диагностировать определенный уровень поражения – до канала Алькока или выше него – и достигаем лишь вершины «айсберга» проблемы нейрогенной тазовой боли, поскольку не можем визуализировать поражение корешков или сплетений.
В то же время, отвечая на комментарий одного из респондентов, появившийся в ходе работы над данной статьей – «…в разделе диагностики тазовой боли надо добавить возможность использовать бульбосакральный рефлекс, что в совокупности с данными, получаемыми с помощью методики с электродом Св. Марка (терминальная латентность, латентность F-волны) позволяет оценивать, как невральный, так и радикулярный уровень (сенсорной и моторной модальности). Использование соматосенсорных вызванных потенциалов и диагностической магнитной стимуляции позволяет оценить состояние супрасегментарного спинального и церебрального уровней ЦНС, ответственных за функцию тазовых органов» – на сегодняшний день мы используем следующий диагностический алгоритм, позволяющий частично дифференцировать уровень поражения: нейрофизиологическое обследование в виде стимуляционной ЭМГ для изучения латентного периода проведения возбуждения по двигательным волокнам полового нерва, а именно латентность М-ответа наружного сфинктера и мышц тазового дна, которая позволяет оценить сохранность эфферентного звена иннервации, а также возможную компрессию в канале Алькока. Дополнительно проводится исследование поздних феноменов смешанного-возвратно-рефлекторного ответа в виде глубокого пудендального (ГПР) как при одиночной, так и при ритмической стимуляции, а также бульбокавернозного рефлексов (БКР) для выявления возможных нарушений как афферентной, так и эфферентной иннервации. Комплексная оценка изолированных эфферентных нарушений (М-ответ) позволит нам использовать оценку латентности поздних феноменов с акцентом на изменение чувствительного звена иннервации.
Безусловно, наличие диагностируемых изменений с возможным воздействием на невральные структуры на уровне позвоночного канала, фораминального канала и после выхода из фораминального канала служит однозначным поводом для направления пациентов к нейрохирургу, в то время как при отсутствии изменений на МРТ и КТ пациенты маршрутизируются дополнительно к неврологу, остеопату, психиатру и т.д.
Проблема лечения нейрогенной тазовой боли, в том числе при пудендальной нейропатии, на сегодняшний день не имеет ни четкого понимания среди специалистов, ни четких алгоритмов, и не описана в отечественных клинических рекомендациях. Сложность в решении проблемы усугубляется ее немаловажными социальными и психологическими аспектами.
Особенностью хронической боли является наличие центральной сенситизации [16–18], приводящей к усугублению проблемы и замыкающей порочный круг болевых импульсов; и чем дольше эта проблема существует, тем сложнее этот круг разорвать.
Мы осознаем, что инструментальная диагностика открывает лишь часть занавеса проблемы хронической нейрогенной тазовой боли при пудендальной невропатии, а лечебное воздействие должно быть мультимодальным. При наличии невропатии полового нерва основной вектор лечебного воздействия должен быть направлен на снятие компрессии с полового нерва (и релаксацию мышц тазового дна). Второй вектор – на проводящие пути головного и спинного мозга – с целью разорвать патологический круг центральной сенситизации. Третий – на восстановление чувствительных и моторных функций.
В консервативном лечении хронической нейрогенной тазовой боли используется совокупность методов. Как правило, стартуют с фармакотерапии, физиотерапии, кинезиотерапии и психотерапии. При недостаточной эффективности консервативного лечения и при наличии соответствующей клинической симптоматики могут быть проведены лечебно-диагностические блокады, импульсная радиочастотная абляция [19–22], и нейростимуляция полового нерва [23, 24]. При подтверждении по результатам нейрофизиологических исследований, а также диагностической блокады диагноза невропатии полового нерва могут применяться более радикальные методы его хирургической декомпресии, с последующей многофакторной консервативной реабилитацией.
В конечном итоге, именно комбинация методов и последовательное их применение будут определять возможность успеха.
На сегодняшний день мы пытаемся заполнить лишь небольшой пробел знаний в применении консервативных методов лечения, а именно методики магнитной стимуляции, с целью расширить инструментарий специалистов и максимально улучшить качество жизни пациента. Речь идет о валидации протоколов высокоинтенсивной импульсной магнитной терапии (ВИМТ) для лечения нейропатии полового нерва, проявляющейся хронической нейрогенной тазовой болью.
В русскоязычной и в зарубежной научно-медицинской литературе мы не нашли данных о существовании протоколов лечения хронической нейрогенной тазовой боли при пудендальной нейропатии методом ВИМТ, но таковые существуют при других видах нейропатии. Очевидно, что протоколы ВИМТ будут схожи.
Учитывая, что на сегодняшний день отсутствуют исследования по эффективности магнитной терапии как в режиме монотерапии, так и в сочетании с другими методами лечения, выбор лечебной тактики может основываться на консолидированном мнении экспертов (консенсус). Согласительный документ, созданный на результатах данного опроса, позволит усовершенствовать представленные протоколы на основе высказанных мнений и предложений, и рекомендовать их внедрение в клиническую практику на всех зарегистрированных в России аппаратах для ВИМТ – с возможностью пересмотра согласительного документа при получении новых научных данных.
Цель: оценить мнение экспертов и разработать согласительный документ по использованию протоколов высокоинтенсивной импульсной магнитной стимуляции для лечения больных хронической нейрогенной тазовой болью.
Материалы и методы
Первым этапом в системах NCBI/PubMed (https://www.ncbi.nlm.nih.gov/pubmed) производили поиск публикаций по использованию нехирургических методов лечения нейрогенной тазовой боли по ключевым словам: «neurogenic pelvic pain» и «magnetic stimulation». Аналогично – в отечественных научных электронных библиотеках eLibrary.ru и CyberLeninka: «нейрогенная тазовая боль», «магнитная стимуляция». Далее, на основании анализа полученных и собственных данных был предложен алгоритм лечения пациентов с ХНТБ методом ВИМТ.
Протокол исследования был представлен для голосования при помощи Яндекс-опросника. Потенциальные респонденты включали специалистов – авторов научных работ по использованию нехирургических методов лечения хронической тазовой боли в клинической практике.
Следующим этапом проводили анонимный онлайн-опрос с использованием программы Yandex Forms, потенциальные участники опроса (далее – респонденты) получали ссылку на анкету: https://forms.yandex.ru/u/630f9c3d95aca3ed0fcc90b8/
Пройти опрос было возможно с 31 августа 2022 г. по 5 февраля 2023 г. Задачей данного опроса является согласование комплексных протоколов экстракорпоральной промежностной, транслюмбосакральной и транскраниальной магнитной стимуляции для лечения хронической нейрогенной тазовой боли как проявления пудендальной невропатии (диагноз был установлен по данным стимуляционной электронейромиографии по увеличению длительности латентного периода М-ответа при проведении возбуждения по двигательным волокнам полового нерва и/или по увеличению длительности латентности смешанного-возвратно рефлекторного ответа и/или по увеличению латентности бульбокавернозного рефлекса). Респонденты отвечали на 4 вопроса: 1) приемлемость предложенной комплексной методики магнитной стимуляции; 2) удобство использования и продолжительность проведения комплексной методики длительность каждого из трех протоколов, в среднем, 14 минут; 3) целесообразность применения стандартизированных протоколов на всех зарегистрированных в России аппаратах, предназначенных для лечения нейрогенной тазовой боли; 4) возможность использования данных протоколов в собственной клинической практике респондента при условии наличия соответствующих аппаратных комплексов с установленными протоколами, утвержденными междисциплинарным консенсусом.
Вопросы в анкете соответствовали прямому закрытому типу с ограниченным количеством простых вариантов ответа. Все комментарии, предложения и замечания относительно обсуждаемой темы респонденты имели возможность внести в свободное поле анкеты. Заполнение анкеты было возможно с одной учетной записи, неоднократно – с возможностью оценить внесенные в ходе обсуждения правки. Финальные результаты анкетирования были обобщены организатором опроса (О.Ю. Фоменко).
Каждый из вопросов рассматривался нами как положение, выносимое на обсуждение, с последующим принятием решения относительно уровня согласованности по критериям, основанным на модифицированном Дельфийском протоколе [25–30]: C1 – консенсус уровня 1 (отличный): констатировался при совпадении во мнении >90% участников опроса; C2 – консенсус уровня 2 (умеренный): при совпадении мнения от 75 до 90% респондентов; C3 – консенсус уровня 3 (отсутствует): когда <75% респондентов были единодушны в выборе ответа. Дизайн исследования представлен на рисунке 1.
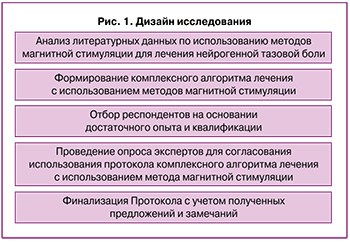
Статистическая обработка результатов анкетирования проходила полуавтоматически помощью программных возможностей Yandex Forms и пакета Statistica 10 (StatSoft Inc, США), для описания результатов использовали методы дескриптивной статистики. Корректность ответов оценивалась по их формальному соответствию заданным вопросам, использования некорректных вариантов ответов в анкете не предполагалось.
Обоснование протокола ВИМТ при лечении хронической нейрогенной тазовой боли
Первый протокол – экстракорпоральная промежностная магнитная стимуляция. Состоит из 3 сессий:
1 сессия. Воздействие осуществляют в положении больного на спине с разведенными и согнутыми в коленях ногами или сидя на магнитном кресле со встроенным индуктором – проводят протокол экстракорпорально, подводя магнитный индуктор к области промежности, амплитуда стимуляции подбирается индивидуально таким образом, чтобы у пациента появились минимальные мышечные сокращения в месте приложения индуктора.
Для этого используют протокол моторной магнитной стимуляции последовательно с частотой 5 и 10 Гц для улучшения сократительной способности мышц тазового дна (МТД) путем воздействия на внутримышечные аксоны (протокол приведен в таблице). При этом, согласно работам Zschorlich V. et al. [31], используют частоты 5 и 10 Гц. Цель данного протокола – экстракорпоральное воздействие на МТД путем стимуляции внутримышечных аксонов для улучшения проводимости по дистальным участкам нервов, отвечающих за иннервацию мышц тазового дна.
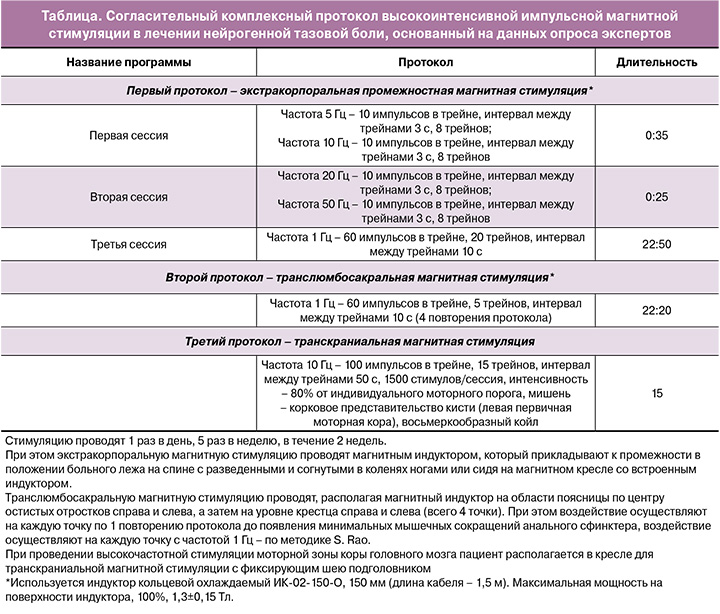
2 сессия. Проводится сначала на частоте 20 Гц, которая, по данным зарубежных авторов [30, 31], позволяет уменьшить спастичность мышц с целью ее релаксации [32].
Так, Dietz V. (2000) в своей работе обнаружил значительное снижение спастического тонуса, проявляющееся в увеличении скорости маха нижними конечностями. Испытуемым проводили магнитную стимуляцию после заполнения шкалы Эшворта и маятникового теста. Курс ритмической магнитной стимуляции состоял из 10 сеансов; каждая серия стимуляций длилась 10 с с частотой 20 Гц. Межстимульный интервал составлял 40 с. Всего было дано 2000 однократных магнитных стимулов. Стимулируемая сторона всегда была клинически более пораженной ногой. Сразу после этого, а также через 2, 4, 24 и 48 ч пациенты были протестированы с использованием шкалы Эшворта и маятникового теста. Здоровые испытуемые оценивались только 3 раза. Удивительно, но снижение спастического тонуса имело тенденцию быть более выраженным контралатерально. Во-вторых, снижение началось уже через несколько часов и продолжалось около 20 ч (в контроле через 4 и 24 ч). В-третьих, двигательный порог для параспинальной магнитной стимуляции у пациентов был достоверно выше, чем в контроле.
Далее воздействие осуществляется на частоте 50 Гц, так как по данным литературного обзора австралийских авторов Stillman B. и Chase J. [34] на основании ограниченных исследований с экспериментальными животными более высокая частота (50 Гц) рекомендуется для стрессового недержания мочи, а также для облегчения боли [35–37].
3 сессия. Проводится с помощью магнитного индуктора, который прикладывают к промежности, при этом осуществляют магнитную стимуляцию до появления минимальных мышечных сокращений в месте приложения индуктора с частотой 1 Гц для достижения «обезболивающего эффекта» [38].
Отвечая на замечание респондента о том, что «выбор данной частоты не может быть основан на представленной работе, т.к. она касалась скелетных мышц, которые анатомически и физиологически не релевантны мышцам промежности, следует предоставить собственные доказательства эффективности», мы вынуждены констатировать тот факт, что работ по выбору частот и интенсивности ВИМТ для поперечно-полосатых мышц тазового дна, которые обладают тонической активностью, что является их основным отличием от скелетной мускулатуры, на сегодняшний день мы не нашли. В связи с этим мы рассчитываем на результаты как минимум собственных, как максимум мультицентровых исследований с данным протоколом лечения хронической нейрогенной тазовой боли, которые позволят подтвердить или изменить предложенные параметры.
Во втором протоколе проводят транслюмбосакральную магнитную стимуляцию, осуществляя воздействие, располагая магнитный индуктор на области поясницы по центру остистых отростков справа и слева, а затем на уровне крестца справа и слева (всего 4 точки). При этом воздействие осуществляют на каждую точку по 1 повторению протокола до появления минимальных мышечных сокращений анального сфинктера, воздействие осуществляют на каждую точку с частотой 1 Гц по методике Rao S., поскольку анальная невропатия, давление сжатия и ректальная емкость значительно улучшились только при частоте 1 Гц (p<0,05) по сравнению с исходным уровнем в опубликованном исследовании [39].
Также в исследовании Sato T. было проведено лечение 5 пациентов с пудендальной невралгией (n=4) и ишиасом (n=1) (ВАШ от 5 до 9 баллов) методом сакральной магнитной стимуляции – круглым койлом 90 мм Magstim на уровне S2–S3 от 30 до 50 импульсов выходной мощностью 75% от 1,5 Тесла с частотой менее 0,5 Гц, затухание нарастания 0,1 миллисекунды и длительность импульса 1 миллисекунда. При этом отмечена положительная динамика по шкале ВАШ с продолжительностью обезболивающего эффекта до 56 дней (контроль стимуляции осуществляли методом игольчатой ЭМГ анального сфинктера) [40].
Однако, для удобства клинического использования мы остановились на частотах 0,5–1 Гц.
В третьем протоколе пациента располагают сидя в кресле с фиксирующим шею подголовником. Наибольшая эффективность в лечении хронической боли показана для высокочастотной транскраниальной магнитной стимуляции (ТМС) первичной моторной коры головного мозга контрлатерально области боли [41]. В настоящее время для локализации мишени для стимуляции применяется 2 подхода: стимуляция зоны, соматотопически соответствующей локализации боли, или стимуляция зоны кисти вне зависимости от локализации боли. Исследования, где проводилось сопоставление двух описанных подходов, немногочисленны, значимых преимуществ стимуляции соматотопической зоны в них не показано, что, вероятно, обусловлено тем, что обезболивающий эффект ритмической ТМС (рТМС) опосредован процессами, модулирующими когнитивную и аффективную оценку боли, а не сенсорными феноменами, связаными со стимуляцией конкретной двигательной зоны. Учитывая отсутствие клинических преимуществ, а также методологическую сложность локализации двигательного представительства мышц тазовой области и необходимость использования для этого нейронавигационных систем ТМС, наиболее предпочтительным выглядит использование стимуляции зоны кисти в первичной моторной коре. Однако сопоставление эффективности двух подходов у данной когорты пациентов – релевантная задача, требующая проведения отдельных исследований. В большинстве исследований используется подпороговая интенсивность стимуляции (чаще 80% от моторного порога покоя), так как надпороговая стимуляция первичной моторной коры ассоциирована с ТМС-индуцированными мышечными сокращениями, что ухудшает переносимость процедуры. Кроме того, важным параметром является выбор частоты стимуляции, длительности трейна и межтрейнового интервала. В контексте терапии нейропатической боли наиболее часто используются 2 основных протокола стимуляции:
- частота стимуляции 5 Гц, длительность трейна – 10 с, межтрейновый интервал – 50 с, 500 стимулов за сессию;
- частота стимуляции 10 Гц, длительность трейна 10 с, межтрейновый интервал – 50 с, 1000/2000 стимулов за сессию. В работе Pinot-Monange A. et al. (2019), продемонстрировавшей эффективность рТМС первичной моторной коры (корковое представительство мышцы кисти) при хронической тазовой боли, использовалась частота стимуляции 10 Гц, длительность трейна – 10 с, межтрейновый интервал – 50 с, 1500 стимулов/сессий [42].
Данный протокол мы использовали для терапии нейропатической боли. Именно для лечения хронической нейрогенной тазовой боли как СХТБ, когда все органические причины болевого синдрома были исключены, мы пытались воздействовать на нейропатический компонент болевого синдрома.
Применение данного подхода основано прежде всего на данных, подтвердивших эффективность ритмической ТМС первичной моторной коры при болевых синдромах различного генеза [41, 43–47]. Перспективным подходом для дальнейших исследований является поиск альтернативных мишеней для стимуляции. В частности, в некоторых исследованиях в качестве мишени для стимуляции использовалась область М1, соответствующая представительству мышц тазового дна [48]. Однако локация данной области является сложной и не стандартной задачей [49–51]. Следует также отметить глубину залегания данного представительств, что может требовать применения специальных койлов, обеспечивающих более глубокое проникновение магнитного поля (например, H-койлов) [48]. Для модуляции активности мышц тазового дна перспективно также воздействие на дополнительную моторную кору (supplementary motor area, SMA) [52]. В проведенных исследованиях показано, что развитие СХТБ ассоциировано со структурными и функциональными изменениями различных других участков коры, что также крайне перспективно для проведения дальнейших исследований с уточнением оптимальной мишени для стимуляции [53–56].
Следует сказать, что, имея собственные клинические наработки по использованию представленного комплексного протокола, мы не располагаем опубликованными данными, что является безусловным минусом, но предоставляет шанс убедиться в его эффективности после проведения клинических исследований, и что немаловажно, мультицентровых. Мы абсолютно согласны с мнением эксперта, что «получается не совсем корректно – это просто коллективное мнение, что важно, но не совсем научно».
Аналогично, ответом на замечание респондента: «Если речь идет о высокоинтенсивной магнитной стимуляции (ВИМС), необходимо определить это понятие, т.е. какой диапазон интенсивности в % выхода магнитного стимулятора (мощность в Тс), либо выраженность в % от пороговых значений двигательных проявлений. Также определить, включает ли понятие ВИМС значения частот стимуляции. С учетом предложения использования ВИМС на разных уровнях (промежностный, транслюмбосакральный и транскраниальный) целесообразно представить более убедительную аргументацию включения в сеансы лечения всех трех протоколов. Использование разных уровней позволяет активировать дополнительные механизмы терапевтического воздействия или усилить эффективность в рамках единых механизмов или сочетать одно с другим? Было бы оправдано аргументировать предлагаемые режимы ВИМС в разных сессиях и протоколах путем предварительного краткого описания механизмов активирующего, релаксирующего, противоболевого действия ВИМС на разных частотах, разной интенсивности (подпороговая, пороговая, супрапороговая) и длительности воздействия. Хорошо бы обозначить основные направления терапевтического воздействия ВМС в заглавии каждой сессии и протокола (например, релаксирующее, тонизирующее регенерирующее, аналгезирующее и др.)», наверное, наиболее точным будет ответ, взятый из публикаций Stillman B. (2006) [33] и Evans B.A. (1991) [57].
По данным авторов, магнитные поля могут возбуждать как вегетативные, так и соматические нервы. В то время как нормальное мочеиспускание и дефекация, несомненно, зависят от комбинированного влияния соматических эфферентных, соматических афферентных и вегетативных эфферентных нервов, баланс воздействия на эти три категории нервов магнитной стимуляцией не был адекватно исследован и в настоящее время находится в основном в области предположений. Что касается воздействию рTMС для облегчения боли – объяснения пока тоже нет [58, 59]. Тем не менее, по аналогии с ЧЭНС [60], в основе механизма лежит теория воротного контроля облегчения боли. Эта теория предполагает, что стимуляция афферентных нервов большого диаметра (проприоцептивных) вызывает блокировку афферентной передачи боли через задние рога спинного мозга.
Следует признать, что четко и аргументированно описать механизмы воздействия, так же как и достигаемые эффекты, при определенных частотных характеристиках ВИМС на сегодняшний день мы не можем, а можем только предполагать патогенетические варианты воздействия – по отдельным разрозненным публикациям. Наверное, в этом и заключается сложность данной работы, которая однозначно требует клинического подтверждения.
Результаты
Все полученные ответы с замечаниями и рекомендациями были проанализированы и сгруппированы. В соответствии с частью поступивших предложений протокол экстракорпоральной сенсорной магнитной стимуляции был удлинен по времени. Также мы разделили во временном протяжении сенсорные и моторные воздействия, включив между ними паузу в 15 минут.
Следует обратить внимание на один немаловажный вопрос, который возникал у многих экспертов по поводу использования протоколов ВИМС при острой нейрогенной боли как профилактики хронизации процесса. По общему мнению экспертов, острая нейрогенная боль (как профилактика хронизации процесса) на сегодняшний день не может являться показанием к назначению данной схемы лечения.
Валидация новых протоколов ритмической магнитной стимуляции, основанных на опубликованных научных данных, на основании экспертной оценки
Приглашены к участию в опросе 55 человек, приняли участие – 55, что составило 100%. Просим обратить внимание, что опросник заполнили 55 респондентов, 1 респондент отказался быть в авторах статьи из-за отрицательного отношения к опроснику. Дополнительно по ходу работы над статьей еще 8 специалистов были привлечены в качестве экспертов-рецензентов. Ниже представлены результаты опроса по основным положениям, вынесенным на обсуждение.
Положение (вопрос 1): Приемлема ли, на Ваш взгляд, комплексная методика высокоинтенсивной импульсной магнитной стимуляции (МС), включающая экстракорпоральную (промежностную) МС, транслюмбосакральную нейромодулирующую терапию и транскраниальную МС?
55 ответов: консенсус уровня С1 (да – 94,54%, нет – 1,81%, другое – 3,63%) (рис. 2).

Относительно возникшего уточнения – вопроса отношения к лечению хронической тазовой боли 1 и 2 сессии 1-го протокола – следует отметить обязательную необходимость воздействия на мышцы тазового дна с целью ингибирующего воздействия на проведение (болевых) импульсов и снятия мышечного спазма пуборектальной мышцы – подтвержденных механизмов нейрогенной тазовой боли [61].
В соответствии с одним из полученных уточнений – метод ВИМС при воздействии на область малого таза подразумевает не только лечение ХНТБ, но и влияние на функции нижних мочевыводящих путей – есть большой опыт успешного лечения гиперактивного мочевого пузыря и других дисфункций. При наличии таких нарушений назначение ВИМС должно иметь место и оцениваться многофакторно. Предложенный респондентом протокол лечения: ежедневное воздействие высокоинтенсивного импульсного магнитного поля (ВИМП) сначала на сакральные отделы, затем на область мышц тазового дна и проекции шейки мочевого пузыря, при этом ВИМП с частотой следования импульсов 0,1–1,0 Гц, длительностью импульсов 100–600 мксек, межимпульсный интервал 50–100 мсек в первые 4 процедуры с начальной индукцией ВИМП от 0,5 Тл с последующим ее увеличением на 0,5 Тл при каждом новом воздействии до величины 1,5 Тл, а следующие 4 процедуры – с последующим ее уменьшением на 0,5 Тл при каждом очередном воздействии до величины 0,5 Тл, причем экспозиция воздействия ВИМП в первые 4 процедуры составляет 12 минут, а в последующие 4 процедуры – 20 минут (Шорников П.В., к.м.н., заведующий отделением функциональной диагностики № 2, ГБУЗ «НИИ – ККБ №1 им. профессора С.В. Очаповского» Минздрава Краснодарского края, «Способ лечения недержания мочи у мужчин после радикальной простатэктомии», патент № 2005112439/14(014364) от 25.04.2005 г.) – однозначно можно сказать, что мы будем использовать данный протокол для лечения пациентов с ХНТБ при сочетании урологических и проктологических нарушений и приносим свою благодарность за представленный экспертом протокол лечения.
Положение (вопрос 2): Удобна ли, на Ваш взгляд, данная методика по времени проведения – общая длительность протоколов 32:06 мин, два повторения с общей продолжительности процедуры 1:04:12 – один раз в день в течение 10 дней?
55 ответов: консенсус уровня С2 (да – 87,27%, нет – 7,27%, другое – 5,45%) (рис. 3).

Возражения связаны с большой, по мнению ряда респондентов, длительностью протоколов, утомительных для пациента. В соответствии с этим можно рекомендовать использование 1 повтора в протоколе. Также поступило предложение о целесообразности разработки протокола с меньшей длительностью воздействия, что является, по всей видимости, вопросом будущего.
Мы оставляем вопрос целесообразности проведения двух сеансов в день (в этом случае рекомендуется интервал не менее 4 ч между сеансами) с целью снизить нагрузку на пациента при проведении ВИМС, до проведения клинических испытаний исправленных протоколов, учитывая, что в этом случае будет получен оптимальный вариант использования в практике метода ВИМС.
Положение (вопрос 3): Считайте ли Вы целесообразным использование стандартизированных протоколов во всех аппаратах, зарегистрированных в России и предназначенных для лечения нейрогенной тазовой боли?
55 ответов: консенсус уровня С2 (да – 87,27%, нет – 5,45%, другое – 7,27%) (рис. 4).
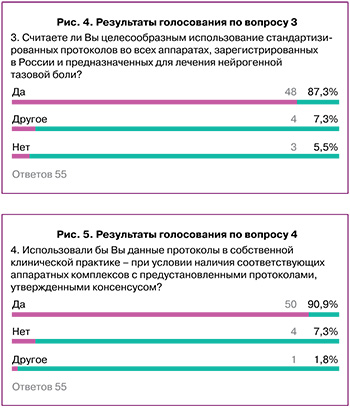
В соответствии с уточнениями респондентов – несомненно, регламентировать возможность использования исключительно предложенных протоколов будет возможно в том случае, если будет доказана их эффективность и безопасность у определенных групп пациентов, в том числе в результате проведения мультицентрового рандомизированного контролируемого клинического исследования. В отсутствие убедительных научных данных использование согласительного документа после его валидации может носить рекомендательный характер.
Положение (вопрос 4): Использовали ли бы Вы данные протоколы в собственной клинической практике – при условии наличия соответствующих аппаратных комплексов с предустановленными протоколами, утвержденными консенсусом?
55 ответов: консенсус уровня С1 (да – 90,90%, нет – 7,27%, другое – 1,81%) (рис. 5).
Основной проблемой, по мнению респондентов, является отсутствие аппаратной обеспеченности и технической оснащенности соответствующего уровня.
Также респондентами отмечено, что проблема центральной сенситизации как проявления нейропластичности (дезадаптивной пластичности), в значимом количестве случаев приводит к меньшему, чем ожидается, или вовсе к отсутствию эффекта декомпрессионной хирургии, и практически во всех случаях эта проблема приводит к долгой, а иногда безуспешной, реабилитации пациентов – поэтому представленная методика может оказаться полезной как на предоперационном, так и послеоперационном этапах.
Схема итогового протокола представлена в таблице. При заполнении предложенного Опросника по протоколам периферической ВИМС от экспертов изначально поступило предложение о возможности использования метода транскраниальной магнитной стимуляции в дополнение к проколам периферической магнитной стимуляции. Мы учли пожелания респондентов и дополнили протоколом рТМС, созданным на основании рекомендации Отчета IFCN (Международной Федерации Клинической Нейрофизиологии), а также рандомизированных контролируемых исследований и Evidence-Based Guidelines по терапевтическому использованию рТМС [41, 52, 62, 63].
Обсуждение
В ходе настоящей работы проведена оценка мнений респондентов относительно вариантов применения указанных методик ВИМТ для лечения хронической нейрогенной тазовой боли и достигнут междисциплинарный консенсус по использованию данного метода терапевтического воздействия в России. Интерес к неинвазивным методам лечения хронической тазовой боли в последнее время существенно возрос, что демонстрируется ростом количества публикаций по данному вопросу в мировой и отечественной литературе. В тоже время, отсутствие согласованного протокола применения метода ВИМТ существенно осложняет более широкое внедрение методики в клиническую практику, что уменьшает возможность включения метода в стандарты лечения больных, в том числе колопроктологического профиля. При отсутствии систематизированных данных применение новых методов лечения возможно на основе консенсусных решений, принятых на основании открытого обсуждения экспертами разных специальностей. Учитывая важность и распространенность проблемы хронической нейрогенной тазовой боли, применение инновационных неинвазивных методов может способствовать снижению дезадаптации и улучшению качества жизни большего числа больных, особенно в тех случаях, когда оперативное лечение не показано или невозможно в силу возрастных особенностей и/или сопутствующей коморбидной патологии. При проведении опроса была получена высокая согласованность мнений экспертов о целесообразности использования разработанного алгоритма лечения уже в ходе первого тура принятия решений – уровень согласия экспертов составил более 80% по всем вопросам, что позволило избежать повторного их вынесения на второй круг голосования. В то же время, высказанные предложения специалистов – видных представителей различных клинических и научных центров – позволили внести ряд улучшений в разрабатываемый терапевтический алгоритм. Поскольку данная публикация является одним из этапов общественного обсуждения, и проекту рекомендаций предстоит утверждение на мультидисциплинарном собрании, мы можем рекомендовать использование согласованного данным анкетированием протокола магнитной стимуляции для лечения нейрогенной тазовой боли, а его окончательный вариант будет приведен в методических рекомендациях.
Выводы
1. Согласованный в настоящей работе протокол ВИМТ для лечения больных с хронической нейрогенной тазовой болью одобрен мультидисциплинарным консенсусом специалистов.
2. Представленный консенсусный протокол нуждается в изучении и апробации в рамках контролируемого клинического исследования.



