Введение
Гиперкоагуляция достаточно часто наблюдается у пациентов с тяжелым COVID-19 и способствует повышению риска неблагоприятных исходов, таких как прогрессирующая дыхательная недостаточность, острый респираторный дистресс-синдром и смерть [1–8].
Наиболее распространенная картина коагулопатии, наблюдаемая у пациентов, госпитализированных с COVID-19, характеризуется повышением уровня фибриногена, D-димера, умеренным удлинением протромбинового времени (ПВ) и активированного частичного тромбопластинового времени (АЧТВ). Это коррелирует с сопутствующим повышением маркеров воспаления (например, C-реактивного белка). В отличие от картины классического ДВС-синдрома (диссеминированного внутрисосудистого свертывания синдром), наблюдаемого при бактериальном сепсисе или травме, степень повышения АЧТВ часто ниже, чем повышение ПВ (вероятно, из-за повышенного уровня фактора VIII), тромбоцитопения умеренная (уровень тромбоцитов около 100 тыс./мкл) и отсутствует микроангиопатия. Для обозначения данного состояния Американское сообщество гематологов (American Society of Hematology) предложило использовать термин «коагулопатия, ассоциированная с COVID-19» [4].
Повышенный уровень D-димера при поступлении и значительное (в 3–4 раза) повышение уровня D-димера за время госпитализации ассоциировано с высокой смертностью, что, вероятно, отражает активацию факторов свертывания в результате инфекции и/или сепсиса, цитокинового шторма и надвигающейся полиорганной недостаточности [4].
Для профилактики тромботических осложнений у пациентов с COVID-19 эмпирически применяются инъекции низкомолекулярных гепаринов (НМГ), а в их отсутствие – нефракционированного гепарина (НФГ) [3, 5, 9]. В клинической практике для этой цели все чаще по причине удобства применения назначаются прямые пероральные антикоагулянты (ПОАК). Данному явлению способствует включение некоторых ПОАК (ривароксабана и апиксабана) во временные методические рекомендации Минздрава и протоколы ведения пациентов с COVID-19, опубликованных рядом клиник и профессиональных сообществ [10, 11].
В настоящем документе анализируется научное обоснование применения ПОАК для профилактики тромботических осложнений у пациентов с COVID-19.
Анализ клинических руководств, протоколов ведения пациентов с COVID-19
В соответствии с Временными методическими рекомендациями (ВМР) Минздрава РФ по профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19), версия 9 (26.10.2020), всем госпитализированным пациентам рекомендуется назначение НМГ как минимум в профилактических дозах, а при недоступности НМГ или наличии противопоказаний к ним возможно применение НФГ [10].
Согласно ВМР, в амбулаторной практике может быть рекомендовано применение ПОАК: апиксабана по 2,5 мг 2 раза в сутки или ривароксабана 10 мг 1 раз в сутки. Данные препараты предлагаются для профилактики тромбоза глубоких вен (ТГВ) нижних конечностей и/или тромбоэмболии легочной артерии (ТЭЛА) проводить пациентам со среднетяжелой формой COVID-19, которые лечатся дома и имеют высокий риск венозных тромбоэмболических осложнений (ВТЭО), низкий риск кровотечений и не получают антикоагулянтного лечения по другим показаниям.
После выписки пациента с COVID-19 при сохраняющемся повышенном риске ВТЭО и низком риске кровотечений в случаях, когда не требуется лечебных доз антикоагулянта по другим показаниям, может быть рассмотрена продленная профилактика. В качестве антикоагулянтов для продленной профилактики ВТЭО, согласно ВМР, имеется доказательная база использования профилактических доз эноксапарина и ривароксабана в дозе 10 мг 1 раз в сутки.
Список возможных к назначению антикоагулянтов для профилактики тромбозов в стационаре в соответствии с ВМР ограничен парентеральными антикоагулянтами (НФГ, НМГ, фондапаринукс натрия).
Пациентам, получающим пероральные антикоагулянты по другим показаниям, при нетяжелых проявлениях COVID-19 их прием можно продолжить. При тяжелой форме COVID-19 или значимых взаимодействиях с другими лекарственными препаратами рекомендуется переход на лечебные дозы гепарина (предпочтительно НМГ).
В соответствии с рекомендациями Московского городского научного общества терапевтов по диагностике и интенсивной терапии ДВС-синдрома при вирусном поражении легких при лечении пациентов с легкой степенью заболевания применяется терапия профилактическими дозами прямых оральных антикоагулянтов с анти-Ха-активностью: апиксабан по 5 мг 2 раза в сутки или ривароксабан по 10 мг 2 раза в сутки, а также возможно применение и прямых антикоагулянтов с анти-IIа-активностью (дабигатран) в профилактических дозах (110 мг 2 раза в сутки) [12].
Согласно клиническим рекомендациям Национальных институтов здоровья США (National Institutes of Health), госпитализированным пациентам с COVID-19 следует назначать профилактическую терапию венозных тромбозов в соответствии со стандартной тактикой, предусмотренной для других госпитализированных пациентов [13]. Амбулаторным пациентам с COVID-19 не следует назначать антикоагулянтную или антиагрегантную терапию для профилактики венозных тромбозов. Для госпитализированных пациентов с COVID-19 профилактика венозных тромбозов проводится в отсутствие противопоказаний и в соответствии с рекомендациями по профилактике венозных тромбозов у пациентов, поступающих по другим показаниям.
В алгоритмах лечения пациентов с COVID-19, представленных Информационным центром COVID-19 медицинского факультета Вашингтонского университета [14], пациентам, находящимся в отделениях интенсивной терапии, рекомендуется проведение профилактики ВТЭО с применением НМГ или НФГ в стандартных профилактических дозах (с коррекцией дозы для пациентов с индексом массы тела [ИМТ]>40 или сниженной функцией почек) в отсутствие противопоказаний (уровень тромбоцитов ≤25 тыс/мкл или наличие кровотечения). Антикоагулянтную терапию ранее состоявшихся ТГВ или ТЭЛА, профилактику ишемического инсульта и системных эмболий при фибрилляции предсердий рекомендуется продолжать при уровне тромбоцитов ≥50 тыс./мкл и уровне фибриногена ≥100 г/дл.
Алгоритмы лечения пациентов с COVID-19 Yale New Haven Health System допускают профилактическое применение апиксабана или ривароксабана при уровне D-димера ≥5 мг/л или при применении реконвалесцентной плазмы [9]:
- режим дозирования апиксабана 5 мг 2 раза в сутки независимо от функции почек;
- ривароксабана (может быть более предпочтительным вариантом для пациентов с ИМТ ≥40 кг/м2) – 20 мг 1 раз в сутки (избегать применения ривароксабана при клиренсе креатинина менее 30 мл/мин).
Американская кардиологическая коллегия (American College of Cardiology) рекомендует проводить оценку риска ВТЭО и кровотечения всем выписывающимся пациентам, госпитализированным с COVID-19, для оценки целесообразности фармакологической профилактики ВТЭО в течение 45 дней после выписки [15]. Фармакологическую профилактику следует рассматривать при высоком риске ВТЭО и низком риске кровотечений. В отношении выбора антикоагулянта для такой пролонгированной профилактики ВТЭО после выписки у рабочей группы экспертов Американской кардиологической коллегии нет согласованного мнения: 51% рекомендуют профилактику с применением ПОАК, 24% рекомендуют применение НМГ (мнение остальных 25% экспертов в публикации не приводится).
В алгоритме антикоагулянтной терапии пациентов с COVID-19 Mount Sinai Hospital (США) [11] предлагается рассмотреть применение апиксабана 2,5–5 мг 2 раза в сутки или эноксапарина 40 мг подкожно 1 раз в сутки пациентам c COVID-19 средней и тяжелой степеней и с относительно невысоким риском, оцененным по комплексу клинических (частота дыхания), инструментальных (сатурация O2) и лабораторных показателей (уровень D-димера, C-реактивного белка).
В клиническом руководстве по ведению пациентов с COVID-19 Brigham and Women’s Hospital для профилактики ВТЭО в коечных отделениях и отделениях интенсивной терапии предлагается применение эноксапарина или НФГ с коррекцией стандартной дозы у пациентов с ожирением или дефицитом массы тела [16]. Следует отметить, что в качестве стандартного режима профилактики венозных тромбозов в отделениях интенсивной терапии пациентов с клиренсом креатинина ≥30 мл/мин предлагается применение эноксапарина 40 мг 2 раза в сутки. Пациентам, в отношении которых применяют ПОАК или варфарин при фибрилляции предсердий или ВТЭО, рекомендуется переход на полную дозу парентеральных антикоагулянтов (НМГ или НФГ в соответствии с функцией почек).
В Руководстве по лечению COVID-19 Massachusetts General Hospital с целью профилактики ВТЭО рекомендовано применение стандартных профилактических доз НМГ всем пациентам, за исключением беременных (≥20 недель беременности), которым следует назначать НФГ [17].
Назначение ПОАК также рекомендовано в руководстве клиники Мейо [18], позиции Итальянского общества по тромбозу и гемостазу (SISET) [19], руководстве по диагностике и интенсивной терапии ДВС-синдрома при вирусном поражении легких Московского городского научного общества терапевтов [20].
Анализ завершенных и запланированных клинических исследований
В настоящий момент на сайте clinicaltrials.gov зарегистрировано 11 клинических исследований с участием пациентов с COVID-19, в группы сравнения которых включены ПОАК: 1 исследование завершено, 9 в стадии набора участников, в 1 исследование набор пока не проводится [21].
Завершено исследование CORONA (NCT04518735) – ретроспективное обсервационное одноцентровое исследование сравнения выживаемости и тромбоэмболических осложнений у пациентов, постоянно принимающих антикоагулянты или антиагреганты, госпитализированных по причине развития COVID-19, по сравнению с пациентами, не принимающими антикоагулянты или антиагреганты. В исследование включены 1707 пациентов. На момент написания обзора результаты исследования CORONA не опубликованы.
Эффективность и безопасность применения ривароксабана оцениваются в 8 запланированных исследованиях. Изучаются следующие режимы дозирования ривароксабана для профилактики ВТЭО у пациентов с COVID-19 (в скобках указаны идентификаторы исследований):
- 2,5 мг 2 раза в сутки (NCT04333407);
- 2,5 мг 2 раза в сутки в течение 28 дней (NCT04324463);
- 5 мг 2 раза в сутки (NCT04351724);
- 10 мг 1 раз в сутки в течение 21 дня (NCT04504032);
- 10 мг 1 раз в сутки в течение 30 дней (NCT04508439);
- 10 мг 1 раз в сутки в течение 35 дней (NCT04508023);
- 20 мг 1 раз в сутки в течение 7 дней, затем 10 мг 1 раз в сутки в течение 28 дней (NCT04416048);
- 20 мг 1 раз в сутки, 15 мг 1 раз сутки для пациентов с клиренсом креатинина 30–29 мл/мин и(или) одновременный прием азитромицина (NCT04394377).
В двух запланированных исследованиях оценивается эффективность применения апиксабана для профилактики ВТЭО при COVID-19. Изучаются следующие режимы дозирования:
- 2,5 мг 2 раза в сутки или 5 мг 2 раза в сутки в течение 45 дней (NCT04498273);
- 5 мг 2 раза в сутки. Для пациентов с двумя из трех следующих признаков следует снизить разовую дозу до 2,5 мг: возраст 80 лет и старше, масса тела ≤60 кг, сывороточный креатинин ≥1,5 мг/дл (NCT04512079).
Исследований, в которых планируется изучение дабигатрана на пациентах с COVID-19, в реестре clinicaltrials.gov не найдено. Тем не менее стоит отметить, что дабигатран включался в комплекс терапии пациентов с COVID-19 в наблюдательных исследованиях – при выписке пациентов с неклапанной фибрилляцией предсердий (протокол ANIBAL) [22], анализе данных пациентов госпиталя г. Кремоны и небольшом исследовании о влиянии антикоагулянтов на смертность при COVID-19 [23, 24].
В крупном исследовании эффективности и безопасности применения ривароксабана для профилактики ВТЭО у госпитализированных нехирургических пациентов (n=8101) продемонстрирована неменьшая эффективность применения ривароксабана в дозе 10 мг 1 раз в сутки по сравнению с применением профилактических доз эноксапарина, относительный риск (ОР) для ривароксабана при этом составил 0,97 (доверительный интервал [ДИ]: 0,71–1,31), р=0,003 для неменьшей эффективности. Кроме того, показана бόльшая эффективность в группе ривароксабана при продленной профилактике – при оценке на 35-й день ОР для ривароксабана составил 0,77 (95% ДИ: 0,62–0,96; р=0,02) [25].
Двойное слепое плацебо-контролируемое исследование апиксабана для профилактики ВТЭО у госпитализированных нехирургических пациентов с хронической сердечной недостаточностью или дыхательной недостаточностью показало, что эффективность продленной профилактики апиксабаном в дозе 2,5 мг 2 раза в сутки не уступает эффективности более короткого курса эноксапарина 40 мг 1 раз в сутки в течение 6–14 дней (ОР для апиксабана=0,87, 95% ДИ: 0,62–1,23; р=0,44), однако ассоциировано с большим числом «больших» кровотечений по сравнению с эноксапарином при оценке на 30-й день терапии апиксабаном (ОР=2,58, 95% ДИ: 1,02–7,24; р=0,04) [26].
По данным шведского когортного исследования, проведенного по данным национальных регистров, в которое были включены 459 402 пациента (103 703 пациента принимали ПОАК по показанию «неклапанная фибрилляция предсердий»), постоянный прием ПОАК пациентами с неклапанной фибрилляцией предсердий не снижал риска госпитализации по поводу COVID-19 (скорректированное отношение моментных рисков – сОР=1,00, 95% ДИ: 0,75–1,33) при сравнении с группой пациентов с фибрилляцией предсердий, не получавших ПОАК (сОР=0,94, 95% ДИ: 0,80–1,10) при сравнении с группой пациентов с другими сердечно-сосудистыми заболеваниями, не получавшими ПОАК), переводов в отделения интенсивной терапии (сОР=0,76, 95% ДИ: 0,51–1,12) и смертности от COVID-19 (сОР=0,90, 95% ДИ: 0,71–1,15) [27].
Анализ других публикаций
Существующие ПОАК могут потенциально взаимодействовать с экспериментальной противовирусной терапией, назначаемой пациентам с COVID-19. Потенциальные взаимодействия ПОАК с ингибиторами гликопротеина P могут выражаться в повышении плазменных концентраций ПОАК, что клинически может выражаться в развитии кровотечений, в т.ч. жизнеугрожающих. По данным исследования S. Testa et al., наименьшая равновесная концентрация ПОАК у пациентов, госпитализированных по поводу COVID-19 и получавших экспериментальную противовирусную пневмонию, более чем в 6 раз превышала наименьшую равновесную концентрацию ПОАК до госпитализации [28].
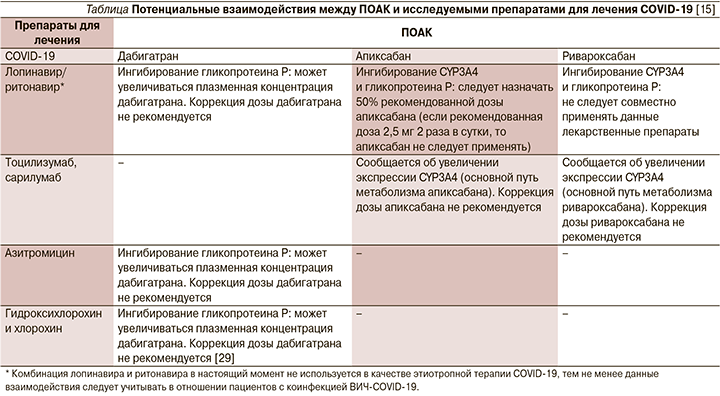
Важные потенциальные взаимодействия между ПОАК и препаратами, применяемыми в настоящее время для лечения COVID-19, приведены в таблице.
Заключение
1. Пациентам с COVID-19, получающим лечение амбулаторно и не нуждающимся в назначении антикоагулянтов по другим показаниям, следует оценивать риск ВТЭО и риск кровотечений. При высоком риске тромбоэмболических осложнений и низком риске кровотечений могут быть рассмотрены к назначению подкожные инъекции НМГ и НФГ в профилактических дозах, а также ривароксабан 10 мг 1 раз в сутки и апиксабан 2,5 мг 2 раза в сутки внутрь (в соответствии с ВМР версии 9 от 26.10.2020).
2. Госпитализированным пациентам с COVID-19, не нуждающимся в приеме пероральных антикоагулянтов по другим показаниям, например при фибрилляции предсердий, недавнем ТГВ, ТЭЛА, целесообразно рассмотреть назначение низкомолекулярных гепаринов (НМГ) как минимум в профилактических дозах. В качестве альтернативы профилактическому применению НМГ госпитализированными пациентами с COVID-19 может быть рассмотрено применение ПОАК в профилактических дозах (ривароксабан 10 мг 1 раз в сутки или апиксабан 2,5 мг 2 раза в сутки). При выборе антитромботической терапии следует учитывать потенциальные межлекарственные взаимодействия между назначенными пациенту лекарственными препаратами и ПОАК.
3. Госпитализированным пациентам с COVID-19, принимающим ПОАК по показаниям, зарегистрированным в инструкции по медицинскому применению, следует оценивать наличие потенциальных взаимодействий с применяемыми во время госпитализации лекарственными препаратами и при наличии значимых взаимодействий целесообразно рассматривать возможность временного перехода с ПОАК на парентеральные антикоагулянты, например НМГ. По завершении применения препаратов, значимо изменяющих фармакокинетику ПОАК, целесообразно возобновить прием ПОАК.
4. При переводе на амбулаторный режим пациентов, не нуждающихся в постоянном приеме антикоагулянтов, следует оценить риск венозных тромбозов и кровотечений. При высоком риске венозных тромбозов и низком риске кровотечений целесообразно рассмотреть возможность пролонгированной (до 45 дней) фармакологической профилактики ВТЭО лекарственным препаратом, применявшимся во время госпитализации. Может быть рассмотрен прием ривароксабана 10 мг 1 раз в сутки или апиксабан по 2,5 мг 2 раза в сутки (в соответствии с результатами исследований продленной профилактики ВТЭО у нехирургических пациентов).
Дополнительная информация
Представленные рекомендации служат для поддержки клинических решений, принимаемых лечащим врачом, и не исключают клинического мышления врача, самостоятельный поиск последней научной информации, сверку с действующими инструкциями по медицинскому применению лекарственных препаратов. Представленная информация основана на результатах научного поиска, проведенного 02.12.2020 экспертами Центра «ФармаCOVID» на базе РМАНПО Минздрава России, Москва.



