Введение
Тетеринг-синдром (синдром натяжения терминальной нити) объединяет группу неоднородных по происхождению, но схожих по патогенезу заболеваний, для которых специфична совокупность выпадения функций каудальных отделов спинного мозга и корешков конского хвоста (ККХ), а клинически проявляется неврологическим дефицитом различной степени интенсивности [1–7].
Тетеринг-синдром может быть как врожденным, так и приобретенным [1–3, 7]. Врожденная форма тетеринг-синдрома всегда развивается вследствие диспропорции остеоневрального развития спинного мозга и позвоночного столба, протекает с грубым неврологическим дефицитом (мозаичным сочетанием двигательных, чувствительных, трофических и тазовых нарушений, костно-суставными деформациями нижних конечностей и различными дисфункциями внутренних органов). К патогенетическим элементам врожденного тетеринг-синдрома относятся ишемия (гипоксия) конуса спинного мозга и ККХ (радикулоишемия), развивающаяся вследствие тракции нервно-сосудистых образований поясничного отдела позвоночного канала [1–7].
Этиология, патогенез, патоморфология, клиника и лечение приобретенной формы тетеринг-синдрома еще не изучены [8–20]. Изучение приобретенной формы тетеринг-синдрома, развивающейся при различных заболеваниях поясничного отдела позвоночника и спинного мозга, остается актуальной проблемой научной медицины.
Исходя из того, что подобные патоморфологические субстраты, вызывающие тракцию ККХ и сосудистых образований позвоночного канала в терминальной цистерне спинного мозга, часто встречаются и у больных поясничным остеохондрозом (ПО), мы решили изучить патоморфологические субстраты ПО, приводящие к развитию тетеринг-синдрома. Так как определение патоморфологических субстратов ПО, приводящих к развитию тракции нервно-сосудистых образований терминальной цистерны спинного мозга и экстрадуральних отрезков нервных корешков, позволяет своевременно диагностировать и выбирать адекватный способ лечения приобретенного тетеринг-синдрома.
Цель исследования: изучение патоморфологических субстратов ПО, приводящих к развитию тетеринг-синдрома.
Методы
Проведено исследование 112 (71 мужчина, 61 женщина) пациентов, прооперированных в нейрохирургическом отделении Самаркандского ГМО по поводу ПО с тетеринг-синдромом. Средняя длительность заболевания – 7,6±2,1 года, вариация от 3 до 12 лет. Средний возраст пациентов составил 42,0±5,4 года (вариация от 30 до 50 лет). Все пациенты получали длительное и безуспешное консервативное лечение.
Критериями включения в исследование послужили:
- Наличие эпи- и субарахноидального фиброза по данным магнитно-резонансной томографии (МРТ).
- Наличие односторонней люмбоишиалгии (высокой интенсивности).
- Неэффективность или кратковременность эффекта от проведенного активного консервативного лечения.
- Установленный диагноз: ПО с тетеринг-синдромом.
Критерии исключения:
- Травмы позвоночника в анамнезе.
- Ранее проведенные операции на позвоночнике.
- Наличие тяжелых соматических заболеваний.
Пациенты были сходными по возрасту, длительности заболевания и выраженности симптоматики.
Вертебро-неврологическая диагностика проведена по критериям H. Hall [21], которая включала тщательное клинико-неврологическое исследование, функционально-спондилографическую, компьютерную томографию (КТ) и МРТ-исследования поясничного отдела позвоночника. При помощи функциональной спондилографии определена патологическая подвижность или наличие функционального блока в пораженном позвоночно-двигательном сегменте (ПДС). При помощи мультиспиральной рентгеновской компьютерной томографии (МСКТ) определены твердотканные патоморфологические элементы ПО.
Исходя из того, что сагиттальные и фасные срезы Т2-режима МРТ являются базовыми в изучении морфологии тетеринг-синдрома [1–7], тщательно изучены данные МРТ-исследования поясничного отдела позвоночника всех больных. На МРТ поясничного отдела позвоночника кроме общих признаков ПО имели также место характерные (патогномичные) МРТ-признаки тетеринг-синдрома: отсутствие радикулографического эффекта на фасных срезах Т2-режима – фиброз и гиперденсивная тень (обусловленная арахноидальной кистой) на сагиттальных срезах Т2-режима [1–7].
Поскольку фиброз и арахноидальная киста в терминальной цистерне спинного мозга, определенные на фасных и сагиттальных срезах Т2-режима МРТ, служат основными патогномическими симптомами тетеринг-синдрома у больных ПО, для ликвидации тетеринг-синдрома мы выбрали операцию «ламинэктомия с проведением менингорадикулолиза».
Для определения эффективности проведенного хирургического способа лечения тетеринг-синдрома у пациентов использовано две шкалы:
1. Для определения интенсивности корешкового болевого синдрома использована специально разработанная шкала самооценки состояния при боли в спине, применяющая принцип визуальной аналоговой шкалы (ВАШ), она предусматривала оценку спонтанной боли в спине, спонтанные боли в ногах, ограничение подвижности при наклоне вперед, ограничение способности сидеть, передвижения, повседневной активности.
Больной должен оценить выраженность каждого из этих симптомов, отметив ее точкой на отрезке 100 мм, при этом 0 на этом отрезке соответствовал отсутствию симптома, противоположенный конец – максимально возможной выраженности симптома. Общая оценка в этой шкале определялась суммированием длины 10 отрезков (в мм) и могла колебаться от 0 до 100 [21].
2. Шкала – общая оценка результатов лечения врачом предусматривала 5 градаций: -1 балл – ухудшение,
0 баллов – отсутствие эффекта; 1 балл – незначительно выраженный эффект, 2 балла – умеренный эффект, 3 балла – значительный эффект [9].
Оценка эффективности проведенного лечения осуществлялась посредством оценки неврологических симптомов до и после проведения хирургического лечения и через год после его проведения.
Данные собирались в специально разработанную форму. Статическая обработка проводилась с использованием дескриптивных методов и модели ANOVA. Оценка изменения показателей осуществлялась по сравнению с исходным уровнем, а также сравнение показателей проводились с помощью t-теста.
Результаты
Результаты клинико-неврологического исследования до проведения хирургического лечения показали, что у всех пациентов имел место люмбоишалгический болевой синдром высокой интенсивности, сопровождавшийся выраженными симптомами натяжения нервных корешков. Грубых неврологических изменений в виде трофических расстройств и деформаций нижних конечностей ни у кого не отмечалось. Изучение клинико-неврологических параллелей показало, что среди клинических симптомов ПО, характерных (патогномичных) только для тетеринг-синдрома, не было.
Результаты функциональной спондилографии поясничного отдела позвоночника показали, что у 23 (20,5%) пациентов присутствовала подвижность ПДС до 4 мм (норма). Патологической подвижности более 4 мм ни у кого не было. На МСКТ у всех пациентов выявлены уменьшение высоты межпозвонкового диска (МПД), субхондральный склероз, внутридисковое перемещение пульпозного ядра, явления артроза дуго-отростчатых суставов с обеих сторон и гипертрофия желтой связки. У 6 (5%) пациентов отмечались грыжи L4–5 дисков (у 4 пациентов парамедианная, у 2 латеральная), у 5 (4%) пациентов – грыжи L5–S1 диска центральной локализации.
На МР-томограммах кроме общих признаков ПО также отмечались характерные морфологические изменения, вызывающие фиксацию ККХ между собой и к твердой мозговой оболочке, т.е. отмечались патогномичные морфологические изменения в виде фиброза в терминальной цистерне спинного мозга. Отсутствие «радикулографического эффекта» на фасных срезах Т2-режима МРТ, указывающих на наличие фиброзирующих спаек между ККХ, между ККХ и твердой мозговой оболочкой, присутствовало у всех пациентов. Гиперденсивные участки серповидной формы – арахноидальная киста в терминальной цистерне, определялась в сагиттальном срезе Т2-режима МРТ у 49 (44%) пациентов (рис. 1). У этих пациентов на фасных срезах Т2-режима МРТ кроме фиброзирующей арахноидальной кисты также определялся фиброз в терминальной цистерне спинного мозга – отсутствие «радикулографического эффекта» (рис. 2).
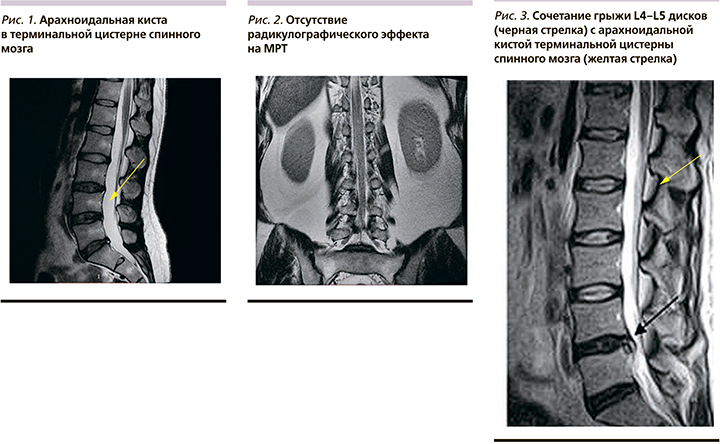
У 5 (4%) пациентов вместе с грыжей МПД на сагиттальных срезах Т2--режима МРТ также отмечалась арахноидальная киста, а явление фиброза в терминальной цистерне спинного мозга сочеталось с грыжей МПД у 11 (10%) пациентов (рис. 3).
Интенсивность болевого синдрома после проведения менингорадикулолиза, т.е. после ликвидации тетеринг-синдрома (натяжения корешков конского хвоста), у всех пациентов уменьшилась (показатели ВАШ) в среднем на 93,6%. Симптомы натяжения нервных корешков регрессировали на следующий день после проведения менингорадикулолиза, остаточный болевой синдром до 7% регрессировал в течение недели.
Общая оценка результатов хирургического лечения врачом показала, что значительный эффект (3 балла) отмечался у 92 (82%) пациентов, умеренный (2 балла) у 20 (18%). Незначительный эффект (1 балл), его отсутствие (0 баллов) и ухудшение (-1 балл) ни у кого отмечено не было.
Обсуждение
Установлено, что в условиях продолжающейся депрессии внутриклеточного энергосинтеза (синтеза АТФ) всегда отмечается активация выброса высокореактивных свободных радикалов и интермедиатров кислорода, в результате чего начинается массивная атака макромолекул МПД (аггреканов) завышенной концентрацией высокореактивных свободных радикалов – окислительный стресс. Усиление окислительного стресса в пораженном МПД приводит к прогрессированию главного патогенетического элемента ПО – катаболического (разрушительного) метаболизма с расщеплением аггреканов на протеин и мукополисахариды.
В результате увеличения концентрации протеина в МПД усиливается аутоиммунный реактивный воспалительный процесс. Вследствие продолжающегося катаболического метаболизма асептический воспалительный процесс распространяется в эпидуральное пространство и на структуры терминальной цистерны спинного мозга с последующим развитием спаечного (фиброзного) процесса, в эпидуральном пространстве – между ККХ, между ККХ и сосудистыми образованиями, между нервно-сосудистыми образованиями терминальной цистерны спинного мозга и твердой мозговой оболочкой – тетеринг-синдром.
Кроме того, в результате распространения реактивного (асептического) воспалительного процесса в эпидуральное пространство и на перинеальную жировую клетчатку развивается демиелинизация аксонов нервных корешков, что приводит к развитию гипералгезии спинномозговых нервов. Сдавление, или тракция, гипералгезированного ККХ или эпиневрального отрезка спинномозговых нервов приводит к развитию корешкового болевого синдрома.
Значит, тракция гипералгезированного (демиелинизированного) нервного корешка вследствие диско-радикулярного, радикуло-радикулярного, радикуло-васкулярного и дурорадикулярного конфликтов является основным механизмом развития радикулоишемии.
Кроме того, набухание МПД вследствие увеличения концентрации мукополисахаридов приводит к повышению внутридискового давления с усилением болевого синдрома.
Уменьшение или отсутствие радикулографического эффекта на фасных срезах Т2, серповидная гиперденсивная тень на сагиттальном срезе Т2-режима МРТ (у 44% пациентов) и хороший эффект от менингорадикулолиза служат подтверждением правильности вышеизложенного механизма развития прибретенного тетерингсиндрома.
Заключение
На основании вышеизложенных и литературных данных можно сделать следующие выводы:
- Патофизиологическим механизмом развития приобретенного тетеринг- синдрома у пациентов ПО является радикулоишемия, развивающаяся вследствие тракции нервно-сосудистых образований терминальной цистерны спинного мозга.
- Основным патоморфологическим элементом ПО, вызывающим тракцию нервно-сосудистых образований терминальной цистерны, является фиброз в каудальной цистерне.



