Введение
Одной из нейроэндокринных систем, представляющих особый интерес в изучении стресса, является гипоталамо-гипофизарно-адренокортикальная система с секрецией кортизола. Данный интерес обусловлен тем, что «телесные эффекты» гормонов гипоталамо-гипофизарно-адренокортикальной системы служат связующим звеном между психосоциальной средой и различными последствиями для здоровья [1, 2].
Стрессовые реакции – безусловно, важный защитный механизм. Но проблемой современной жизни стал постоянный высокий уровень стресса с недостатком отдыха и восстановления [3, 4]. В связи с этим наблюдается ежегодный рост числа пациентов с постстрессовыми компенсаторными функциональными нарушениями нейроэндокринной системы, обусловленными хроническим психоэмоциональным перенапряжением и стрессом [5, 7]. Такие пациенты характеризуются широким разнообразием клинических проявлений, выходящих за рамки одной медицинской специальности. Это влечет за собой неэффективность или значительное снижение эффективности диагностических и лечебных мероприятий, что обусловлено ведением данной группы пациентов несколькими специалистами без общего плана обследования и лечения, а также полипрагмазией [8, 9].
Одним из путей решения этой проблемы является использование междисциплинарного подхода. Данные современной литературы свидетельствуют о том, что особенно важно использование междисциплинарного подхода к пациентам эндокринологического, неврологического и гинекологического профиля [10, 11].
В настоящее время уже опубликована масса исследований, подтверждающих значительный вклад междисциплинарного подхода к оптимизации ведения пациентов с сочетанной патологией, которая обеспечивается согласованным подходом к диагностике и возможностью выбора наилучшей тактики лечения пациента [12, 13].
Клинический пример
Пациентка А. в возрасте 36 лет, 1984 г.р. обратилась к неврологу с жалобами на нарушение сна, которое проявлялось позднем засыпанием и частым пробуждением, на частые ночные позывы к мочеиспусканию (до 5 раз за ночь), на тяжелый подъем и головные боли по утрам, на отсутствие аппетита утром, пациентка выпивала только чашку кофе в первой половине дня. Крепкий сон у пациентки наблюдался только с 7 до 9 утра, если в это время было нужно вставать, то днем был полный упадок сил. Головные боли распирающего характера чаще в утренние часы наблюдались после пробуждения до 4–5 раз в неделю. Судороги ног отмечались ночью и при вождении автомобиля. Пациентка отмечает, что раньше очень любила водить автомобиль, теперь это вызывает сильную усталость. Также наблюдались жалобы на отеки переорбитальной области в первой половине дня, периодические отеки ног, тремор рук. В течение всего дня пациентка отмечала выраженную слабость, постоянное чувство волнения и раздражения. Со слов пациентки: «Любое предстоящее дело вызывало волнение, которое выливалось в паническую атаку». Три месяца назад появились боли в крупных суставах, в пояснице, боли по всему телу, «рези в желудке». За последние 2–3 года частые простудные заболевания. Также пациентка предъявляет жалобы на скудные менструации, масталгию в период лютеиновой фазы, снижение либидо, сухость влагалища и боли при мочеиспускании. Эмоциональная нестабильность усиливалась во вторую фазу менструального цикла. У пациентки наблюдалась тяга к соленой пище, низкое артериальное давление – до 80/50 мм рт.ст.
Анамнез жизни: пациентка замужем, имеет двух детей – 14 и 16 лет. Роды в срок, осложнений течения беременности не было выявлено. Хронических заболеваний нет. Профессиональная деятельность – предприниматель. Пациентка отмечает выраженные психоэмоциональные нагрузки на работе в течение последних 6–7 лет, по роду деятельности частые трансконтинентальные перелеты по 10 и более часов.
Семейный анамнез: ничем не отягощен.
Гинекологический анамнез: к настоящему времени пациентка 13 лет получает оральные контрацептивы. При этом в течение 12 лет к гинекологу не обращалась ввиду занятости на работе.
Анамнез заболевания: вышеперечисленные жалобы появлялись постепенно в течение последних 3 лет. Со слов пациентки, 6 месяцев назад женщина поняла, что нуждается в медицинской коррекции, и начала поиск причин ухудшения здоровья. Она обращалась к врачам разных специальностей (неврологам, гинекологам, гастроэнтерологам, мануальным терапевтам, психиатрам и психотерапевтам). Врачами в рамках своей врачебной специальности было назначено лечение, исходя из соответствия жалоб их профилю, что не привело к результату. Пациентке были рекомендованы психотропные препараты, назначение которых приводило к усугублению слабости и другой симптоматики. Также пациентке было проведено стационарное обследование в стационаре общего профиля в одной из стран Европы, где была проведена позитронно-эмиссионная томография, совмещенная с компьютерной томографией (ПЭТ/КТ), – эффективный метод ранней доклинической диагностики онкологических заболеваний, со стороны внутренних органов изменений не было выявлено. Также были исключены заболевания щитовидной железы и аутоиммунные заболевания.
Первое посещение: на приеме у невролога при тщательном осмотре, сопоставлении с жалобами и анамнезом выявлены признаки дефицита гормонов. Безусловно, данные признаки не являются абсолютно специфическими, но в совокупности позволяют осуществить правильный диагностический поиск. Очаговой неврологической симптоматики не выявлено, выраженная вегетативная симптоматика, дистальный гипергидроз, общая гипеалгезия. Синдромы, выставленные на первом приеме: диссомнический синдром; астенический синдром; вегетативная дисфункция, симпатоадреналовые кризы; нарушение водно-электролитного обмена; умеренный болевой суставной синдром.
С учетом достаточно продолжительного периода диагностического поиска в рамках одной врачебной специальности был создан консилиум, в котором учувствовали невролог, эндокринолог и гинеколог.
Лечение по результатам первого консилиума: поскольку пациентка не имела полноценного сна длительное время, что повлекло за собой другую симптоматику, а также отсутствие психиатрической патологии, препаратом выбора на первом приеме стал содержащий в качестве активного вещества полипептиды из головного мозга эмбрионов свиней Целлекс. По схеме: инъекции подкожно 0,1 мг/мл в 13.00 и в 21.00 в течение 5 дней. Препарат Целлекс относится к классу веществ средней продолжительности действия и средним временем удерживания в организме (MRT) – 18.30. Кинетические кривые носят моноэкспоненциальный характер. Кинетика распределения в органах гетерогенна и не зависит от степени васкуляризации ткани. Отношения значений AUC0-t к параметру AUC0-∞ для органов и ткани составляют более 99% (свидетельствует о полноте описания фармакокинетических процессов Целлекса в исследуемых органах и тканях). Период полуэлиминации t1/2el – 32 часа. Препарат содержит более 1200 сигнальных белков и регуляторных пептидов, включая факторы роста и дифференцировки нервных клеток и сосудов, обладает нейропротективным и репаративно-регенеративным действием на нервную ткань.
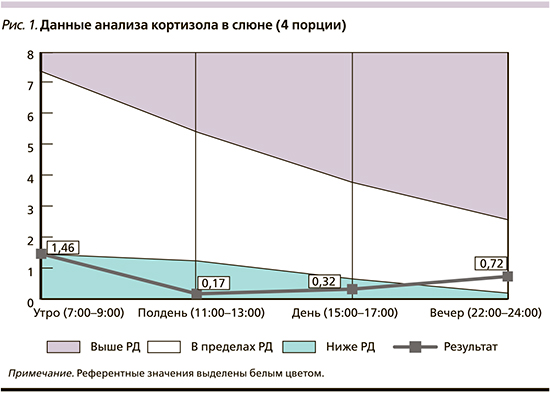
Обследование по результатам первого консилиума: спектр диагностического поиска был назначен коллегиально на основании решения консилиума невролога, эндокринолога и гинеколога. В него вошли анализ уровня кортизола в слюне (рис. 1), кортизола в плазме крови и суточной моче, исследования гормонального статуса и другие лабораторные анализы (см. таблицу, результаты от 14.08.2020).
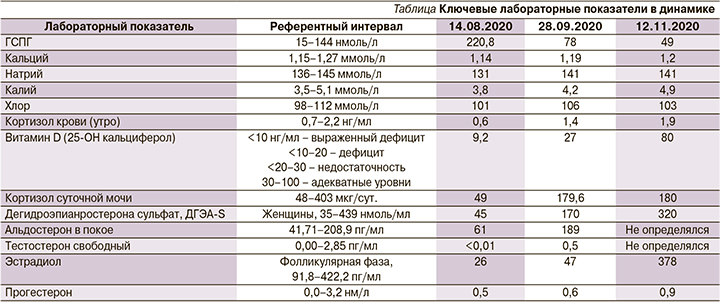
Второе посещение: уже на втором посещении через 5 дней от начала лечения препаратом Целлекс пациентка отмечала, что на фоне проводимой терапии в значительной степени улучшился сон («наконец выспалась»), при этом никтурия сократилась до 2 раз за ночь, полиурия в дневное время купировалась, судороги купировались, симпатоадреналовые кризы появлялись значительно реже. При осмотре выявлено уменьшение вегетативной симптоматики. Интерпретация лабораторных анализов и назначение дальнейшего лечения при втором посещении пациентки проводились также на основании консилиума (невролог, эндокринолог и гинеколог). Из полученных данных анализа уровня кортизола в слюне сделан вывод о снижении концентрации этого гормона в дневное время ниже референтных значений. Результаты лабораторного анализа свидетельствовали о снижение ниже референтных значений уровней эстрадиола и прогестерона, а также кальция, натрия, кортизола крови (утро), витамина D (25-ОН кальциферол). Уровень калия плазмы крови и кортизола (суточная моча) был практически на нижней границе референтного интервала. Уровень глобулин-связывающего полового гормона (ГСПГ) значительно превышал верхнюю рефрентную границу. Результаты ключевых лабораторных показателей представлены в таблице в динамике на разных этапах лечения пациентки.
На основе полученных лабораторных данных у пациентки выявлены синдром недостаточности надпочечников, высокий уровень ГСПГ, что автоматические повлекло гипогонадотропное состояние и нарушения вегетативного и эмоционального плана.
На основании результатов проведенных исследований решением консилиума пациентке назначена следующая схема лечения:
- соблюдение режима сон–бодрствование;
- соблюдение гигиены труда и отдыха, исключение длительных авиационных перелетов на период лечения;
- ноотропный препарат, содержащий в качестве активного вещества полипептиды из головного мозга эмбрионов свиней Целлекс, по схеме: инъекция подкожно 0,1 мг/мл 2 раза в неделю в течение 60 дней;
- поливитаминно-минеральные комплексные препараты на 60 дней;
- витамин D3 в дозе 5000 МЕ до достижения оптимального лабораторного показателя;
- гинеколог отменил оральные контрацептивы (учтя клиническую ситуацию и повышение уровня ГСПС) и назначил препарат комплексного действия – гидролизат человеческой плаценты Лаеннек, содержащий в основе помимо ингредиентов, улучшающих состояние печени, полипептид дегидроэпианростерон для поддержания функции надпочечников и стероидогенеза), 2 мл внутримышечно 3 раза в неделю 60 дней.
Спустя 2 месяца пациентка вернулась к работе, лабораторные анализы с референтными интервалами от 12.11.2020 представлены в таблице.
Обсуждение
Представленный клинический случай относится к категории «трудных диагнозов», поскольку его решение находится в междисциплинарном поле (ведущие неврологические жалобы являются проявлением гормонального дисбаланса и не могут быть решены в рамках классической неврологической помощи). Для решения данной проблемы в результате проведенного консилиума в составе врачей невролога, эндокринолога и гинеколога нами был разработан следующий алгоритм диагностического поиска в рамках междисциплинарного подхода (рис. 2).
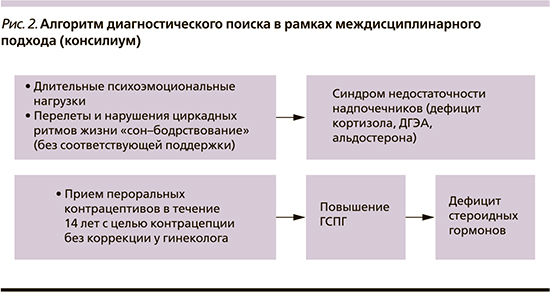
У обследуемой пациентки были выделены ведущие синдромы, беспокоившие пациентку, – это диссомнический синдром и астенический синдром, вегетативная дисфункция. Данные синдромы были причиной, по которой пациентка не могла далее вести активную жизнь и интенсивно работать. То есть в этом случае мы наблюдаем функциональную мультисистемную патологию, которая приобретает медико-социальную значимость. Стойкий астенический синдром был обусловлен хронической надпочечниковой недостаточностью (усталостью надпочечников), что подтверждено результатами лабораторных исследований. Научно доказано, что длительный диссомнический синдром приводит к дисбалансу гормонов надпочечников, и наоборот, в данном случае к дефициту кортизола и альдостерона [14, 15].
Препаратом выбора для начала коррекции диссомнического синдрома в сочетании с психоэмоциональными нарушениями в этом клиническом случае стал ноотропный препарат Целлекс, содержащий в качестве активного вещества полипептиды из головного мозга эмбрионов свиней. Целлекс представляет собой тканеспецифический высокомолекулярный белково-полипептидный комплекс с массой протеинов от 10 до 250 кДа, полученный из эмбриональной мозговой ткани, обусловливающий нейропротективное действие за счет активации аминобутиратного шунта (уменьшающего повреждающее действие чрезмерного выделения возбуждающих нейротрансмиттеров и увеличивающего синтез ГАМК); активации синтеза ферментов антиоксидантной защиты; торможения цитотоксической активности макрофагов; генерации антиапоптотичиеских сигналов, и нейрорепаративное действие за счет активации ангиогенеза, нейрогенеза (пролиферации нейробластов, хоуминга нейробластов к очагу поражения, активации процессов спраутинга и арборизации, синаптогенеза), а также торможения пролиферации соединительной ткани. Этот оригинальный препарат обладает выраженным первичным, а также вторичным нейропротективным действиями на нейроны головного мозга. К преимуществам данного препарата можно отнести возможность подкожного введения, быстрый эффекте по восстановлению сна у молодых и уменьшение вегетативного дисбаланса. Его использование обеспечивает снижение сроков восстановления и реабилитации пациентов с функциональным нарушением центральной и периферической нервной системы, стрессового генеза и восстановлением центральной нейроэндокринной регуляции. Представленные в современной литературе результаты исследований подтверждают эффективность использования Целлекса пациентами с неврологической патологией [16–19]. Но стоит отметить, что ввиду отсутствия широкой доказательной базы нет точных данных, согласно которым этот препарат будет эффективным во всех случаях, однако его безопасность и быстрое наступление клинического эффекта позволяют быстро менять тактику врача в случае неэффективности. С учетом молодого возраста пациентки, элиминации стрессогенных факторов, восстановления сна и правильно подобранного симптоматического лечения наблюдалось достаточно быстрое улучшение здоровья пациентки. То есть приведенный клинический пример описывает применение Целлекса с положительным клиническим эффектом.
Кроме того, у пациентки мы наблюдали повышение уровня ГСПГ, приведшее к дефициту половых стероидов. Таким образом, молодая женщина была в состоянии, по клинической картине похожем на менопаузу с психоэмоциональными, вегетативными проявлениями. Как известно, ГСПГ – это производимый печенью белок, который соединяется с тестостероном и эстрадиолом, затем транспортирует гормоны в плазме крови в метаболически неактивной форме [20]. Уровень ГСПГ у взрослых достаточно стабилен. Концентрация ГСПГ может изменяться при заболевании печени и по другим причинам. Препаратом выбора для коррекции гормональной дисфункции (улучшения эндогенного синтеза половых стероидов) стал полипептидный препарат человеческой плаценты (Лаеннек). Биологически активные вещества, содержащиеся в гидролизате, стимулируют регенерацию (пролиферацию) гепатоцитов, проявляют дезинтоксикационные свойства и повышают активность тканевого дыхания, а также нейроэндокринную регуляцию за счет пептида дегидроэпиандростерона, входящего в его состав [21–24]. Важно отметить, что полипептидные препараты оказывают более быстрый эффект при условии возмещения нутритивных дефицитов, в частности 25-ОН – кальциферола.
Заключение
Лечение молодых пациентов с постстрессовыми компенсаторными функциональными нарушениями нейроэндокринной системы требует от врача высокой квалификации или коллегиального взаимодействия врачей разных специальностей (междисциплинарный подход). Представленный клинический случай подтверждает эффективность полипептидных препаратов для пациентов молодого возраста при наличии функциональной мультисиндромной патологии.



