Введение
Микробиота влагалища и ее роль
Влагалище представляет собой динамичную микробиологическую экосистему, в которой ведущую роль играют микроорганизмы рода Lactobacillus. Поддержание сбалансированного вагинального микробиома имеет ключевое значение для защиты от патогенных микроорганизмов, регуляции местного иммунитета и профилактики воспалительных заболеваний. У здоровых женщин репродуктивного возраста микрофлора влагалища в основном представлена лактобациллами, которые составляют до 90–95% всех микроорганизмов. Эти бактерии поддерживают кислую среду (pH 3,5–4,5) за счет продукции молочной кислоты, перекиси водорода и бактериоцинов, тем самым создавая неблагоприятные условия для роста анаэробной и факультативно-патогенной флоры [1, 2].
Роль Lactobacillus spp.
Наиболее значимыми представителями здорового вагинального микробиома считаются Lactobacillus crispatus, Lactobacillus jensenii и Lactobacillus gasseri, поскольку они обладают высокой способностью к адгезии к эпителию и выраженной антагонистической активностью в отношении патогенов [2]. В частности, L. crispatus считается наиболее стабильным и «защитным» видом, ассоциированным с низким риском бактериального вагиноза, рецидивов кандидозного вульвовагинита и воспалительных заболеваний органов малого таза [3].
Кроме того, L. jensenii и L. gasseri демонстрируют способность модулировать врожденный иммунный ответ и ингибировать рост Candida albicans и Gardnerella vaginalis [4]. Нарушение доминирования лактобацилл в пользу анаэробной микрофлоры (например, Prevotella spp., Atopobium vaginae) связано с развитием бактериального вагиноза, аэробного вагинита и повышенной восприимчивостью к инфекциям, передающимся половым путем (ИППП).
Влияние антибиотиков и антимикотиков на микробиоту
Применение системных и местных антибиотиков, а также антимикотиков нередко нарушает микробный гомеостаз влагалища. Хотя антибактериальная и антимикотическая терапия эффективно устраняет патогены, она также может приводить к дефициту лактобацилл и избыточному росту условно-патогенных видов [5]. Это, в свою очередь, повышает риск рецидивов и снижает эффективность последующего лечения.
В этой связи растет интерес к применению пробиотиков на основе Lactobacillus spp. в составе восстановительной терапии. Согласно современным данным, восстановление микробиоты с участием L. crispatus, L. rhamnosus и L. reuteri способствует снижению частоты рецидивов бактериального вагиноза и кандидоза [6, 7].
Не менее значимое влияние антимикробная терапия оказывает и на микробиоту кишечника. В реальной клинической практике наиболее частым побочным эффектом антимикробной терапии следует признать антибиотик-ассоциированную диарею (ААД). Диарея, связанная с приемом антибиотиков, развивается у 5–35% пациентов, в зависимости от типа препарата, общего состояния здоровья и наличия воздействия патогенных микроорганизмов [8].
С целью коррекции микробиоты кишечника эксперты Всемирной ассоциации гастроэнтерологов рекомендуют включать в терапию пробиотики, содержащих живые штаммы микроорганизмов [9, 10].
Особое внимание заслуживает комбинация HOWARU® – комбинация бактерий: L. acidophilus (HOWARU NCFM™) + L. paracasei (HOWARU Lpc-37™) + B. lactis (HOWARU Bi-07™) + B. lactis (HOWARU Bl-04™, одобренная Всемирной организацией гастроэнтерологов при приеме антибиотиков, которая включена в пробиотический комплекс Probielle® Bio [9, 10].
По данным исследований частота ААД при приеме комбинации HOWARU® была примерно вдвое ниже, чем в группе плацебо. Продолжительность диареи значительно сократилась примерно на 2–3 дня по сравнению с плацебо. Также при приеме высоких доз комбинации HOWARU® реже развивается диарея, связанная с Clostridium difficile [11].
Таким образом, комплексное восстановление микробиоты становится важным элементом поддерживающей терапии при приеме антибиотиков и антимикотиков – как для кишечника, так и для микробиоты влагалища.
Общее понятие пробиотиков в гинекологии
Согласно определению Всемирной организации здравоохранения (ВОЗ), пробиотики – это «живые микроорганизмы, которые при приеме в адекватных количествах приносят пользу для здоровья хозяина» [12]. В гинекологии их применение направлено на восстановление нормальной микрофлоры, особенно после нарушений, вызванных антибиотикотерапией, воспалительными заболеваниями или гормональными изменениями [13].
Формы пробиотиков
На сегодняшний день в гинекологической практике используются две основные формы пробиотиков.
- Пероральные пробиотики, содержащие штаммы Lactobacillus и Bifidobacterium, способные транслоцироваться из кишечника во влагалище и с целью профилактики антибиотико-ассоциированной диареи [14];
- Интравагинальные формы (капсулы, суппозитории, гели), обеспечивающие локальную доставку пробиотических культур непосредственно к слизистой влагалища, что может ускорять колонизацию [15].
Учитывая преимущества каждой из форм пробиотиков, оптимальным подходом считается комбинированная терапия, сочетающая пероральные и интравагинальные формы. Такой подход обеспечивает как системную поддержку, так и быстрое локальное восстановление влагалищного микробиоценоза, что особенно важно для профилактики рецидивов инфекций и повышения эффективности терапии [16, 17].
Наиболее изученные пробиотические штаммы в гинекологии
Среди большого числа исследуемых пробиотиков наибольшую клиническую значимость приобрели следующие штаммы:
- Lactobacillus rhamnosus GR-1 и Lactobacillus reuteri RC-14 – используются в пероральных формах, способны транслоцироваться из кишечника и заселять вагинальный эпителий;
- Lactobacillus crispatus CTV-05 (LACTIN-V) – интравагинальный штамм с доказанной способностью снижать рецидивы бактериального вагиноза [7, 18, 19].
Эти штаммы демонстрируют высокую устойчивость к воздействию кислот, способность к адгезии к вагинальному эпителию и продуцируют вещества, препятствующие росту патогенной микрофлоры.
Механизмы действия пробиотиков
Пробиотики обеспечивают защиту влагалища за счет нескольких взаимодополняющих механизмов:
- конкуренция за эпителиальные рецепторы с патогенными микроорганизмами (например, Gardnerella vaginalis, Candida albicans);
- продукция молочной кислоты, которая снижает pН и создает неблагоприятную среду для роста анаэробных бактерий;
- синтез бактериоцинов и перекиси водорода, обладающих антимикробной активностью;
- иммуномодулирующее действие, влияющее на врожденные механизмы защиты слизистой [4, 20, 21].
Благодаря этим эффектам пробиотики рассматриваются не только как средство восстановления микрофлоры, но и как перспективное направление профилактики рецидивов бактериального вагиноза, кандидозного вульвовагинита и даже мочевых инфекций у женщин [22].
Бактериальный вагиноз (БВ)
Этиология, патогенез, клиническая картина
Бактериальный вагиноз (БВ) представляет собой наиболее распространенное нарушение вагинального биоценоза у женщин репродуктивного возраста. Его развитие связано с замещением доминирующей флоры, представленной Lactobacillus spp., на условно-патогенные анаэробные микроорганизмы, такие как Gardnerella vaginalis, Atopobium vaginae, Mobiluncus spp. и др. [23].
Патогенез включает разрушение защитного слизистого слоя, снижение выработки молочной кислоты, повышение pH влагалища (>4,5), а также образование биопленок, устойчивых к действию антибактериальных препаратов [24, 25]. Клинически БВ проявляется обильными гомогенными серо-белыми выделениями с характерным «рыбным» запахом.
Стандартная терапия и проблема рецидивов
Терапия первой линии включает применение метронидазола (перорально или вагинально) либо клиндамицина. Эти препараты обладают высокой эффективностью в отношении анаэробной флоры. Однако основной проблемой остается высокая частота рецидивов – до 50–70% в течение 6–12 месяцев после лечения [26]. Это обусловлено неполным восстановлением вагинального микробиома и сохранением бактериальных биопленок, особенно Gardnerella vaginalis [27].
Применение пробиотиков после лечения БВ
Эффективность по данным мета-анализов и рандомизированных контролируемых исследований (РКИ)
Согласно данным метаанализа 22 РКИ, опубликованного в 2023 г., применение пробиотиков после антибактериальной терапии достоверно снижает риск рецидива БВ, особенно при использовании штаммов Lactobacillus crispatus, L. rhamnosus и L. reuteri [28]. В частности, использование препарата LACTIN-V (L. crispatus CTV-05) после метронидазола снижало частоту рецидивов до 30% по сравнению с 70% в группе плацебо [19].
Доказательная база: пероральные и вагинальные формы
Сравнительный анализ показал, что интравагинальное введение пробиотиков обеспечивает более высокую частоту колонизации и восстановление нормофлоры по сравнению с пероральными формами [29]. Однако L. rhamnosus GR-1 и L. reuteri RC-14 в пероральной форме также продемонстрировали способность к транслокации и колонизации влагалищного эпителия, особенно при длительном применении [18].
Рекомендации международных организаций
На сегодняшний день ни одна международная организация не включает пробиотики в стандартные протоколы лечения БВ, однако допускает их использование в рамках вспомогательной терапии.
- В рекомендациях CDC (США) по лечению инфекций, передаваемых половым путем (2021), представлен подробный алгоритм ведения пациентов с БВ, однако пробиотики не входят в число рекомендованных методов лечения. Несмотря на наличие отдельных исследований по применению лактобацилл для восстановления вагинальной микрофлоры, авторы подчеркивают, что доказательная база в настоящий момент ограничена, и ни одна пробиотическая формула не утверждена для лечения или профилактики БВ [30].
- Руководство NICE (UK) и ACOG (США) аналогично отмечают, что применение пробиотиков может рассматриваться как дополнительная мера, особенно при рецидивирующем течении заболевания, однако требуют дальнейших доказательств в РКИ [31, 32].
- Европейские рекомендации IUSTI/ВОЗ по ведению пациентов с вагинальными выделениями (2023) рассматривают БВ и аэробный вагинит (АВ) как самостоятельные клинические состояния. Отмечается, что применение пробиотиков, в частности интравагинальных форм лактобацилл, может быть полезно для восстановления нормального биоценоза влагалища после проведения антибактериальной терапии. Однако авторы не включают их в стандарт лечения, ссылаясь на нехватку РКИ высокой методологической строгости [33].
- В совместных немецко-австрийско-швейцарских рекомендациях по лечению БВ (2022), разработанных Немецким обществом гинекологии и акушерства (DGGG), Австрийским общестом гинекологии и акушерства (OEGGG), Швейцарским обществом гинекологии и акушерства (SGGG), приводится более подробный анализ восстановительной терапии после антибиотиков. Авторы допускают применение пробиотиков у пациенток с рецидивирующим БВ как дополнение к основному лечению. Тем не менее такой подход рассматривается как вспомогательный и зависит от индивидуальных клинических обстоятельств [34].
Аэробный вагинит (АВ)
Этиология, патогенез, отличие от бактериального вагиноза (БВ)
Аэробный вагинит (АВ) представляет собой воспалительное заболевание влагалища, характеризующееся выраженной деградацией эпителиального слоя, повышенным уровнем воспалительных цитокинов и снижением количества лактобацилл с одновременным ростом аэробных условно-патогенных микроорганизмов – преимущественно Escherichia coli, Staphylococcus aureus, Enterococcus faecalis и Streptococcus agalactiae [6, 35].
В отличие от БВ, при котором преобладает анаэробная флора и формируются устойчивые биопленки (Gardnerella vaginalis, Atopobium vaginae), АВ сопровождается более выраженным воспалением, лейкоцитозом, десквамацией эпителия и повышенной болезненностью. Диагноз АВ требует микроскопического исследования и оценки показателей воспаления, в отличие от БВ, который диагностируется по критериям Амселя или шкале Ньюджента [36].
Стандартная терапия и ее ограничения
Терапия АВ не стандартизирована и в большинстве случаев основывается на эмпирическом применении антисептиков или системных антибиотиков, таких как амоксициллин/клавуланат, ципрофлоксацин или клиндамицин. Однако, в отличие от БВ, антибиотикотерапия при АВ часто сопровождается рецидивами и может усугублять дисбиоз за счет дальнейшего подавления лактобацилл.
Отсутствие консенсуса в выборе препаратов и частое сочетание АВ с другими вагинальными инфекциями затрудняют эффективность лечения. Кроме того, использование антибиотиков без последующего восстановления микрофлоры может приводить к хроническому течению заболевания и переходу в форму резистентного воспаления [37].
Применение пробиотиков после лечения АВ
Влияние пробиотиков на воспаление и аэробную флору
Несмотря на ограниченность данных, некоторые исследования демонстрируют, что пробиотики способны снижать уровень вагинального воспаления и способствовать восстановлению доминирования Lactobacillus spp. В частности, Lactobacillus rhamnosus GR-1 и Lactobacillus reuteri RC-14 показали способность угнетать рост E. coli и S. aureus in vitro и в моделях с животными. Также сообщалось о снижении экспрессии провоспалительных цитокинов после применения пробиотиков в составе восстановительной терапии.
Комбинированная терапия: антибиотики + пробиотики
Первые данные об эффективности комбинированной терапии (антибиотик + пробиотики) при АВ появились в клинических наблюдениях и небольших пилотных РКИ. Применение пробиотиков способствует более быстрому восстановлению вагинального эпителия и нормализации pH [38].
Недостаточность исследований и необходимость стандартизации
На данный момент использование пробиотиков при АВ остается экспериментальным: отсутствуют крупные РКИ с адекватным дизайном, а гайдлайны ведущих организаций (CDC, ACOG, IUSTI) не включают АВ как отдельную нозологию с конкретными рекомендациями по лечению. Требуется дальнейшая стандартизация подходов к диагностике, терапии и посттерапевтической реабилитации, в т.ч. с применением пробиотиков как компонента восстановительной терапии [33].
Кандидозный вульвовагинит (КВВ)
Этиология и факторы риска
Кандидозный вульвовагинит (КВВ) является одной из наиболее частых причин вагинальных инфекций у женщин репродуктивного возраста. До 75% женщин испытывают хотя бы один эпизод КВВ в течение жизни, а до 8% страдают от рецидивирующего течения (≥4 эпизодов в год) [39].
Основным возбудителем является Candida albicans, ответственная за 80–90% случаев. Однако наблюдается рост заболеваемости, вызванной non-albicans видами (C. glabrata, C. parapsilosis, C. krusei), которые отличаются меньшей чувствительностью к азолам [40]. К факторам риска относятся: антибактериальная терапия, гормональные контрацептивы, беременность, диабет, иммунодефицитные состояния и частое использование агрессивных средств интимной гигиены [41].
Проблемы резистентности и рецидивов
Несмотря на высокую эффективность азольных препаратов (например, флуконазола, клотримазола), до 20–30% женщин сталкиваются с рецидивами инфекции в течение 6 месяцев после лечения [42] Это может быть связано с персистенцией грибов в биопленках, нарушением вагинального микробиома и повышенной устойчивостью Candida spp., особенно non-albicans, к антимикотикам [43]. Повторные курсы лечения могут усугублять дисбиоз, снижать качество жизни пациенток и повышать риски системных осложнений.
Роль пробиотиков после антимикотической терапии
Антагонизм Lactobacillus к Candida spp.
Lactobacillus spp., в первую очередь L. rhamnosus, L. reuteri и L. crispatus, демонстрируют выраженную антагонистическую активность в отношении Candida albicans и других видов. Механизмы включают:
- конкуренцию за адгезию к эпителию;
- продукцию молочной кислоты, бактериоцинов и перекиси водорода;
- разрушение грибковых биопленок и ингибирование морфогенеза (перехода в патогенную мицелиальную форму) [44].
Эффективность пробиотиков: данные метаанализов
Систематический обзор и метаанализ, включающий 15 рандомизированных исследований, показал, что добавление пробиотиков к антимикотической терапии достоверно снижает частоту рецидивов КВВ (относительный риск 0,65; 95% ДИ: 0,50–0,84), особенно при интравагинальном введении L. rhamnosus и L. reuteri [45]. Наиболее выраженный эффект отмечался у пациенток с частыми эпизодами инфекции.
Недавний метаанализ 35 рандомизированных контролируемых исследований, охватывающий 3751 пациента, подтвердил, что применение пробиотиков значительно повышает частоту излечения КВВ (отношение рисков [ОР] 3,425; 95% доверительный интервал [ДИ]: 2,404–4,879) и снижает частоту рецидивов (ОР 0,325; 95% ДИ: 0,175–0,606). Эти данные подчеркивают потенциал пробиотиков в качестве вспомогательного средства при лечении гинекологических инфекций.
Применение при рецидивирующем КВВ
У женщин с рецидивирующим КВВ пробиотики рассматриваются как часть поддерживающей терапии. Пероральное или вагинальное применение Lactobacillus spp. после завершения антимикотического курса может способствовать восстановлению pH, усилению местного иммунного ответа и снижению колонизации Candida spp. Рекомендуется длительное применение (≥10–14 дней) и повторные курсы, особенно после антибактериальной терапии.
Современные клинические рекомендации, в частности руководство CDC по лечению инфекций, передающихся половым путем (2021), содержат сдержанную позицию в отношении использования пробиотиков при вагинальных инфекциях. В частности, подчеркивается, что в отношении бактериального вагиноза (БВ) отсутствуют достаточные клинические данные, подтверждающие эффективность пробиотиков в качестве основной или адъювантной терапии. Тем не менее в ряде источников упоминаются отдельные исследования, согласно которым интравагинальное применение Lactobacillus crispatus после курса метронидазол-геля ассоциировалось с более низкой частотой рецидивов БВ в течение 12 недель наблюдения [30].
Что касается кандидозного вульвовагинита (ВВК), CDC также указывает на недостаточность доказательной базы для рутинного включения пробиотиков в схемы лечения. Однако систематический обзор Cochrane [45], охватывающий 10 рандомизированных контролируемых исследований с участием 1656 небеременных женщин, показал, что добавление пробиотиков к стандартной антимикотической терапии может улучшать краткосрочные показатели лечения. В частности, было зафиксировано достоверное повышение клинического излечения (ОР 1,14; 95% ДИ: 1,05–1,24) и микологического излечения (ОР 1,06; 95% ДИ: 1,02–1,10), а также снижение частоты рецидивов в течение первого месяца (ОР 0,34; 95% ДИ: 0,17–0,68) [45].
В то же время анализ долгосрочных результатов не выявил значимого улучшения через один и три месяца после лечения, а общее качество доказательств было оценено как низкое или очень низкое ввиду ограничений методологии, небольшого размера выборок и возможной предвзятости. Тем не менее пробиотики не были ассоциированы с увеличением частоты серьезных или легких побочных эффектов, что свидетельствует об их безопасности при комбинированном применении с противогрибковыми средствами.
Влияние на иммунный ответ
Помимо прямого антагонизма, пробиотики способны модулировать врожденный и адаптивный иммунитет. L. crispatus и L. rhamnosus снижают экспрессию провоспалительных цитокинов (IL-1β, TNF-α) и одновременно повышают продукцию защитных факторов (секреторного IgA, IL-10), улучшая барьерную функцию слизистой и снижая уровень воспаления [21, 46].
Таким образом, хотя пробиотики могут улучшить краткосрочные результаты лечения ВВК и снизить риск ранних рецидивов, текущие доказательства недостаточно надежны для их рутинного применения. Необходимы дополнительные высококачественные исследования с более длительным периодом наблюдения и стандартизированными методологиями для окончательной оценки их эффективности и безопасности.
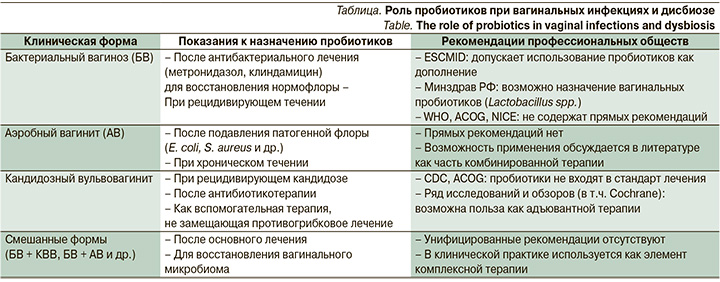
Современные международные клинические рекомендации отражают растущий интерес к применению пробиотиков в качестве дополнительной меры в лечении и профилактике вагинальных инфекций, особенно в случае их рецидивирующего течения (таблица).
Заключение
В последние годы пробиотики все чаще рассматриваются как перспективный компонент комплексной терапии вагинальных инфекций, особенно в условиях рецидивирующего течения. Несмотря на отсутствие универсальных клинических рекомендаций, накопленные данные подтверждают, что пробиотики на основе штаммов Lactobacillus spp. могут способствовать восстановлению вагинальной микробиоты, снижать частоту рецидивов бактериального вагиноза, кандидозного вульвовагинита и аэробного вагинита, а также оказывать иммуномодулирующее действие.
Также не менее важна роль пробиотиков и в профилактике побочных эффектов антибиотикотерапии, в частности антибиотико-ассоциированной диареи (ААД). Таким образом, пробиотики являются значимым дополнением как в гинекологической практике, так и в гастроэнтерологической практике, обеспечивая комплексную защиту микробиоты.
Однако включение пробиотиков в стандарты лечения требует дальнейших исследований, соответствующих критериям доказательной медицины: крупномасштабных рандомизированных контролируемых исследований с унифицированными критериями эффективности и безопасности. До тех пор применение пробиотиков следует рассматривать как адъювантную меру, особенно у пациенток с хроническими или часто рецидивирующими формами вагинальных инфекций.
Внедрение персонализированного подхода к восстановительной терапии, выбор эффективных штаммов, оптимальных дозировок и форм доставки пробиотиков, а также разработка национальных и международных протоколов – важные шаги на пути к улучшению женского репродуктивного здоровья.



