Введение
Проблема острых цереброваскулярных заболеваний – одна из наиболее актуальных в медицине в связи с высокой заболеваемостью, большим процентом инвалидизации и смертности. В последние годы острые нарушения мозгового кровообращения (ОНМК) вышли в России на 3-е место среди всех причин смерти населения, основную позицию в их структуре занимает ишемический инсульт (ИИ), распространенность которого последовательно увеличивалась за счет улучшения методов диагностики в последние десятилетия. На протяжении последних десятилетий во всем мире ведется активный поиск эффективных методов профилактики и лечения ОНМК [1, 2].
Системная тромболитическая терапия (ТЛТ) служи «золотым» стандартом лечения больных в острейшем периоде ИИ в отсутствие противопоказаний.
В то же время тромбы в сосудах большего диаметра, в особенности с уже стабилизированным фибрином, труднее поддаются эффективному фармакологическому воздействию, что ограничивает эффективность системной ТЛТ при окклюзии в проксимальных отделах крупных интракраниальных артерий [4]. Кроме того, на фоне применения алтеплазы увеличивается риск развития кровотечений различной локализации, в первую очередь внутричерепных [7].
В настоящее время тромбоэкстракция считается самым перспективным и активно развивающимся методом интервенционного лечения ИИ.
В 2015 г. были опубликованы результаты 5 рандомизированных исследований: MR CLEAN, EXTEND-IA, ESCAPE, SWIFT-PRIME, REVASCAT. Во всех исследованиях в большинстве случаев были использованы стент-ретриверы и современные протоколы нейровизуализации с применением КТ/МР-ангиографии и оценкой перфузии. Мета-анализ этих исследований, включивший в общей численности 1287 пациентов, показал, что комбинация тромбоэкстракции с системным внутривенным тромболизисом улучшает функциональный результат лечения ИИ без влияния на общую смертность или риск внутричерепных кровоизлияний. В том же году American Heart Association/American Stroke Association обновили рекомендации по ведению пациентов с ИИ в острейшем периоде, присвоив тромбоэкстракции класс доказательности I, уровень A. Тем не менее системную тромболитическую терапию алтеплазой необходимо выполнить во всех случаях, кроме наличия противопоказаний к ее проведению, даже если планируется эндоваскулярное вмешательство [12–16].
В данной статье мы представляем собственное клиническое наблюдение успешного применения сочетанной реканализации в отношении пациентки с ИИ.
Клинический случай
Пациентка Г. 77 лет. Была доставлена в смотровой кабинет невролога первичного сосудистого отделения Городской клинической больницы № 31 в 11.30 01.04.2017 бригадой скорой медицинской помощи.
Жалобы при поступлении: на слабость и ощущение онемения в левых конечностях, речевые нарушения по типу «каша во рту».
Анамнез заболевания. Заболела утром 01.04.2017 в 10.00, когда дочь заметила вышеуказанные жалобы. Потери сознания, судорог, ударов головой не отмечено.
Анамнез жизни. Артериальная гипертензия 3-й стадия, 3-я степень, очень высокой степени риска сердечно-сосудистых осложнений. Постоянно принимает спиронолактон 25 мг, эналаприл 10 мг 2 раза в день. Инсульт, инфаркт, сахарный диабет, язвенную болезнь отрицает.
Объективно при поступлении. Состояние больной тяжелое, положение активное. Телосложение нормостеническое. Кожный покров нормальной окраски, сухой, теплый на ощупь. При аускультации дыхание везикулярное, проводится во все отделы. Хрипы не выслушиваются. Частота дыхательных движений – 17 в минуту. Аускультативно тоны сердца приглушены, аритмичные, шумы не выслушиваются. Частота сердечных сокращений – 70 ударов в минуту. Артериальное давление – 170/90 мм рт.ст. на левой руке, на правой – 172/88 мм рт.ст. Пульс на периферических артериях удовлетворительного качества, дефицита пульса нет. Живот мягкий, наличия распространенной и локальной болезненности, напряжения брюшных мышц, опухолевых образований и грыж не обнаружено. Мочеиспускание не затруднено, безболезненное. Симптом «поколачивания» отрицательный.
Неврологический статус при поступлении. Сознание ясное, ориентирована во времени и личности, дезориентирована в пространстве. Менингеального синдрома нет. Левосторонняя гомонимная гемианопсия. Острота зрения снижена (дальнозоркость: OD +2.0 OS +2.0).
Глазные щели равномерные, одинаковой ширины, птоза нет. Поворот головы и глаз вправо. Величина, форма зрачков нормальные, анизокории нет, реакция на свет живая, содружественная. Конвергенция, аккомодация не нарушены. Чувствительность на коже лица снижена слева. Лобные складки, глазничные щели в покое симметричны, имеется сглаженность носогубной складки слева. Асимметрия при надувании щек слева. Нистагма нет. Глотание и фонация не нарушены. Глоточный рефлекс сохранен с обеих сторон. Глотание свободное, дисфагии нет. Подвижность мягкого неба достаточная, язычок мягкого неба занимает срединное положение. Язык девиирует влево. Грубая дизартрия. Объем пассивных движений сохранен во всех суставах, контрактур и анкилозов нет. Объем активных движений снижен в левых конечностях со снижением мышечной силы в левой руке и левой ноге до 0 баллов по шкале Комитета медицинских исследований. Мышечный тонус в левой руке и ноге снижен. Рефлексы с двуглавой и трехглавой мышц, коленный и ахиллов рефлексы снижены слева. Патологические разгибательные рефлексы (Бабинского, Оппенгейма, Гордона, Шеффера) слева. Пальце-носовую, пяточно-коленную, пальце-пальцевую пробы выполняет удовлетворительно правыми конечностями, левыми не выполняет из-за снижения мышечной силы. Болевая, температурная, тактильная чувствительность справа сохранена, слева – снижена. Глубокая чувствительность сохранена справа, слева – снижена. Тазовые органы: задержки, недержания мочи и кала нет.
Балл по шкале ком Глазго – 15, балл по шкале инсульта Национального института здоровья (NIH) – 16.
По данным лабораторных анализов: глюкоза крови – 8,3 ммоль/л, МНО – 1,08, АЧТВ – 25,7 с; тромбоциты – 210×109/л. Общий анализ крови, биохимический анализ сыворотки крови и общий анализ мочи без особенностей.
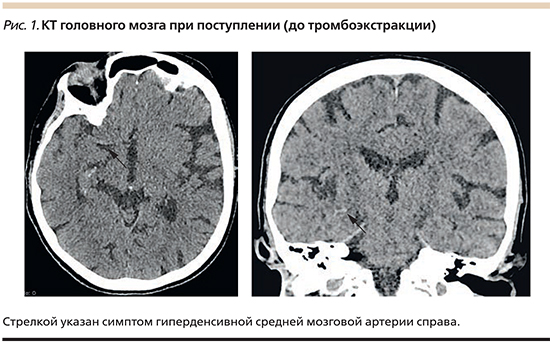
По данным компьютерной томографии головного мозга 11.50 01.04.2017 (рис. 1): КТ-признаки тромба (атеросклеротической бляшки?) в М1-сегменте правой средней мозговой артерии. По шкале: http://www.aspectsinstroke.com/Alberta для оценки начальных изменений на КТ при инсульте (ASPECTS) 9 баллов.
ЭКГ: ЧСС – 60 в минуту. PQ – 0,18 с, QRS – 0,09 c, QT – 0,42 c. Ритм синусовый. Умеренное отклонение электрической оси сердца влево. Гипертрофия левого желудочка с диффузными изменениями миокарда.
В 12.00 (через 30 минут от момента поступления в клинику) начата внутривенная ТЛТ, доза алтеплазы составила 55,8 мг.
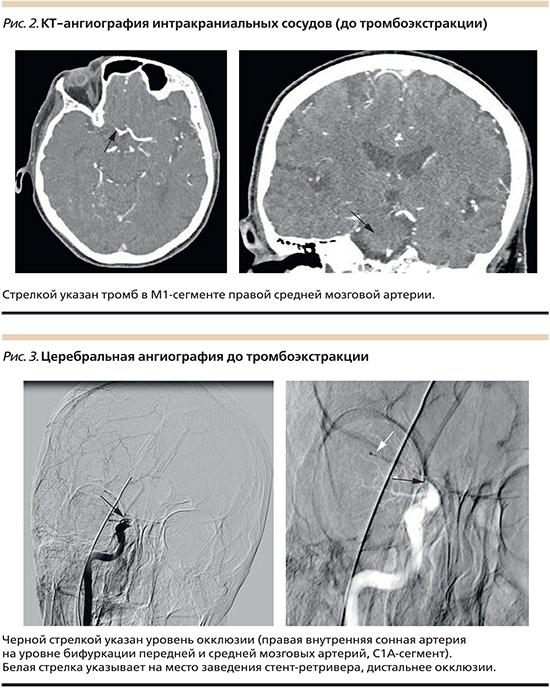
По данным КТ-ангиографии интракраниальных сосудов 12.15 01.04.2017 (рис. 2): КТ-признаки отсутствия кровотока в М1-сегменте правой средней мозговой артерии (вероятно, тромбоз).
В 12.25 пациентка была доставлена в рентгеноперационную.
Протокол церебральной ангиографии 12.40–12.45 01.04.2017 (рис. 3). Под местной анестезией 20 мл 0,25%-ного раствора новокоина выполнена пункция правой общей бедренной артерии, установлен интродьюсер 5F, выполнена церебральная ангиография. Заключение. Окклюзия правой внутренней сонной артерии на уровне бифуркации передней и средней мозговой артерий (С1А сегмент), контрастирования последних не получено. По шкале оценки коллатерального кровотока ACG – 2 балла, по шкале оценки окклюзионного поражения артерии AOL – 0 баллов.
Протокол тромбоэкстракции 13.00–14.50 01.04.2017. Общая анестезия с искусственной вентиляцией легких. Вводный наркоз: пропофол – 100 мл, рокурония бромид – 50 мг. Выполнена оротрахеальная интубация эндотрахеальной трубкой 8,0. Начата ИВЛ в режиме VCV. Поддержание анестезии: пропофол 500 мг. Кураризация – рокурония бромид 100 мг. Интродьюсер правой общей бедренной артерии заменен на интродьюсер 6 Fr. В правую внутреннюю сонную артерию проведен гайд-катетер. Через гайд-катетер по микропроводнику за зону окклюзии правой внутренней сонной артерии на уровне сегмента С1А проведен микрокатетер, через который проведен стент-ретривер. Трехкратно выполнена тромбэкстракция, извлечен бело-красный тромб. При контрольной ангиографии (рис. 4) отмечено восстановление кровотока по правой внутренней сонной артерии, получено контрастирование передней мозговой и средней мозговой артерий, кровоток по модифицированной шкале восстановления перфузии при ишемическом инсульте mTICI 3 (рис. 4). Гайд-катетер извлечен, интродьюсер удален, пункционное отверстие ушито с помощью устройства AngioSeal 6 Fr, наложена асептическая давящая повязка.
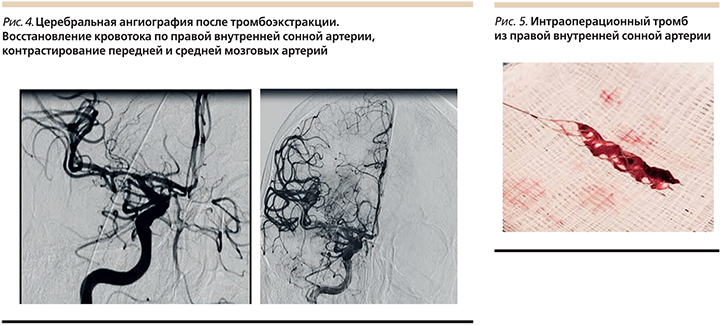
Патогистологическое исследование интраоперационного материала (рис. 5) Макроскопическое описание: тромботические массы размером 0,7×0,4×0,2 см. Микроскопическое исследование (окраска гематоксилином и эозином): белый тромб, представленный неизмененными эритроцитами и небольшим количеством сегментоядерных нейтрофилов.
После операции сознание не восстановлено, медикаментозная седация, миоплегия. Декураризация не проведена. Пациентка переведена в ОРИТ для больных ОНМК в 15.20 в условиях ИВЛ, состояние тяжелое. Параметры контроля: АД – 150/90 мм рт.ст., ЧСС – 85 в минуту, SaО2 – 99%.
Через 3 часа после тромбоэкстракции (в 18.00 01.04.2017) произведена экстубация трахеи.
Объективно при осмотре: в сознании. Кожный покров и видимые слизистые оболочки без особенностей. Температура тела – 36,8°С. Дыхание жесткое, хрипов нет, проводится во все отделы легких, подача увлажненного кислорода через носовую канюлю со скоростью 4 л/мин. АД – 140/80 мм рт.ст., ЧСС – 72 в минуту, ритм правильный. Живот мягкий, безболезненный. Перитонеальные симптомы отрицательные. Мочеиспускание по катетеру мочевого пузыря.
Неврологический статус: в сознании. Менингеальная симптоматика отсутствует, локальных менингеальных знаков нет. Черепные нервы: зрачки округлой формы, средней величины, OD=OS, глазные яблоки по средней линии, движения глаз в полном объеме, фотореакции сохранены, верхнеквадрантная левосторонняя гемианопсия. Умеренный центральный прозопарез слева, нистагма нет, глотание сохранно, язык девиирует влево. Умеренная дизартрия. Двигaтельная сфера: мышечный тонус не изменен, левосторонний гемипарез со снижением силы до четырех баллов, сухожильные рефлексы D>S, симптом Бабинского слева. Левосторонняя гемигипестезия. Координаторные пробы выполняет удовлетворительно справа, слева – в рамках пареза. Балл по шкале инсульта Национального института здоровья (NIH) – 8.
Через 24 часа от начала заболевания в 12.00 02.01.2017:
Объективно при осмотре: в сознании. Кожный покров и видимые слизистые оболочки без особенностей. Температура тела – 36,7°С. Дыхание жесткое, хрипов нет, проводится во все отделы легких. АД – 140/80 мм рт.ст., ЧСС – 75 в минуту, ритм правильный. Живот мягкий, безболезненный. Перитонеальные симптомы отрицательные. Мочеиспускание самостоятельное.
Неврологический статус: сознание ясное, контактна, ориентирована в полном объеме. Менингеальная симптоматика отсутствует, локальных менингеальных знаков нет. Черепные нервы: зрачки округлой формы, средней величины, OD=OS, глазные яблоки по средней линии, движения глаз в полном объеме, фотореакции сохранены, гемианопсии, диплопии, нистагма нет. Сглаженность левой носогубной складки, глотание сохранно, язык девиирует влево. Умеренная дизартрия. Двигaтельная сфера: мышечный тонус не изменен, левосторонний гемипарез со снижением мышечной силы до пронационного феномена в руке, 4 баллов в ноге, сухожильные рефлексы D>S, симптом Бабинского слева. Чувствительность не изменена. Координаторные пробы выполняет удовлетворительно с двух сторон. Балл по шкале инсульта Национального института здоровья (NIH) – 2, балл по модифицированной шкале Рэнкина – 1.
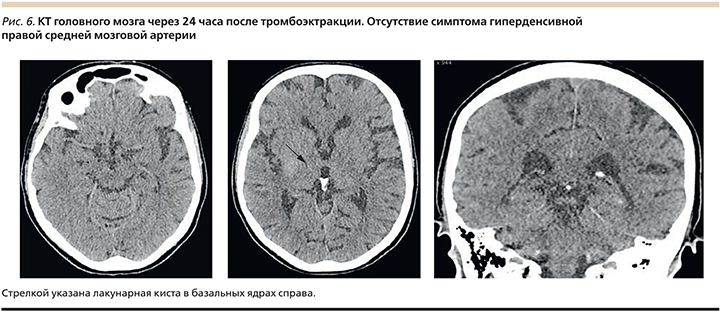
Компьютерная томография головного мозга в динамике, выполненная через 24 часа после тромбоэктракции – в 15.00 02.01.2017 (рис. 6): при сравнении с предыдущим исследованием гиперденсивности средняя мозговая артерия справа не определяется. КТ-признаки лакунарной кисты (8×10 мм) в базальных ядрах справа со слабогиперденсивным участком (остаток контрастного вещества). По шкале: http://www.aspectsinstroke.com/Alberta для оценки начальных изменений на КТ при инсульте (ASPECTS) – 9 баллов.
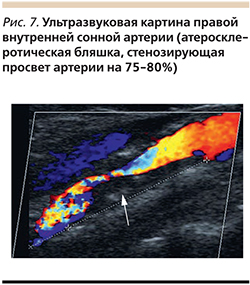
Дуплексное сканирование брахиоцефальных артерий (рис. 7): эхо-признаки выраженного стеноза правой внутренней сонной артерии до 75–80%, слева гемодинамически значимого стеноза не выявлено.
 ЭхоКГ: уплотнение аорты, створок аортального и митрального клапанов. Гипертрофия левого желудочка. Зон нарушенной локальной сократимости не выявлено. Фракция выброса – 55%. Допплерография: митральная регургитация 2-й ст., трикуспидальная регургитация 2-й ст., аортальная регургитация 1-й ст. Перикард без особенностей.
ЭхоКГ: уплотнение аорты, створок аортального и митрального клапанов. Гипертрофия левого желудочка. Зон нарушенной локальной сократимости не выявлено. Фракция выброса – 55%. Допплерография: митральная регургитация 2-й ст., трикуспидальная регургитация 2-й ст., аортальная регургитация 1-й ст. Перикард без особенностей.
Ультразвуковая допплерография вен нижних конечностей: признаков нарушения проходимости на момент осмотра не выявлено.
С учетом данных анамнеза и инструментальных методов исследования (стенозирующий атеросклероз правой внутренней сонной артерии до 80%, отсутствие фибрилляции предсердий) у пациентки был диагностирован атеротромботический патогенетический вариант ИИ по критериям TOAST.
При выписке из стационара (через 13 дней от начала заболевания):
Объективно при осмотре: в сознании. Кожный покров и видимые слизистые оболочки без особенностей. Температура тела – 36,6°С. Дыхание жесткое, хрипов нет, проводится во все отделы легких. АД – 130/70 мм рт.ст., ЧСС – 63 в минуту, ритм правильный. Живот мягкий, безболезненный. Перитонеальные симптомы отрицательные. Мочеиспускание самостоятельное.
В неврологическом статусе: сознание ясное, контактна, ориентирована в полном объеме. Менингеальная симптоматика отсутствует, локальных менингеальных знаков нет. Черепные нервы: зрачки округлой формы, средней величины, OD=OS, глазные яблоки по средней линии, движения глаз в полном объеме, фотореакции сохранены, гемианопсии, диплопии, нистагма нет. Сглаженность левой носогубной складки, глотание сохранно, язык девиирует влево. Элементы дизартрии. Двигaтельная сфера: мышечный тонус не изменен, движения в полном объеме, рефлексы повышены D>S, симптом Бабинского слева. Чувствительность не изменена. Координаторные пробы выполняет удовлетворительно с двух сторон.
Балл по шкале инсульта Национального института здоровья (NIH) – 2, балл по модифицированной шкале Рэнкина – 1, балл по шкале оценки мобильности Ривермид – 14, балл по шкале оценки активности жизнедеятельности Бартел – 100.
При выписке из стационара пациентке были даны рекомендации:
- Соблюдение диеты с пониженным содержанием животных жиров и соли.
- Консультация сосудистого хирурга для решения вопроса о выполнении каротидной эндартерэктомии из правой внутренней сонной артерии.
- Ацетилсалициловая кислота 75 мг/сут – длительно.
- Эналаприл 5 мг 2 раза в день – длительно, под контролем АД.
- Аторвастатин 80 мг/сут – длительно, под контролем липидного спектра и биохимических показателей крови (КФК, АСТ, АЛТ) каждые 3 месяца.
Через 6 месяцев после тромбоэкстракции (02.10.2017): балл по шкале инсульта Национального института здоровья (NIH) – 2, балл по модифицированной шкале – 1, балл по шкале оценки мобильности Ривермид – 15, балл по шкале оценки активности жизнедеятельности Бартела – 100.
Адекватное соблюдение рекомендаций по вторичной профилактике, назначенных пациентке при выписке, может предотвратить более половины повторных ИИ, сведя их риск к минимуму.
Обсуждение
В данном клиническом наблюдении представлено описание пациентки с атеротромботическим ИИ в бассейне правой средней мозговой артерии, которой была выполнена процедура сочетанной реперфузии.
Существует два метода лечения ИИ в острейшем периоде, доказавших свою эффективность и безопасность в крупных многоцентровых рандомизированных плацебо-контролируемых клинических исследованиях с классом доказательности I, уровнем A: внутривенная ТЛТ и тромбоэкстракция (с применением как кастент-ретриверов, так и тромбоаспирации) [3, 4, 11].
Внутривенная ТЛТ при помощи рекомбинантного активатора плазминогена (rt-PA) служит рутинным методом лечения больных первые 4,5 часа от начала ИИ в отсутствие противопоказаний [3]. Помимо доказанного положительного эффекта в виде улучшения функционального исхода у данного метода есть ряд ограничений, таких как большой перечень противопоказаний, «узкое терапевтическое окно», повышение риска геморрагических осложнений [3, 5]. При анализе эффективности и безопасности ТЛТ установлено, что с летальным исходом были ассоциированы такие факторы, как, прежде всего, время от дебюта заболевания до начала ТЛТ, что было показано в ряде крупных исследований, а так же возраст, уровень систолического АД при поступлении, выраженность неврологического дефицита по шкале NIH [3, 6]. При анализе вероятности возникновения геморрагической трансформации очага поражения головного мозга (как симптомной, так и асимптомной) показано, что на развитие таковой оказывали влияние такие факторы, как наличие ранних КТ-признаков инфаркта головного мозга, возраст, а также выраженность неврологического дефицита по шкале инсульта NIH [6–8]. На положительный эффект применения системной ТЛТ оказывают влияние калибр окклюзированной церебральной артерии и протяженность тромба (чем дистальнее сегмент и меньшая протяженность тромба, тем более вероятна успешная реканализация) [9, 10].
Эндоваскулярные методы лечения на первых этапах своего развития включали селективный внутриартериальный тромболизис, при котором алтеплаза вводится непосредственно в окклюзированную артерию в зону локализации тромба. Этот метод лечения применялся в тех случаях, когда системный тромболизис не давал эффекта или пациент поступал в стационар позднее первых 4,5 часов, но временной интервал от начала заболевания не превышал 6 часов. Методика селективного внутриартериального тромболизиса имела ряд преимуществ, таких как уточнение локализации окклюзии, выяснение индивидуальных особенностей кровоснабжения головного мозга, уменьшение дозы алтеплазы, что снижало риск геморрагических осложнений, возможность дополнительного механического воздействия на тромб, контроль процесса восстановления циркуляции [5]. В мета-анализе 27 исследований внутриартериальной ТЛТ показано, что данный метод лечения приводил к значимому улучшению степени функционального восстановления у большего числа пациентов и снижению летальности, несмотря на более высокую частоту развития симптомных внутричерепных кровоизлияний [6]. Впервые в Российской Федерации селективный внутриартериальный тромболизис применен в клинике НИИ инсульта Российского государственного медицинского университета на базе ГКБ № 31 в 2006 г. Таким образом, согласно рекомендациями American Heart Association/American Stroke Association от 2015 г., селективная внутриартериальная ТЛТ является одним из методов лечения ИИ у группы больных с окклюзией крупных мозговых артерий, класс доказательности II, уровень B [16].
В 2015 г. New England Journal of Medicine опубликовал результаты 5 крупнейших мировых клинических исследований, доказавших эффективность механической тромбоэкстракции: MRCLEAN, EXTEND-IA, ESCAPE, SWIFT-PRIME, REVASCAT [12–16].
«Терапевтическое окно» для тромбоэкстракции пациентов с ИИ в каротидном бассейне в крупных мировых исследованиях достигает 6, 8 или даже 12 часов и превышает значения, установленные для системной ТЛТ (4,5 часа). В 2017 г. опубликовано исследование DAWN, «терапевтическое окно» для эндоваскулярного лечения в котором было расширено с 6 до 24 часов.
В данном исследовании использовано специальное программное обеспечение RAPID (обязательное выполнение МР-перфузии с оценкой зоны ишемической «пенумбры») [14, 18]. По результатам данного исследования установлено значимое преимущество тромбоэктракции по сравнению с консервативной терапией за пределами 6-часового «терапевтического окна». Балл 0–2 по модифицированной шкале Рэнкина в группе тромбоэкстракции отмечен у 48,6% пациентов при сравнении с группой медикаментозной терапии, в которой он наблюдался лишь у 13,1%. Балл 2b–3 по модицифированной шкале восстановления перфузии при ИИ (mTICI) встречен в группе тромбоэкстракции в 84% случаев [14, 15, 18].
Тромбоаспирация при ИИ эффективна так же, как применение стент-ретриверов, по данным клинического исследования ASTER, опубликованного в 2017 г. [17].
Согласно рекомендациям 2018 г. American Heart Association/American Stroke Association, показанием к механической тромбоэкстракции является верифицированный ИИ (балл по NIHSS ≥6, балл по ASPECTS ≥6) у пациентов старше 18 лет, вызванный окклюзией внутренней сонной артерии или M1-сегмента средней мозговой артерии, после проведения внутривенной ТЛТ или в качестве самостоятельного метода (при противопоказаниях к внутривенной ТЛТ), если время от появления первых симптомов заболевания до момента начала лечения не превышало 6 часов (класс доказательности I, уровень A). У пациентов с окклюзией передних мозговых, позвоночных, базилярной или задних мозговых артерий тромбоэкстракция показана, если время от появления первых симптомов заболевания до момента начала лечения не превышает 6 часов (класс доказательности II, уровень B). Также рекомендовано проведение тромбоэкстракции пациентов с «терапевтическим окном» 6–16 часов с предварительным выполнением КТ/МР-перфузии с оценкой зоны «пенумбры» (уровень рекомендации IА). Снижение времени от появления первых симптомов до реканализации значимо связано с лучшими клиническими результатами (класс доказательности I, уровень A) [19].
Заключение
Представленный нами клинический случай продемонстрировал как отсутствие осложнений, так и высокую эффективность метода сочетанной реперфузии – внутривенной ТЛТ при помощи рекомбинантного активатора плазминогена (rt-PA) и механической тромбоэкстракции с применением стент-ретривера. Данный метод помог пациентке с тяжелым ИИ (балл при поступлении по шкале инсульта NIH – 16) избежать глубокой инвалидизации и остаться способной выполнять всю повседневную деятельность.



