Введение
По данным Международной диабетической федерации, численность больных сахарным диабетом (СД) в мире за последние 10 лет увеличилась более чем в 2 раза и к концу 2021 г. достигла 537 млн человек, а по прогнозам, к 2030 г. достигнет 643 млн [1]. По данным Московского сегмента Федерального регистра сахарного диабета, в Москве за период с 2013 по 2018 г. общее число пациентов с СД увеличилось на 9,8% (с 314,4 до 345,1 тыс. человек). При этом на долю СД2 приходится 94% от общего числа больных [2].
Современные подходы к лечению СД2 предполагают своевременную диагностику атеросклеротических, сердечно-сосудистых заболеваний (АССЗ) либо факторов их риска, а также хронической сердечной недостаточности (ХСН) и/или хронической болезни почек (ХБП). В консенсусе ADA/EASD по ведению пациентов с гипергликемией при СД2 (2023) именно наличие вышеуказанных состояний является основным критерием для выбора ключевой стратегии использования классов сахароснижающих препаратов, обладающих кардио- и нефропротективными свойствами [3].
В случае ХСН у больного СД2 приоритет отдается использованию препаратов из группы ингибиторов натрий-глюкозного котранспортера 2-го типа (иНГЛТ-2). В случае же наличия АССЗ, факторов их риска и/или ХБП в структуре терапии должны быть использованы иНГЛТ-2 или агонисты рецепторов глюкагоноподобного пептида-1 (арГПП-1) с доказанной эффективностью в отношении вышеуказанных состояний [3]. Обращает на себя внимание, что с точки зрения влияния как на уровень гликемии, так и на массу тела наиболее выраженные эффекты демонстрируют арГПП-1 [3].
В Российских Алгоритмах специализированной медицинской помощи больным СД также даны рекомендации по выбору сахароснижающих препаратов в зависимости от доминирующей клинической проблемы, которые также рекомендуют приоритетное использование иНГЛТ-2 и арГПП-1 в отношении пациентов с АССЗ (либо факторами риска АССЗ) и ХБП, а также применение иНГЛТ-2 больными СД2 с ХСН [4].
В России для лечения СД2 применялись следующие препараты из группы арГПП-1: эксенатид, лираглутид, дулаглутид, семаглутид. В настоящее время в реальной клинической практике в Москве для лекарственного обеспечения в рамках льготного лекарственного обеспечения из препаратов группы арГПП-1 доступен только дулаглутид (Трулисити). Препараты группы арГПП-1 усиливают глюкозозависимую секрецию инсулина, подавляют секрецию глюкагона, замедляют опорожнение желудка, снижают уровень HbA1c, нивелируют постпрандиальные колебания глюкозы, уменьшают аппетит, потребление пищи и массу тела. В частности, применение дулаглутида приводит к эффективному контролю гликемии (снижение уровня HbA1c на 1–2%) и улучшению остальных показателей метаболического синдрома (масса тела, систолическое артериальное давление [АД], липидный спектр) [5–7]. В клинических исследованиях показано, что дулаглутид влияет на комбинированную точку МАСЕ (major adverse cardiovascular events), т.е. снижает риск нефатального инфаркта миокарда (ИМ), нефатального острого нарушения мозгового кровообращения (ОНМК) и смерти из-за сердечно-сосудистой причины у пациентов с СД2 и АССЗ или из-за множественных факторов риска АССЗ [8].
Одним из наиболее значимых исследований последнего времени, посвященных изучению кардиопротективных свойств арГПП-1, стало исследование REWIND, которое проводилось с целью оценки влияния дулаглутида в еженедельной дозе 1,5 мг на риск развития сердечно-сосудистых исходов у взрослых больных СД2 по сравнению с плацебо. Треть пациентов, включенных в исследование REWIND, имели в анамнезе АССЗ (перенесенный ИМ, ишемический инсульт, нестабильную стенокардию, операции по поводу реваскуляризации коронарных, сонных, периферических сосудов, госпитализации по поводу ишемической болезни сердца с нестабильной стенокардией или зарегистрированной ишемией миокарда) [9].
По результатам исследования отмечено положительное влияние дулаглутида на уровни HbA1c, систолического АД, липопротеидов низкой плотности, массы тела. В группе пациентов, получавших дулаглутид, отмечено снижение частоты наступления МАСЕ на 12%, нефатального инсульта на 24% [9]. В субанализе данных исследования REWIND показано, что снижение частоты МАСЕ не зависит от наличия или отсутствия ССЗ в анамнезе пациентов (р=0.97). Это легло в основу рекомендаций по применению дулаглутида как для первичной, так и для вторичной профилактики ССЗ [9].
Использование дулаглутида ассоциировано с улучшением комбинированных почечных исходов, которые впервые включили возникшую макроальбуминурию, снижение на 40% скорость клубочковой фильтрации (СКФ) или начало заместительной почечной терапии, смерти, связанной с почечной патологией у людей с СД2 с предшествующими ССЗ или факторами сердечно-сосудистого риска (р=0.0004). В post hoc-анализе оценивались исходы, связанные с функцией почек, за исключением впервые возникшего компонента макроальбуминурии у участников исследования REWIND. Риск развития состояний, входящих в композитную почечную точку, был на 25% ниже среди пациентов, получавших дулаглутид, чем плацебо (отношение рисков [ОР]=0,75, 95% доверительный интервал [ДИ]: 0,62–0,92; р=0,004), в подгруппе с оценкой как соотношения альбумин/креатинин в моче, так и с оценкой СКФ [11]. Устойчивое снижение рСКФ на ≥40% наблюдалось на 28% реже среди пациентов на дулаглутиде, чем на плацебо (ОР=0,72; 95% ДИ: 0,58–0,88; р=0,002) [10]. Среднегодовое снижение СКФ было значительно меньше в группе пациентов на дулаглутиде, чем плацебо (-1,37 против -1,56 мл/мин/1,73 м2/год; р<0,001) [10].
Таким образом, снижение риска почечных исходов на 25% на терапии дулаглутидом позволяет рекомендовать его пациентам с СД2 для замедления развития и прогрессирования ХБП.
По данным Московского сегмента ФРСД (рис. 1), число больных СД2 увеличилось за период с 2008 по 2023 г. более чем в 1,7 раза (с 194,6 до 338,9 тыс. человек).
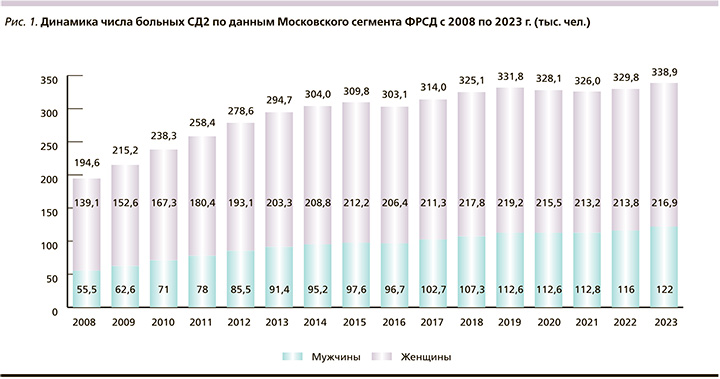
При этом отмечается значительный рост регистрации таких жизненно важных состояний, как ИМ, ОНМК и ХСН, ассоциированных с показателями сердечно-сосудистой смертности больных СД2 (рис. 2).
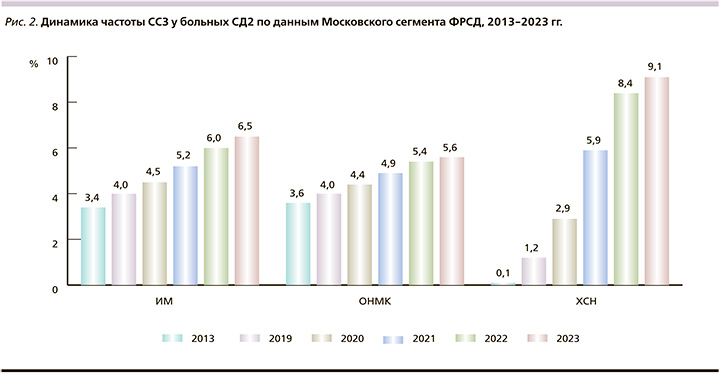
Реальная клиническая практика терапии СД2 в Москве демонстрирует значимые изменения в подходах к выбору сахароснижающих препаратов. Отмечается стабильно высокая частота использования препаратов метформина одновременно со стойкой тенденцией сокращения использования препаратов сульфонилмочевины (СМ). Так, доля использования СМ снизилась с 2020 по 2023 г. с 45,6 до 36,7% (рис. 3).
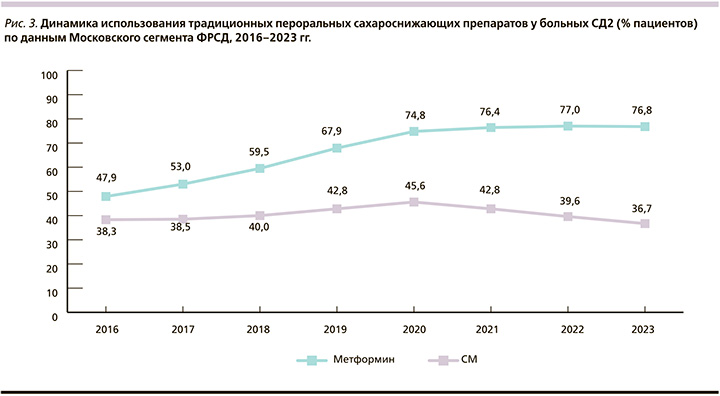
По данным Московского сегмента ФРСД, с каждым годом все более активно в терапии СД2 применяются современные неинсулиновые препараты: арГПП-1, ингибиторы дипептидилпептидазы-4 (иДПП-4), иНГЛТ-2. Так, в 2023 г. более половины больных СД2 в Москве получали как минимум 1 препарат из этих классов (рис. 4).
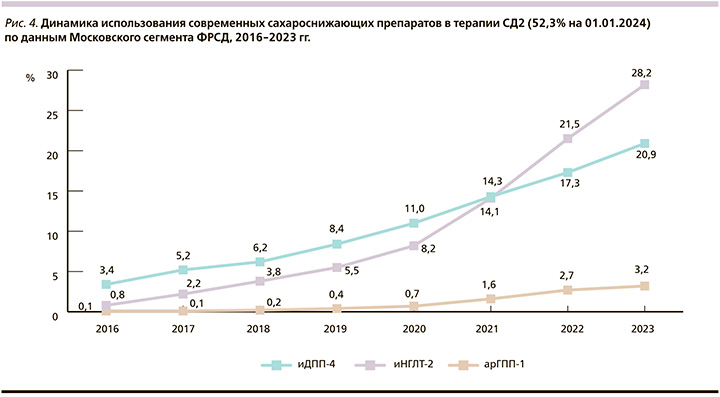
На протяжении длительного времени самой используемой группой новых препаратов были иДПП-4. Но в начале 2021 г. отмечен значительный рост использования препаратов класса иНГЛТ-2, которые по числу пациентов опередили препараты из группы иДПП-4 и до настоящего времени сохраняют лидирующие позиции среди всех препаратов новых классов. Одновременно с 2011 г. отмечен значительный рост использования препаратов группы арГПП-1. За период с 2020 по 2023 г. доля использования препаратов данного класса среди больных СД2 выросла более чем в 4 раза (с 0,7 до 3,2%) (рис. 4).
Наиболее выраженная динамика прироста числа пациентов, получающих препараты группы арГПП-1, отмечена среди больных, получающих дулаглутид. Число таких пациентов выросло с 2017 по 2023 г. с 6 до 4707 человек (рис. 5). По данным Московского сегмента ФРСД, дулаглутид чаще (60,7%) назначался женщинам. При этом средний возраст пациентов составлял около 60 лет, а длительность СД – 9–10 лет. Средний показатель индекса массы тела (ИМТ) составлял 36,9 кг/м2 (табл. 1).
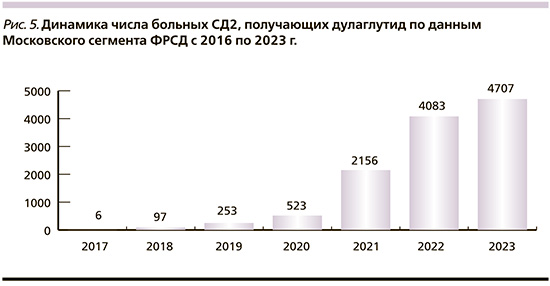
Средний уровень HbA1c у данных пациентов составлял 7,3%, что говорит о контроле углеводного обмена, близком к целевым показателям для данной возрастной категории. При анализе распространенности осложнений СД2 у пациентов, получающих дулаглутид, отмечено, что более 30% мужчин и 25% женщин имели в анамнезе ССЗ. При этом распространенность ИМ среди мужчин была в 3 раза выше, чем среди женщин, при сопоставимой распространенности ОНМК (табл. 1).
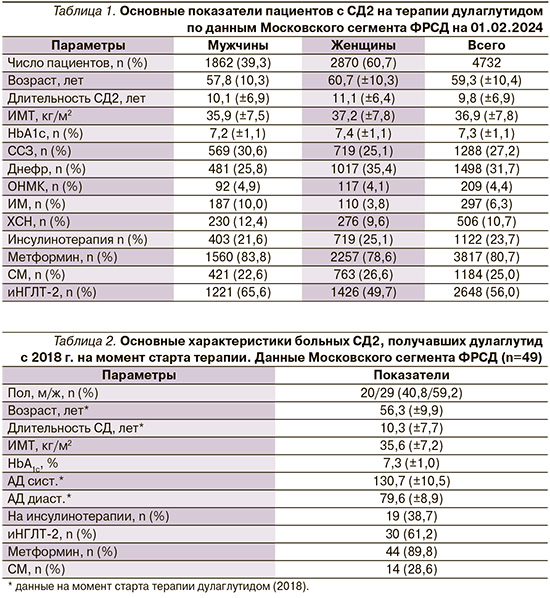
Более 80% пациентов в составе комбинированной терапии СД2 получали метформин, 56% – иНГЛТ-2 и 25% – препараты СМ (табл. 1).
Методы
С целью оценки эффективности использования дулаглутида с точки зрения влияния на уровень HbA1c и массу тела на протяжении длительного периода проведен анализ данных больных СД2, начавших терапию дулаглутидом в 2018 г.
Была сформирована выборка из Московского сегмента ФРСД согласно следующим критериям:
- пациенты, начавшие лечение дулаглутидом в 2018 г., для которых дулаглутид стал первым препаратом класса арГПП-1, и получавшие данный препарат на протяжении всего периода наблюдения (2018–01.02.2024);
- пациенты, у которых в ФРСД имелась информация о динамике уровня HbA1c и массы тела за период наблюдения (2018–01.02.2024).
Критериям включения в данный анализ соответствовали 49 человек (20 мужчин и 29 женщин). На момент старта терапии дулаглутидом (2018) пациенты имели средний возраст 56,0±9,9 года и длительность СД2 около 10 лет. ИМТ составлял 35,6 кг/м2. Средний уровень HbA1c на момент старта терапии дулаглутидом – 7,3%, АД – 130/80 мм рт.ст. (табл. 2). Абсолютное большинство (90,0%) пациентов получали метформин, менее 30% – препараты СМ, на инсулинотерапии находились 39,0% пациентов. Данная когорта пациентов также характеризовалась высокой частотой использования иНГЛТ-2 (61,0%). У 40,8% больных СД2 данной когорты отмечено наличие ССЗ, из которых чаще всего встречались ишемическая болезнь сердца (20,4%) и ХСН (12,2%). ОНМК в анамнезе отмечалось у 6,1%, ИМ – у 4,1% пациентов (табл. 2).
Результаты
При оценке динамики показателей контроля углеводного обмена более чем за 5-летний период наблюдения (2018–01.02.2024) отмечена тенденция к снижению уровня HbA1c с 7,3 до 7,0% (p>0,05) (рис. 6).
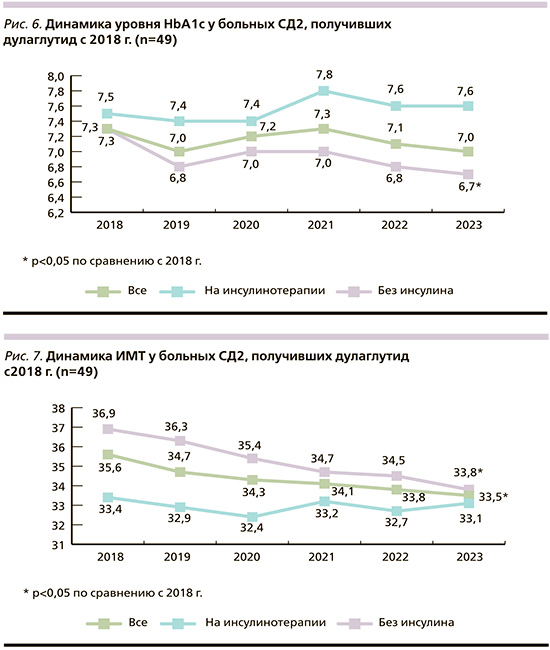
При этом в подгруппе пациентов, не получавших инсулинотерапию, наблюдалось статистически значимое снижение уровня HbA1c (с 7,3 до 6,7%; p=0,04). В подгруппе пациентов на инсулинотерапии статистически значимой динамики уровня HbA1c отмечено не было (рис. 6).
При оценке динамики ИМТ зарегистрировано статистически значимое снижение данного показателя с 35,6 по 33,5 кг/м2 (p<0,05) за период наблюдения (2018–01.02.2024) – в первую очередь за счет пациентов, не использовавших инсулинотерапию (p<0,05). Не было отмечено статистически значимых различий в динамике ИМТ у пациентов на инсулинотерапии (рис. 7).
При этом масса тела пациентов снизилась на 4,5 кг (с 102,9±21,8 до 98,4±19,6).
Обсуждение
Если сопоставить результаты проведенного нами анализа с результатами исследования REWIND, можно отметить, что основные характеристики пациентов значимо различались. Так, пациенты московской популяции были значительно моложе (их средний возраст – 56,3 года, в исследовании REWIND – 66,2 года), имели больший ИМТ, значительно чаще получали препараты инсулина и реже препараты группы СМ. При этом длительность СД и исходный уровень HbA1c пациентов в двух этих исследованиях практически не различались (табл. 3).
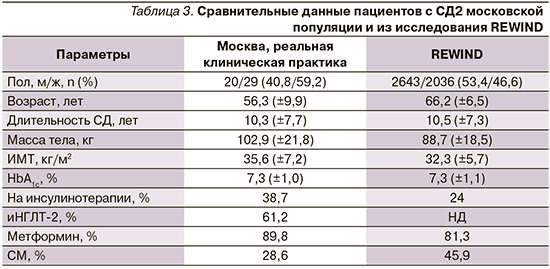
Несмотря на значимые различия, в обоих исследованиях продемонстрирован похожий результат по снижению уровня HbA1c (7,3 до 7,0%) у пациентов, получавших терапию дулаглутидом. Сопоставимой была и динамика снижения массы тела (снижение на 4,5 кг в московской популяции пациентов и на 3,5 кг в исследовании REWIND)(табл. 3).
Заключение
Использование дулаглутида в реальной клинической практике демонстрирует длительное удержание показателей гликемического контроля в рамках целевых значений или близко к ним. При этом бóльшая эффективность в достижении показателей гликемического контроля продемонстрирована в когорте больных СД2, не получавших инсулинотерапии.
При использовании дулаглутида в реальной клинической практике у больных СД2 отмечается выраженная тенденция к снижению массы тела, которая носит статистически значимый характер у пациентов, не получавших инсулинотерапии.



