Введение
Роботическая система daVinci традиционно используется в урологической практике для выполнения радикальной простатэктомии. В некоторых странах удельный вес робот-ассистированных простатэктомий в 2012 г. достиг 80%.
С увеличивающимся опытом использования роботической системы и совершенствованием мастерства хирургов расширяется список операций, осуществляемых с ее помощью. Одним из перспективных направлений применения робота daVinci являются реконструктивно-пластические операции на мочеточниках и мочевом пузыре. Нарушение адекватного пассажа мочи по верхним мочевыводящим путям зачастую вызвано травмой мочеточников различного генеза, в частности ятрогенной. В зависимости от типа, давности нанесения и локализации травмы мочеточника хирургическое лечение варьируется от простого удаления случайно наложенной лигатуры до выполнения уретероцистонеоанастомоза (УЦНА). При локализации повреждения мочеточника ниже места его пересечения с общими подвздошными сосудами, а также при протяженном повреждении тазового отдела мочеточника выполнить уретероуретеростомию технически сложно. В этих случаях показано выполнение УЦНА по той или иной методике. Бурное развитие эндоскопической техники в конце XX в. сделало возможным выполнение УЦНА лапароскопическим доступом, позволяющим значительно снижать риск развития осложнений, ассоциированных с открытыми операциями, и отказаться от выполнения операции Боари в пользу менее травматичного прямого уретероцистоанастомоза. Внедрение роботической системы daVinci (Intuitive Surgical, Inc., Sunnyvale, CA) укрепило позиции лапароскопии в урогинекологической, тазовой и реконструктивной хирур-гии.
В настоящем клиническом наблюдении мы приводим опыт лечения пациентки с ятрогенной травмой левого мочеточника, которой было выполнено оперативное лечение в объеме робот-ассистированной уретероцистонеостомии.
Описание случая
Пациентка Ж. 37 лет в августе 2012 г. по месту жительства перенесла оперативное лечение в объеме лапароскопической резекции яичников, удаления очагов эндометриоза. С 25.09.2012 пациентка стала отмечать боли в левой поясничной области.
05.10.2012 пациентка обратилась в нашу клинику. По данным обследования (физикальное обследование, ультразвуковое исследование мочевыделительной системы) заподозрено наличие обструкции левого мочеточника.
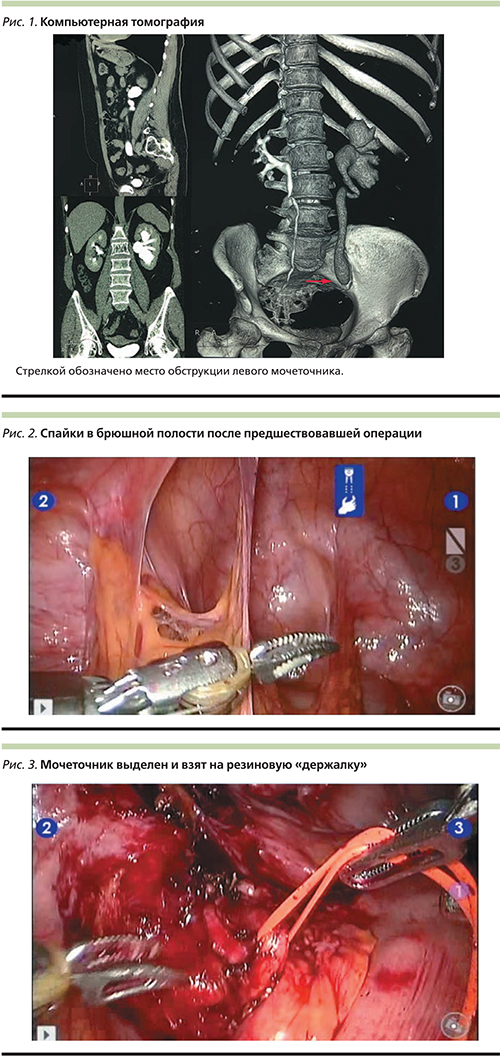
С целью уточнения диагноза пациентке была выполнена компьютерная томография, по данным которой отмечены ретенционные изменения чашечно-лоханочной системы левой почки (лоханка размером 38×25 мм) и левого мочеточника (19 мм) вплоть до перекреста с подвздошными сосудами. Ниже перекреста с подвздошными сосудами определено сужение мочеточника на протяжении около 70 мм, просвет мочеточника сужен до 1–1,5 мм (рис. 1).
08.10.2012 выполнена цистоскопия, попытка дренирования левого мочеточника стентом, не увенчавшаяся успехом ввиду наличия непреодолимого препятствия на расстоянии 7 см от устья мочеточника. Для восстановления оттока мочи из левой почки 08.10.2012 выполнена чрескожная пункционная нефростомия слева.
При повторной госпитализации через месяц выполнено оперативное вмешательство – уретероцистонеостомия с роботической ассистенцией.
Ход операции
Под комбинированной анестезией пациентка помещена в позицию Тренделенбурга с ногами, разведенными до 50–60° и несколько согнутыми в коленях. Интраоперационно мочевой пузырь был дренирован по уретре специально разработанным катетером, предусматривающим возможность орошения слизистой мочеиспускательного канала лекарственными препаратами в послеоперационном периоде [9]. Рабочая консоль робота размещена у ножного конца стола, между ног пациентки. Расположение роботических троакаров следующее: 12-мм порт для камеры помещен по срединной линии на 2 см выше пупка; два 8-мм порта располагаются симметрично, с двух сторон по среднеключичной линии на уровне пупка; третий 8-мм порт помещается контралатерально пораженному мочеточнику на 10 см латеральнее ипсилатерального 8-мм порта. Два порта для ассистента располагаются на стороне операции. 5-мм порт размещается между камерой и 8-мм роботическим портом, а 12-мм порт – сбоку на 3 см выше гребня подвздошной кости.
В брюшной полости имел место спаечный процесс, обусловленный предшествующими операциями. Выполнен адгезиолиз (рис. 2).
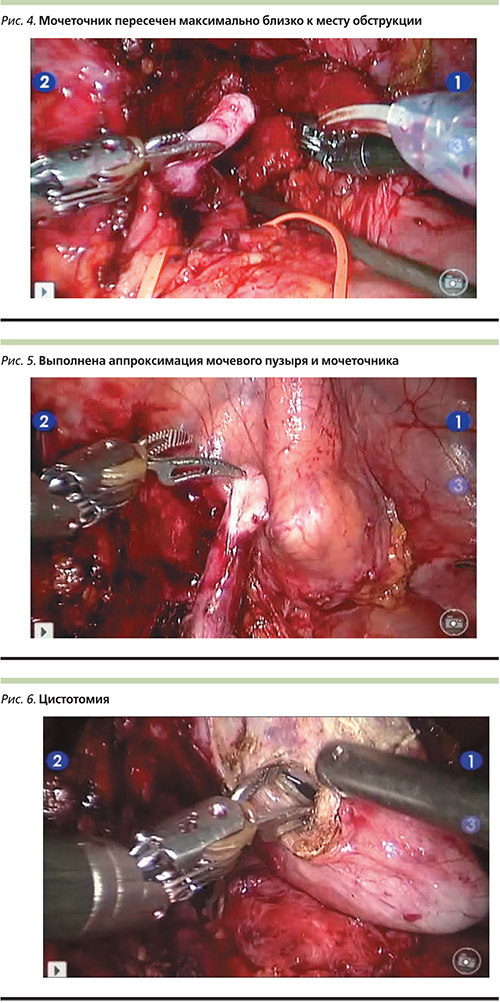
После мобилизации сигмовидной кишки мочеточник выделен в месте пересечения с общими подвздошными сосудами и взят на «держалку», зафиксированную в натянутом положении 4-й роботической «рукой» (рис. 3).
Выполнена мобилизация мочеточника в дистальном направлении, вплоть до места повреждения. Следует отметить, что для осуществления гемостаза помимо прошивания сосудов для экономии времени нами также применялись сосудистые клипы Hem-O-Lock (Hem-o-lok® Polymer Locking Ligation System, Teleflex Inc., Morrisville, US). Мочеточник пересечен максимально близко к стриктуре (рис. 4). Сразу после пересечения мочеточника произведена его спатуляция на 12 часах.
При помощи бужа, проведенного через уретру, определена зона мочевого пузыря, анатомически наиболее близко расположенная к проекции пересеченного мочеточника (рис. 5). Поскольку длины выделенной части мочеточника было достаточно для выполнения анастомоза «без натяжения», дополнительной мобилизации мочевого пузыря не потребовалось. Выполнена цистотомия электорокоагуляцией (рис. 6).
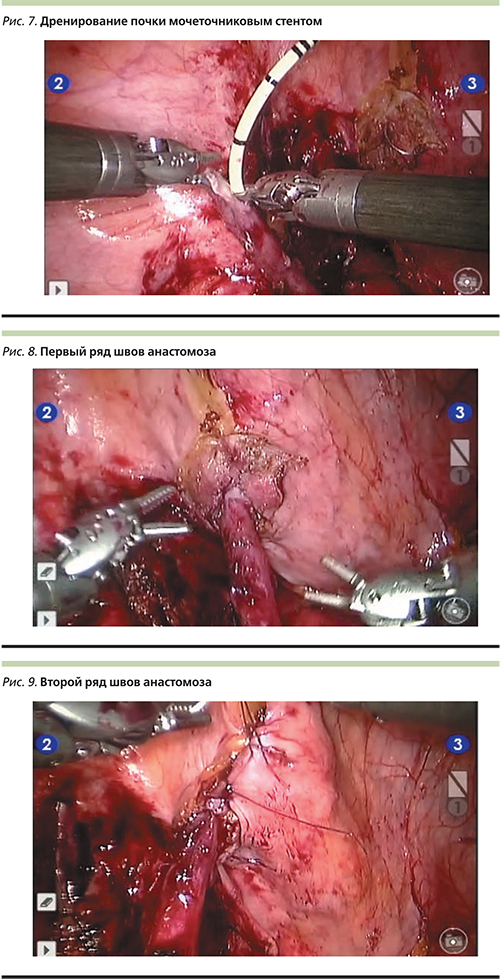
Перед началом формирования анастомоза через мочеточник в почку проведен JJ-стент 6-Ch 26 см (Universa® Soft Ureteral Stent Set, Cook Ireland Ltd., Limerick, Ireland) (рис. 7).
Мочеточник подведен к цистотомическому отверстию, после чего шовным материалом Quill (QUILL™ Knotless Tissue-Closure Device, Surgical Specialties Corporation, Wyomissing, US) выполнен непрерывный шов, соединивший мочевой пузырь и мочеточник (рис. 8).
Далее между серозной оболочкой мочевого пузыря и адвентицией мочеточника наложен второй ряд швов Викрилом 4-0 (Coated VICRYL® (polyglactin 910) Suture Ethicon Endo-Surgery (Europe) GmbH, Johnson & Johnson, Norderstedt, Germany) (рис. 9).
Для проверки герметичности швов мочевой пузырь наполнен 200 мл стерильного физиологического раствора.
Завершающим этапом операции выполнена экстраперитонизация мочеточника и зоны анастомоза отдельными швами из викрила 2-0.
Результаты
Продолжительность операции составила 155 минут. Кровопотеря – 35 мл. Не было отмечено каких-либо осложнений, связанных с анестезией или непосредственно с оперативным вмешательством. Время пребывания в стационаре после операции составило 4 суток.
Уретральный катетер удален по прошествии 2 недель после операции, мочеточниковый стент – через месяц.
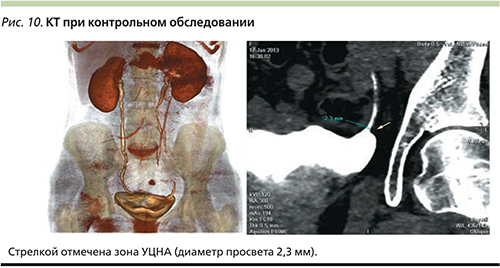
При контрольном обследовании через 6 месяцев отмечается нормальный пассаж мочи по верхним мочевыводящим путям слева, признаков стенозирования уретероцистоанастомоза не выявлено (рис. 10).
Обсуждение
Травма мочеточника – одно из наиболее серьезных осложнений операций на органах малого таза. Несмотря на тот факт, что подобные травмы встречаются не так часто, как повреждение мочевого пузыря или прямой кишки, ранение мочеточника является гораздо более серьезным осложнением и часто ассоциируется со значительным риском для жизни пациента. Это обусловлено высокой вероятностью формирования мочеточниковых свищей, мочевого перитонита, уриномы, острого обструктивного пиелонефрита на стороне поражения с последующей утратой почечной функции [1].
Не существует методов медикаментозного лечения ятрогенной травмы мочеточника. В зависимости от типа, сроков и локализации травмы мочеточника хирургическое лечение варьируется от удаления лигатуры до выполнения уретероцистоанастомоза или лоскутной пластики мочеточника фрагментом мочевого пузыря [2].
С начала XXI в. операционная система daVinci традиционно используется в урологической практике для выполнения радикальной простатэктомии [3]. Так, в 2009 г. из 180 тыс. роботических операций радикальная простатэктомия составила 50%. С приобретением опыта использования роботической системы расширяется и потенциальный список операций, выполняющихся с роботическим ассистированием. Так, уже в 2010 г. из 278 тыс. операций на долю простатэктомии пришлось только 35% вмешательств.
Данные мировой литературы, посвященной реконструктивно-пластическим операциям на верхних мочевых путях с использованием системы daVinci, как правило, ограничиваются описаниями отдельных клинических случаев [4]. Доступные публикации сводятся к описанию серий случаев реимплантации дистального отдела мочеточника в связи с различными состояниями. Так, Megan O. Schimpf и соавт. демонстрируют серию из 11 пациентов обоего пола различных возрастных категорий, которым роботическая уретероцистонеостомия выполнялась как по поводу ятрогенного повреждения дистального отдела мочеточника, так и в связи со стриктурой мочеточника различного генеза, а также раком мочеточника [3]. N.N. Patil и соавт. приводят опыт лечения 12 пациентов, перенесших в различных медицинских центрах роботическую реимплантацию мочеточника [5]. Недавно опубликованное сообщение M. Musch описывает наиболее крупную серию из 16 пациентов, которым проводились различные робот-ассистированные реконструктивные операции на дистальной трети мочеточника. Из них 6 операций были выполнены по методике Боари [6]. Во всех случаях результат операций был вполне удовлетворительным.
Заключение
Робот-ассистированная лапароскопическая методика выполнения прямого уретероцистоанастомоза демонстрирует высокий уровень безопасности и воспроизводимости, а также хорошую эффективность данной операции для больных с нарушением проходимости мочеточника в дистальной трети. Улучшенная 3D-визуализация всех анатомических структур, тщательная и «бережная» диссекция, нивелирование тремора, прецизионное прошивание необходимых структур, минимальная тракция и смещение окружающих органов и тканей, а также эргономичность роботической системы делают ее совершеннее традиционной лапароскопической и открытой методик [7]. Необходимо отметить, что роботическая хирургия не лишена недостатков. К ним можно отнести отсутствие обратной связи, довольно длительный процесс установки консоли пациента, а также высокую стоимость обучения и внедрения роботической техники [8]. Тем не менее, не уступая по своей эффективности традиционной открытой операции, лапароскопическая операция с роботической ассистенцией снижает травматичность вмешательства, позволяет уменьшать риск развития осложнений и сокращать послеоперационное время нахождения пациента в стационаре до нескольких суток, обеспечивая при этом прекрасный косметический эффект.
Работа выполнена при поддержке РНФ, соглашение № 16-15-00233



