Введение
Стрии (striae distensae), широко известные как растяжки, представляют собой линейные участки кожной атрофии, локализующиеся в местах наибольшего растяжения кожи [1]. Распространенность линейных атрофий в популяции варьируется от 50 до 80%, причем у женщин они встречаются вдвое чаще, чем у мужчин [2]. В развитии striae distensae немаловажную роль играет генетическая предрасположенность, о чем свидетельствует выявление стрий у монозиготных близнецов [3].
Как известно, линейные атрофии могут появляться во время беременности (от 43 до 88%), полового созревания (от 6 до 86%), при ожирении, быстром наборе и резком снижении массы тела (43%). [4] Кроме того, стрии наблюдаются при патологических состояниях и заболеваниях – синдроме/болезни Кушинга, синдроме Марфана, хронических заболеваниях печени, а также как побочный эффект, связанный с использованием препаратов определенных фармакологических групп: системных или местных кортикостероидов, противовирусных препаратов группы ингибиторов протеаз (индинавир), контрацептивов, нейролептиков, и др. [2, 4, 5].
Патогенез
На сегодняшний день считается, что в основе патогенеза формирования стрий лежит снижение резистентности кожи к растяжению. Это в первую очередь обусловлено генетической предрасположенностью, гормональным дисбалансом, нарушением структуры соединительной ткани дермы с участием компонентов внеклеточного матрикса [5].
В образцах кожи, взятых из очагов линейных атрофий, наблюдается снижение синтеза фибробластами фибриллина, эластина, фибронектина и коллагена, в то время как способность продуцировать коллагеназу, эластазу и гиалуронидазу остается на прежнем уровне. Основная функция последних заключается в активном разрушении структурных белков, участвующих в поддержании прочности кожи. В связи с этим при избыточном растяжении кожи происходит необратимое разрушение структур сетчатого слоя дермы, при сохранении целостности эпидермиса [6].
Роль гормональных нарушений в патогенезе стрий была продемонстрирована в исследовании R.C. Cordeiro et al. Авторы выявили повышение чувствительности рецепторов к эстрогенам в 2,2 раза, к андрогенам в 1,8, к глюкокортикоидам в 1,7 раза в образцах ткани из пораженной области по сравнению с непораженной кожей. Таким образом, можно предположить, что повышенная чувствительность рецепторов к гормонам в областях с большим механическим растяжением кожи влияет на метаболизм экстрацеллюлярного матрикса, что ведет к формированию стрий [7].
Клиническая картина
Клинически линейные атрофии представлены единичными или множественными полосами, расположенными перпендикулярно линиям натяжения кожи. Так, типичной локализацией стрий у беременных женщин является кожа живота, груди, бедер и ягодиц; у молодых людей они обычно располагаются в области поясницы, коленей и наружных поверхностей бедер, у спортсменов – в областях активного роста мышечной массы [5, 8].
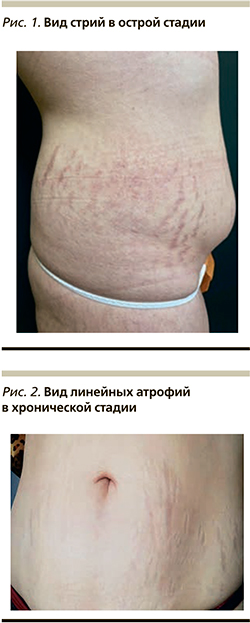
Процесс формирования стрий происходит в три стадии. Острая стадия (striae rubrae) характеризуется наличием параллельных или радиально расходящихся полос буро-красного цвета, которые незначительно возвышаются или располагаются на одном уровне с окружающей кожей (рис. 1). В подострой стадии формирования стрий происходит их уплощение, они приобретают пурпурную окраску. В хронической стадии (striae alba) поврежденные участки кожи имеют вид гипопигментированных западающих очагов серо-белого цвета (рис. 2) [9].
Патоморфология
Первые гистологические описания striae distensae появились в медицинской литературе в 1889 г. Уже тогда было замечено, что с течением времени гистологическая картина линейных атрофий изменяется [2]. На начальном этапе формирования линейных атрофий наблюдается выраженная периваскулярная лимфоцитарная инфильтрация дермы, стойкое расширение сосудов. Коллагеновые и эластические волокна теряют свою извитость, выявляется их очаговое утолщение и множественные поперечные разрывы. Вокруг поврежденных волокон формируются клеточные скопления, представленные преимущественно фибробластами, макрофагами и тучными клетками. Со временем клеточные элементы вытесняются коллагеновыми волокнами, уменьшается количество сосудов, что говорит о постепенной реорганизации структуры соединительной ткани. На данном этапе происходит истончение эпидермиса c потерей сетчатого рисунка. В дерме наблюдается снижение компонентов экстрацеллюлярного матрикса – коллагена, фибронектина, фибриллина и эластина. Тонкие, плотно упакованные коллагеновые пучки располагаются горизонтально и ориентированы параллельно слоям эпидермиса [4].
Лечение
На сегодняшний день все существующие методы коррекции линейных атрофий можно разделить на три группы, исходя из возможности их влияния на определенные звенья патологического процесса (см. таблицу).
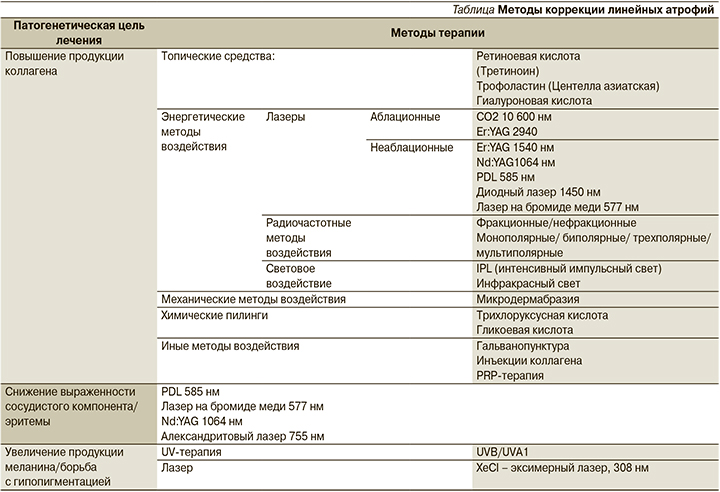
Среди вышеперечисленных подходов к лечению наибольший интерес представляют высокоэнергетические методы воздействия благодаря их высокой результативности и скорости наступления эффекта.
Радиочастотные методики основаны на физическом принципе трансформации электрической энергии в тепловую вследствие высокого сопротивления кожи, что позволяет применять их вне зависимости от фототипа. Целевые участки нагреваются до температуры в 40–42°C, при этом эпидермис остается неповрежденным. Термическое воздействие на уровне дермы и гиподермы вызывает частичную денатурацию эластических и коллагеновых волокон, что приводит к немедленному сокращению тканей, а в дальнейшем стимулирует неоколлагеногенез [10]. В исследовании W. Manuskiatti et al. два независимых эксперта оценили выраженность клинического эффекта после 6 недель лечения с использованием триполярного RF (1 процедура 1 раз в неделю) у 32% пациентов как умеренную (25–50% улучшение), а у 26,5% как высокую (51–75% улучшение), 65% пациентов оценили результаты проведенной терапии как очень высокие [11]. Исследование эффективности фракционного аблационного RF, проведенное V. Mishra et al., продемонстрировало следующие результаты: среднее улучшение по шкале выраженности стрий после 4 процедур с интервалом в 2 недели составило 20%, а по данным опросника, большинство пациентов заявили о хорошем эстетическом эффекте [12]. В одном из исследований авторы предположили, что применение топического третиноина сразу после фракционного RF-воздействия может оказать положительный синергический эффект в виде ускорения синтеза коллагена и повышения активности фибробластов [13].
Одним из наиболее эффективных лазерных методов лечения линейных атрофий является фракционный CO2-лазер (10 600 нм). Излучение с данной длиной волны поглощается всеми водосодержащими структурами тканей, однако благодаря фракционированию луча на множество микролучей вапоризация участков эпидермиса и дермы не приводит к выраженной травматизации. После элиминации некротического дебриса отмечается активная регенерация тканей с ускорением процессов неоколлагеногенеза. Исследование E.I. Crocco et al. продемонстрировало изменение гистологической картины в биоптатах кожи, взятых из очагов линейных атрофий после проведения четырех процедур фракционного фототермолиза. Так, в зонах, подвергнутых лазерному воздействию, отмечалось значительное увеличение количества коллагеновых волокон. Кроме того, не было выявлено различий в содержании коллагена в данных участках по сравнению со здоровой кожей. В то же время проведенное лечение не сопровождалось увеличением количества эластина, что может быть объяснено большей термостабильностью данного белка по сравнению с коллагеном. Результаты лечения через 30 дней после последней процедуры 12 из 13 пациентов оценили как хорошие или очень хорошие [15].
На сегодняшний день аблационный эрбиевый лазер (Er:YAG 2940 нм) широко используется для коррекции линейных атрофий. В ранних исследованиях авторы отметили, что, несмотря на сходство механизмов воздействия, эрбиевый лазер более щадящий по сравнению с CO2-лазером, а также вызывает меньше побочных эффектов в виде болезненных ощущений, эритемы, нарушения пигментации. Однако использование эрбиевого лазера сопровождается менее выраженным клиническим эффектом, в связи с чем требуется проведение большего числа процедур [15]. Эти различия обусловлены тем, что эрбиевый лазер вызывает меньшее термальное повреждение тканей, воздействуя более поверхностно за счет лучшего поглощения молекулами воды (коэффициент абсорбции эрбиевого лазера – 12 тыс., CO2-лазера – 800). Однако по мере совершенствования лазерных аппаратов, их программного обеспечения и техник проведения процедур клинические результаты применения вышеперечисленных методик становятся сопоставимыми. Так, исследование W. Manuskiatti et al. не показало различий в исходах лечения атрофических рубцов с помощью эрбиевого и CO2-лазеров. Стоит отметить, что пациенты испытывали меньше неприятных ощущений во время процедур на стороне, где использовался Er:YAG-лазер [16].
При использовании неаблационных лазерных методик эффект в виде ремоделирования тканей, активации фибробластов и неоколлагеногенеза достигается за счет теплового воздействия на дерму. При данном типе воздействия не происходит повреждения эпидермиса.
Исследование F. de Angelis продемонстрировало высокую эффективность лазера на эрбиевом стекле Er:YAG (1540 нм) в лечении как красных, так и белых стрий. Независимые эксперты отметили улучшение по визуальной шкале оценки в среднем на 51–75%. При гистологическом исследовании тканей, проведенном после курса процедур, выявлено утолщение дермы и эпидермиса, увеличение содержания коллагена и эластина. Кроме того, при осмотре через 24 месяца достигнутый положительный эффект сохранялся у всех пациентов [17].
Эксимерный лазер XeCl (308 нм) используется для восстановления пигментации striae albae. Для достижения видимого эстетического результата требуется несколько процедур. При гистологическом исследовании в местах применения данного лазера отмечается увеличение содержания меланина и гипертрофия меланоцитов, а увеличения компонентов внеклеточного матрикса не происходит. Следует также отметить, что достигнутый клинический эффект имеет нестойкий характер – через 6 месяцев степень пигментации возвращается к исходному уровню [18].
Схожим механизмом действия и эффектами обладает UVB/UVA1-терапия. В исследовании N.S. Sadick et al. репигментация белых стрий отмечалась почти у 100% пациентов после лечения. В то же время через 3 месяца наблюдения только у двух из девяти пациентов сохранялся приемлемый эстетический эффект. Как и при применении эксимерного лазера, использование данной методики не сопровождалось повышением содержания коллагена и эластина в зонах, подвергнутых воздействию [19].
Неодимовый лазер (Nd:YAG 1064 нм) преимущественно используется с целью эстетической коррекции ранних форм стрий (striae rubrae), поскольку имеет аффинитет к нескольким хромофорам: воде, гемоглобину и меланину. Из 20 пациентов с красными стриями, принявших участие в исследовании A. Goldman et al., 16 оценили результаты лечения неодимовым лазером как отличные и хорошие. Кроме того, при использовании Nd:YAG нежелательные побочные эффекты возникают крайне редко, что позволяет использовать данный метод лечения у пациентов с темной кожей. Исследование M.L. Elsaie et al. продемонстрировало, что при воздействии большей энергии хорошо поддаются коррекции и белые стрии (75 Дж/см2 для красных и 100 Дж/см2 для белых стрий), а в биоптатах кожи после лечения выявляется увеличение содержания коллагена и эластина [20, 21].
IPL-терапия – некогерентный нелазерный метод воздействия, физической основой которого является высокоинтенсивный широкополосный свет с различными длинами волн. Исследование E. Hernández-Pérez et al. продемонстрировало высокую эффективность и безопасность IPL с длиной волны 645 нм в коррекции striae alba: у 60% пациентов после проведенного лечения отмечено утолщение ранее атрофичных участков кожи, что было обусловлено активацией синтеза компонентов внеклеточного матрикса. Другое исследование подтвердило возможность применения данного способа лечения для коррекции ранних форм стрий (striae rubrae). Так, использование IPL с длиной волны 590 нм оказалось более эффективным в уменьшении размеров красных стрий по сравнению с длиной волны 650 нм; однако при его использовании чаще отмечались такие побочные эффекты, как эритема и поствоспалительная гиперпигментация [22, 23].
Заключение
Линейные атрофии кожи не оказывают прямого негативного влияния на здоровье человека, но их наличие является косметическим дефектом, способным вызывать значительный психологический дискомфорт и снижать качество жизни пациентов. Несмотря на то что на сегодняшний день существует широкий выбор методов коррекции линейных атрофий, ни один из них не универсален и не может обеспечивать полного и стойкого избавления от данного косметического дефекта. Для достижения хорошего эстетического результата потребуются несколько сеансов процедур, сочетание различных видов аппаратных способов воздействия, а также применение топических средств и инъекционных методик. В связи с этим поиск новых и совершенствование уже существующих способов лечения стрий остаются актуальной проблемой современной эндокринологии, дерматологии и косметологии.



