Введение
Боль в спине (БВС) – одна из наиболее частых причин, по которой пациенты обращаются за медицинской помощью и оформляют больничный лист. Спектр возможных причин БВС очень широк, наиболее часто встречаются боли, связанные с механическим повреждением (ноцицептивные), или неспецифические БВС (порядка 90%), которые считаются относительно доброкачественными. С другой стороны, БВС могут встречаться при тяжелых заболеваниях, имеющих плохой прогноз, например боли при синдроме конского хвоста. Эти боли относятся к т.н. красным флажкам и составляют около 0,00001% (1 на 100 тыс. человек) случаев БВС. Сосредоточившись только на наиболее распространенных и наиболее опасных причинах БВС, медработники упускают значительную часть случаев. По данным некоторых работ, до 30% случаев механических БВС по происхождению суставные, однако при дифференциальной диагностике на них часто не обращают внимания. Например, зачастую не учитываются случаи анкилозирующего спондилита, которые обусловливают 15–30% хронических нерадикулярных БВС [1]. Таким образом, несмотря на кажущуюся тривиальность, задача диагностики и терапии БВС далеко не проста.
При БВС приходится проводить дифференциальный диагноз со множеством состояний: воспалительными и инфекционными заболеваниями, злокачественными новообразованиями, беременностью, травмами, остеопорозом, компрессией нервных корешков, радикулопатией, плексопатией, грыжей диска, дегенеративными заболеваниями и стенозом позвоночного канала, дисфункцией крестцово-подвздошных или фасеточных суставов, и это только часть дифференциального диагноза. Некоторые из причин БВС могут иметь плохой прогноз для выздоровления и жизни пациента. В связи с этим выявление «красных флажков» – симптомов, которые должны настораживать врача, является важным аспектом постановки диагноза.
К ним относят:
- возраст моложе 20 и старше 50 лет;
- быстрое нарастание или повторяющиеся эпизоды интенсивных болей;
- усиление боли в ночное время;
- постоянная интенсивная боль, не зависящая от движения и положения тела;
- прогрессирование неврологического дефицита;
- тазовые расстройства;
- быстрая и значительная потеря веса;
- лихорадка;
- папулезные высыпания и покраснения в области болей (герпетические боли);
- высокое артериальное давление, аритмия, одышка, усиление болей на холоде и при физической нагрузке (характерно для сердечной патологии);
- усиление болей в грудном отделе позвоночника при кашле и дыхании (указывает на легочную патологию);
- связь болей в нижней части спины с приемом пищи и другими диспепсическими явлениями, усиление болей при дефекации и мочеиспускании.
Знание данных «красных флажков» может помочь врачу правильно оценить ситуацию и вовремя выявить тяжелое, иногда угрожающее жизни заболевание.
Дорсалгии
Боли неврологической природы (дорсалгии) составляют большую часть БВС. Они делятся на специфические, включающие ноцицептивные и невропатические боли, связанные с конкретным повреждением (мышц, фасций, сухожилий, остеоартрозом, остеопорозом, сдавлением корешка и т.д.), и неспецифические, не имеющие определенной патологоанатомической причины. Последний вид болей оказывается самым частым [2], в его развитии большую роль играют функциональные и психосоциальные механизмы (например, страх перед движением), а не структурная патология [3].
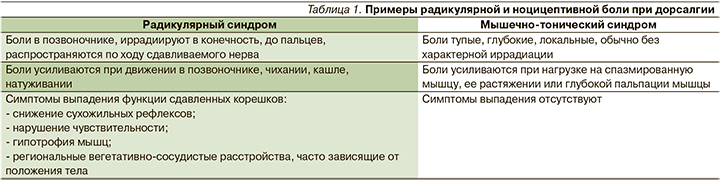
Необходимым шагом в дифференциальной диагностике является выделение ноцицептивного и/или нейропатического (радикулярного) компонента. Для этого можно использовать характерные клинические симптомы, основные из которых представлены в табл. 1. Наличие нейропатичекой боли – это признак повреждения нервных структур, обеспечивающих болевую чувствительность на любом уровне, от периферических нервов до коры головного мозга. Для нейропатической боли свойственны персистирующий характер, большая длительность, многообразие сенсорных проявлений (гиперестезия, гипералгезия, аллодиния, выпадение разных видов чувствительности), сочетание с вегетативными расстройствами (снижение кровотока, гипер- и гипогидроз в болевой области) и двигательными нарушениями [4]. Нейропатическая боль не реагирует на терапию анальгетиками и НПВП и требует отдельного специфического лечения.
Большинство случаев БВС при надлежащем лечении со временем проходят, однако у части пациентов (до 40%) она длится свыше 12 недель, т.е. становится хронической [5, 6]. Следует отметить, что хроническая БВС остается наиболее частой причиной всех хронических болей. Хронизация боли значительно ухудшает прогноз и усложняет лечение, кроме того, она тесно связана с депрессивной симптоматикой [7], которая отмечается у 2/3 пациентов с хронической дорсалгией [8, 9]. Эта взаимосвязь объясняется общими патогенетическими механизмами и нейромедиаторными сдвигами в ЦНС [10]. Становясь хронической, боль часто утрачивает механическую причину и имеет неспецифический характер (дисфункциональная боль). Соответственно, терапия хронического болевого синдрома обязательно должна включать препараты, действующие на центральные механизмы боли и тревожно-депрессивную симптоматику.
Лечение дорсалгий
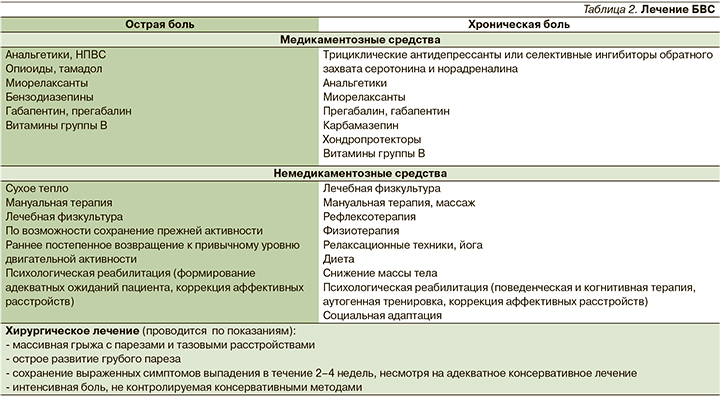
Терапия дорсалгий всегда носит комплексный характер, включает этапы борьбы с острыми приступами болей и поддерживающее, профилактическое лечение, на обоих этапах должны активно применяться как медикаментозные, так и немедикаментозные средства (табл. 2) [11]. Абсолютно доказана необходимость срочного обезболивания пациента во время острой боли: чем раньше начато лечение и быстрее будет достигнут адекватный анальгетический эффект, тем лучше общий прогноз и меньше вероятность хронизации боли.
Фармакотерапия боли должна учитывать длительность и патогенетические механизмы боли (ноцицептивная, невропатическая, дисфункциональная), участие как периферических, так и центральных механизмов, наличие аффективных и невротических расстройств [1].
Нестероидные противовоспалительные препараты (НПВП) считаются лекарственным средством первой линии для уменьшения боли и воспаления у пациентов с хроническими и острыми БВС. К сожалению, эти препараты не лишены недостатков, которые хорошо известны.
Наиболее распространены нежелательные явлений со стороны желудочно-кишечного тракта (ЖКТ) – эпидемиологические исследования показывают, что прием НПВП увеличивает риск серьезных побочных эффектов со стороны ЖКТ более чем в 4 раза, и что на их долю приходится 20–25% всех зарегистрированных случаев побочного действия лекарственных препаратов [12]. К факторам риска НПВП-индуцированных поражений ЖКТ относятся пожилой возраст, высокая доза принимаемого НПВП, связанное с приемом НПВП поражение ЖКТ или язвенная болезнь двенадцатиперстной кишки в анамнезе, одновременный прием глюкокортикостероидов, антикоагулянтов или нескольких НПВП (включая низкие дозы ацетилсалициловой кислоты).
НПВП также могут оказывать негативное влияние на функцию почек и систему кровообращения, что также характерно для лиц пожилого и старческого возраста. К факторам риска почечных и сердечно-сосудистых побочных эффектов НПВП относятся застойная сердечная недостаточность, цирроз печени, гломерулонефрит, гиперкальцемия, обезвоживание. Следует отметить, что у большинства пожилых пациентов с сопутствующей соматической патологией имеется средний или высокий риск развития нежелательных побочных явлений. Поэтому НПВП не рекомендуется применять длительное время и подбор препарата должен осуществляться индивидуально с учетом имеющихся сопутствующих заболеваний.
Как полезное, так и нежелательное действие НПВП основано на ингибировании циклооксигеназы (ЦОГ) с последующим уменьшением синтеза простагландиновых медиаторов боли. Считается, что положительные эффекты в основном опосредованны ингибированием циклооксигеназы-2 (ЦОГ-2), тогда как ряд побочных эффектов, особенно со стороны ЖКТ, в значительной степени опосредован действием на циклооксигеназу-1 (ЦОГ-1) [13]. Соответственно, все НПВП должны ингибировать ЦОГ-2, чтобы оказывать какое-либо влияние на боль и воспалительные процессы. Тем не менее НПВП представляют собой химически разнообразную группу лекарств со значительной неоднородностью по химической структуре, свойствам и селективности действия на ЦОГ-2 по сравнению с ЦОГ-1, причем эту группу нельзя просто разделить дихотомически на селективные или неселективные по отношению к ЦОГ-2, скорее тут имеется плавный переход [14].
ПНВП – селективные ингибиторы ЦОГ-2 (производные сульфонанилидов – нимесулид, оксикамов – мелоксикам и коксибов – целекоксиб, валдекоксиб, эторикоксиб) имеют менее выраженное действие на ЖКТ, чем неселективные.
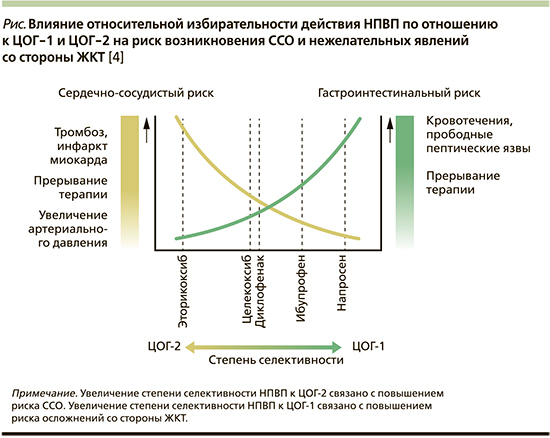
Лекарства с патентованными названиями, оканчивающимися на «коксиб», такие как эторикоксиб или целекоксиб, считаются наиболее избирательными по влиянию на ЦОГ-2. Они были разработаны для снижения токсического действия на ЖКТ, связанного с использованием традиционных НПВП, но следует отметить, что это преимущество зависит от дозы и длительности приема препарата. Селективные НПВП также оказались не идеальными, из их недостатков иногда отмечают более низкий анальгетический эффект и повышенный риск сердечно-сосудистых осложнений (ССО) [3]. На рисунке представлен график влияния селективности НПВП на риск развития нежелательных явлений. Из графика следует, что увеличение селективности к ЦОГ-2 повышает риск ССО, а к ЦОГ-1 – риск осложнений со стороны ЖКТ [15].
Тем не менее результаты большого мета-анализа рандомизированных контролируемых исследований показали, что традиционный неселективный НПВП диклофенак ассоциирован с риском ССО, сравнимым с коксибами, если рассматривать их как общий класс [16]. В связи с этим недавно обновлены руководство, разработанное EMA (Европейским агентством по лекарственным средствам) [17], и рекомендации Европейского общества кардиологов [3]. Теперь в случаях с установленными сердечно-сосудистыми заболеваниями, заболеваниями периферических артерий и/или цереброваскулярным заболеванием для диклофенака (150 мг/сут) приводятся те же противопоказания, что и для селективных ингибиторов ЦОГ-2 [18].
Между препаратами группы коксибов также имеются значительные различия по селективности влияния на ЦОГ-1 и ЦОГ-2: в большинстве исследований целекоксиб обладает таким же соотношением селективности по ЦОГ-2, что и диклофенак [19], а эторикоксиб обычно имеет соотношение на порядок выше in vitro [20].
Эторикоксиб (Аркоксия) наиболее селективен из всех НПВП (соотношение ингибирующей концентрации ЦОГ-1/ЦОГ-2 равняется 344) с хорошими фармакокинетическими параметрами. Он быстро всасывается, и его биодоступность приближается к 100%, пиковая концентрация в крови достигается уже через час, таким образом, действие наступает быстро (уже через 24 минуты), после однократного приема стабильный обезболивающий и противовоспалительный эффект сохраняется в течение суток. Фармакокинетика препарата не зависит от возраста, и коррекции дозы у пожилых людей не требуется, также не имеет влияния прием антацидов. Препарат хорошо проникает через гематоэнцефалический барьер в центральную нервную систему, обеспечивая хорошее обезболивающее действие при приеме 1 раз в сутки [21].
Выраженное анальгетическое действие эторикоксиба подтверждено в ряде сравнительных клинических исследований с неселективными НПВП и другими анальгетиками: эффект минимальной дозы эторикоксиба 60 мг оказался сопоставимым с таковым при использовании диклофенака и ибупрофена пациентами с остеоартритом [22, 23], обезболивающий эффект препарата при радикулярном синдроме был сильнее эффекта трамадола [22].
Касательно безопасности применения, препарат продемонстрировал хорошие показатели. Во-первых, согласно данным мета-анализа 10 международных клинических исследований с участием более 5000 человек, тяжелые осложнения со стороны ЖКТ (перфорация, кровотечения, язвы) при его приеме развивались в 2 раза реже, чем при применении диклофенака, ибупрофена и напроксена [24]. Во-вторых, хотя многочисленные рандомизированные исследования показали, что применение коксибов связано с повышением систолического и диастолического давления (в среднем на 3,85 и 1,06 мм рт.ст. соответственно), серия клинических испытаний больных ревматическими заболеваниями и пациентов с БВС не показали существенного повышения риска ССО на фоне приема эторикоксиба, более того, его применение связано с меньшим риском ССО по сравнению с диклофенаком и ибупрофеном, но он проигрывал напроксену [25]. Тем не менее при назначении препарата пациентам с сердечно-сосудистой патологией необходимо тщательно взвесить все риски.
Заключение
Таким образом, эторикоксиб показал себя эффективным препаратом для купирования острых и хронических болей. При острых болях (постоперационных, травматических) рекомендуемая доза составляет 120 мг – 1 раз в сутки не более 8 дней. При хронических БВС рекомендуемая доза препарата составляет 60 мг/сут. Согласно данным международных исследований и мета-анализа, риск негативного влияния эторикоксиба на ЖКТ ниже, чем у диклофенака, и он сравним с последним по ССО.
Проблема терапии пациентов с БВС состоит в частой хронизации болевого синдрома, резко ухудшающей прогноз выздоровления. Своевременное купирование острой боли и адекватный подбор обезболивающих препаратов позволяют решать этот вопрос более чем половине пациентов. Назначение НПВП, необходимое при острой дорсалгии и часто требующееся в случаях хронической боли, должно осуществляться с учетом не только эффективности, но и безопасности применения препарата, индивидуально для каждого пациента.



