Введение
Дисфункция желчевыводящих путей (ДЖВП) определен а международными экспертами по изучению функциональных заболеваний желудочно-кишечного тракта (ЖКТ) на Римском консенсусе-III в 2006 г. как первичные дискинезии, развившиеся в результате моторно-тонических нарушений желчного пузыря (ЖП), желчных протоков и их сфинктеров, обусловившие нарушение оттока желчи и/или панкреатического секрета в двенадцатиперстную кишку (ДПК) в отсутствие органических препятствий [1].
Основным клиническим симптомом, характеризующим дисфункциональные расстройства билиарного тракта, является абдоминальная боль различной интенсивности: от ощущений дискомфорта до выраженных болей билиарного типа без какой-либо органической патологии, объясняющей ее. Однако, несмотря на современные достижения инструментальной диагностики, установление такой органической причины нередко представляется сложной задачей. Моторнотонические нарушения ЖП и сфинктера Одди (СО) могут иметь вторичный характер, т. е. быть одним из проявлений или осложнений деструктивно-воспалительных поражений билиарного тракта или развиваться на фоне имеющейся патологии органов пищеварения. Диагноз ДЖВП по своей сути – это диагноз исключения, и на любом этапе диагностического поиска при выявлении органической патологии вполне возможно его снятие.
Эпидемиология
С учетом трудности дифференциальной диагностики ДЖВП с органическими изменениями, низкой обращаемости пациентов к врачу и недостаточно внимательного отношения врача общей практики к этой нозологии, а также отсутствия эпидемиологических исследований достоверных данных о распространенности этой патологии нет. Согласно наблюдениям W. Hess, среди лиц с заболеваниями желчевыводящих путей (ЖВП) пациенты с функциональной патологией в целом составляли не более 10 %, пациенты с гипертонусом СО – 0,7 и 2,2 % после операции по поводу желчекаменной болезни – ЖКБ [2]. В последние годы наряду с увеличением заболеваемости органов билиарной системы отмечается рост частоты функциональной патологии ЖП и СО, который в среднем составляет около 15 % всех заболеваний ЖВП. При ультразвуковом исследовании (УЗИ) ЖВП пациентов с абдоминальной болью билиарного типа у 28,3 % из них не было обнаружено признаков воспаления и конкрементов, что может свидетельствовать о функциональном характере боли [3]. ДЖВП встречаются преимущественно среди женщин молодого возраста, астенического телосложения, пониженного питания, с выраженной эмоционально лабильной нервной системой, предъявляющих множество жалоб, как правило, не имеющих четкой связи с приемом пищи, физической нагрузкой, покоем или сном [4].
Классификация
Классификация функциональных расстройств билиарного тракта, согласно Римскому консенсусу-III, выделяет в разделе E “Функциональные заболевания билиарного тракта” следующие варианты:
E1. Функциональное расстройство ЖП.
E2. Функциональное расстройство СО билиарного типа.
Е3. Функциональное расстройство СО панкреатического типа.
Клиническим критерием диагностики является наличие рецидивирующих с различными интервалами (не обязательно ежедневно) эпизодов абдоминальной боли в эпигастрии и/или в правом верхнем квадранте живота длительностью более 30 минут с постоянным уровнем интенсивности во время приступа. Боль способна нарушить повседневную активность и даже привести пациента в отделение неотложной помощи, не уменьшается после стула, при перемене положения тела, после приема антацидов, в отсутствие других структурных заболеваний, которые могли бы объяснить симптоматику. К подтверждающим клиническим критериям ДЖВП относятся следующие симптомы, сопровождающие абдоминальную боль: тошнота или рвота, иррадиация боли в спину и/или правую лопатку и нередко возникновение боли в ночные часы [1]. При функциональных расстройствах ЖП учитываются все вышеперечисленные признаки, которые сочетаются с нормальными показателями активности печеночных ферментов, конъюгированного билирубина и амилазы/липазы.
Функциональные расстройства СО могут встречаться в отсутствие ЖП у пациентов после холецистэктомии. Функциональное расстройство СО билиарного типа характеризуется нормальными показателями амилазы/липазы в сыворотке крови и повышением активности сывороточных трансаминаз, щелочной фосфатазы или конъюгированного билирубина на фоне не менее двух эпизодов боли. Критерием, подтверждающим функциональное расстройство СО панкреатического типа, является повышение уровня амилазы/ липазы сыворотки крови.
Этиопатогенез
Среди множества причин возникновения дисфункциональных расстройств билиарного тракта следует выделить следующие [5]:
- нейрогуморальные нарушения регуляции моторной функции билиарной системы;
- изменения висцеро-висцеральных связей с повышением болевой чувствительности – т. н. гиперсенситивные состояния;
- нарушение тонуса ДПК – кислый химус, дуоденит, язвенная болезнь желудка и ДПК, дуоденальный папиллит, панкреатит, раздражение большого дуоденального сосочка (БДС), спазм СО;
- внутрипротоковая и внутриполостная гипертензия – спазм гладкой мускулатуры стенок ЖКТ, синдром раздраженного кишечника, энтерит с моторными нарушениями;
- состояния после холецистэктомии (ДЖВП развивается у 80 % больных);
- качество и количество пищи, режим питания;
- психоэмоциональное состояние самого пациента, окружающая его обстановка в семье и на работе, особенности воспитания и отношение к своему здоровью.
Как правило, к формированию функциональных нарушений приводит наличие нескольких взаимосвязанных причин.
Диагностика
Диагноз дисфункциональных расстройств желчевыводящей системы основывается на жалобах больного, данных анамнеза, результатов объективного обследования, неинвазивных методов лабораторно-инструментального обследования (биохимического анализа крови, УЗИ с определением диаметра общего печеночного протока, магнитно-резонансной холангиопанкреатографии [МРХПГ], эндоскопической ретроградной панкреатохолангиографии [ЭРХПГ] с манометрией СО, фракционного хроматического дуоденального зондирования, макроскопического и биохимического исследования желчи) [5, 6].
Болевой синдром имеет свои особенности в зависимости от вида функциональных расстройств и чаще всего дает возможность поставить предварительный диагноз уже на этапе сбора анамнеза. Нередко ему сопутствуют многочисленные диспепсические жалобы – чаще всего тошнота, горечь во рту и рвота.
При сборе анамнеза представляется важной оценка болевого синдрома: характер боли (схваткообразная, ноющая, ощущение тяжести в правом подреберье), длительность болевого синдрома, наличие типичной иррадиации, провоцирующих факторов. Целесообразно уточнить, что сопровождает боль, факторы ее усиления и ослабления, наличие психоэмоциональных нагрузок; возраст пациента (у лиц старшего возраста чаще возникают вторичные дискинезии); наличие в прошлом желчных колик.
При оценке объективного статуса необходимо провести оценку симптомов воспаления желчного пузыря (Ортнера, Мерфи, Кера и др).
Комплексный подход к сбору анамнестических данных и результатов объективного обследования позволяет с большой долей вероятности исключить вторичный характер ДЖВП. Среди лабораторно-инструментальных методик следует выделить скрининговые и уточняющие методы. Первая группа методов (биохимические показатели, УЗИ органов брюшной полости, эзофагогастродуоденоскопия с осмотром БДС) на основе исключения позволяет заподозрить органическую патологию, объясняющую клинические симптомы. Вторая группа методов дает возможность детализировать уровень функциональных нарушений и их характер [6]. При проведении диагностического поиска среди пациентов с подозрением на ДЖВП в первую очередь необходимо исключить больных, имеющих симптомы, отражающие воспалительные, деструктивные, неопластические и другие органические изменения (снижение массы тела, повышение температуры, наличие маркеров воспаления в общих анализах крови и мочи, биохимическом анализе сыворотки крови, отсутствие признаков анемии и крови в кале и др.).
Среди биохимических показателей к уточняющим методикам ДЖВП принято относить уровни сывороточных трансаминаз, конъюгированного билирубина, амилазы/липазы. Это дает возможность определить тип дисфункции СО в соответствии с клиническими критериями [1].
Трансабдоминальное УЗИ – самый доступный в практике и важный в диагностическом плане метод исключения органической патологии ЖВП и поджелудочной железы, позволяющий выявлять билирный сладж и конкременты даже небольших размеров. Перспективным представляется внедрение в широкую клиническую практику эндосонографии (эндоУЗИ) – высокочувствительного метода для определения микролитов, особенно в протоках, патологии БДС (стенозирующего папиллита, неопроцесса) и протоковой системы поджелудочной железы.
Фракционное дуоденальное зондирование – достаточно информативный метод функциональных расстройств сфинктерного аппарата ЖВП, кроме того, он дает возможность представлять микроскопические и биохимические характеристики желчи. С целью исключения микролитиаза необходимо проводить микроскопическое исследование пузырной фракции желчи, полученной при дуоденальном зондировании из ДПК или во время ЭРХПГ. Если т. н. рутинные методы диагностики не дают желаемого результата, возможно проведение ЭРХПГ, в т. ч. с анализом желчи и манометрией СО.
При наличии дисфункции СО панкреатического типа целесообразно проведение диагностических мероприятий в следующей последовательности [5]:
- исключение основной этиологии панкреатита (ЖКБ, алкогольного воздействия);
- лабораторная диагностика (печеночные биохимические пробы, панкреатические ферменты);
- инструментальная диагностика (УЗИ органов брюшной полости, эндоУЗИ и/или МРХПГ).
Принципы лечения пациентов с ДЖВП
Что касается выбора лечебной тактики, пациенты с функциональной патологией ЖВП курируются, как правило, амбулаторно. Однако для проведения диагностических мероприятий, дифференциальной диагностики возможна госпитализация в стационар кратковременного пребывания.
Лечение пациентов с билиарной дисфункцией должно быть комплексным, его целями являются купирование боли, восстановление нормального поступления желчи в ДПК, а также профилактика развития и прогрессирования осложнений. В связи с этим необходимо восстанавливать проходимость и сократительные способности ЖВП, нормализовывать химический состав желчи, моторику кишечника и состав его микрофлоры, а также процессы пищеварения. Основными направлениями в купировании билиарной боли как основного симптома ДЖВП является нормализация моторных расстройств ЖВП, снижение висцеральной чувствительности и коррекция механизмов восприятия боли.
Остается актуальным соблюдение общих рекомендаций рационального режима труда и отдыха, дозированных физических нагрузок – желательно под наблюдением специалиста по лечебной физической культуре.
Важными являются рекомендации по лечебному питанию, направленные на регуляцию секреции пищеварительных соков, моторной функции кишечника и нормализации массы тела. Лечебное питание должно быть частым, дробным, с соблюдением режима приема пищи, контроля ее качества и количества.
Медикаментозная терапия ДЖВП независимо от формы должна быть комплексной. Для купирования билиарной боли в настоящее время принято использовать релаксанты гладкой мускулатуры, которые подразделяются на средства миотропного и нейротропного действия (см. рисунок).
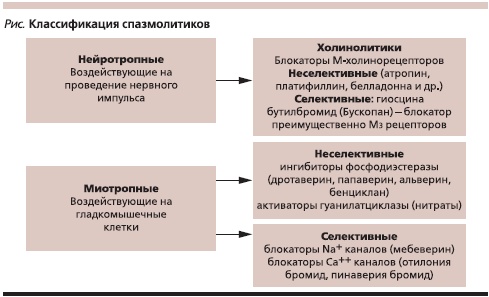
Антихолинергические средства.
К данной группе препаратов относятся широко известные М-холиноблокаторы (препараты красавки, платифиллин, метацин, гиосцина бутилбромид). Особенностью этих препаратов является выраженная индивидуальная зависимость релаксирующего эффекта от исходного тонуса парасимпатической нервной системы и широкий спектр побочных системных эффектов (сухость во рту, нарушение зрения, затруднение мочеиспускания), что значительно ограничивает сферу применения указанных лекарственных средств. Препараты данной группы, за исключением гиосцина бутилбромида, в настоящее время редко используются для лечения функциональных расстройств ЖВП. Именно гиосцина бутилбромид (Бускопан) в настоящее время является препаратом выбора для быстрого устранения боли как основного клинического проявления ДЖВП. Это селективный М-холинолитик, который имеет высокую степень аффинности преимущественно к М3 рецепторам [7], локализованных в гладкомышечных клетках ЖКТ и ЖП, в экзо-/эндокринных железах, в детрусорной мышце мочевого пузыря. Препарат плохо всасывается в желудочно-кишечном тракте: после применения внутрь или ректального применения всасывание препарата составляет 8 % и 3 %, соответственно. Бускопан обладает низкой системной биодоступностью – менее 1 % и поэтому риск развития системных антихолинергических побочных эффектов минимален. После приема внутрь экскреция препарата происходит с калом и мочой. После применения пре-парата внутрь: почечная элиминация составляет от 2 до 5 %, элиминация через кишечник – 90 %. Несмотря на низкую системную биодоступность, гиосцина бутилбромид оказывает локальный спазмолитический эффект (в силу высокой аффинности к мускариновым рецепторам преимущественно 3 типа), а также оказывает ганглиоблокирующее действие путем связывния с никотиновыми рецепторами. Данный нейротропный селективный спазмолитик распределяется главным образом в мышечных клетках органов брюшной полости и малого таза, а также в интрамуральных ганглиях органов брюшной полости. Блокада мускариновых рецепторов на постсинаптических мембранах органов-мишеней приводит к снижению внутриклеточной концентрации ионов кальция и расслаблению мышц. Степень миорелаксации зависит от тонуса парасимпатической нервной системы, что определяет существенные различия индивидуальной эффективности препаратов данной группы.
Так как препарат действует местно, плохо всасывается и не проникает через гематоэнцефалический барьер, частота развития типичных системных антихолинергических (атропиноподобных) нежелательных явлений при использовании гиосцина бутилбромида является низкой и сопоставимой с таковой при использовании плацебо [7].
По данным О.Н. Минушкина и соавт. (2010), отличная и хорошая эффективность гиосцина бутилбромида (Бускопана) при лечении пациентов с дисфункцией билиарного тракта наблюдалась в 91,6 % случаев. Высокая эффективность препарата может быть обусловленной двойным механизмом действия препарата: расслабляющим – на СО и стимулирующим – на моторику ДПК [9].
Блокаторы медленных кальциевых каналов.
Неселективные блокаторы (верапамил, дилтиазем, нифедипин и др.) вызывают релаксацию гладкой мускулатуры, при этом обладая многочисленными кардиоваскулярными эффектами. При их применении происходит закрытие кальциевых каналов клеточных мембран, что мешает входу ионов кальция в цитоплазму и вызывает расслабление гладкой мускулатуры. Для достижения гастроэнтерологических эффектов требуются высокие дозы этих препаратов, что практически исключает их использование.
Селективные блокаторы (пинаверия бромид, отилония бромид) действуют главным образом на уровне толстой кишки. Лишь 10–15 % препарата действуют на уровне билиарного тракта и имеют опосредованные эффекты, связанные с уменьшением внутрипросветного давления, что облегчает пассаж желчи. Пинаверия бромид – это спазмолитик миотропного действия. Препарат избирательно блокирует потенциал-зависимые кальциевые каналы L-типа гладкой мускулатуры кишечника и препятствует избыточному поступлению кальция внутрь клетки. Препарат не обладает антихолинергическим, вазодилататорным и антиаритмическим действиями.
Миотропные спазмолитики (неселективные).
К ним относятся препараты, влияющие на активацию ферментов, ответственных за состояние гладкой мускулатуры в организме (фосфодиэстеразы, гуанилатциклазы): дротаверин, папаверин, метамизол натрия; нитраты. Механизм действия известного в течение многих десятилетий дротаверина основан на подавлении активности фосфодиэстеразы. Данный фермент присутствует в гладкомышечных клетках желчевыводящих и мочевыводящих путей, его блокада дротаверином оказывает спазмолитическое действие. К основным эффектам дротаверина можно отнести противовоспалительный и противоотечный. Препараты для данной группы больных ДЖВП обычно применяют кратковременно для купирования болевого приступа. Механизм действия нитратов (нитроглицерина, изосорбида динитрата и др.) заключается в образовании в гладких мышцах свободных радикалов окиси азота, которые активируют гуанилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Однако в связи с выраженными кардиоваскулярными эффектами и развитием толерантности они мало приемлемы для курсовой терапии ДЖВП.
Миотропные спазмолитики (селективные).
В этой группе наиболее широко применяются в клинической практике мебеверин, альверина цитрат, гимекромон. Мебеверин обладает двойным механизмом действия: снижает проницаемость клеток гладкой мускулатуры для ионов натрия (антиспастический эффект) и ограничивает выход ионов калия из клетки (предотвращение развития гипотонии). Препарат не действует на холинергическую систему. Альверина цитрат – миотропный спазмолитик с папавериноподобным действием, обладает модулирующим эффектом на моторику. Гимекромон – фенольное производное кумарина. Препарат оказывает избирательное спазмолитическое действие на СО и другие сфинктеры ЖВП, усиливая образование и отделение желчи.
С учетом необходимости комплексного подхода к лечению ДЖВП и основных задач лечения в ряде случае целесообразно прибегать к назначению ряда вспомогательных лекарственных средств. Прокинетики (сульпирид, метоклопрамид, домперидон, итоприда гидрохлорид) способствуют нормализации давления в ДПК и улучшению градиента давления в билирном тракте. Желчегонные средства растительного происхождения и/или препараты, содержащие желчные кислоты (препараты урсодезоксихолевой кислоты, настой кукурузных рылец, панкреатин и др.), усиливают моторику ЖП, уменьшают литогенность желчи, улучшают ее отток и нормализуют состояние микробиоценоза кишечника. При наличии сопутствующего синдрома избыточного бактериального роста в кишечнике показано применение кишечных антисептиков (рифаксимина) и пре-/пробиотиков с содержанием бифидои лактобактерий.
Особое внимание заслуживают препараты, уменьшающие висцеральную гиперчувствительность. У пациентов с выраженной висцеральной гиперчувствительностью, психогенными болями целесообразно применять трициклические антидепрессанты (например, амитриптилин). Установлено, что антидепрессанты и нейролептики оказывают влияние на психогенную боль и способны повышать порог висцеральной чувствительности. Влиянием на висцеральную гиперчувствительность обладают также М-холинолитики – гиосцина бутилбромид (Бускопан) и синтетический аналог энкефалина тримебутин [9].
При гипокинетических расстройствах ЖП наряду с прокинетиками, холеретиками и холекинетиками показаны полиферментные препараты. Следует помнить, что наилучшего эффекта можно достичь при применении препаратов панкреатина IV поколения в виде минимикросфер и микротаблеток в дозе 10000/25000 ЕД липазы, особенно при внешнесекреторной недостаточности поджелудочной железы. Ферментные препараты вызывают благоприятную реакцию со стороны поджелудочной железы и в целом положительно влияют на процесс пищеварения.
Профилактика
Среди профилактических мероприятий при ДЖВП наиболее важными представляются следующие: достаточная физическая активность; соблюдение режима питания, включение в рацион продуктов, обладающих желчегонным действием; исключение стрессовых ситуаций, седативная терапия; коррекция избыточной массы тела и гормонального статуса при эндокринной патологии [10].
Прогноз
Больному с ДЖВП необходимо представлять четкую информацию о природе его заболевания, возможных осложнений. Должна быть разработана схема профилактических мероприятий. При проведении своевременной и адекватной терапии прогноз заболевания является благоприятным: функциональные расстройства могут быть полностью устранены. При несвоевременной или неадекватной терапии функциональные расстройства ЖВП при длительном течении могут приводить к развитию органической патологии (бескаменному холециститу, желчекаменной болезни, билиарнозависимому панкреатиту, вторичным изменениям печени, нарушениям полостного пищеварения, атрофическому гастриту, дуоденогастральному рефлюксу и рефлюксгастриту, гастроэзофагеальной рефлюксной болезни на фоне дуоденогастрального и гастроэзофагеального рефлюкса с формированием пищевода Барретта и др.).
Информация об авторах:
Маев Игорь Вениаминович – доктор медицинских наук, профессор, заведующий кафедрой пропедевтики
внутренних болезней и гастроэнтерологии ГОУ ВПО МГМСУ Минздравсоцразвития России.
Тел. 8 (495) 681-22-29; e-mail: proped@mail.ru;
Вьючнова Елена Станиславовна – кандидат медицинских наук, доцент кафедры пропедевтики
и гастроэнтерологии ГОУ ВПО МГМСУ Минздравсоцразвития России.
Тел. 8 (495) 490-18-01; e-mail:es.vyuchnova@gmail.com;
Лебедева Екатерина Геннадиевна – кандидат медицинских наук, доцент кафедры пропедевтики
и гастроэнтерологии ГОУ ВПО МГМСУ Минздравсоцразвития России.
Тел. 8 (495) 490-18-01; e-mail: eg_lebedeva@mail.ru;
Левченко Ольга Борисовна – клинический ординатор кафедры пропедевтики и гастроэнтерологии
ГОУ ВПО МГМСУ Минздравсоцразвития России.
Тел. 8 (495) 490-18-01



