Общие сведения о топических глюкокортикостероидных препаратах
Глюкокортикостероиды (ГКС) представляют собой группу синтетических химических соединений, обладающих свойствами кортикостероидов, вырабатываемых корой надпочечников. Топические ГКС (ТГКС) стали применяться в дерматологии более 60 лет назад и с тех пор служат препаратом первой линии в терапии различных по этиологии и патогенезу неинфекционных дерматозов главным образом благодаря их универсальному механизму действия: иммунодепрессивному, противовоспалительному, антипролиферативному, антиаллергическому и сосудосуживающему. Значительную часть показаний к назначению ТГКС составляют иммуновоспалительные, аллергические, аутоиммунные заболевания кожи. При этом следует отметить, что ТГКС позволяют воздействовать как на раннюю, так и на позднюю фазу воспалительного процесса, что определяет целесообразность их назначения при различных стадиях острых и хронических кожных болезней [1].
Мультипатентный механизм действия ТГКС основан на внутриклеточном взаимодействии активного вещества со стероидчувствительными регуляторными элементами (специализированные ГКС-рецепторы) (см. рисунок).
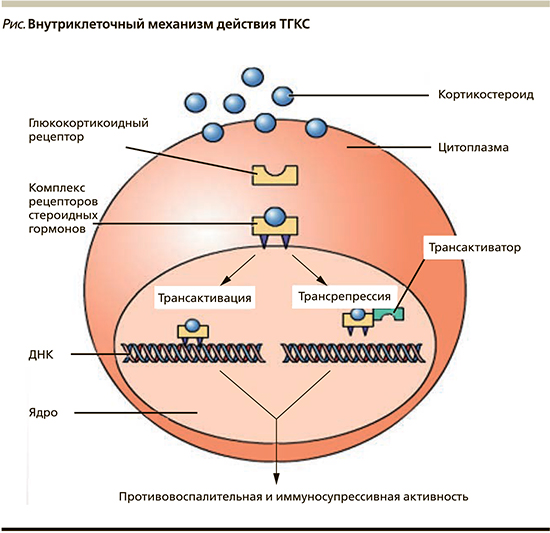
Расположенная в цитозоле клетки α-изоформы ГКС-рецептора связывается с ГКС и перемещается в участок ядерной ДНК, известный как реагирующий на ГКС элемент, в котором данный комплекс способен стимулировать или тормозить транскрипцию соседних генов, тем самым регулируя воспалительный процесс. β-изоформа ГКС-рецептора не связывается с ГКС, но способна связаться с веществом RU-486, обладающим антиглюкокортикостероидной и антипрогестиновой активностью. Данный рецептор способен ослаблять опосредованную лигандом трансактивацию α-изоформой гормон-чувствительных генов и может быть важным маркером нечувствительности к ГКС. Результатом транскрипции РНК на рибосомах является синтез регуляторных белков и подавление выработки ключевых факторов воспаления (простагландинов, тромбоцитактивирующего фактора и лейкотриенов). Помимо активации выше описанных стероидчувствительных рецепторов в реализации механизмов действия ТГКС важную роль играют различные сигнальные молекулы (АР-1, NF-kB и 1-kBx), а также стабилизация клеточных мембран посредством влияния на фосфолипиды [2].
Формирование противовоспалительного эффекта ТГКС происходит за счет вышеописанных механизмов и зависит от клеток-мишеней. Так, противоаллергический эффект обусловлен преимущественно подавлением синтеза цитокинов и хемокинов, участвующих в формировании аллергических реакций, стабилизации мембран тучных клеток, базофилов и эозинофилов. Иммуносупрессивный эффект формируется за счет влияния ТГКС на миграцию иммунокомпетентных клеток в зону воспаления, индукцию апоптоза Т- и В-лимфоцитов, снижение продукции антител и провоспалительных/регуляторных цитокинов (интерлейкина-1 – ИЛ-1, -2, -3, -4, -5, -6, -10, фактора некроза опухоли α, интерферона-γ). Антипролиферативное действие реализуется как в эпидермисе, например при псориазе подавление избыточной пролиферации кератиноцитов, так и в дермальных слоях в виде угнетения синтеза коллагена, мукополисахаридов, снижения миграционной активности клеток, что лежит в основе терапевтического эффекта при очаговой склеродермии, но в то же время может быть причиной формирования атрофии кожи как побочного эффекта применения ТГКС. Сосудосуживающее действие ТГКС, с одной стороны, связано с усилением действия катехоламинов, с другой – с уменьшением образования и выделения в ткани медиаторов воспаления и аллергии [1].
В настоящее время применение ТГКС является ведущим терапевтическим методом лечения ряда иммуноопосредованных дерматозов, связанных с воспалением и зудом. Традиционно используются различные формы ТГКС – мази, кремы, лосьоны, спреи, шампуни. Хотя выбор лекарственной формы препарата зависит от клинической картины и локализации процесса, исследования, сравнивающие формы препаратов и молекулы ТГКС, показали, что мази обладают наибольшей эффективностью по сравнению с кремами и лосьонами [3].
Классификация активности ГКС
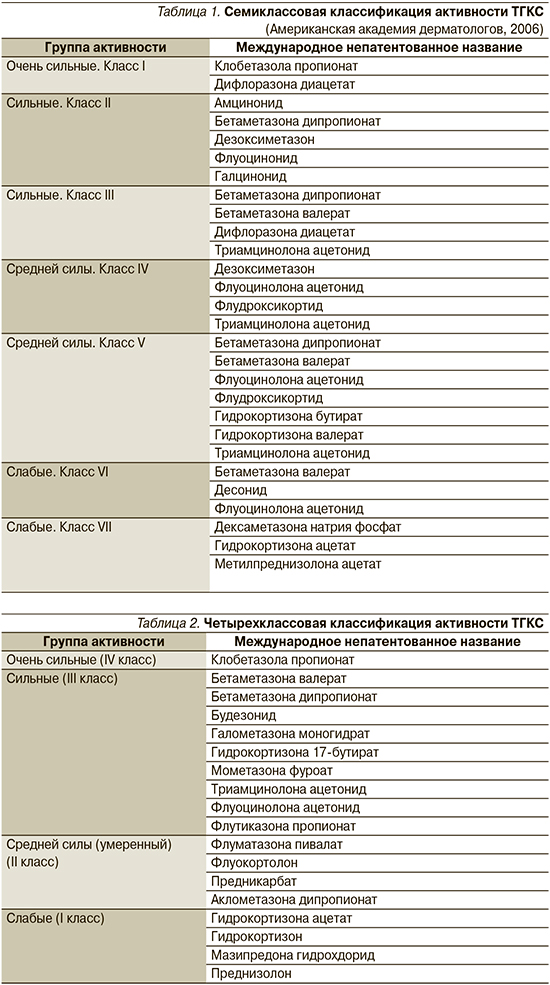
В 1985 г. Стоутон и Корнелл впервые классифицировали активность ГКС в соответствии с их вазоконстриктивными свойствами. На сегодняшний день наиболее используемая в клинической практике американская классификация, в которой принято выделять семь групп ТГКС (табл. 1) [1], в европейских странах рассматривают четыре класса соответственно их силе противовоспалительного действия (табл. 2) [4]. Вне зависимости от классификации клобетазола пропионат является представителем класса сильных ТГКС, при этом по вазоконстрикторному эффекту он в 1800 раз превосходит гидрокортизон [5] и в 3 раза более активен, чем беклометазон-17-дипропионат [6].
Применение ТГКС
Важным аспектом эффективности и безопасности ТГКС считается правильное назначение с учетом факторов, влияющих на время и глубину проникновения препарата в кожу, которое происходит преимущественно трансэпидермально и в меньшей степени через открытые волосяные фолликулы, сальные и потовые железы. При назначении ТГКС практическим врачам необходимо учитывать следующие факторы: со стороны пациента – возраст, локализация процесса, преобладающая клиническая картина; с точки зрения выбора препарата – активность/проникающая способность, лекарственная форма, методика применения.
Возраст пациента, как правило, служит ограничением к применению в детской практике (для различных классов ТГКС различается) или по площади нанесения и длительности курса. Локализация процесса (всасываемость на лице и в складках значительно выше), клиническая картина заболевания, стадия процесса по активности влияют на выбор не только ТГКС, но и лекарственной формы, а например, при фациальной локализации (толщина эпидермиса на щеке – 0,08–0,3 мм, в области век – 0,05–0,15, красной кайме губ – до 0,3 мм) имеется ограничение по длительности применения (не более 2 недель) [7].
В соответствии с общими правилами ТГКС с низкой активностью рекомендуется применять в складках кожи и на лице, а также в отношении младенцев и детей, тогда как ГКС со средней и высокой активностью обычно используются в качестве начальной терапии на всех других участках кожного покрова у взрослых. Суперпотентные ТГКС для достижения более быстрого эффекта в клинической практике в основном используются в качестве стартовой терапии при таких заболеваниях, как хроническая экзема, дискоидная красная волчанка, красный плоский лишай, резистентный атопический дерматит, ладонно-подошвенный псориаз, при заболеваниях, не отвечающих регрессом кожного процесса при использовании ТГКС слабой и средней степеней активности и при ладонно-подошвенной локализации поражений.
Клобетазола пропионат 0,05% в дерматологической практике
В зависимости от конкретной клинической ситуации для врачей-дерматовенерологов одной из главных задач остается правильный выбор адекватного наружного лекарственного средства, обладающего наибольшей эффективностью и меньшим числом побочных эффектов. Представителем наиболее сильного класса ТГКС является 0,05%-ный клобетазола пропионат (Дермовейт, GlaxoSmithKline Pharmaceuticals S.A., Польша). Препарат выпускается в двух формах: крем и мазь. Клобетазол – аналог преднизолона, обладает высокой степенью глюкокортикоидной активности и небольшой минералокортикоидной активностью. Использование клобетазола пропионата, относящегося в группе препаратов очень высокой активности, открывает новые возможности в лечении аллергических, пролиферативных и аутоиммунных заболеваний кожи. Основные показания к применению клобетазола пропионата: псориаз, дискоидная красная волчанка, красный плоский лишай, другие дерматозы при неэффективности ТГКС умеренной и слабой активности. Однако следует иметь в виду, что сверхвысокая сила и активность препарата, особенно при нерациональном использовании, могут быть сопряжены c появлением ряда побочных эффектов. Наиболее часто встречаются следующие побочные эффекты: атрофические изменения кожи (стрии, истончение кожи), расширение поверхностных кровеносных сосудов, нарушения пигментации, гипертрихоз.
При использовании препарата в соответствии с инструкцией угнетение гипоталамо-гипофизарно-надпочечниковой системы наблюдается крайне редко – с частотой менее 1 случая на 10 тыс. пациентов.
Рациональное использование лекарственного средства, адекватная длительность терапии, а также частота и методика нанесения препарата имеют большое значение в предотвращении развития местных и системных побочных эффектов. Так, в соответствии с инструкцией крем/мазь следует наносить на пораженные участки кожи тонким слоем 1–2 раза в сутки до наступления улучшения. При этом следует также отметить, что лечение более 4 недель подряд не рекомендуется в связи с потенциальной возможностью препарата подавлять ось гипоталамус–гипофиз–надпочечник. Кроме того, при использовании препарат не должен попадать в глаза. Следует ограничивать применение данного препарата, как и других сильных местных ГКС, в области лица, подмышечных впадинах и паховой области. Основные противопоказания к применению клобетазола пропионата: акне, розацеа, периоральный дерматит, перианальный и генитальный зуд, первичные инфекции кожи вирусной, бактериальной и грибковой этиологии, а также возраст до 1 года.
На сегодняшний день накоплен большой клинический опыт по применению клобетазола пропионата 0,05% в лечении заболеваний кожи. Эффективность клобетазола пропионата 0,05% при псориазе подтверждена многочисленными научными публикациями и многолетним клиническим опытом [5, 8–10].
Следует упомянуть многоцентровое двойное слепое исследование C. Jacobson et al. в котором сравнивалась эффективность двух местных ГКС-препаратов – мази клобетазола пропионата 0,05% и мази бетаметазона дипропионата 0,05% – для 130 пациентов с тяжелым и среднетяжелым течением псориаза. Лекарственные средства применялись 2 раза в сутки в течение 2 недель. Оба препарата хорошо переносились пациентами, однако клобетазол оказался статистически более эффективным и при его применении была зафиксирована более длительная ремиссия (p<0,001) [5]. По нашим наблюдениям, основное показание к применению клобетазола пропионата при псориазе – это стартовая терапия при ладонно-подошвенном псориазе, в т.ч. пустулезном, а также при псориазе волосистой части головы.
Еще одно показание к применению высокоактивных ТГКС – атопический дерматит, при котором применение клобетозола пропионата вкладывается в концепцию терапии «по нисходящей». В сравнительном исследовании (16 мужчин и 14 женщин; средний возраст – 24 года; возрастной диапазон от 18 до 71 года) эффективности различных ТГКС и ингибиторов кальциневрина при атопическом дерматите применяли четыре различных средства, ежедневно наносимых в течение 2 недель на каждое поражение, за исключением лица и кожи головы: эмолент, пимекролимус 1%, дипропионат бетаметазона 0,05% и клобетазола пропионат 0,05% в объеме 30 мкл на применение (примерно 1,5–2,0 мг/см2) без окклюзии. Наибольшее снижение трансэпидермальной потери воды на 15-й день наблюдалось с клобетазолом (75,5%), за которым следовали бетаметазон (66,7%), пимекролимус (39,6%) и эмолент (29,8%). Все препараты, включая эмолент, показали значительное улучшение в оценках эффективности после 2 недель ежедневного применения. Тем не менее только ТГКС показали нормализацию аберрантных иммунных и барьерных тканевых реакций (эпидермальная гиперплазия и терминальная дифференцировка) в пораженной коже по сравнению с минимальными изменениями при применении эмолента и пимекролимуса. Кроме того, местные ГКС (в частности, клобетазола пропионат) способствовали достижению значительного клинического улучшения по сравнению с эмолентом и пимекролимусом, уровни клеточных инфильтратов и цитокинов (ИЛ-13, -22 и S100As) снизились только под действием ГКС. Уменьшение трансэпидермальной потери воды коррелировало с изменениями в отношении гиперплазии, инфильтрации и маркеров дифференцировки [11]. Авторы сделали выводы: ТГКС, в частности клобетазола пропионат, не только купируют воспаление, но и восстанавливают барьерную функцию кожи при атопическом дерматите.
Особый интерес представляют данные по применению клобетазола пропионата в терапии экземы. Так, исследование H. Moller et al. было сфокусировано на минимизации объема терапии с целью предотвращения развития тахифилаксии у пациентов с хронической экземой кистей. В данном исследовании принял участие 61 пациент с длительностью заболевания более 6 месяцев. В качестве терапии использовался 0,05%-ный крем клобетазола пропионата 2 раза в сутки в течение 21 дня. Значительное клиническое улучшение отметили 50 (82%) пациентов к 14-му дню и 55 (90%) – к концу 3-й недели лечения. Следующий этап исследования подразумевал участие последних в двойном слепом рандомизированном сравнении 0,05%-ного крема клобетазола с кремом флупреднидена ацетата, применяемых 2 раза в неделю в поддерживающем режиме в среднем в течение 138 дней (55–193 дня). У 46 пациентов, завершивших исследование, в 70% случаев на руке, на которую наносился клобетазол, рецидива экземы не наблюдалось. Для пациентов с отмеченными рецидивами среднее время до обострения составило 66 дней на стороне, где применялся клобетазол, и 36 – на стороне, где при лечении был использован флупредниден [12].
В статье C.L. Goh et al. сопоставляется эффективность двух лекарственных препаратов: крема мометазона фуроата 0,1%, применяемого 1 раз в сутки, и крема клобетазола пропионата 0,05%, используемого 2 раза в сутки на протяжении 3 недель. В исследование были включены 60 пациентов с хронической экземой кистей и стоп средней и тяжелой степенями тяжести. Учитывались клинические проявления в виде эритемы, шелушения и зуда как до, так и после терапии. После 3 недель лечения отмечено уменьшение выраженности клинических проявлений при использовании обоих препаратов, однако в случае применения клобетазола пропионата достигался статистически более значимый эффект в виде полного регресса очагов [13].
В работе Д.К. Нажмутдиновой представлены результаты собственных сравнительных исследований по изучению эффективности лечения больных красным плоским лишаем клобетазола пропионатом и бетаметазона валератом и показано преимущество использования клобетазола пропионата [14].
Актуальна последовательная схема применения клобетазола пропионата и ингибиторов кальциневрина, в т.ч. в детской практике. По нашим данным, эта комбинация оправдала себя при атопическом дерматите, псориазе и очаговой склеродермии. Так, в статье K. Anderson et al. [15] приводятся данные об эффективности применения клобетазола пропионата 0,05% лицами женского пола (возраст от 2 до 10 лет) с диагнозом «склероатрофический лихен аногенитальной и экстрагенитальной областей». Проводимая терапия включила применение 0,05%-ной мази клобетазола пропионата, которая ежедневно 2 раза в сутки наносилась на очаги, расположенные в области слизистых оболочек и гладкой кожи. После достижения клинического улучшения переходили на следующую схему: мазь такролимус 0,1% 1 раз в сутки в будние дни и мазь клобетазола пропионат 0,05% 2 раза в сутки в выходные дни. После достижения клинической ремиссии применение мази клобетазола пропионата 0,05% полностью прекращали, а поддерживающую терапию проводили с использованием мази такролимус 0,1% только в выходные дни. Эффективность комбинированного метода составила 93% (клиническая ремиссия) и 7% (значительное улучшение). При возникновении рецидива или усилении существующих симптомов заболевания пациентам рекомендовалось либо вновь начать применение, либо увеличить использование клобетазола пропионата. Данная схема помимо улучшения клинического течения заболевания способствовала уменьшению побочных эффектов ТГКС, включавших телеангиэктазии и атрофию кожи.
В исследовании V. Madan et al. показана более высокая эффективность комбинированного применения клобетазола пропионата и ингибиторов кальциневрина по сравнению с монотерапией ТГКС и такролимусом пациентами с дискоидной красной волчанкой [16].
Вопросы безопасного применения таких высокоактивных ТГКС, как клобетазола пропионат, весьма актуальны. В исследовании G.A. Sara et al. была проанализирована безопасность клобетазола пропионата 0,05% в форме мази для пациентов с тяжелым атопическим дерматитом [17]. В исследование были включены 25 пациентов с тяжелой формой атопического дерматита в возрасте от 18 лет до 71 года. В первый день пациентам 1–2 раза на всю поверхность тела (исключая лицо и гениталии) было нанесено 20–30 г клобетазола пропионата 0,05%. На второй день были оценены сывороточные уровни клобетазола и кортизола. У всех пациентов в сыворотке крови был обнаружен клобетазол и у почти всех (96%) – снижение уровня кортизола. При этом различия в степени супрессии надпочечников и площади поражения кожи (BSA – Body Surface Area) были незначительными в случае одно- или двукратной аппликации. Авторы сделали вывод: клобетазол пропионат даже после применения 20–30 г подвергается системной абсорбции и может вызывать подавление функции коры надпочечников. В то же время, по данным других авторов, использование клобетазола пропионата 2 раза в сутки на протяжении 28 дней приводило к истончению кожных покровов, но через 28 дней толщина эпидермально-дермального слоя восстанавливалась [18]. В другом исследовании применение клобетазола пропионата 1 раз в сутки в течение 3 дней на здоровой коже добровольцев видимых клинических отклонений и изменения трансэпидермальной потери воды не вызывало [19]. Эти данные свидетельствуют о необходимости соблюдать осторожность при применении клобетазола пропионата, особенно в детской практике и длительными курсами [20]. Так, по нашим данным, длительность курса не должна превышать 4 недель (за исключением аутоиммунных заболеваний, где оправдан более длительный курс), площадь, на которую максимально возможно нанесение препарата, не должна превышать 20% поверхности тела, а максимальная еженедельная доза не должна превышать 50 г/нед.
Выводы
На сегодняшний день, обладая выраженным противовоспалительным, противоаллергическим, сосудосуживающим и противозудным действиями, ТГКС позволяют достигать клинически значимого результата при многих неинфекционных заболеваниях кожи, что делает их препаратом первого выбора. В качестве начальной терапии для достижения более быстрого эффекта в клинической практике, как правило, используются суперпотентные ТГКС, например клобетазола пропионат, обладающие мощным противовоспалительным потенциалом, способные в максимально короткие сроки эффективно купировать иммуновоспалительные процессы в коже. Однако при применении данных препаратов следует учитывать возможность развития побочных эффектов, которые могут быть выражены в различной степени. Побочные эффекты, как правило, служат проявлением собственно глюкокортикоидного действия лекарственных средств, но в степени, превышающей терапевтическую. При соблюдении необходимых мер предосторожности, правильном подборе дозы, кратности и длительности применения, а также постоянном наблюдении за ходом лечения частоту развития побочных эффектов можно значительно снизить.



