Андрогены (мужские половые гормоны) физиологически необходимы клеткам предстательной железы (ПЖ) для роста, функционирования и пролиферации. С другой стороны, тестостерон, который сам по себе не является туморогенным, представляет собой фактор, необходимый для роста и размножения опухолевых клеток ПЖ [1]. Наибольшее количество андрогенов вырабатывается в организме мужчины
в яичках, однако биосинтез 5–10 % этих гормонов происходит в надпочечниках. Интенсивность секреции тестостерона находится под контролем гипоталамо-гипофизарной системы. В гипоталамусе происходит выработка рилизинг-гормона лютеинизирующего гормона (ЛГРГ), который стимулирует секрецию ЛГ и фолликулостимулирующего гормона (ФСГ) передней долей гипофиза. ЛГ стимулирует выработку тестостерона в клетках Лейдига яичек. Поступая внутрь клеток ПЖ, тестостерон превращается в 5α-дигидротестостерон, который по активности в 10 раз превосходит его. Тестостерон, продолжающий вместе с другими андрогенами циркулировать в крови, по механизму отрицательной обратной связи тормозит секрецию ЛГРГ в гипоталамусе.
Если клетка ПЖ лишается андрогенной стимуляции, она подвергается апоптозу (запрограммированная смерть клетки). Любое лечение, в результате которого происходит подавление активности андрогенов, называется андроген-депривационной терапией (АДТ). В 1941 г. Huggins и Hodges описали влияние хирургической кастрации и применения эстрогенов на прогрессирование метастатического рака ПЖ (РПЖ) [2]. С тех пор АДТ является стандартом лечения распространенного РПЖ. В последующие годы гормональную терапию (ГТ) стали применять на более ранних стадиях РПЖ
(без метастазов), при развитии рецидива болезни после первичного лечения и даже в качестве монотерапии или одного из звеньев мультимодального лечения [3]. В рамках данной статьи мы остановимся на наиболее дискутабельных вопросах ГТ РПЖ.
Методы АДТ
Андрогенная депривация может достигаться двумя методами. Это, во-первых, угнетение секреции андрогенов яичками путем хирургической или медикаментозной кастрации, во-вторых, блокада связывания циркулирующих андрогенов с их рецепторами – антиандрогенная терапия. Использование двух этих методов (сочетание хирургической или медикаментозной кастрации с терапией антиандрогенами) известно под термином “максимальная андрогенная блокада” (МАБ).
1. Снижение концентрации тестостерона (кастрация):
Билатеральная орхидэктомия (хирургическое удаление яичек) – легковыполнимая хирургическая манипуляция, проводимая даже под местной анестезией. При ее применении быстро (через 12 часов) достигается кастрационный уровень тестостерона, однако данный метод является необратимым видом ГТ, оказывающим негативный психологический эффект на пациента.
Эстрогенотерапия – кастрационный эффект осуществляется за счет нескольких механизмов: подавления секреции ЛГРГ, инактивации андрогенов, прямого подавления функции клеток Лейдига; в экспериментах описано также прямое цитотоксическое действие эстрогенов на клетки ПЖ. К побочным эффектам эстрогенотерапии относится выраженная кардиотоксичность, поэтому в настоящее время применение эстрогенов в качестве первой линии ГТ при РПЖ не рекомендуется.
Аналоги (агонисты) ЛГРГ (лейпрорелин, гозерелин, бусерелин, трипторелин) используются в терапии
РПЖ уже более 15 лет и представляю наиболее распространенный вид ГТ. Являются синтетическими аналогами природного ЛГРГ, обычно применяются в виде депо-форм с продолжительностью действия 1–6 месяцев. Изначально аналоги ЛГРГ стимулируют рецепторы гипофиза, что приводит к временному повышению концентраций ЛГ и ФСГ с временным повышением уровня тестостерона (феномен вспышки). Активность различных агонистов ЛГРГ неодинакова. В настоящее время принято считать,
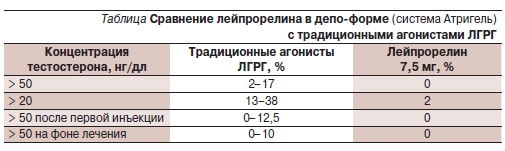
что достижение оптимальных результатов их применения возможно только при снижении уровня тестостерона < 20 нг/дл. При использовании традиционных форм агонистов ЛГРГ концентрация тестостерона > 20 нг/дл выявляется в 18–38 % случаев, тогда как при применении специальной системы доставки лейпрорелина Атригель (биодеградирующий полимерный матрикс) в составе препарата Элигард превышение целевой концентрации тестостерона в 20 нг/дл наблюдается лишь среди 2 % пациентов (см. таблицу) [4].
Антагонисты ЛГРГ – в противоположность агонистам ЛГРГ антагонисты конкурентно связываются с рецепторами ЛГРГ на питуицитах, что приводит к немедленному снижению секреции ЛГ, ФСГ и тестостерона без развития феномена вспышки. Представителем данной группы является абареликс.
При прямом сравнении абареликса и лейпрорелина в исследовании III фазы не отмечено существенных различий в группах больных РПЖ между средними значениями концентраций тестостерона и простат-специфического антигена (ПСА) [5].
2. Антиандрогенная терапия:
Препараты данной группы подразделяются по химической структуре на:
• стероидные антиандрогены (ципротерона ацетат, мегестрола ацетат), не должны назначаться в качестве монотерапии [6];
• нестероидные антиандрогены (нилутамид, флутамид, бикалутамид).
ГТ перед хирургическим лечением РПЖ
Теоретически проведение ГТ перед хирургическим лечением должно способствовать уменьшению размеров опухоли. С целью изучения этого вопроса на базе отделения урологии РОНЦ им. Н.Н. Блохина было проведено исследование, в котором анализировались результаты лечения 386 больных локализованным и местнораспространенным РПЖ, подвергнутых радикальной простатэктомии.
Медиана возраста составила 61,0 ± 6,4 (43–74) года (моложе 60 лет – 40,4 %, 60 лет и старше – 59,6 %), медиана концентрации ПСА до начала лечения – 10,3 ± 12,4 нг/мл (< 10 нг/мл – 48,1 %, ≥ 10 нг/мл – 51,9 %). Отдаленных метастазов ни в одном случае выявлено не было. Во всех наблюдениях до начала лечения верифицирована аденокарцинома (< 7 баллов по Глисону – 71,76 %, ≥ 7 баллов – 28,24 % пациентов). Всем 386 больным выполнена радикальная позадилонная простатэктомия
(с неоадъювантной ГТ агонистами ЛГРГ – 16,1 %). По результатам исследования не выявлена взаимосвязь между проведением предоперационной андрогенной аблации и местной распространенностью аденокарциномы ПЖ (экстракапсулярная экстензия, инвазия семенных пузырьков и вовлечение регионарных лимфоузлов в опухолевый процесс) [7]. По данным ряда авторов, неоадъювантная ГТ снижает частоту выявления опухолевых клеток по краю операционного разреза [8]. Эти данные не нашли подтверждения в нашем исследовании. В завершенных рандомизированных исследованиях и крупном мета-анализе андрогенная аблация перед радикальной простатэктомией не улучшала безрецидивную и общую выживаемость пациентов [9]. Аналогично в нашей серии наблюде-
ний неоадъювантная ГТ агонистами ЛГРГ не влияла на отдаленные результаты хирургического лечения РПЖ (р = 0,944).
ГТ и лучевое лечение при РПЖ
Дистанционная лучевая терапия наряду с хирургическим подходом является радикальным методом лечения локализованного и местнораспространенного РПЖ.
В каких же случаях больные получат преимущество при добавлении АДТ к лучевому лечению? В первую очередь это пациенты с высоким риском развития рецидива заболевания (высокий уровень [> 20 нг/мл] ПСА до начала лечения, низкодифференцированные опухоли). В подобных случаях ГТ начинается перед курсом облучения, продолжаясь во время лучевой терапии и в течение 6 месяцев после ее окончания. Данный подход обеспечивает увеличение как беспрогрессивной, так и общей выживаемости пациентов [10]. При местнораспространенных стадиях заболевания (Т3-4N0М0) сопутствующая и адъювантная ГТ общей продолжительностью 3 года обе
спечивает повышение общей выживаемости [11].
В группе больных очень высокого риска развития рецидива РПЖ (с наличием метастатического поражения регионарных лимфатических узлов) лучевая терапия в сочетании с немедленной долгосрочной АДТ является строго рекомендованным методом лечения, поскольку подобный подход приводит к увеличению общей, опухолево-специфической и безметастатической выживаемости [12].
ГТ при метастатическом РПЖ
ГТ диссеминированного РПЖ является сегодня, по мнению Американского (AUA) и Европейского
(EAU) обществ урологов, стандартом лечения пациентов этой категории. Однако остается ряд дискуссионных вопросов, по поводу которых в мировом научном сообществе нет единого мнения, а именно: сравнение немедленной и отсроченной ГТ, целесообразность добавления антиандрогенов
к кастрационной терапии, возможность применения интермиттирующего режима ГТ.
В настоящее время монотерапия агонистами ЛГРГ является “золотым” стандартом ГТ распространенного РПЖ. Медикаментозная кастрация – привлекательная альтернатива хирургической, поскольку изменения гормонального профиля обратимы, нет хирургических осложнений и моральной травматизации пациента. Равная эффективность данного режима ГТ и хирургической кастрации доказана в 6 рандомизированных исследованиях, частота объективных ответов при ее применении достигает 80–90 %, а время до прогрессирования – 12–33 месяцев.
Однако, хотя гормональная АДТ является сегодня стандартом терапии метастатического РПЖ, по сути
своей это паллиативный метод лечения, который не оказывает значимого влияния на общую выживаемость пациентов. Кроме того, данный вид терапии ассоциирован с рядом нежелательных явлений, таких как импотенция, приливы, остеопения, анемия, гинекомастия, кардиоваскулярная и
гастроинтестинальная токсичность, тромбоэмболия легочной артерии. Это диктует необходимость оптимизации гормональной АДТ с целью улучшения качества жизни больных. В качестве возможных вариантов рассматривают отсроченное ГТ, уменьшение количества назначаемых препаратов и/или
длительности терапии.
РПЖ является относительно медленнопрогрессирующим заболеванием, вследствие чего у пациентов с бессимптомным течением метастатического процесса возможна отсрочка начала ГТ до появления жалоб. Еще до широкого внедрения в клиническую практику определения ПСА при РПЖ было проведено 4 рандомизированных исследования (VACURG I, VACURG II, MRC, ECOG 7887) по сравнению c
немедленной и отсроченной ГТ. Три из указанных исследований были включены в крупный мета-анализ Agency for Health Care Policy and Research (AHCPR) [13], показавший, что немедленное начало ГТ может замедлить прогрессирование заболевания, уменьшать частоту осложнений при распространенном РПЖ (компрессия спинного мозга, патологические переломы, обструкция мочеточников). Однако немедленная ГТ не улучшает опухолево-специфической выживаемости, обеспечивая лишь небольшое
преимущество в общей выживаемости (абсолютное уменьшение риска смерти на 5,5 % после 10 лет наблюдения). В прошлом году были опубликованы результаты исследования EORTC 30891 [14], в котором при сравнении немедленной и отложенной ГТ определение ПСА позволяло более точно контролировать течение заболевания. Медиана наблюдения составила 12,9 года, при этом отсроченное лечение потребовалось более 52 % пациентов. Было показано, что немедленная ГТ действительно обеспечивает небольшое преимущество в общей выживаемости пациентов с распространенным РПЖ, однако отсутствует преимущество в опухолево-специфической выживаемости. Авторы выделили группу пациентов, которые действительно получат преимущество от немедленного начала ГТ – это молодые мужчины (< 60 лет) с высокими значениями ПСА (> 50 нг/мл) на момент установки диагноза.
Таким образом, согласно результатам крупных рандомизированных исследований, немедленная ГТ достоверно, но незначительно увеличивает общую выживаемость, достоверно снижает риск развития осложнений опухолевого процесса, ассоциирована с увеличением частоты развития нежелательных
явлений, но увеличивает стоимость лечения. Исходя из всего вышеперечисленного, имеющейся доказательной базы недостаточно, чтобы рекомендовать немедленную ГТ как стандарт лечения метастатического ПЖ.
Следующий вопрос – целесообразность добавления антиандрогенов к проводимой кастрационной терапии, т. е. проведения МАБ. Обоснованием усиления проводимого режима лечения с помощью добавления антиандрогенной терапии является тот факт, что местом выработки 5 % мужских половых гормонов является ткань надпочечников. Проводимая кастрационная терапия направлена на прекращение секреции тестостерона гонадами, однако никак не влияет на функцию надпочечников. Дополнительный блок андрогеногенеза в надпочечниках может повысить эффективность про-
водимой ГТ распространенного РПЖ. Оценка ГТ в режиме МАБ по сравнению с кастрационной монотерапией проводилась в ряде работ. Согласно мета-анализу [15], объединившему результаты 26 рандомизированных исследований, важную роль играет тип используемого антиандрогена. Так,
добавление к кастрационному лечению стероидных антиандрогенов приводит к снижению показателей выживаемости по сравнению с монотерапией. Напротив, проведение ГТ в режиме
МАБ с применением нестероидных антиандрогенов (в частности, 50 мг бикалутамида) снижает риск смерти на 20 % при сроках наблюдения более 5 лет. Обратной стороной медали в данном случае является повышение токсичности проводимого лечения (в основном за счет нежелательных явлений со стороны желудочно-кишечного тракта и печени), что увеличивает риск отмены терапии в 2–6 раз.
Важным показанием к использованию антиандрогенов в ГТ распространенного РПЖ является подавление феномена вспышки, описанного Dijkman и соавт. (1995). После первой инъекции агониста ЛГРГ в течение 10–14 суток происходит гиперстимуляция рецепторов ЛГРГ, что вызывает следующий каскад реакций: гиперстимуляцию рецепторов ЛГРГ → гиперсекрецию ЛГ → гиперсекрецию тестостерона в яичках → увеличение интенсивности симптомов РПЖ. В данном случае назначение на 10–14 суток нестероидных антиандрогенов, которые блокируют повышенную выработку тестостерона в гонадах, позволяет избегать усугубления проявлений заболевания.
Применение антиандрогенов также возможно при проведении второй линии ГТ, целью которой является отсрочка начала химиотерапевтического лечения за счет увеличения беспрогрессивной выживаемости. Согласно рекомендациям EAU, добавление антиандрогенов к проводимой
кастрационной терапии приводит значимому снижению уровня ПСА (> 50 %) на срок 4–6 месяцев у 60 % пациентов. При регистрации неэффективности ГТ в режиме МАБ (повторный рост ПСА) рекомендована замена одного нестероидного антиандрогена на другой, что также позволяет добиваться снижения уровня ПСА приблизительно 60 % больных. К сожалению, данная манипуляция со сменой препарата для антиандрогенной терапии теряет свою эффективность спустя 4–6 месяцев. В дальнейшем отмена антиандрогенной терапии также способна приводить к улучшению состояния 30–40 % пациентов на срок до 6 месяцев.
Большой интерес вызывает и возможность применения интермиттирующего режима ГТ при распространенном РПЖ. Проведено более 10 рандомизированных исследований III фазы, оценивающих возможность данного подхода. Дизайн исследований был схожим: в них включали как первичных пациентов с вновь установленным диагнозом диссеминированного РПЖ, так и больных с рецидивами после лечения по поводу локализованного и местнораспространенного рака (после лучевой терапии и радикальной простатэктомии). На первом этапе всем пациентам проведен индукционный курс в режиме МАБ в течение 6 месяцев. Затем больные, у которых уровень ПСА снизился < 4 нг/мл и/или более чем на 90 % от исходного уровня, были рандомизированы
в две группы: постоянной и интермиттирующей терапии. Пациенты 1-й группы продолжали получать лечение в режиме МАБ, больные 2-й группы находились без лечения. ГТ по схеме МАБ возобновлялась при концентрации ПСА > 10 нг/мл. По результатам проведенных исследований оказалось, что интермиттирующая АДТ обеспечивает общую выживаемость, равную таковой при постоянном режиме терапии, характеризуясь лучшим качеством жизни в периоды без лечения. По данным исследования SEUG 9401 (2009) [16], у больных группы интермиттирующего режима реже развивались такие нежелательные явления, как приливы, гинекомастия, головная боль, кожная сыпь. В периоды
без лечения восстанавливалась сексуальная активность в 30 % случаев. Установлено, что критериями неблагоприятного прогноза ПСА-ответа на индукционную ГТ (18–37 % пациентов) являются исходный высокий уровень ПСА, показатель Глисона ≥ 7 баллов, категория M+ (наличие ≥ 6 метастатических очагов).
При проведении ГТ в интермиттирующем режиме не выявлено увеличения гормонально-чувствительного статуса, не получено данных на увеличение специфической выживаемости. Применение интермиттирующего режима не ухудшало результатов лечения пациентов с рецидивами заболевания после предыдущего радикального хирургического [17] или лучевого лечения [18] по сравнению с постоянной терапией, при этом выраженность побочных эффектов достоверно реже
регистрировалась в группе прерывистой терапии. С экономической точки зрения интермиттирующий режим выглядит предпочтительней, поскольку в среднем около 50 % времени при прерывистом режиме пациент не получает терапию, за счет чего снижается его стоимость. В экспериментальных
моделях было, что прерывистая терапия замедляет развитие рефрактерности к кастрации.
Таким образом, кандидатами на проведение интермиттирующей ГТ являются хорошо информированные и готовые к регулярным обследованиям пациенты, у которых подтверждено наличие местнораспространенного или диссеминированного РПЖ с минимальным количеством метастазов (категория М+ без костных метастазов или с единичными очагами в костях), относительно низким уровнем ПСА до начала лечения (< 100 нг/мл), у которых после проведения индукционного курса в течение 6–9 месяцев зарегистрировано выраженное снижение уровня ПСА (< 4 нг/мл у пациентов с метастазами, < 0,5 нг/мл у пациентов с рецидивами заболевания).
Можно ли улучшить качество интермиттирующей ГТ? Было показано, что препараты группы ингибиторов 5α-редуктазы увеличивают периоды без лечения. Согласно ретроспективным данным Bruchovsky и соавт. (1998), финастерид удваивает интервалы между лечебными курсами. В пилотном проспективном исследовании Scholz (2006) [19] использование финастерида в периоды без специфического лечения больных, получающих интермиттирующую ГТ, также удваивало продолжительность этих интервалов, при этом восстанавливалась чувствительность к повторной ГТ. В
настоящее время проводится рандомизированное исследование (AVIASDUT 104923) [20], в котором сравниваются результаты интермитирующей ГТ в сочетании с плацебо или дутастеридом в периоды вне специфического лечения.
Подводя итог, следует сказать, что немедленное начало ГТ целесообразно для пациентов с симптомным, агрессивным течением РПЖ, значительной распространенностью патологического процесса, низким риском смерти от других причин. Пациентам с медленным прогрессированием опухолевого процесса и высоким риском смерти от сопутствующих заболеваний назначение немедленной ГТ нецелесообразно. МАБ с включением нестероидных антиандрогенов достоверно, но незначительно увеличивает общую выживаемость больных распространенным РПЖ по сравнению с кастрационной терапией, однако реализуется это преимущество только при продолжительных сроках наблюдения (5 лет и более). МАБ увеличивает частоту нежелательных явлений и риск отмены терапии из-за повышения токсичности. Поэтому ГТ в режиме МАБ не рекомендуется к рутинному использованию при распространенном РПЖ. Интермиттирующая ГТ сегодня больше не является экспериментальным методом лечения и может быть рекомендована больным без прогрессирования на этапе индукции, с адекватным ответом ПСА на индукционный курс (< 4 нг/мл при распространенном РПЖ, < 0,5 нг/мл
при рецидивах после хирургического лечения). С осторожностью следует применять данный подход к пациентам с потенциально низким ожидаемым ответом на лечение, т. е. при ПСА >100 нг/мл до начала терапии, при значительной распространенности опухолевого процесса.



