Обоснование
Средняя продолжительность жизни растет последние 100 лет. С конца 2021 до конца 2022 г. ожидаемая продолжительность жизни женщин выросла примерно на 2 года и уже удалось вернуться к значениям до пандемии новой коронавирусной инфекции. При этом одна из приоритетных задач в мире и нашей стране – увеличение средней продолжительности жизни более 80 лет. Достигнуть эту цель планируется к 2030 г. Кроме общей продолжительности жизни имеет значение и еще один фактор – показатель здоровья. В России его впервые рассчитали в 2019 г., и он составил 60,3, в 2020 г. – 58,9 года. Таким образом, современная женщина более трети своей жизни проживает в состоянии постменопаузы, ассоциированной с проявлениями вульвовагинальной атрофии.
Вульвовагинальная атрофия (ВВА) является распространенным и малоизученным состоянием, связанным со снижением эстрогенизации тканей половых органов [1]. Это хроническое прогрессирующее заболевание, поражающее женские половые органы и нижние мочевыводящие пути. Его вызывает снижение уровня гормонов после наступления менопаузы или в некоторых случаях после хирургического или фармакологического вмешательства. В 2014 г. на консенсусной конференции экспертов с участием Международного общества изучения сексуального здоровья женщин (ISSWSH) и Североамериканского общества менопаузы (NAMS) [2] предложена новая номенклатура. С того момента термины «вульвовагинальная атрофия» и «атрофический вагинит» заменены на генитоуринарный синдром менопаузы, который считается более точным и всеобъемлющим, т.к. включает изменения со стороны не только половых органов, но и нижнего мочевого тракта женщин, эпителий которого эстрогензависим. Среди женщин в постменопаузе распространенность этого синдрома оценивается как минимум в 50%, но некоторые исследования описывают даже 80% женщин в менопаузе, жалующихся по крайней мере на один симптом, относящийся к этому синдрому [3]. В дополнение сообщается, что ВВА является основным фактором ухудшения качества жизни пациенток с раком молочной железы (РМЖ), а также является побочным эффектом адъювантной химиотерапии [4].
Несмотря на частоту встречаемости ВВА, плохая осведомленность врачей об этом заболевании и тенденция рассматривать ее симптомы как часть нормального процесса старения [5] приводят к значительной недооценке реальной распространенности этого синдрома. В исследованиях, изучающих влияние генитальных расстройств среди женщин с ВВА, сообщалось о жалобах на нарушения сексуальной жизни, негативных последствиях для отношений и брака, снижение качества жизни, самооценки и социальных взаимодействий [6]. Более того, с учетом увеличения среднего возраста женщин легко увидеть, что атрофия влагалища представляет собой серьезную проблему для здоровья.
Наиболее распространенным симптомом ВВА является сухость влагалища (от 5 до 83% женщин в постменопаузе в зависимости от исследования) [6, 7], за которой следуют диспареуния (38–59%) и раздражение влагалища (37–77%) [5, 8]. С другой стороны, мочевые симптомы включают императивные позывы, учащенное мочеиспускание, недержание мочи, дизурию и рецидивирующие инфекции мочевыводящих путей [9]. Больные РМЖ сообщают о тех же генитальных симптомах, но усугубляющихся следующим фактором: их онкологическое заболевание и получаемая терапия обусловливают менопаузальные жалобы в более молодом возрасте, что оказывает большое влияние на качество жизни [4].
Патогенез этих нарушений основан на снижении уровня эстрогенов, вызванном наступлением менопаузы и адъювантной терапией пациентов с РМЖ. Гипоэстрогения приводит к истончению вагинального эпителия, снижению активности фибробластов и продукции коллагена, уровня гликогена, как следствие – к повышению рН влагалища и нарушению микробиома [10].
ВВА – хроническое прогрессирующее состояние, требующее длительного, зачастую пожизненного лечения, при прекращении которого симптомы имеют тенденцию к повторному появлению [11]. Терапия первой линии при более легких симптомах включает вульварные и вагинальные лубриканты и увлажняющие средства [12]. Терапия низкими дозами вагинальных эстрогенов является предпочтительным фармакологическим выбором, если пациентки с симптомами не реагируют на безрецептурную терапию [13].
Для пациенток, перенесших РМЖ, существуют ограничения в устранении симптомов ВВА с помощью локальных эстрогенов, и обычные методы лечения включают вагинальные увлажнители и лубриканты, которые обеспечивают временное облегчение [14].
Физические методы лечения ВВА, такие как вагинальная лазерная терапия и динамическая квадриполярная радиочастотная терапия, представляют собой неинвазивные немедикаментозные варианты второй линии, особенно полезные для женщин, которые не реагируют и/или не соблюдают режим лечения локальными и системными эстрогенами, а также для тех, у кого есть противопоказания к гормональной терапии. В связи с этим использование новых технологий становится все более популярным и актуальным в последние годы [15].
Радиочастота (RF), используемая в медицинских процедурах, – это передовая технология, основанная на прео-бразовании электромагнитной волны в тепло: радиоволны взаимодействуют с тканями кожи, вызывая контролируемые термические изменения. В отличие от лазеров, которые производят тепло посредством селективного воздействия на определенный хромофор, неаблативная радиочастота его генерирует в результате сопротивления тканей движению электронов, подверженных полю воздействия радиочастоты. В результате воздействия динамической квадриполярной радиочастоты (ДКРЧ™) происходят поэтапное накопление тепла с повышением температуры до 40–43°С с микроповреждением белковых структур подслизистого слоя (эластина, коллагена), активация резервных капилляров и улучшение васкуляризации тканей вульвы и влагалища, а также активация фибробластов и образование новых молодых коллагеновых и эластиновых волокон. Наряду с тепловым эффектом радиоволн отмечают и нетепловой, или «осцилляторный», – совокупность изменений в организме, вызванных воздействием переменного электромагнитного поля с заряженными частицами биологических тканей, к числу которых относятся молекулы воды, происходит активация молекул свободной и гидратной воды, что в свою очередь вызывает пространственные изменения в молекулах коллагена, он становится более гидратированным и упорядоченным, согласно силовым линиям электромагнитного поля. Этот эффект лежит в основе визуального лифтинга тканей.
Терапия с использованием технологии ДКРЧТМ проводится на аппарате EVA™ (Novavision, Италия), который представляет собой первое в мире мультиполярное радиоволновое устройство, зарегистрированное для использования в гинекологии. Отличительной особенностью данного прибора является ряд встроенных запатентованных технологий, которые позволяют проводить вагинальные и вульварные процедуры с высокой эффективностью и безопасностью:
- • ДКРЧ™ – динамическая квадриполярная радиочастота основана на попеременной работе 4 электродов, испускающих и принимающих волну в динамической конфигурации 1 против 3, с рабочим циклом в 5 секунд, что гарантирует безопасность и эффективность процедуры;
- • VDR™ – вагинальная динамическая радиочастота: динамический квадриполярный режим радиочастоты при работе вагинальной насадки с частотой 1–1,3 MHz, для обеспечения фокусного воздействия без потери энергии;
- • RSS™ – радиочастотная система безопасности включает встроенные в насадки датчики контроля температуры и движения, а также кнопку биологической обратной связи;
- • UPR™ – ультраимпульсная радиопорация, технология, основанная на адаптации частоты радиоволн, открывающая водные каналы клеток для улучшения проникновения активных ингредиентов и обеспечения их таргетной трасслизистой и трансдермальной доставки (например, производных гиалуроновой кислоты, эстрогенсодержащих препаратов, глюкокортикостероидов и т.д.).
Цель исследования: оценка эффективности и безопасности применения ДКРЧТМ терапии в лечении ВВА у женщин в постменопаузе.
Методы
Группы наблюдения составили женщины в постменопаузе, обратившиеся для терапии симптомов ВВА, прошедшие обследование и соответствующие критериям включения/исключения. В исследование были включены 180 женщин. Средний возраст пациенток составил 52±4,3 года.
Пациентки были распределены в три группы:
- • 1-я группа – 60 женщин, проведено 4 сеанса радиочастотного воздействия с помощью ДКРЧТМ на аппарате EVA™ (Novaclinical, Италия) влагалищной и вульварной насадками 4 процедуры с интервалом 14–16 дней. Параметры воздействия: время воздействия влагалищной насадкой – 15 минут, время воздействия вульварной насадкой – 10 минут, температура нагрева тканей – 38–42°С, частота – 1–1,3 МГц;
- • 2-я группа – 58 женщин, проведено 4 сеанса радиочастотного воздействия на аппарате EVA™ (Novaclinical, Италия) влагалищной и вульварной насадками, 4 процедуры с интервалом 14–16 дней в режиме радиопорации с кремом эстриол 0,5 мг. Параметры воздействия: время воздействия влагалищной насадкой – 15 минут, время воздействия вульварной насадкой 10 минут, температура нагрева тканей – 38–42°С, частота – 1–1,3 МГц;
- • 3-я группа – 62 женщины, локально применявшие крем с эстриолом 0,5 мг по схеме ежедневно 2 недели, далее 2 раза в неделю до 8 недель.
Критерии включения: возраст пациенток – 45–65 лет, менопауза в течение 12 месяцев, подписанное информированное согласие. Критерии исключения: новообразования в области воздействия, беременность, инфекции, передаваемые половым путем, генитальный герпес, острые воспалительные заболевания, лихорадка, татуировка или татуаж в обрабатываемой области в течение 3 недель после нанесения, наличие металлических имплантов в обрабатываемой области, нарушение целостности кожи в зоне воздействия радиоволн, тяжелая соматическая патология (эпилепсия, декомпенсированные болезни сердечно-сосудистой системы, сахарный диабет и др.), психические заболевания, трудности коммуникации, прием антикоагулянтов, низкая чувствительность к теплу/боли.
Полученные данные обработаны в программе StatSoft Statistica 10.0.1011 Eneterpise (IBM, США). Для клинических данных каждой из групп проведено сравнение параметров после лечения (каждая из 5 временных точек) с нулевой временнóй точкой с использованием парного и непарного теста Манна–Уитни. Изменение клинических параметров для каждой группы в каждой временнóй точке относительно нулевой точки проверено на равенство нулю с использованием теста Стьюдента. Сравнение изменений клинических параметров 1-й и 2-й групп с контрольной группой в каждой временнóй точке проведено с использованием теста Манна–Уитни. Статистически значимыми различия признавались при p<0,05.
Проспективное интервенционное исследование проводилось на базе отделения эстетической гинекологии и реабилитации ФГБУ НМИЦ АГП им. В.И. Кулакова. Все пациентки дали добровольное письменное информированное согласие на их участие в исследовании. Исследование проводилось с декабря 2019 по январь 2022 г.
Всем пациенткам перед началом терапии выполнен комплекс стандартного обследования, включивший сбор анамнеза, физикальное и лабораторное обследования, ультразвуковое исследование органов малого таза, мазок на флору из половых путей (C, V, U) и мазок на онкоцитологию.
Также всем включенным в исследование пациенткам проведены следующие специальные методы обследования в 6 точках (до начала лечение и через 1, 3, 6, 9 и 12 месяцев после лечения):
- • подсчет индекса вагинального здоровья;
- • исследование сексуальной функции: анкеты и опросники – Индекс женской сексуальной функции FSFI (Female Sexual Function Index) и анкета шкалы вульвовагинальных симптомов VSQ (Vulvovaginal Symptoms Questionnaire), ВАШ (визуальная аналоговая шкала) удовлетворенности внешним видом вульвы;
- • пробы Вальсальвы и кашлевая;
- • степень опущения и/или выпадения по POP-Q;
- • перинеометрия (оценка тонуса мышц тазового дна).
В рамках ответов на анкету FSFI пациентка оценивает качество своей сексуальной жизни на протяжении последних 4 недель. Полученный индекс позволяет проводить оценку состояния сексуальной функции в баллах с учетом 6 основных ее составляющих: наличие полового влечения, степень чувствительности и возбудимости, а также удовлетворенности сексуальной жизнью, интенсивность лубрикации (увлажнения), оргазмичность, выраженность коитального/посткоитального дискомфорта и боли. Анкета включает 19 вопросов. Максимальная оценка составляет 63 балла, минимальная – 2. Снижение индекса ниже 26,55 балла свидетельствует о признаке сексуальной дисфункции.
Опросник VSQ, разработанный в 2013 г. E.A. Erekson et al. в Йельском университете (США), предназначен для заполнения пациенткой и состоит из 21 вопроса для изучения вульвовагинальных симптомов (зуд, боль, жжение, сухость), влияния данных симптомов на эмоциональное состояние женщины, качество жизни и сексуальные отношения. Максимальное число баллов по VSQ – 20, что соответствует выраженному атрофическому процессу, имеющему непосредственное влияние на качество жизни пациентки.
В работе подтверждены безопасность и эффективность процедур ДКРЧТМ в течение 12-месячного периода наблюдения после окончания сеансов лечения. Показано, что показатели индекса вагинального здоровья, значения pH влагалища, удовлетворенность внешним видом вульвы и индекса женской сексуальной функции (FSFI) быстро улучшились, достигнув почти нормального уровня.
Все пациентки подписали добровольное информированное согласие на участие в исследовании; исследование соответствовало требованиям Хельсинкской декларации, Международной конференции по гармонизации (ICF), Стандартов надлежащей клинической практики (GCP), ФЗ «Об основах охраны здоровья граждан в Российской Федерации» № 323-ФЗ от 21.11.2011. Исследование одобрено Комитетом по биоэтике ФГБУ НМИЦ АГП.
Полученные данные были обработаны в программе StatSoft Statistica 10.0.1011 Eneterpise (IBM, США). Для клинических данных каждой из групп произведено сравнение параметров после лечения (каждая из 5 временных точек) с нулевой временнóй точкой с использованием парного и непарного тестов Манна–Уитни. Изменение клинических параметров для каждой группы в каждой временнóй точке относительно нулевой точки проверено на равенство нулю с использованием теста Стьюдента. Сравнение изменения клинических параметров 1-й и 2-й групп с контрольной группой в каждой временнóй точке произведено с использованием теста Манна–Уитни. Статистически значимыми отличия признавались при p<0,05.
Результаты
После 12 месяцев наблюдения за пациентками трех групп выполнен углубленный анализ полученных результатов. Во всех группах были получены статистически значимые результаты, указывающие на успешность проводимой терапии для коррекции симптомов ВВА (рис. 1–3; табл. 1–3). Оценка эффективности выполненного лечения проводилась на основании оценки индекса вагинального здоровья, pH-метрии влагалища, оценки сексуальной функции и качества жизни по данным анкетирования с помощью FSFI, анкеты шкалы вульвовагинальных симптомов (VSQ) и оценки удовлетворённости внешним видом вульвы (ВАШ) через 1, 3, 6, 9, 12 месяцев после проведенного лечения.
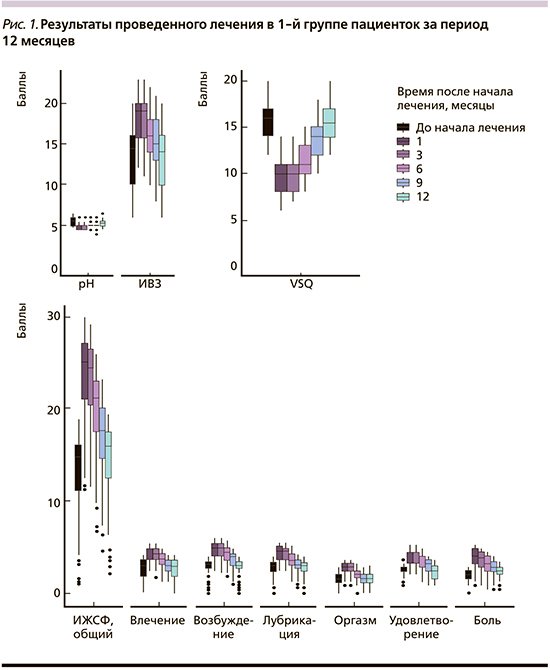
При анализе результатов исследования выявлено статистически значимое снижение степени тяжести симптомов ВВА через месяц после лечения во всех группах.
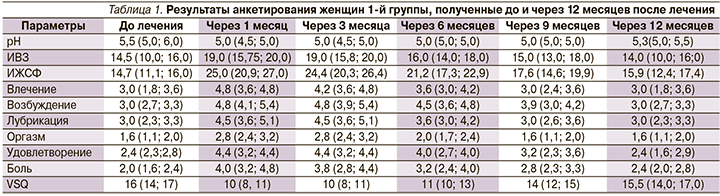
В 1-й группе отмечено повышение среднего индекса вагинального здоровья у 40 (67%) женщин от 21,3 до 23,1 балла (р<0,001), снижение среднего значения pH влагалища у 39 (65%) женщин от 6,8 до 4,9 (р<0,001), увеличение средних значений удовлетворенности внешним видом вульвы у 48 (80%) пациенток по ВАШ от 6,5 до 9,2 балла (р<0,001). По данным анкетирования, увеличение индекса женской сексуальной функции (FSFI) по следующим показателям: влечение на 13% (р<0,001), возбуждение на 23% (р<0,001), лубрикация на 30% (р<0,001), оргазмичность на 25% (р<0,001), удовлетворенность на 39% (р<0,001), снижение диспареунии на 25% (р<0,001). Результаты отображены на рис. 1 и в табл. 1.
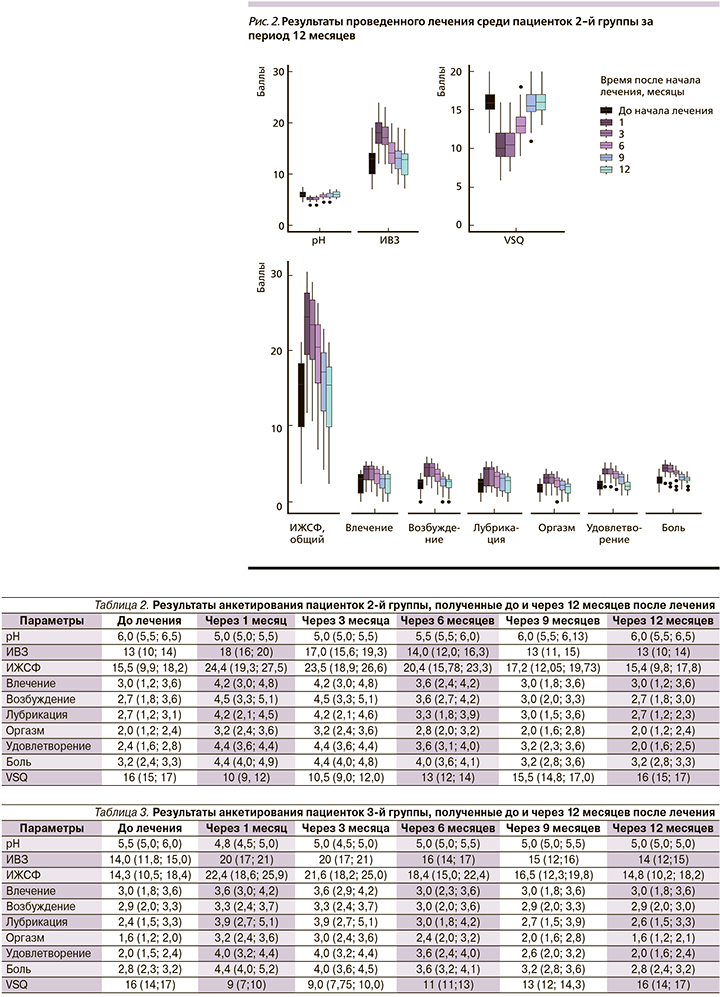
Во 2-й группе отмечено повышение среднего индекса вагинального здоровья у 50 (87%) женщин от 18,1 до 24,1 балла (р<0,001), снижение среднего значения pH влагалища у 49 (85%) женщин от 7,0 до 4,5 (р<0,001), увеличение средних значений удовлетворенности внешним видом вульвы у 48 (83%) пациенток по ВАШ от 5,5 до 9,0 (р<0,001). По данным анкетирования, увеличение индекса женской сексуальной функции (FSFI) по следующим показателям: влечение на 10% (р<0,001), возбуждение на 33% (р<0,001), лубрикация на 35% (р<0,001), оргазмичность на 30% (р<0,001), удовлетворенность на 45% (р<0,001), снижение диспареунии на 35% (р<0,001). Результаты отображены на рис. 2 и в табл. 2.
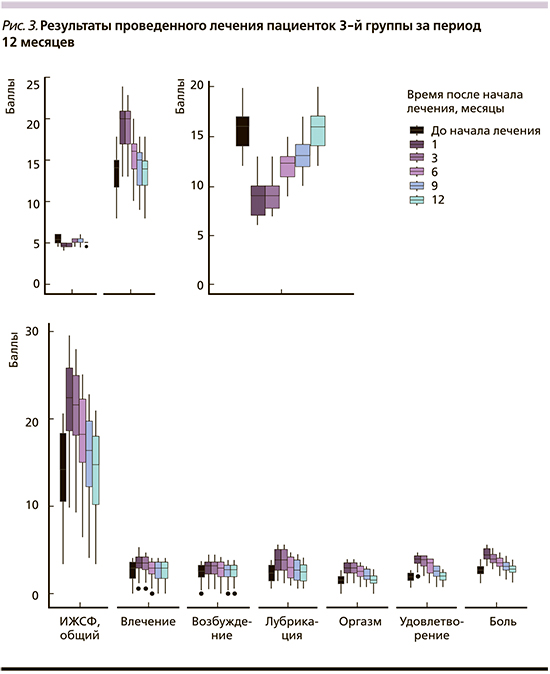
Анализ результатов 3-ей группы выявил повышение среднего индекса вагинального здоровья у 56 (90%) женщин от 19,1 до 24,5 баллов (р<0,001); снижение среднего значения pH влагалища у 53 (87%) от 7,0 до 4,3 (р<0,001); увеличение средних значений удовлетворенности внешним видом вульвы у 12 (20 %) пациенток по ВАШ от 5,5 до 7,0 (р<0,001). По данным анкетирования увеличение индекса женской сексуальной функции (FSFI) по следующим показателям: влечение на 25% (р<0,001), возбуждение на 40% (р<0,001), лубрикация на 38% (р<0,001), удовлетворенность на 47% (р<0,001), оргазмичность на 15% (р<0,001); снижение диспареунии на 45% (р<0,001). Результаты отображены на рис. 3 и в табл. 3.
Во всех группах отмечено снижение показателей клинической эффективности после проведенной терапии через 9–12 месяцев – pH, ИВЗ, ИЖСФ, VSQ.
Однако особый интерес вызывает сравнение трех стратегий терапии и выявление наиболее эффективной (рис. 4, табл. 4).
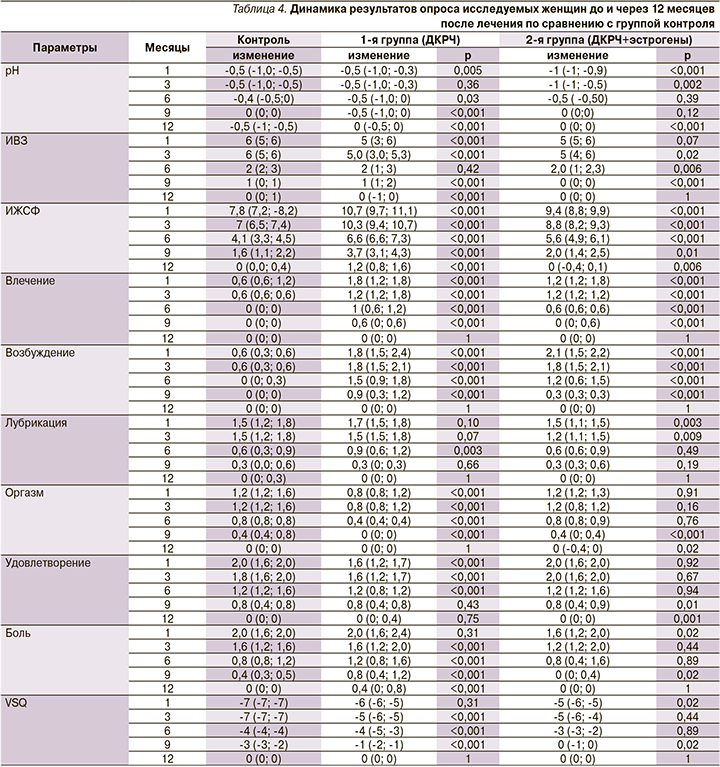
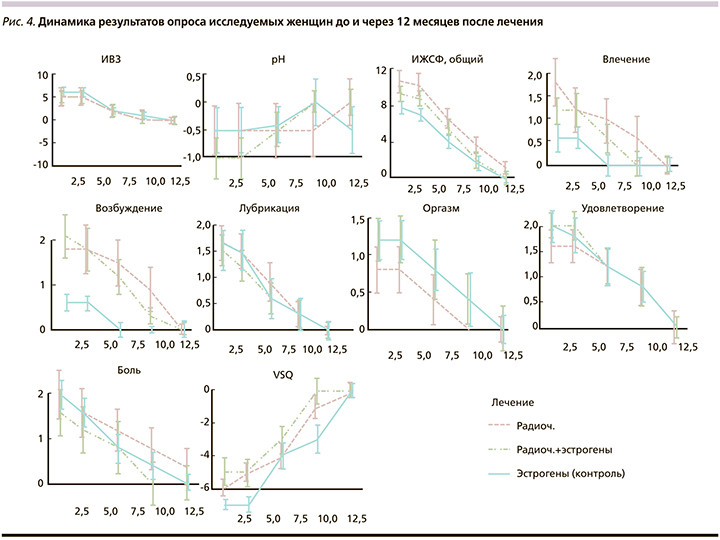
Все запланированные сеансы ДКРЧТМ хорошо переносились в 1-й и 2-й группах исследования, побочных эффектов отмечено не было (боль, термические повреждения) во время всех процедур. Все обследованные женщины завершили запланированные сеансы лечения ДКРЧТМ в обеих группах исследования. Отсева участниц не было, лишь несколько случайных пропущенных посещений в течение 12-месячного периода наблюдения. Имело место быстрое субъективное улучшение таких симптомов, как неудовлетворительные половые отношения, диспареуния и аноргазмичность. Участвовавшие женщины сообщали врачу о выраженных клинических улучшениях к концу запланированных сеансов ДКРЧТМ. Клинические улучшения оставались стабильными в течение всего периода наблюдения.
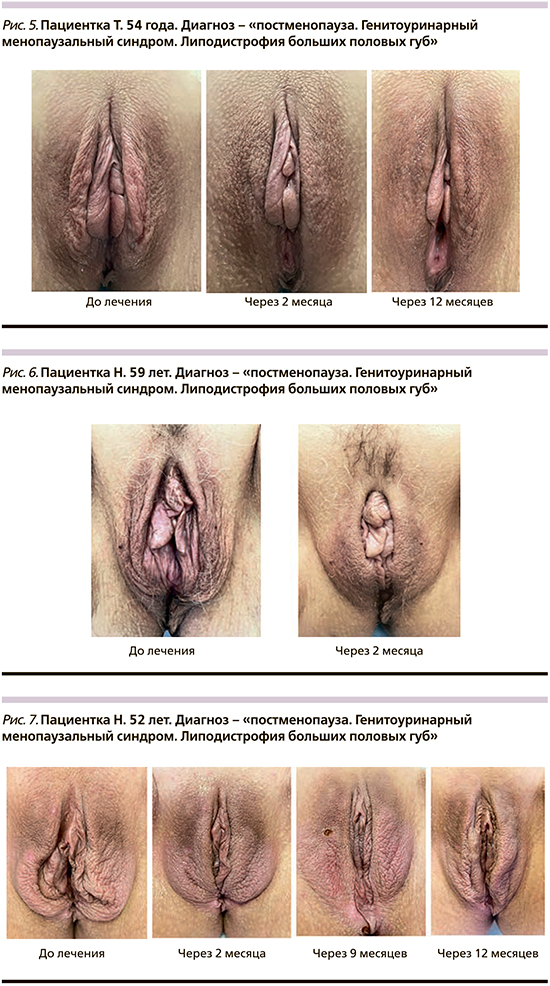
Достоверно значимо наиболее выраженный эффект от проведенной терапии наблюдался в группах с применением ДКРЧТМ. Так, увеличение индекса женского здоровья, по данным FSFI по всем показателям, кроме лубрикации, сохранялось до 9 месяцев. Лубрикация достоверно значимо снизилась уже после 6 месяцев от проведенной терапии, тогда как эффективность терапии по оцениваемому показателю рН в группах с применением ДКРЧТМ сохранялась все 12 месяцев. Также нами было отмечено улучшение эстетического вида промежности у пациенток с липодистрофией больших половых губ – повышение тургора и эластичности кожи, выраженный эффект лифтинга тканей (рис 5–7).
Обсуждение
ВВА является серьезной проблемой в гинекологической практике из-за ее очень широкого распространения и значительного негативного влияния на качество жизни женщин. Учитывая, что это хроническое и прогрессирующее заболевание легко понять, насколько принципиально важен поиск эффективных терапевтических альтернатив для этих пациентов. Важно найти инновационные инструменты, которые могут быть полезными в этой области. Признаки и симптомы ВВА, включая диспареунию, сухость, раздражение слизистых оболочек, зуд и дизурию, как правило, ухудшаются в течение 4–5 лет после менопаузы. В ряде работ посредством on-line-опросов были проанализированы данные 56 тыс. женщин с симптомами ВВА и обнаружено, что сухость (55%), диспареуния (44%) и раздражение (37%) являются наиболее частыми симптомами [17, 18].
Местное гормональное лечение считается «золотым» стандартом терапии постменопаузальных вагинальных симптомов, способствуя восстановлению целостности эпителия, вагинальной флоры и улучшению симптомов ВВА. Также было показано, что низкие дозы вагинального эстрогена превосходят системную терапию в улучшении вульвовагинальных симптомов [19]. Это лечение, однако, связано с плохой приверженностью из-за многократного и неудобного самостоятельного применения, увеличения выделений из влагалища, а также частым отказом пациенток от длительной терапии в связи с гормонофобией. Также противопоказано назначение местных эстрогенов женщинам с РМЖ, эстроген-чувствительными опухолями и тромбоэмболиями в анамнезе, что обусловливает необходимость альтернативных методов лечения.
В контексте персонифицированной терапии симптомов ВВА использование физических методов лечения, основанных на применении таких энергий, как динамическая квадриполярная радиочастота и фракционное лазерное лечение, стало альтернативным вариантом в борьбе с вульвовагинальными симптомами [16, 20]. Данные эффекты достигнуты путем ремоделирования коллагена, усиления васкуляризации [20] и восстановления вагинальной флоры до пременопаузального состояния с преобладанием лактобацилл [21]. R.R. Maia et al. в 2022 г. на когорте из 30 женщин в постменопаузе провели оценку клинических и гистологических изменений, вызванных фракционным радиочастотным воздействием (FRF) и микронидлингом тканей вульвы, выполненным с помощью системы дермароллеров. Авторы путем гистологического анализа биопсийного материала больших половых губ доказали высокую эффективность физических методов воздействия при ВВА. В образцах ткани, полученных от женщин группы FRF, отмечено значительное увеличение числа фибробластов, кровеносных сосудов и жировой ткани (p<0,05) по сравнению с контрольной группой. Кроме того, образцы ткани групп FRF и микронидлинга показали высокую экспрессию коллагена III типа и виментина при иммуногистохимическом анализе (p<0,05) [22].
Вагинальное радиочастотное воздействие с помощью аппарата EVAТМ (Novaclinical, Италия) влагалищной насадкой с использованием технологии ДКРЧТМ представляет собой инновационную и минимально инвазивную терапию для лечения симптомов вульвовагинальной атрофии. Проведенное нами исследование продемонстрировало эффективность и полную безопасность данного терапевтического подхода.
В современных исследованиях отмечается статистически значимое улучшение всех вульвовагинальных симптомов и половой функции пациенток, прошедших курс ДКРЧТМ. Это заключение делается сразу после лечения, а также имеет тенденцию оставаться в силе при длительном наблюдении. Так F. Vicariotto et al. в своем исследовании достигли хорошей эффективности при использовании ДКРЧТМ, сохранившейся до 12 месяцев, на фоне отсутствия побочных эффектов [16].
Таким образом, полученные в результате нашей работы данные подтверждают эффективность вагинального ДКРЧТМ, что может быть использовано для женщин не только с атрофией половых органов, связанной с менопаузой, но и перенесших РМЖ, для которых ряд ограничений в возможностях применения гормональной терапии затрудняют лечение.
В проведенном исследовании нам удалось как продемонстрировать высокую эффективность и безопасность метода ДКРЧТМ по сравнению с применением гормональной местной терапии, так и обозначить статистически значимые сроки для проведения повторного курса терапии для пациенток с ВВА. В данном исследовании впервые проведен сравнительный анализ ДКРЧ™-терапии/ДКРЧ™-терапии+UPR™/терапии эстриолом, также отследили в течение 12 месяцев сохранение визуального эффекта на область вульвы. Таким образом, повторные курсы рекомендованы к повторению через 6–9 месяцев.
Стратегия, основанная на своевременном повторении сеансов терапии ДКРЧТМ у данного контингента пациенток, позволит добиться стойкой ремиссии заболевания и качества жизни, а также снизить гормональную нагрузку и связанные с ней риски. Это может быть важно для более индивидуальной терапии вульвовагинальной атрофии и служить следующим шагом на пути решения данной проблемы.
Заключение
Безопасность и эффективность процедур ДКРЧТМ за время наблюдения, включившего 12 месяцев после окончания сеансов лечения, подтверждены полученными результатами исследования. Показатели индекса вагинального здоровья, значения pH влагалища, удовлетворенность внешним видом вульвы и индекса женской сексуальной функции (FSFI) по следующим параметрам: влечение, возбуждение, лубрикация, оргазмичность, удовлетворенность, быстро улучшились, достигнув почти нормального уровня к последнему сеансу ДКРЧТМ. Было показано, что возможно прохождение нового курса лечения ДКРЧТМ через 6–9 месяцев после предыдущего цикла, а не через 9–12 месяцев, как было предложено ранее. Данный алгоритм позволит поддерживать уровень показателей женского здоровья и качество жизни на высоком уровне в случае отказа женщины в постменопаузе от применения гормональных препаратов для коррекции ГУМС.
Проведенная нами работа показала, что возможно использование только процедур ДКРЧТМ без использования местной гормональной терапии с сопоставимыми, а иногда даже превосходящими результатами. Это может быть особенно актуально для пациенток, перенесших онкологические и/или сердечно-сосудистые заболевания, а также для пациенток, отказывающихся от гормонального лечения.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы: «Оптимизация тактики лечения женщин с вульвовагинальной атрофией в постменопаузе при использовании квадриполярной динамической радиочастоты».



