Хронические заболевания вен (ХЗВ) являются одной из самых распространенных патологий периферических сосудов, частота которой во взрослой популяции варьируется от 20 до 85%. Столь выраженный разброс можно объяснить нестандартизированным дизайном и оценочными критериями проводимых эпидемиологических исследований. Лишь с появлением единой международной классификации СЕАР стала возможной истинная оценка частоты и структуры ХЗВ, наиболее полное представление о которых дала программа «VEIN CONSULT». Это масштабное интернациональное исследование на единой классификационной базе СЕАР включило 91 545 пациентов из 20 стран и продемонстрировало, что 83,6% людей трудоспособного возраста имеют различные проявления ХЗВ, в структуре которых начальные стадии болезни, проявляющиеся в основном разнообразными субъективными жалобами, занимают 41,4% [1, 2]. Интересно, что именно последние, а не факт наличия варикозных вен выступают основным фактором, снижающим качество жизни пациентов [3].
Изучение характера и патогенетического механизма возникновения жалоб больных ХЗВ привело к появлению понятия «веноспецифичность», а также к разработке дифференциально-диагностического алгоритма, позволяющего отличать эти симптомы от других патологических состояний. Так, на веноспецифичность жалоб указывает их появление или усиление после длительных статических нагрузок, в результате перегревания нижних конечностей, а также на фоне физиологических или медикаментозных колебаний гормонального фона у женщин [4, 5].
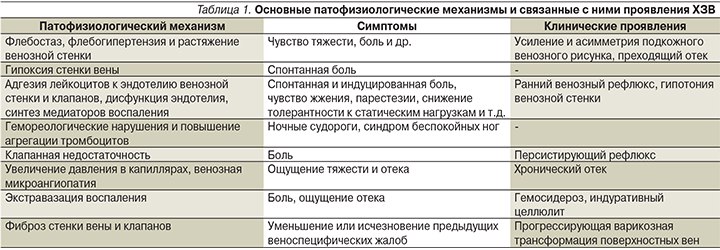
В основе появления веноспецифических жалоб лежат различные молекулярно-клеточные механизмы, в результате которых, с одной стороны, образуются многочисленные альгогены, стимулирующие болевые С-ноцицепторы, с другой – создаются предпосылки к патологическому ремоделированию стенки и клапанного аппарата вен. Схематично современный патогенез ХЗВ можно представить в виде некоего порочного круга последовательных событий: стаз венозной крови и гипоксия эндотелия; эндотелиальная дисфункция со снижением образования оксида азота (NO); активация синтеза неэндотелиального NO; релаксация гладкомышечных элементов венозной стенки и усиление флебостаза; образование и накопление свободных радикалов; асептическое воспаление венозной стенки и клапанов; фиброз стенки вены и клапанов с прогрессирующей варикозной трансформацией; нарастание флебостаза и динамической венозной гипертензии; прогрессирование повреждения сосудистой стенки и экстравазация воспаления (табл. 1) [6].
Комплекс молекулярно-клеточных механизмов повреждения венозной стенки и клапанов часто называют веноспецифическим воспалением и именно на его подавление направлены различные флеботропные препараты. Следует отметить, что до момента экстравазации веноспецифическая воспалительная реакция может быть обратимой.
Лечение начальных форм ХЗВ, сопровождающихся веноспецифическими симптомами, как правило, проводят с использованием средств консервативной терапии, которые регламентируются различными регулярно обновляемыми международными и национальными рекомендациями. Не следует отождествлять термины «консервативная» и «фармакологическая терапия». Консервативная терапия – более широкое понятие, которое кроме использования различных фармакологических агентов подразумевает ряд мероприятий, направленных на устранение важнейших факторов риска, таких как гиподинамия и избыточная масса тела. Ну и конечно же, неотъемлемым компонентом консервативного лечения ХЗВ служит компрессионная терапия [7–10].
Вместе с тем доказано, что именно к фармакотерапии пациенты демонстрируют максимальную приверженность. Наиболее низкая комплаентность (15–25%) отмечена по отношению к компрессионному лечению, несмотря на его относительно мягкий режим при начальных проявлениях ХЗВ [11]. Вот почему в настоящей публикации мы решили сделать акцент на фармакотерапии, основой которой при ХЗВ служат флеботропные лекарственные препараты (синонимы – веноактивные препараты, ВАП, флебопротекторы, венотоники и др.).
ВАП представляют собой гетерогенную группу лекарственных препаратов, получаемых из растительного сырья или путем химического синтеза, объединенных по трем основным критериям: уменьшение веноспецифических симптомов, повышение тонуса венозной стенки и снижение выраженности хронического венозного отека. Кстати, по последнему признаку флебопротекторы ранее классифицировали как «противоотечные препараты». Природа ВАП различна. Подавляющее большинство этих препаратов получают из растительного сырья, и лишь малая их часть является продуктом полностью химического синтеза (табл. 2). Несмотря на то что в клинической практике ВАП используют достаточно давно, механизм их действия в точности не изучен и для разных препаратов может иметь различия. Например, повышение венозного тонуса при использовании препаратов на основе диосмина связывают с повышением аффинитета рецепторов венозной стенки к норадреналину, в то время как производные троксерутина снижают активность ферментов, расщепляющих последний. Производное эсцина (Эскузан) стимулирует синтез гормонов коры надпочечников и способствует повышению уровня простагландинов в венозной стенке.
В качестве дополнительных опций ВАП снижают выраженность веноспецифического воспаления, нормализуют проницаемость стенки сосудов микроциркуляторного русла, улучшают лимфатический дренаж, оказывают профибринолитическое и дезагрегантное действия [12–14].
На эффективность и безопасность ВАП влияют два основных фактора:
- химическая структура активного вещества – определяет силу/прочность связывания с мишенью, т.е. избирательность флеботропного эффекта, а также возможные точки воздействия на патогенез ХЗВ;
- концентрация/количество активного вещества в непосредственной близости от мишени действия – влияет на скорость наступления и продолжительность действия препарата, т.е. величину флеботропного эффекта.
Для понимания вопросов, связанных с клинической эффективностью и безо-пасностью ВАП, необходимо иметь общие представления об их пространственной структуре и особенностях химического строения, а также информацию о «дорожной карте» – последовательных этапах высвобождения ВАП из таблетки/капсулы в желудочно-кишечном тракте, всасывания, транспорта к месту действия, инактивации (местный и системный метаболизм). Важная роль в своевременной адресной доставке ВАП к месту действия принадлежит вспомогательным компонентам, входящим в состав препарата.
Как правило, ВАП состоит из двух частей: активного вещества или их комбинации и вспомогательных веществ, состав которых определяется лекарственной формой препарата (таблетки, гранулы, капсулы и др.).

Как уже отмечалось выше, подавляющее большинство ВАП является продуктом растительного происхождения или биофлавоноидами, влияющими на синтез соединительной ткани, в частности коллагена. Гидроксилирование пролиновых и лизиновых остатков в полипетидных цепях проколлагена происходит одновременно со сборкой цепей в фибробластах. В этом процессе участвуют молекулярный кислород и альфа-кето-глутарат, а в качестве кофакторов – ион двухвалентного железа и аскорбиновая кислота. Биофлавоноиды увеличивают стабильность аскорбиновой кислоты, ингибируя активность фермента аскорбиноксидазы. Кроме того, часть фармакологических эффектов ВАП может быть реализована во внеклеточном пространстве или в сосудистом русле. В частности, некоторые флеботропные препараты влияют на активность свертывающих факторов крови, матричных металлопротеиназ, а также выступают в качестве ловушки свободных радикалов. Одной из особенностей фармакологического действия биофлавоноидов является чрезвычайно широкий спектр потенциальных мишеней, на которые они могут воздействовать в организме. Механизм этого феномена объясняется способностью биофлавоноидов выступать в роли хелаторов, т.е. образовывать стабильные комплексы с ионами металлов (Zn, Fe, Cu, Cr, Mn), служащх кофактором различных ферментных систем. Описано более двух десятков различных ферментов (фосфолипаза, циклооксигеназа, липооксигеназа и др.) и провоспалительных медиаторов (цитокины, простагландины, лейкотриены, NO), активность которых изменяется под действием биофлавоноидов. На этом основан противовоспалительный и анальгетический эффекты ВАП. Еще одной мишенью для флеботропных препаратов служит дисфункция эндотелия, обусловленная нарушением образования NO, простациклина, повышением синтеза эндотелина 1 и др. [15].
Согласно различным международным и национальным рекомендациям, основным показанием к назначению ВАП служит наличие веноспецифических симптомов, хронического венозного отека и трофических нарушений кожи голени. Также ВАП назначают превентивно с целью профилактики негативного воздействия на венозную систему таких стрессов, как длительный авиационный перелет, высокая температура окружающей среды, прием препаратов женских половых гормонов и других факторов, которые могут провоцировать обострение ХЗВ.
Выбор конкретного препарата, как правило, происходит эмпирически и определяется множеством критериев, среди которых можно отметить наличие солидного научного досье с описанием результатов клинических исследований, доступность в аптечной сети, индивидуальный или коллективный опыт по его применению. Немаловажное значение имеет стоимость курса лечения, продолжительность которого при начальных формах ХЗВ, как правило, колеблется от 1,5 до 3 месяцев, а при наличии хронического венозного отека и трофических нарушений кожи может достигать 6 и более месяцев. Кстати, именно при планировании длительной терапии следует учитывать известный профиль безопасности конкретного флеботропного препарата.
В современных клинических рекомендациях рейтинг и показания к назначению различных лекарственных препаратов выстраивают в соответствии с критериями доказательной медицины, применение которых в отношении ВАП не всегда обоснованно. Дело в том, что, с одной стороны, многие ВАП имеют анамнез успешного клинического применения, более длительный, чем постоянно трансформирующаяся концепция доказательной медицины. С другой – возникают обоснованные сомнения в возможности объективной оценки субъективных веноспецифических жалоб, в отношении которых доказан почти 50%-ный плацебо-эффект.
В качестве резюме следует отметить, что как адепты доказательной медицины, так и их противники сходятся во мнении, согласно которму при начальных стадиях ХЗВ хороший терапевтический эффект обеспечивают все известные флеботропные лекарственные препараты. В такой ситуации на выбор препарата основное влияние оказывают удобство приема и критерий цена/качество.
Говоря об удобстве приема и параметре цена/качество, нельзя обойти вниманием известный и чрезвычайно популярный препарат Эскузан – смесь тритерпеновых сапонинов (протоаэсцигинин, барингтогенол, альфа- и бетааэсцин, криптоаэсцин и др.), получаемых из конского каштана в комбинации с тиамином (витамин В1). Эскузан обладает антиоксидантным, противоотечным, антиэкссудативным, капилляропротективным и венотонизирующим действиями. Его основным действующим веществом является эсцин, относящийся к группе тритерпеновых гликозидов. Эсцин стимулирует выработку гормонов коры надпочечников, увеличивает в сосудистой стенке количество простагландинов, улучшает сократительную способность гладких мышц венозной стенки, снижает ломкость сосудов, улучшает метаболизм в тканях, нормализует состояние капилляров. Капилляропротективные свойства эсцина проявляются также за счет его способности угнетать активность лизосомальных ферментов и тем самым блокировать расщепление мукополисахаридов (в частности, протеогликана) в стенках сосудов. Эскузан стимулирует высвобождение норадреналина и ускоряет проводимость импульсов в сосудистой стенке, уменьшает флебостаз и улучшает функцию венозных клапанов.
Благодаря способности эсцина нормализовывать проницаемость плазмолимфатического барьера и улучшать лимфооток, а также снижать выход электролитов и воды в интерстиций Эскузан оказывает противоотечное действие. Кроме этого препарат подавляет веноспецифическое воспаление и снижает агрегацию форменных элементов крови. Тиамин, входящий в состав Эскузана, усиливает антиоксидантное действие за счет подавления перекисного окисления липидов.
В результате процессов фосфорилирования тиамин превращается в кокарбоксилазу, которая является коферментом многих ферментных реакций и играет важную роль в углеводном, белковом и жировом обменах, а также в процессах проведения нервного возбуждения в синапсах. Тиамин защищает мембраны клеток от токсического воздействия продуктов перекисного окисления.
Эскузан быстро всасывается из желудочно-кишечном тракте после перорального приема. Его связывание с белками плазмы достигает 85%. Метаболизируется преимущественно в печени, выводится с желчью. Небольшой процент препарата выводится почками в неизмененном виде.
В силу разных причин и прежде всего благодаря отсутствию современных клинических исследований сложилось ошибочное мнение, будто Эскузан является одним из самых слабых флеботропных препаратов, терапевтическая эффективность которого не имеет объективных доказательств. Это абсолютно не соответствует действительности. В Кокрановской базе данных описано 17 рандомизированных контролируемых исследований (РКИ), посвященных Эскузану и подтверждающих целесообразность его применения пациентами с различными веноспецифическими симптомами. Более того, в 1996 г. в The Lancet – одном из самых авторитетных медицинских журналов, были опубликованы результаты РКИ, которое показало, что при хроническом венозном отеке (С3 клинический класс ХЗВ по классификации СЕАР) Эскузан оказывает терапевтический эффект, сопоставимый с компрессионной терапией – общепризнанным эталоном консервативного лечения тяжелых форм хронической венозной недостаточности [16, 17].
Своеобразной визитной карточкой Эскузана, выделяющей его среди других ВАП, служит жидкая лекарственная форма, которая значительно облегчает прием, что весьма актуально для пациентов, имеющих проблемы с глотанием. В официальной аннотации предлагается принимать Эскузан по 10–15 капель с небольшим количество воды 3 раза в сутки. Мы предлагаем несколько другой вариант приема, когда те же 10–15 капель препарата наносят на кусочек сахара или хлеба и держат его во рту до максимально полного всасывания. Такой способ приема ускоряет высвобождение активной фракции эсцина и повышает его биодоступность.
В заключение следует отметить, что в силу чрезвычайно высокой распространенности начальных форм ХЗВ прогрессивно растет актуальность адекватной консервативной терапии, которую в свою очередь невозможно представить без уже известных и новых флеботропных лекарственных препаратов.
Можно утверждать, что ВАП в современной флебологической практике играют такую же важную роль, как гипотензивные или сахароснижающие препараты в клинике внутренних болезней. Эволюция использования ВАП не возможна без тщательного изучения их механизма действия и разработки оптимальных схем применения, адекватных клиническим проявлениям и стадиям ХЗВ.



