Клиническая значимость всех составляющих метаболического синдрома (МС) заключается в том, что их сочетание в значительной степени ускоряет развитие и прогрессирование сердечнососудистых заболеваний (ССЗ), в основе которых лежит атеросклероз. Кроме того, распространенность МС растет с каждым годом, принимая характер эпидемии, и в настоящее время эксперты ВОЗ оценивают ситуацию следующим образом: “Мы сталкиваемся с новой пандемией XXI в., охватывающей индустриально развитые страны… Распространенность метаболического синдрома в 2 раза превышает распространенность сахарного диабета, и в ближайшие 25 лет ожидается увеличение темпов его роста на 50 %” [1, 2].
В России демографическая ситуация развивается таким образом, что очень быстро растет число пожилых лиц. Уже сегодня пятую часть населения нашей страны составляют лица пенсионного возраста, около 11 % – старше 80 лет. В докладе “Старение и здоровье человека” (“Men ageing and health”. ВОЗ, 2001) к пожилым отнесены люди в возрасте ≥ 65 лет. По данным различных авторов, доля лиц с МС в возрасте старше 60 лет составляет 42–43,5 %.
Артериальная гипертензия (АГ) является не только составляющей МС, но и одним из важнейших звеньев его патогенеза. Распространенность повышенного артериального давления (АД) у больных МС составляет 30,5 %, и в подавляющем большинстве (90 %) случаев АГ сопряжена с различными его компонентами [3]. У лиц старше 65 лет АГ встречается в 50 % случаев, и приблизительно в 2/3 случаев диагностируется изолированная систолическая артериальная гипертензия (ИСАГ). Острота проблемы ИСАГ связана с распространением ошибочных представлений о физиологическом характере повышения АД с возрастом и нежелательности его снижения у пожилых людей из-за риска усиления цереброваскулярной недостаточности. Это важно, поскольку у пожилых лиц профилактические и лечебные мероприятия имеют целью не только продление жизни, но и сохранение достаточно высокого уровня качества жизни.
Согласно рекомендациям ВОЗ и Международного общества по изучению артериальной гипертензии, под ИСАГ понимают повышение уровня систолического АД (САД) до 140 мм рт. ст. и выше при диастолическом АД (ДАД) менее 90 мм рт. ст. Повышенное САД при ИСАГ – уже установленный фактор риска развития всех сердечнососудистых осложнений (ишемической болезни сердца – ИБС, инсульта, сердечной и почечной недостаточности) и смертности от ССЗ [4, 5].
Этиопатогенез ИСАГ
Этиология ИСАГ требует уточнения. Есть основания полагать, что частично она определяется возрастными изменениями в организме, в т. ч. в сосудах. Хотя, конечно, повышение АД не является закономерным следствием старения. В генезе повышения АД имеют значение как гемодинамические факторы, так и нейрогормональная дисфункция.
Результаты Фрамингемского исследования, другие эпидемиологические наблюдения позволяют утверждать, что существуют возрастные изменения АД [6].
Они заключаются в следующем:
- повышение САД в возрасте от 5 до 20 лет;
- плато САД и пульсового АД в возрасте от 20 до 40 лет;
- повышение САД и пульсового АД в возрасте старше 40 лет;
- снижение ДАД в возрасте старше 50 лет;
- относительное постоянство среднего АД у взрослых.
Гемодинамические механизмы первичной ИСАГ у пожилых лиц окончательно не установлены. Абсолютное большинство исследователей считают основной ее причиной снижение растяжимости аорты и артерий, что в свою очередь связано с процессом старения (потеря эластичности волокон стенки артерий и отложение в ней коллагена, эластина, гликозаминогликанов и кальция). Многие гистологические изменения в стенке сосудов, связанные с возрастом, схожи с атеросклеротическими. Тем не менее вопрос о роли атеросклероза в патогенезе ИСАГ остается спорным. С одной стороны, атеросклеротический процесс, широко распространенный среди лиц пожилого возраста, уменьшает растяжимость крупных артерий. Это приводит к повышению САД в результате того, что выброс крови из левого желудочка осуществляется в более ригидную и менее эластичную аорту. Такое снижение эластичности аорты и других крупных артерий вследствие атеросклероза может явиться одним из патофизиологических факторов развития ИСАГ. С другой стороны, у многих больных с тяжелой формой распространенного атеросклероза САД остается в пределах нормы и, наоборот, в некоторых группах населения с низкой распространенностью атеросклероза САД с возрастом повышается и развивается ИСАГ [7].
В основе патогенеза ИСАГ при МС лежит инсулинорезистентность (ИР) и вызванная ею компенсаторная гиперинсулинемия. Предполагается, что концентрация инсулина связана с АГ независимо от наличия нарушения толерантности к глюкозе или ожирения. В настоящее время не вызывает сомнений факт чрезвычайно частого сочетания АГ и нарушений углеводного обмена [8].
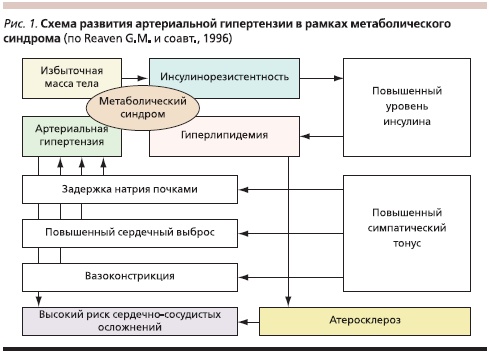
Как известно, инсулин является прямым вазодилататором и формирование АГ при его участии происходит во взаимодействии с нейрогуморальными механизмами. Рассматриваются следующие механизмы возникновения и прогрессирования АГ при гиперинсулинемии (рис. 1) [9, 10]:
- Стимуляция активности симпатической нервной системы. Инсулин принимает участие в регуляции активности симпатической нервной системы в ответ на прием пищи. После приема пищи секреция инсулина увеличивается. Острое и хроническое повышение концентрации инсулина в крови стимулирует активность симпатоадреналовой системы и повышает содержание катехоламинов в крови. Кроме того, постоянная гиперсимпатикотония способствует нарушению микроциркуляции в скелетных мышцах, что ведет к снижению количества функционирующих капилляров (Ortlepp J.R., Breuer J. и соавт., 2002). В результате происходит нарастание ИР и гиперинсулинемии. Таким образом, повышение активности симпатоадреналовой системы приводит к повышению АД.
- Активация ренин-ангиотензин-альдостероновой системы (РААС). Одним из ведущих компонентов развития АГ при МС является активация РААС, индуцированная гиперсимпатикотонией. Существует тесная связь между пострецепторными сигналами системы ангиотензина II и инсулина, который после взаимодействия со своими рецепторами на поверхности клеток индуцирует тирозинфосфолирирование белков IRS-1 и IRS-2. Далее молекулы IRS активируют PI3-K, через которую осуществляются передача сигнала и реализация метаболических и сосудорасширяющих эффектов инсулина (транспорт глюкозы в клетки, синтез оксида азота). Ангиотензин II блокирует PI3-K – сигнальный путь инсулина в клетках сосудов и других инсулинозависимых тканей, одновременно стимулируя другую сигнальную систему инсулина (ras, raf, MEK, MARK), ведущую к активации митогенных и пролиферативных процессов. Таким образом, ангиотензин II блокирует основной метаболический эффект инсулина (транспорт глюкозы в клетки) и усиливает атерогенное действие инсулина [11].
- Повышение реабсорбции натрия в проксимальных и дистальных канальцах нефрона способствует задержке жидкости и развитию гиперволемии, повышению содержания натрия и кальция в стенках сосудов.
- Блокада трансмембранных ионообменных механизмов (натрий-, калий-, кальций-зависимой АТФазы) повышает содержание натрия и кальция и уменьшает содержание калия, что в итоге приводит к увеличению чувствительности сосудистой стенки к прессорным воздействиям.
- Стимуляция пролиферации гладкомышечных клеток сосудистой стенки влечет за собой сужение артериол и повышение общего периферического сопротивления.
- Гиперлептинемия. В настоящее время активно обсуждается роль гиперлептинемии в патогенезе АГ в рамках МС. Оказалось, что концентрация лептина в плазме больных МС прямо пропорциональна степени ожирения, а уровень лептина тесно коррелирует с индексом массы тела, уровнем АД, ангиотензина и норадреналина. В исследовании, проведенном в Японии, была выявлена причинная связь между гиперлептинемией, повышенной активностью симпатической нервной системы и АГ у пациентов, страдающих ожирением [12].
- Эндотелиальная дисфункция. В настоящее время установлено, что ИР и эндотелиальная дисфункция, в т. ч. продукция основного вазодилататора оксида азота, являются тесно ассоциированными состояниями и формируют порочный круг [13, 14]. У больных МС в условиях ИР и гиперинсулинемии наблюдается снижение реакции эндотелия на вазодилатационное и усиление на вазоконстрикторное воздействия, что обусловлено снижением активности оксида азота, уменьшением образования простациклина и увеличением продукции вазоконстрикторных субстанций (эндотелина-1, тромбоксана А2, простагландина F2).
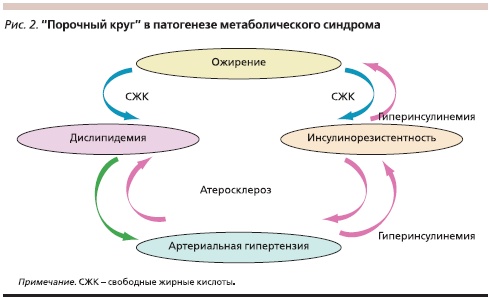
Роль ИР в развитии АГ трудно переоценить. Однако и АГ может быть первичным звеном в патогенезе МС. Длительная, нелеченая или неадекватно леченная АГ вызывает ухудшение периферического кровообращения, что приводит к снижению чувствительности тканей к инсулину и как следствие – к относительной гиперинсулинемии и ИР, а последняя в свою очередь запускает развитие всех составляющих МС (рис. 2) [15].
Особенности клинической картины ИСАГ
Клиническая картина и течение ИСАГ у пожилых больных имеют ряд особенностей:
- Уровень САД позволяет прогнозировать сердечно-сосудистый риск.
- АГ характеризуется высоким пульсовым давлением, являющимся дополнительным фактором риска ССЗ. По данным Фрамингемского исследования, повышение пульсового давления более 60 мм рт. ст. является неблагоприятным прогностическим фактором в отношении риска сердечнососудистых осложнений и смертности. Высокое пульсовое давление – маркер биологического возраста артерий и по определению является основной характеристикой ИСАГ.
- Примерно у половины больных ИСАГ протекает практически бессимптомно, у другой части отмечаются различные субъективные расстройства. Больные, как правило, имеют большую давность заболевания, а повышение АД дает очень скудную клиническую симптоматику вплоть до полного отсутствия жалоб у пациентов. Вместе с тем клинически выявляются метаболические нарушения (дислипидемия, сахарный диабет, подагра и другие составляющие МС).
- При ИСАГ отмечается гипокинетический тип гемодинамики с увеличением общего периферического сопротивления.
- Во многих наблюдениях отмечается высокая соль-чувствительность АД [16].
- Частота симптоматических АГ значительно меньше, чем в популяции молодых пациентов, однако выявление АГ в пожилом возрасте часто требует исключения клинически значимого стеноза почечных артерий.
- Кроме перечисленных особенностей течения АГ у пожилых больных отмечается нарушение циркадного ритма АД.
Тактика обследования больных ИСАГ
Обследование больных ИСАГ должно проводиться в соответствии с международными и российскими рекомендациями по диагностике и лечению больных АГ [17]. Кроме того, диагностический поиск должен быть направлен на выявление всех возможных компонентов МС (см. таблицу), комплексная оценка которых позволяет определить прогноз и выбрать оптимальную тактику лечения таких больных.
Таблица.Различные критерии диагностики метаболического синдром.
Следует остановиться на некоторых особенностях измерения АД у пожилых больных: во время первого визита рекомендуется измерять АД на обеих руках, в положениях сидя, стоя и лежа; постуральные изменения АД регистрируют после 1–3 минут пребывания пациента в положении стоя.
Существуют особые ситуации при измерении АД у больных пожилого возраста:
- Псевдогипертония. С возрастом наблюдается утолщение и уплотнение стенки плечевой артерии, она становится ригидной. Требуется более высокий (выше внутриартериального) уровень давления в манжетке для достижения компрессии ригидной артерии, в результате чего происходит ложное завышение уровня АД (феномен “псевдогипертонии”, феномен Ослера).
- Изолированная “офисная” гипертензия (т. н. гипертензия белого халата). У ряда пациентов пожилого возраста имеется неоспоримое повышение АД исключительно на приеме у врача, тогда как значения АД за 24 часа находятся в пределах нормы. Современные данные говорят о высокой распространенности данного феномена (до 10 % в общей популяции), а также о том, что он встречается достаточно часто у пожилых пациентов с уже диагностированной АГ. Данное состояние не является абсолютно “невинным” с клинической точки зрения и требует обязательного суточного мониторирования АД [18] .
- Аускультативный провал. У больных пожилого возраста часто регистрируется феномен аускультативного провала – периода временного отсутствия звука между фазами I и II тонов Короткова, который может продолжаться до 40 мм рт. ст. Аускультативный провал наблюдается на фоне высокого САД. В этой ситуации необходимо нагнетать воздух не менее чем до 250 мм рт. ст. и спускать его очень медленно.
В настоящее время основным объективным методом оценки уровня АД является его суточное мониторирование (СМАД). Анализ результатов СМАД позволяет определенным образом характеризовать суточный профиль, вариабельность, нагрузку давлением, величину и скорость утреннего подъема АД, которые являются независимыми факторами риска развития сердечно-сосудистых и церебральных осложнений. И наконец, данная методика позволяет изучить действие различных антигипертензивных препаратов на все эти показатели во времени [19, 20].
Суточный профиль АД у пожилых пациентов с ИСАГ имеет ряд особенностей [21], которые увеличивают риск развития сердечно-сосудистых осложнений:
- Вариабельность АД является самостоятельным фактором риска развития сердечно-сосудистых катастроф и имеет тенденцию к росту вместе с увеличением возраста.
- Выявлена высокая частота различных нарушений циркадного ритма АД (по различным данным – от 75 до 85 %), при этом основную массу составляют пациенты с недостаточным снижением АД в ночные часы и с ночной АГ. Преобладание в группе пожилых гипертоников “nondippers” является прогностическим фактором, отражающим степень риска сердечно-сосудистых осложнений, поскольку частота осложнений именно на фоне ночной АГ приближается к 100 %.
- Вследствие высокой частоты атеросклеротического поражения сосудов головного мозга у больных АГ пожилого возраста они более чувствительны и к противоположному нарушению суточного профиля АД – чрезмерному его снижению во время сна. Пациенты с таким изменением суточного профиля (т. е. степенью ночного снижения АД > 20 %, или over-dippers) имеют больший риск развития как симптомных (транзиторных ишемических атак, инсультов), так и “немых” повреждений головного мозга, в т. ч. лакунарных инфарктов.
- У пожилых больных имеет свои особенности и утренний подъем АД. Так, по данным Carmona J. и соавт., при сравнении величины и скорости подъема АД в течение 6 утренних часов (3 часов до подъема пациента и 3 часов после) у пациентов старше 60 лет внезапный скачок АД регистрируется значительно чаще, чем у пациентов молодого и среднего возраста.
Лечение ИСАГ у пожилых пациентов с МС
Краеугольным камнем в лечении ИСАГ у больных МС являются немедикаментозные мероприятия, направленные на снижение массы тела путем изменения стереотипов питания и увеличения приверженности пациентов дозированной физической активности. Кроме того, важными мерами является отказ от курения и злоупотребления алкоголем. Параллельно, с учетом оценки степени риска ССЗ должна проводиться лекарственная терапия, направленная на достижение целевых уровней АД, а также коррекцию всех метаболических нарушений.
Препарат, использующийся для лечения ИСАГ у пожилых пациентов с МС, не должен иметь отрицательное воздействие на метаболизм, в первую очередь глюкозы и липидов. Он должен влиять на основные патогенетические механизмы развития заболевания (повышение реабсорбции натрия, повышенную соль-чувствительность, повышение общего периферического сопротивления из-за нарушения эластичности и функции расслабления сосудов и миокарда), не вызывая ортостатической гипотензии.
На вопрос, с чего начать лечение пожилого больного ИСАГ, дали ответ многие многоцентровые исследования: SYST-EUR – Systolic Hypertension in Europe trial (Европейское исследование плацебо против блокатора кальциевых каналов, ингибитора ангиотензинпревращающего фермента – ИАПФ), MRC – Medical Research Council (сравнивался эффект диуретика, β-адреноблокатора и плацебо), SHEP – Systolic Hypertension in theEldery Program (лечение ИСАГ тиазидным диуретиком, при необходимости добавлялся β-адреноблокатор), STOP-Hypertension 2 – Swedish Trial in Old Patients with Hypertension 2 (сравнивали влияние диуретиков, β-адреноблокаторов, блокаторов кальциевых каналов и ИАПФ на уровень сердечно-сосудистой смертности и частоту инсульта, инфаркта миокарда и внезапной смерти у пожилых больных АГ) [4]. Результаты проведенных исследований показали высокую эффективность диуретиков, ИАПФ и блокаторов кальциевых каналов в лечении пожилых пациентов с АГ.
В настоящее время средством первого выбора для лечения ИСАГ у пожилых больных являются диуретики. Их отличают низкая или умеренная стоимость, высокая эффективность, хорошая переносимость, доказанное положительное влияние на ССЗ и смертность. Кроме того, при выборе терапии следует учитывать, что большинство международных руководств рекомендует применять низкие дозы антигипертензивных препаратов пролонгированного действия, обладающих высоким соотношением эффективность/безопасность, что способствует повышению приверженности пациентов лечению.
Второй группой препаратов, рекомендованной пациентам с ИСАГ, являются блокаторы кальциевых каналов дигидропиридинового ряда. Способность пролонгированных блокаторов кальциевых каналов снижать частоту сердечно-сосудистых осложнений и улучшать качество жизни больных продемонстрирована в исследованиях: SYST-EUR, SYST CHINA, ELSA, STONE, STOP-Hypertension 2 и др. [4].
Блокада активности РААС составляет важную часть комплексной антигипертензивной терапии пожилого гипертоника. Как уже отмечалось, для больных пожилого возраста характерна полиморбидность. Пациенты имеют не только повышенные цифры АД, но часто и патологию суставов, нарушения липидного обмена, бронхообструктивные заболевания, сахарный диабет и неалкогольную жировую болезнь печени. При выборе препарата большое значение имеет наличие последней патологии.
В данных клинических ситуациях привлекает применение ИАПФ, минимально метаболизирующихся печенью, в частности лизиноприла. Надежный контроль гемодиномики поддерживается однократным приемом лизиноприла, препарат не требует превращения в активный метаболит в печени, а также практически не связывается с белками плазмы. Все эти свойства обусловлены высокой гидрофильностью лизиноприла. В настоящее время в арсенале врача имеется неплохой выбор генерических препаратов лизинорила. Одним из первых на российском рынке появился Диротон® компании Гедеон Рихтер, применяемый как в виде монотерапии, так и в комбинации с гидрохлоротиазидом – Ко-Диротон®. В зависимости от клинического профиля пациента применение этих лекарственных форм часто служит основой многокомпонентной антигипертензивной терапии пожилого больного АГ с проявлениями МС. Грамотно подобранная антигипертензивная терапия способствует улучшению показателей углеводного, липидного обменов, повышает чувствительность тканей к инсулину [23].
Таким образом, лечение лиц пожилого возраста с ИСАГ и МС – это искусство и оно требует от пациентов и врачей неустанного внимания и кропотливой работы.
Информация об авторе:
Драпкина Оксана Михайловна – профессор, заведующая отделением кардиологии клиники пропедевтики
внутренних болезней ММА им. И.М. Сеченова.
Тел. 8 (499) 248-35-88



