Введение
Язвенный колит (ЯК) – это воспалительное заболевание, затрагивающее слизистую оболочку толстой кишки. Оно характеризуется протяженным воспалением начиная с прямой кишки и распространяется проксимально[1]. Для ЯК характерны эпизодические обострения с симптомами, характеризующимися частым жидким стулом с примесью крови в сочетании с императивными позывами и тенезмами. Активность заболевания может варьироваться от полной ремиссии до фульминантной формы с системными токсическими проявлениями [2]. Несмотря на то что патогенез ЯК еще недостаточно изучен, наиболее подробно описана теория, согласно которой кишечная флора запускает аберрантный кишечный иммунный ответ и последующее воспаление у генетически предрасположенных людей [3–4]. Медикаментозное лечение направлено на контроль симптомов и разрешение основного воспалительного процесса классически с помощью комбинации различных агентов, таких как 5-аминосалицилаты (5-АСК), кортикостероиды и иммунодепрессанты, в т.ч. антиметаболиты пурина и циклоспорин [5–6]. Медикаментозная терапия ЯК недавно вступила в эпоху биологических препаратов с того момента, как в 2005 г. FDA разрешила к применению инфликсимаб – моноклональное антитело, направленное против фактора некроза опухоли-альфа [7].
В России препарат стал систематически применяться с 2008 г. Несмотря на его клинически подтвержденную эффективность, при использовании этого препарата может проявляться первичная или вторичная неэффективность. Первичной неэффективностью называют отсутствие клинического ответа на препарат. Она выявляется во время индукционного курса, и обычно терапия таким больным этим препаратом не продолжается [8]. В исследовании, проведенном в ГНЦ колопроктологии, было показано, что 82% пациентов, оперированных по поводу ЯК в связи с неэффективностью терапии инфликсимабом, подверглись хирургическому вмешательству в период индукционного курса [9]. К вторичной неэффективности относят т.н. потерю ответа. Тем не менее данный термин не имеет общего объяснения и определяется индивидуально лечащим врачом или исследователем. Как правило, потерей ответа считают возникновение рецидива на фоне эффективной проводимой поддерживающей терапии [10]. В связи с этим в большинстве случаев при возникновении рецидива на фоне биологической терапии пациенту назначают удвоенную дозу инфликсимаба для преодоления вторичной неэффективности или переход на другой препарат [11].
В условиях российского здравоохранения пациенты в большинстве своем не имели возможности получения удвоенной дозы препарата при возникновении первого рецидива на фоне ранее эффективной терапии инфликсимабом. Целью настоящего исследования было оценить дальнейшее течение заболевания у пациентов с ЯК, имеющих рецидивы на фоне поддерживающей терапии инфликсимабом.
Материал и методы
В ретроспективном исследовании течение ЯК было отслежено у пациентов, начавших терапию инфликсимабом в ФГБУ ГНЦ колопроктологии МЗ РФ в период с апреля 2008 по апрель 2013 г. Общее число таких пациентов составило 46 человек (мужчин – 47,8%, средний возраст на момент начала терапии – 31,7, интерквантильный интервал – 17–47 лет). Судьба пациентов прослеживалась до апреля 2014 г. Все пациенты наблюдались как минимум год после начала терапии в случае ее первичной эффективности. Контрольная колоноскопия выполнена через год после начала терапии в случае отсутствия клинических обострений.
Терапия инфликсимабом пациентам назначалась в случае гормональной зависимости или гормональной резистентности. В качестве сопутствующей терапии азатиоприн принимали 29 пациентов (в отношении остальных препарат был отменен ранее или в ходе наблюдения в связи с нежелательными явлениями или непереносимостью), 25 пациентов продолжали снижать дозу кортикостероидов в течение индукционного курса и 13 пациентов продолжали принимать препараты 5-АСК. Инфликсимаб назначался пациентам в дозе 5 мг/кг по стандартной схеме: индукционный курс – 3 инфузии на 0, 2-й и 6-й неделе, далее при наличии ответа на терапию проводился поддерживающий курс каждые 8 недель.
При каждом случае возникновения клинического рецидива ЯК (появления жалоб на учащение стула и наличие примеси крови) на фоне поддерживающей терапии инфликсимабом (и азатиоприном или без него) всем пациентам выполнялась ректосигмоидоскопия для выявления эндоскопической активности. В случае возникновения рецидива более чем за неделю до введения пациенты получали также местную терапию микроклизмами Салофальк 4 г или микроклизмами с гидрокортизоном 125 мг, или свечами с препаратами 5-АСК в зависимости от распространенности и выраженности воспалительного процесса по данным ректосигмоидоскопии. В случае вторичной неэффективности пациентам назначалось увеличение дозы до 10 мг/кг, однако, как правило, ближайшая после обострения инфузия инфликсимаба проводилась в прежней дозе (5 мг/кг) в связи с административными причинами. В случае возникновения среднетяжелого и тяжелого обострения пациентам выполнялась колоноскопия. При минимальной или умеренной активности пациентам назначалась терапевтическая доза препаратов 5-АСК. При тяжелой атаке и выраженной активности задолго до очередного введения назначались системные кортикостероиды и решался вопрос о хирургическом лечении.
Результаты
Из 46 пациентов, начавших терапию инфликсимабом, 1 пациент прекратил ее самостоятельно после второго введения, 1 пациентом терапия была прекращена в связи с острой тяжелой аллергической реакцией на препарат. Из 44 пациентов ответ на индукционный курс был получен от 31 (70,5%) пациента. Ответом считалось отсутствие или наличие минимальных клинических проявлений заболевания. Данным больным был продолжен поддерживающий курс терапии. Из 31 пациента у 13 (41,9%) имел место хотя бы один рецидив на фоне поддерживающей терапии, из них у 7 (22,6%) рецидив произошел в первый год терапии.
Среди всех пациентов, продолживших лечение инфликсимабом, тяжелые обострения, потребовавшие хирургического лечения, возникли у 2. У остальных 11 пациентов обострения носили легкий (7 человек) или среднетяжелый характер (3 человека) и купированы назначением 5-АСК, местной терапии или очередным введением инфликсимаба. В ходе наблюдения было выявлено несколько вариантов течения ЯК на фоне поддерживающей терапии инфликсимабом в зависимости от характера возникновения рецидива (тяжести и времени его возникновения и частоты). У 22,6% (7 из 31) пациентов рецидивы возникали за несколько дней или недель до очередного введения инфликсимаба по графику и купировались на фоне инфузии препарата. У 9,7% (3 из 31) пациентов обострения возникали между введениями и исходной дозой инфликсимаба, полностью купированы не были. И у аналогичного числа пациентов (9,7% [3 из 31]) рецидивы возникали эпизодически 1 раз в год или несколько лет независимо от введений препарата и купировались с помощью местной терапии.
Обсуждение
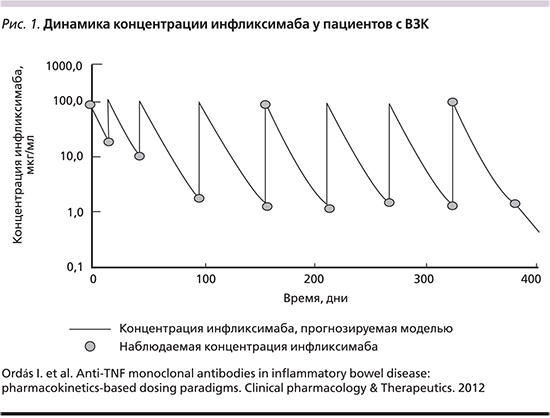
Данное ретроспективное исследование показывает, что течение ЯК на фоне биологической терапии пациентов инфликсимабом имеет разный характер. Большая часть пациентов на поддерживающей терапии оставалась в ремиссии в течение как минимум года, что аналогично данным многих существующих исследований [12–14]. В зависимости от дизайна исследований, параметров выборок и стран эти цифры колеблются в среднем от 60 до 70% [7, 9, 15–17]. Что касается вторичной потери ответа, то данные исследований объединить не просто. В мировой литературе самым распространенным термином для вторичной неэффективности является термин «loss of response» (дословно «потеря ответа»), однако единого мнения по поводу того, что именно называть потерей ответа, нет. В связи с этим частота потери ответа лежит в достаточно большом диапазоне значений – в среднем от 23 до 46% [18–19]. В ходе данного исследования мы выявили два типа вторичной неэффективности для пациентов на поддерживающей терапии инфликсимабом. Для одного из них характерно наличие рецидива заболевания, возникающее между введениями и не купирующееся инфузией препарата в прежней дозе. Это явление мы рассматриваем как собственно потерю ответа. В то время как для другого типа характерно возникновение регулярных (2 и более) обострений за несколько дней или недель до очередного введения и полностью купирующихся инфузией препарата в прежней дозе. Этот тип вторичной неэффективности мы определили как ускользание эффекта. Такие наблюдения хорошо подтверждаются данными по фармакокинетике инфликсимаба и связаны с тем, что перед очередным введением препарата концентрация вещества в крови минимальна (рис. 1) [20].
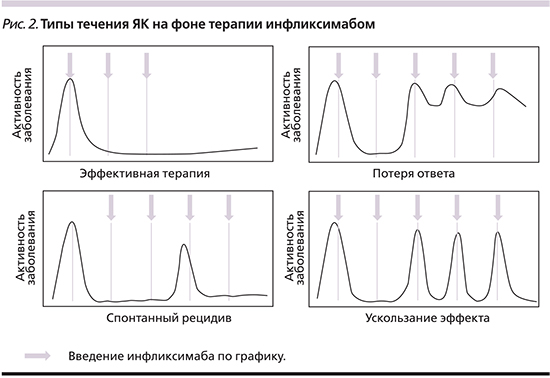
По нашим данным, существует еще один тип течения ЯК на фоне поддерживающей терапии инфликсимабом. У части пациентов встречаются единичные спонтанные рецидивы, возникающие крайне редко и купирующиеся добавлением местной терапии на короткий срок. Такое течение заболевания мы не рассматриваем как вторичную неэффективность препарата. Таким образом, в ходе исследования было выявлено 4 типа течения ЯК на фоне антицитокиновой терапии инфликсимабом. Данные графически представлены на рис. 2. Однако требуется дальнейшее наблюдение за массой пациентов для уточнения частоты встречаемости данных типов и их применения на практике.



