Постановка и кодировка диагноза могут базироваться на определении преобладания выраженности воспаления того или иного отдела ротоглотки.
Исключение составляют состояния, являющиеся клиническим проявлением других заболеваний:
- герпетический гингивостоматит и фаринготонзиллит (вызванный вирусом простого герпеса) (В 00.2);
- гриппозный (вирус гриппа идентифицирован (J 10.1), вирус гриппа не идентифицирован (J 11.1);
- при инфекционном мононуклеозе (В 27.-);
- энтеровирусный везикулярный фарингит, или «герпангина» (В 08.5).
В настоящее время предлагается отказаться от термина «ангина», т.к. ее классификация, основанная на фарингоскопической картине не коррелирует как с этиологией, так и терапевтической тактикой.
В зарубежной научно-медицинской литературе для обозначения острых воспалительных заболеваний глотки используют взаимозаменяемые термины «фарингит» и «тонзиллофарингит», под которыми понимают воспаление слизистой оболочки глотки и/или небных миндалин.
ЭПИДЕМИОЛОГИЯ
Острым тонзиллофарингитом болеют люди практически всех возрастов. Исключение составляют лишь дети первого года жизни, которые имеют материнский антитоксический и антимикробный стрептококковый иммунитет и болеют очень редко. В различных регионах России на долю острого тонзиллофарингита приходится 3–7% от общего числа регистрируемых заболеваний и от 17 до 42% среди инфекционных форм. Известно, что острый тонзиллофарингит и метатонзиллярные болезни (особенно ревматизм) широко распространены в странах с низким уровнем социально-экономического развития и плохими материально-бытовыми условиями. Наиболее восприимчивы к острому тонзиллофарингиту люди молодого возраста. До 75% заболеваемости острым тонзиллофарингитом дают лица в возрасте до 30 лет. Из них 40% и больше приходятся на тех, кому от 20 до 30 лет. Источником инфекции при стрептококковом тонзиллите являются больные, а также здоровые носители стрептококков (БГСА). Наибольшую эпидемиологическую опасность представляют больные острым тонзиллофарингитом, которые при разговоре и кашле выделяют во внешнюю среду большое количество возбудителей. Основной путь заражения – воздушно-капельный. Способность возбудителей ангины размножаться на некоторых видах пищевых продуктов служит предпосылкой возникновения пищевых вспышек заболевания. Острый тонзиллофарингит наблюдается обычно в виде спорадических заболеваний, преимущественно в осенне-зимние месяцы. Чаще болеют люди, проживающие в общежитиях, казармах. В организованных коллективах заболеваемость может приобретать эпидемический характер, в этих ситуациях восприимчивость людей к острому тонзиллофарингиту составляет примерно 10–15%.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
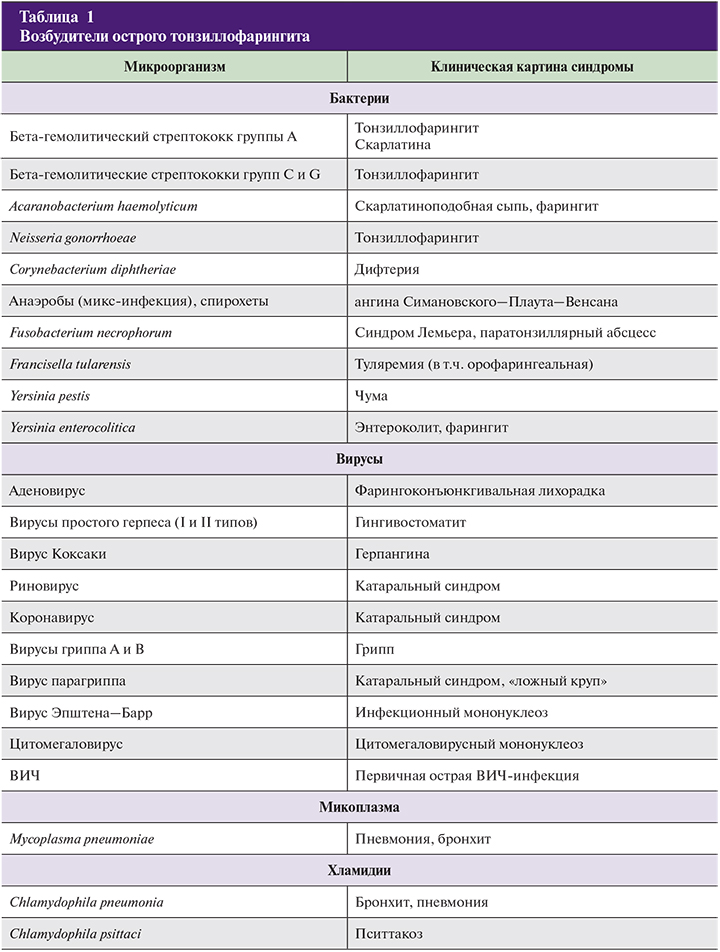
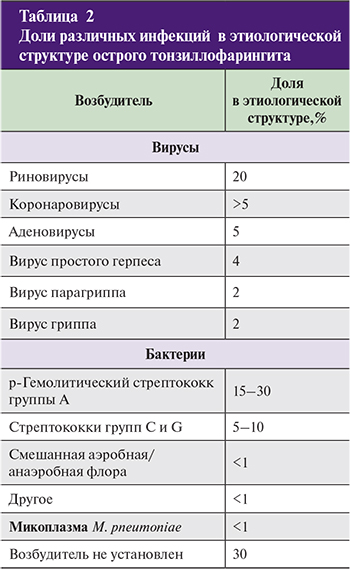
Наиболее частыми возбудителями острого тонзиллофарингита являются респираторные вирусы (аденовирус, вирус парагриппа, респираторно-синтициальный вирус, риновирус и другие). Возможна роль энтеровирусов (Коксаки В и др.), вируса Эпштейна–Барр. Среди бактериальных возбудителей первостепенное значение имеет бета-гемолитический стрептококк группы А (БГСА, или Streptococcus pyogenes). С данным возбудителем связано от 5 до 15% случаев острых тонзиллофарингитов во взрослой популяции и 20–30% – у детей.
Ряд авторов указывают на определенную роль других бактериальных возбудителей, таких как стрептококки групп С и G, Streptococcus pneumoniae, Arcanabacterium haemolyticum, анаэробы, Mycoplasma pneumonia и Chlamydia pneumonia.
Возбудители острого тонзиллофарингита и доли различных инфекций в его этиологической структуре представлены в табл. 1 и 2.
КЛАССИФИКАЦИЯ
 Классификация острого тонзиллофарингита основана на этиологическом принципе. В зависимости от степени поражения воспаления небных миндалин и задней стенки глотки выделяют несколько классических клинических форм острого тонзиллофарингита: катаральную (поражение слизистой оболочки), лакунарную (вовлечение лакунарного аппарата с образованием в лакунах налетов и гноя), фолликулярную (воспаление лимфоидных фолликулов), а также фибринозную, флегмонозную, язвенно-некротическую и смешанную формы.
Классификация острого тонзиллофарингита основана на этиологическом принципе. В зависимости от степени поражения воспаления небных миндалин и задней стенки глотки выделяют несколько классических клинических форм острого тонзиллофарингита: катаральную (поражение слизистой оболочки), лакунарную (вовлечение лакунарного аппарата с образованием в лакунах налетов и гноя), фолликулярную (воспаление лимфоидных фолликулов), а также фибринозную, флегмонозную, язвенно-некротическую и смешанную формы.
ДИАГНОЗ
Основной целью диагностики острого тонзиллофарингита является разграничение бактериальной (наиболее актуально стрептококковой (БГСА)) и вирусной этиологии заболевания.
Клинические признаки и симптомы
Жалобы
Основной жалобой при остром тонзиллофарингите является дискомфорт или боль в горле, усиливающиеся при глотании. При неосложненном течении, как правило, боль имеет симметричный характер. При выраженном вовлечении в воспалительный процесс боковых столбов глотки и/или реактивном отеке паратонзиллярной клетчатки возможна иррадиация в ухо, особенно выраженная при глотании. В раннем детском возрасте при невозможности вербализовать или правильно описать болевые ощущения обращает на себя внимание отказ ребенка от еды или от проглатывания пищи, предпочтение гомогенной или жидкой пищи.
Системные проявления:
- лихорадка (уровень лихорадки не коррелирует с этиологическим фактором и не может являться ориентиром для определения показаний к системной антибактериальной терапии; в редких случаях острый стрептококковый тонзиллофарингит может протекать с нормальной или субфебрильной температурой тела);
- ухудшение самочувствия (явления инфекционного токсикоза).
Местные проявления:
- гиперемия и отек небных миндалин, небных дужек, задней стенки глотки (реже – мягкого неба и язычка);
- налеты на небных миндалинах (реже, на задней стенке глотки) – явления регионарного лимфаденита (увеличение, уплотнение, болезненность, передне-шейных лимфатических узлов) – петехиальная энантема на мягком небе и язычке (симптом инфекционного заболевания БГСА-генеза – скарлатины).
Изолированная оценка наличия того или иного симптома (в т.ч. и налетов на миндалинах) не позволяет дифференцировать вирусную и бактериальную этиологию заболевания. В течение последних десятилетий был предложен ряд ориентировочных клинических и клинико-параклинических шкал для балльной оценки вероятности стрептококковой инфекции и, соответственно, определения показаний к системной антибактериальной терапии (шкалы Walsh, Breese, Centor). Наибольшее распространение получила шкала McIsaac. Тем не менее, опыт использования подобных шкал продемонстрировал их относительную неточность.
 В табл. 3 приведены наиболее характерные сочетания симптомов при БГСА и вирусном остром тонзиллофарингите, хотя точная верификация диагноза должна включать этиологическую расшифровку (отсутствие или наличие БГСА).
В табл. 3 приведены наиболее характерные сочетания симптомов при БГСА и вирусном остром тонзиллофарингите, хотя точная верификация диагноза должна включать этиологическую расшифровку (отсутствие или наличие БГСА).
Для орофарингеального кандидоза характерны относительно меньшая выраженность местных воспалительных реакций и наличие творожистых или крошковидных наложений, зачастую выходящих за пределы небных миндалин, при удалении которых обнажается эрозированная поверхность.
При поражении глотки филаментозными грибами (Aspergillus, Penicillium, Mucor и др.) клиническая картина несколько отличается, в основном характером патологических налетов и выраженностью местных симптомов.
Так, при аспергиллезе больных беспокоит сильная боль в горле, иногда иррадиирующая в ухо. Температура тела при этом остается субфебрильной. Явления интоксикации, как правило, выражены незначительно.
Лабораторные и инструментальные исследования
Выяснение причины заболевания (разграничение БГСА и вирусной этиологии) является ведущим в определении тактики лечения.
Однако информативность традиционных лабораторных исследований – уровня маркеров воспаления (лейкоцитоз, нейтрофилез, «сдвиг влево», СОЭ, С-реактивный белок, прокальцитонин) – является крайне низкой. Несмотря на то, что высокий уровень маркеров воспаления несколько чаще отмечается при бактериальном остром тонзиллофарингите, он возможен и при вирусном происхождении воспаления, в то время как низкие их уровни ни в коем случае не исключают стрептококковой этиологии.
В связи с этим единственным инструментом диагностики остается выделение БГСА в материале с небных миндалин и задней стенки глотки путем:
а) бактериологического культурального исследования;
б) использования экспресс-тестов на поверхностный антиген БГСА.
Бактериологическое культуральное исследование
Чувствительность и специфичность бактериологического исследования при соблюдении всех условий забора материала, транспортировки и инкубации оцениваются как близкие к 100%. Бактериологическое исследование материала с небных миндалин и задней стенки глотки проводится в микробиологической лаборатории с использованием 5% бараньего кровяного агара или с добавлением эритроцитарной массы. Предварительный результат может быть оценен через 24, окончательный – через 48–72 часа.
Экспресс-тесты
Из средств экспресс-диагностики в настоящее время используются тесты II поколения, основанные на методе иммуноферментного анализа или иммунохроматографии (в зависимости от производителя). Экспресс-тестирование предполагает получение результата «у постели больного» в течение 4–10 минут. Анализ выполняется врачом и не требует наличия специальной лаборатории. Средние специфичность и чувствительность современных тест-систем составляют 94 и 97% соответственно. Подобные характеристики позволяют избегать дублирующего бактериологического исследования при отрицательном результате экспресс-теста, как это делалось раньше.
Условия забора материала для бактериологического исследования или выполнения экспресс-теста:
- до начала антибактериальной терапии;
- до утреннего туалета полости рта, натощак или через 2 часа после еды;
- под контролем орофарингоскопии;
- следует избегать контакта с зубами и языком;
- материал получают из устьев крипт небных миндалин и задней стенки глотки.
При несоблюдении описанных выше условий информативность диагностических методов снижается, в связи с чем приходится принимать во внимание данные анамнеза и клинической картины.
Исследование уровня антистрептолизина-О (АСЛ-О) сыворотки крови является инструментом исключительно ретроспективной диагностики, т.к. он повышается лишь на 7–9-й день стрептококковой инфекции, а также может отражать ранее перенесенные заболевания или хроническую инфекцию.
Кроме того, согласно МУ 3.1.1082–01 «Эпидемиологический надзор за дифтерийной инфекцией», для наблюдения за распространением токсигенных коринебактерий дифтерии бактериологическое обследование на их наличие необходимо проводить с диагностической целью всем больным при подозрении на дифтерийную этиологию заболевания, в т.ч. больным острым тонзиллофарингитом с патологическим выпотом на миндалинах.
Верификация конкретного возбудителя (аденовирус, вирус парагриппа и др.) при вирусном заболевании в большинстве случаев не имеет практической ценности, т.к. не влияет на лечебную тактику и может быть использована только для научно-исследовательских целей. Исключение могут составлять лишь случаи подозрения на грипп и инфекционный мононуклеоз в связи с особенностями ведения таких пациентов с применением средств этиотропного лечения.
Выделение при микробиологическом исследовании грибов должно интерпретироваться в контексте клиники заболевания и фарингоскопической картины, т.к. они могут присутствовать в ротоглотке и в норме.
Дифференциальный диагноз
Дифференциальной диагностики требует обычно синдром боли в горле и фарингоскопические признаки воспаления. Необходимо помнить, что боль в горле может быть симптомом многих местных и системных воспалительных процессов.
Боль в горле и фарингоскопические изменения могут возникать при механическом и химическом раздражении (гастро-эзофагеальный рефлюкс, курение, использование ингаляционных глюкокортикостероидов, стекание отделяемого по задней стенке глотки при постназальном синдроме и интраназальных лекарственных препаратов и т.д). В связи с особенностями иннервации боль в глотке также может быть симптомом нефарингеальных нозологических процессов – патологии уха, сердечно-сосудистых заболеваний, заболеваний щитовидной железы, невралгии языкоглоточного нерва, инородных тел респираторного тракта, синдрома Игла–Стерлинга и некоторых других.
Далее представлена дифференциальная диагностика различных состояний, которые могут быть причиной болей в горле.
Самая вероятная причина
Вирусный фарингит.
Наиболее опасные заболевания, симулирующие ОТФ:
Сердечно-сосудистые (иррадиация болей в области глотки):
- стенокардия;
- инфаркт миокарда.
Злокачественные новообразования:
- рак ротоглотки и полости рта.
Инфекции
- острый эпиглоттит (чаще в детском возрасте);
- перитонзиллярный абсцесс;
- окологлоточный, боковоглоточный и заглоточный абсцессы;
- дифтерия;
- ВИЧ-инфекция.
Болезни крови:
- агранулоцитоз, острый лейкоз.
Источники неверного диагноза
Инородные тела
Инфекционный мононуклеоз
Кандидозный стоматит:
- у грудных детей;
- при ингаляциях кортикостероидов;
- на фоне сахарного диабета.
Болезни, передающиеся половым путем:
- фарингит, вызванный Neisseria gonorrhoeae;
- фарингит, вызванный вирусом простого герпеса 2-го типа;
- сифилис.
Острый тиреоидит
Раздражение верхних дыхательных путей (табачным дымом, химическими веществами).
Дыхание ртом.
Редкие причины:
- системная склеродермия;
- саркоидоз;
- срединная гранулема лица;
- туберкулез.
Состояния, вызывающие боли в горле
Побочное действие лекарственных средств и интоксикация.
Анемия.
Болезни щитовидной железы (острый тиреоидит).
Болезни позвоночника.
Психические нарушения и симуляция
Для исключения инфекционного мононуклеоза (острой Эпштейна–Барр-вирусной или цитомегаловирусной инфекции) необходима оценка всех доступных пальпации групп лимфатических узлов, определение размеров печени и селезенки.
В подозрительных на инфекционный мононуклеоз случаях необходимо лабораторное исследование, однако необходимо помнить, что даже такие ранние маркеры, как «атипичные мононуклеары» и иммуноглобулины М к EBV или CMV, могут появляться только на 4–7-е сутки заболевания.
Любые признаки асимметрии зева, задней стенки глотки, боковых столбов глотки, односторонний отек шеи в обязательном порядке должны рассматриваться как возможный гнойный процесс в клетчаточных пространствах шеи, а также вызывать онкологическую настороженность.
Язвенно-некротические процессы в ротоглотке зачастую могут быть следствием специфической инфекции, иммунодефицита или аутоиммунных процессов.
При атипичной фарингоскопической картине и/или неэффективности стандартной терапии необходимо исключение таких инфекций, гонорея, сифилис.
Также как при упорных, не поддающихся обычной терапии болях в горле требуется проведение дифференциальной диагностики с рядом синдромов, развивающихся при некоторых системных заболеваниях и болезнях нервной системы.
Синдром Plummer–Vinson возникает у женщин в возрасте от 40 до 70 лет на фоне железодефицитной анемии. Синдром Шегрена – аутоиммунное заболевание, сопровождающееся помимо выраженной сухости слизистой оболочки желудочно-кишечного тракта, диффузным увеличением слюнных желез. Для синдрома Eagle (стилалгии) характерны сильные постоянные, часто односторонние боли в горле, вызванные удлинением шиловидного отростка, который расположен на нижней поверхности височной кости и может прощупываться над верхним полюсом небной миндалины. Целый ряд невралгий (языкоглоточного или блуждающего нерва) также может быть причиной болей в горле, особенно у пожилых людей.
ЛЕЧЕНИЕ
В подавляющем большинстве случаев лечение может проводиться амбулаторно. Учитывая инфекционный характер заболевания (как при вирусной, так и при бактериальной этиологии), в ряде случаев пациенты требуют изоляции из организованных коллективов и назначение соответствующего эпидемиологического режима дома (использование масок, проветривание).
Показания к госпитализации:
- тяжелое состояние (инфекционный токсикоз, требующий инфузионной терапии);
- социальные (необходимость изоляции из ограниченных коллективов (детские дома, интернаты, воинские части, тюрьмы и т.п.) или заведомо низкая комплаентность (дети из «неблагополучных» семей и т.п.);
- наличие гнойных осложнений (паратонзиллярный, парафарингеальный, ретрофарингеальный абсцессы, гнойный лимфаденит и т.п.);
- наличие фоновых заболеваний с вероятностью декомпенсации на фоне острого воспалительного процесса.
Немедикаментозное лечение
В первые дни заболевания рекомендуется ограничение физической активности с целью предупреждения осложнений. Больному необходимо выделить отдельную посуду, полотенце, максимально ограничить контакт с окружающими, особенно с детьми. Рекомендуют обильное питье (фруктовые соки, чай с лимоном, настой шиповника, боржоми и пр.), щадящую, нераздражающую, преимущественно молочно-растительную диету, богатую витаминами.
После ликвидации местных и общих проявлений заболевания следует выждать 2–3 дня перед тем, как разрешить приступить к работе. В последующие 3–4 недели рекомендуют соблюдать щадящий режим: ограничить физическую нагрузку, избегать переохлаждения.
Хирургическое лечение
В случае диагностики паратонзиллярного абсцесса проводят хирургическое лечение, которое состоит в широком вскрытии абсцесса или проведении абсцесстонзиллэктомии. После вскрытия абсцесса показана тонзиллэктомия, которая обычно проводится через месяц.
Медикаментозное лечение
Системная антибактериальная терапия
В настоящее время единственным показанием к системной противомикробной терапии иммунокомпетентных лиц является стрептококковый (БГСА) генез воспаления (за исключением крайне редких случаев дифтерии, гонококкового тонзиллита и некоторых других специфических бактериальных процессов). В связи с этим крайне важна этиологическая дифференциальная диагностика, о чем было сказано выше. Таким образом, системная антибактериальная терапия показана 20–30% детей и 5–15% взрослых с острым тонзиллофарингитом.
Целями системной антибактериальной терапии при остром стрептококковом тонзиллофарингите являются:
- эрадикация возбудителя (БГСА);
- профилактика осложнений («ранних» гнойных и «поздних» аутоиммунных);
- ограничение очага инфекции (снижение контагиозности);
- клиническое выздоровление.
Выбор препарата
Антибиотикотерапия острого стрептококкового тонзиллофарингита отличается от таковой при других респираторных бактериальных инфекциях (острый бактериальный риносинусит, острый средний отит, пневмония) в силу известности целевого микроорганизма. 100% штаммов бета-гемолитического стрептококка группы А in vitro чувствительны к природному пенициллину и, соответственно, ко всем бета-лактамным препаратам последующих генераций.
В связи с этим стартовым препаратом для лечения острого стрептококкового тонзиллофарингита остается пенициллин (феноксиметилпенициллин внутрь).
Альтернативным препаратом с меньшей кратностью приема является амоксициллин. Необходимо помнить, что аминопенициллины (в т.ч. амоксициллин) противопоказаны при инфекционном мононуклеозе в связи с высокой вероятностью развития токсико-аллергических реакций (т.н. ампицилиновой, или амоксициллиновой, сыпи). Поэтому в случаях острого тонзиллофарингита, подозрительных на инфекционный мононуклеоз и требующих при этом назначения системной антибактериальной терапии рационально использование феноксиметилпенициллина, цефалоспоринов и макролидов.
Несмотря на существующую по сей день 100% чувствительность in vitro всех известных штаммов БГСА к пенициллину, появились наблюдения случаев его клинической и микробиологической неэффективности в связи с инактивацией антибиотика беталактамазами ко-патогенов в глотке и феноменом интернализации (внутриклеточным расположением) БГСА.
О клинической неэффективности можно говорить при отсутствии положительной динамики (купирование лихорадки, уменьшение болевого синдрома) в течение 48–72 часов. В подобном случае необходим пересмотр диагноза (вероятное течение ОРВИ, инфекционного мононуклеоза), а при уверенности в стрептококковом генезе – смена антибактериального препарата.
У пациентов с доказанной аллергией на бета-лактамные антибиотики возможно назначение пероральных цефалоспоринов II–III поколений, т.к. вероятность перекрестных аллергических реакций с пенициллинами составляет 1,9 и 0,6% для II и III поколений соответственно.
В случае наличия в анамнезе анафилактических реакций на бета-лактамные препараты или доказанной аллергии на цефалоспорины II–III поколений, предшествовавшего приема бета-лактамных антибиотиков по другим показаниям, или неэффективности стартовой терапии бета-лактальным антибиотиком целесообразно использовать макролиды или линкосамиды.
Преимуществом макролидов является их способность действовать как на атипичные ко-патогены, так и на внутриклеточно расположенный БГСА (при феномене интернализации). Среди макролидных антибиотиков кларитромицин (Клацид®) имеет наиболее сбалансированную фармакокинетику: высокие тканевые концентрации, что позволяет достичь эрадикации возбудителя, а также достаточно высокую концентрацию в плазме крови, что может быть важно для предотвращения осложнений.
Длительность терапии, необходимая для эрадикации БГСА, составляет 10 дней за исключением азитромицина (5 дней). В прямом сравнительном исследовании эффективности 10-дневного курса кларитромицина и 5-дневного курса азитромицина было продемонстрировано преимущество кларитромицина по проценту эрадикации возбудителя. Также последние данные демонстрируют, что широкое использование азитромицина вследствие его фармакокинетических особенностей (длительное, в течение 3 недель, выведение из организма) может ускорять развитие резистентности.
При заведомо низкой комплаентности (по социальным показаниям), а также при наличии в анамнезе у пациента или ближайших родственников ревматической лихорадки) в качестве альтернативы курсу пероральной антибактериальной терапии возможно однократное внутримышечное введение бензатин-пенициллина.
Суточные дозы, режим введения антибиотиков отражены в табл. 4.
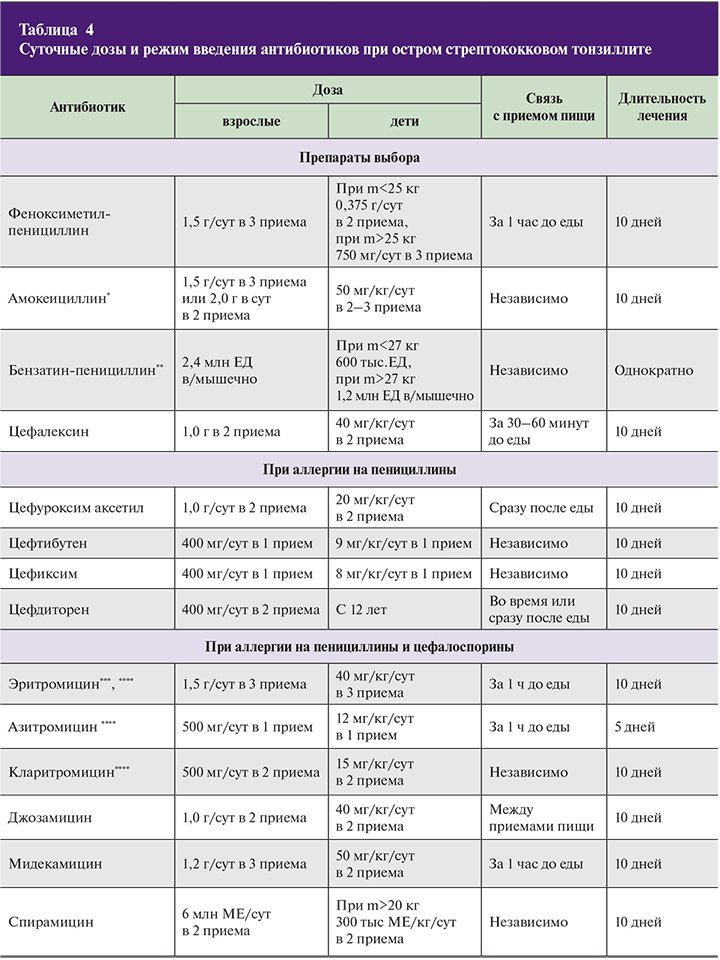
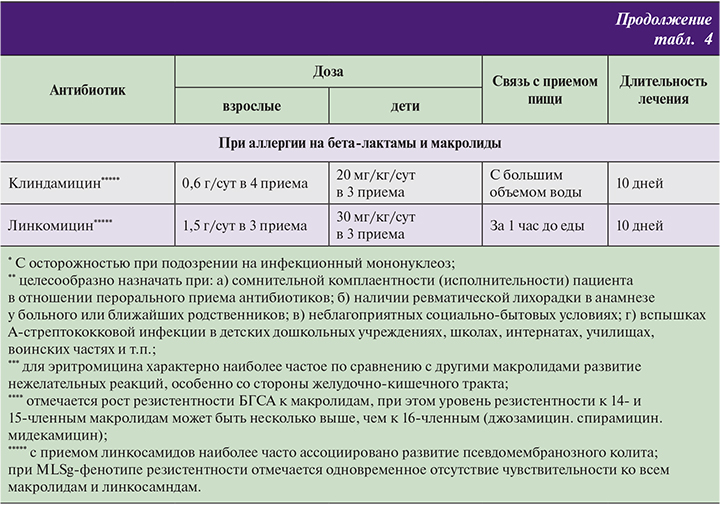
При рецидивирующем течении острых стрептококковых тонзиллофарингитов с целью преодоления механизмов, обуславливающих микробиологическую неэффективность предшествующего лечения, целесообразно назначение амоксициллин/клавуланата в дозе 875/125 мг 2 раза в день (детям – 40–50 мг/кг/сут в 2–3 приема) внутрь в течение 10 дней или терапия пероральными цефалоспоринами II–III поколений (цефуроксим аксетил, цефтибутен, цефиксим, цефдиторен), по указанным выше схемам. 14-членные макролиды (кларитромицин) способны разрушать бактериальные биопленки, которые образуются при рецидивирующем течении заболевания, и также могут быть фактором неэффективности терапии.
Местная антибактериальная терапия
В случаях нестрептококковой этиологии острого тонзиллофарингита, а также, при БГСА-инфекционных процессах комплексно с системной антибактериальной терапией возможно топическое применение антимикробных препаратов, например ингаляционно. При ингаляционном пути введения отмечается быстрый терапевтический эффект при более низких концентрациях лекарственных средств и быстрой доставке препарата в очаг инфекции, уменьшается риск развития нежелательных явлений. Введение лекарственного вещества безболезненно, осуществляется в процессе естественного акта дыхания (возможно даже во сне), при этом непосредственно в очаге микробного поражения создается высокая концентрация лекарственного вещества.
Одним из лекарственных средств для местного лечения респираторных заболеваний бактериальной этиологии является тиамфеникола глицинат ацетилцистеинат (Флуимуцил антибиотик ИТ). Флуимуцил антибиотик ИТ – это уникальная комбинация антибиотика широкого спектра действия тиамфеникола глицината и муколитика прямого действия N-ацетилцистеина.
Тиамфеникол является производным хлорамфеникола и относится к синтетическим антибиотикам группы амфениколов. Механизм его действия связан с бактериостатическим эффектом, т.е. с нарушением синтеза белка в клетках патогенных бактерий. Доказано его влияние на наиболее частые возбудители инфекций дыхательных путей, как на грамположительные бактерии он активен в отношении многих штаммов, устойчивых к бета-лактамным антибиотикам, внутриклеточных возбудителей (Legionella, Сhlamidia, Mycoplasma), штаммов Streptococcus pyogenes, Staphylococcus aureus, Haemophilus influenzaе, Moraxella catarrhalis, т.е. наиболее частых возбудителей респираторных инфекций, в то время как некоторые их штаммы становятся более устойчивыми к пенициллину и/или эритромицину.
N-ацетилцистеин оказывает прямое муколитическое действие за счет свободной сульфгидрильной группы, которая разрушает дисульфидные связи между молекулами мукополисахаридов секрета и, таким образом снижает вязкость, в том числе при гнойном характере секрета.
N-ацетилцистеин обладает выраженными антиоксидантными свойствами и связанным с ними противовоспалительным и антитоксическим эффектом. N-ацетилцистеин имеет ряд свойств, имеющих большое значение при бактериальных инфекциях респираторной системы:
- снижение адгезии бактерий на эпителиальных клетках слизистой оболочки бронхов,
- ингибирующее действие на бактериальные биопленки.
При изучении фармакокинетики продемонстрировано, что препарат Флуимуцил антибиотик ИТ при аэрозольном пути введения (500 мг) достигает в плазме максимальных концентраций, ненамного уступающих концентрациям препаратов, вводимых перорально. Также была выявлена его низкая сывороточно-протеиновая связь. Все это способствует высокой фармацевтической биодоступности.
Препарат ТГА (Флуимуцил антибиотик ИТ®) выпускается в виде лиофилизата для приготовления раствора, имеет разные пути введения. Наиболее частым является его ингаляционное применение.
Применение Флуимуцила антибиотика позволяет улучшить течение заболевания, любой бактериальной этиологии, сократить применение системных антибиотиков или избежать его при нестрептококковых тонзиллофарингитах.
В результате применения антибактериальных средств могут отмечаться побочные эффекты в виде развития дисбактериоза и негативного влияния на иммунную систему, что может обусловливать снижение интенсивности местного иммунного ответа. В ряде случаев на фоне неадекватной антимикробной терапии их действие может вызвать парадоксальный эффект – воспаление принимает затяжное течение, рецидивирует или становится хроническим. В связи с этим все большее внимание уделяется применению иммунотропных лекарственных средств. Применение топического бактериального лизата Имудон® на втором этапе лечения острого тонзиллофарингита способствует восстановлению защитных свойств слизистой оболочки и препятствует хронизации воспаления.
Вирусный острый тонзиллофарингит
При вирусном остром тонзиллофарингите антибиотики не показаны в качестве стартовой терапии, но могут быть назначены в случае присоединения бактериальной инфекции. Рекомендуют топические антимикробные, противовоспалительные, анестезирующие и иммуннотропные средства в виде полосканий, спреев и пастилок для рассасывания. Противовирусные препараты назначают обычно при герпетическом поражении. Обычно применяют ацикловир по 0,2 г в таблетках 3–5 раз в сутки в течение 5 дней, тилорон по 0,125 г в таблетках 2 раза в сутки в первые 2 дня, затем по 1 таблетке каждые 48 часов в течение недели, эргоферон по 1 таблетке каждые 30 минут в первые 2 часа, затем еще три приема через равные промежутки времени, со 2-х суток и далее до выздоровления по 1 таблетке 3 раза в день. Профилактическое назначение системных антибиотиков при вирусном остром тонзиллофарингите не предотвращает развития бактериальных осложнений и поэтому необоснованно.
Системная противогрибковая терапия
При орофарингеальном кандидозе, сопровождающемся субъективными клиническими жалобами и общей симптоматикой, большой площадью поражения и неэффективностью местной терапии, возможно назначение флуконазола внутрь в дозе 50–100 мг/сут (детям: в дозе 3–6 мг/кг/сут) в 1 прием на срок 7–14 дней.
Для лечения обострений хронического фарингомикоза у пациентов с иммунодефицитом доза флуконазола увеличивается до 200 мг/сут, а продолжительность терапии – до 28 дней, при этом обязателен прием «противорецидивной» дозы – 100 мг флуконазола 3 раза в неделю пожизненно. Препаратами резерва для проведения системной терапии фарингомикоза являются итраконазол и кетоконазол. Они назначаются пациентам, у которых при выявлении возбудителя доказана его резистентность к флуконазолу. Альтернативными препаратами являются амфотерицин В, вориконазол, позаконазол и каспофунгин. Они назначаются только в стационаре, только по жизненным показаниям пациентам с иммунодефицитом различного генеза. Лечение обострения фарингомикоза должно продолжаться в среднем 2–3 недели и в течение 1 недели после стихания жалоб и клинических признаков заболевания.
Симптоматическая системная терапия
Для купирования лихорадки и/или болевого синдрома возможно использование нестероидных противовоспалительных средств (НПВС) в стандартных рекомендованных дозах. В детском возрасте предпочтение необходимо отдавать препаратам парацетамола или ибупрофена в дозах 10–15 и 8–10 мг/кг/прием соответственно. Следует предостеречь от необоснованного приема жаропонижающих средств (у детей старше 3 месяцев без фебрильных судорог в анамнезе, согласно рекомендациям ВОЗ, необходимо снижать температуру >39,5°С). Необоснованное медикаментозное купирование лихорадки может затруднить объективную оценку эффективности начатой антибактериальной терапии при стрептококковом тонзиллите.
В ряде клинических случаев у пациентов с острым тонзиллофарингите развивается кашель. В этом случае целесообразно назначение комплексного препарата Ренгалин. Кроме противокашлевого действия Ренгалин за счет входящих в него компонентов оказывает противовоспалительное, противоотечное, антиаллергическое, спазмолитическое (антитела к гистамину, антитела к брадикинину) и анальгезирующее действия (антитела к морфину).
Активный компонент Ренгалина на основе антител к морфину избирательно снижает возбудимость кашлевого центра продолговатого мозга, тормозит центральные звенья кашлевого рефлекса. Угнетая центры болевой чувствительности в таламусе, блокирует передачу болевых импульсов к коре головного мозга. Ингибирует поток болевой импульсации с периферии вследствие уменьшения высвобождения тканевых и плазменных альгогенов (гистамина, брадикинина, простагландинов и др.). В отличие от наркотических анальгетиков не вызывает угнетение дыхания, лекарственной зависимости, не обладает наркогенным и снотворным действиями. Ренгалин облегчает проявления острого фарингита, ларингита и бронхита, уменьшая бронхоспазм, а также купирует системные и местные симптомы аллергических реакций за счет влияния на синтез и высвобождение гистамина и брадикинина из тучных клеток.
Местная терапия
Лекарственные средства для топического использования могут рассматриваться в качестве вспомогательного лечения при остром стрептококковом тонзиллофарингите, однако в случае вирусной инфекции обоснованна местная монотерапия.
В настоящее время на фармацевтическом рынке представлен широкий спектр местных средств для терапии острого тонзиллофарингита в виде полосканий, спреев, ингаляций, а также таблеток и пастилок для рассасывания.
Целью местной терапии является быстрое уменьшение выраженности болевого синдрома и других воспалительных явлений, а также профилактика вторичного инфицирования поврежденной слизистой оболочки.
Это определяет основные направления местной терапии:
- противовоспалительные и обезболивающие вещества;
- антисептики и антибиотики с местноанестезирующим, антисептическим, противовоспалительным действиями;
- иммунотропные препараты.
К наиболее широко используемым синтетическим местным антисептикам относятся бензалкония хлорид, гексэтидин, дихлорбензил, амилметакрезол, хлоргексидин, препараты йода, октенидин, мирамистин, биклотимол, сульфаниламиды и другие. При назначении местных антисептиков следует придерживаться разрешенной кратности приема и возрастных ограничений в связи с определенной токсичностью некоторых из них (хлоргексидин) и учитывать возможность развития аллергических реакций (препараты йода, сульфаниламиды).
Местные нестероидные противовоспалительные препараты (НПВП) могут входить как в состав комплексных средств или применяться в виде монопрепаратов. Среди них наиболее часто используются флурбипрофен, кетопрофен, бензидамина гидрохлорид (Тантум верде, Оралсепт). НПВП обладают сравнительно быстрым и выраженным анальгетическим эффектом за счет локального блокирования продукции медиаторов боли. Бензидамин (действующее вещество препарата Оралсепт) – НПВП, который обладает неспецифичным противовоспалительным действием, не подавляет выработку простагландинов, поэтому он не имеет побочных эффектов, характерных для классических НПВП. Также бензидамин обладает широким спектром противомикробного действия; оно обусловлено его способностью быстро проникать через мембраны патогенов, приводя к повреждению клеточных структур. Высокая липофильность бензидамина по градиенту рН (слабощелочная) позволяет ему проникать в очаг воспаления и накапливаться в нем в высокой концентрации; имеет минимальную системную биодоступность при местном применении. Структура молекулы бензидамина подобна таковым у местных анестетиков, что обеспечивает достаточно быстрое купирование боли. Таким образом, бензидамин оказывает противовоспалительное действие, благодаря чему уменьшает все местные признаки воспаления, включая не только боль, но и гиперемию, отек и другие. Многие препараты в качестве обезболивающего компонента включают ментол.
Примерами таблеток и пастилок для рассасывания являются Имудон, Фарингосепт, Стрепсилс, Колдакт Лорпилс, Гексализ, Септолете, Граммидин, Лизобакт и др.
Аэрозоли для местной терапии ХТ включают Гексорал, Стоматидин, Стопангин, Гексаспрей, Ингалипт, Каметон и др.
Местная терапия не может заменить системную антибактериальную терапию при остром стрептококковом тонзиллите, т.к. не влияет на вероятность развития поздних аутоиммунных осложнений.
Оценка эффективности лечения
При своевременном и адекватном лечении острого тонзиллофарингита излечиваются за 7–10 дней. Критериями эффективности лечения являются улучшение общего состояния, снижение температуры тела, постепенное исчезновение дискомфорта и болевых ощущений, уменьшение воспалительной реакции регионарных ЛУ, стихание воспалительного процесса в слизистой оболочке миндалин и глотки, очищение лакун от экссудата. Отсутствие положительной динамики от лечения в течение 2–3 суток прежде всего свидетельствует о неадекватности выбранного антимикробного ЛС и требует его замены. Отсутствие лечебного эффекта может быть связано с неправильной диагностикой формы острого тонзиллофарингита на первичных этапах обследования и в силу этого неверно рекомендованным лечением (например, ангина при инфекционном мононуклеозе). Пациенты с острым тонзиллофарингитом нуждаются в динамическом наблюдении терапевтом и отоларингологом; при неэффективности выбранного метода лечения показана консультация инфекционистом.
Осложнения и побочные эффекты лечения
Осложнения и побочные эффекты лечения соответствуют неблагоприятным побочным эффектами ЛС, применяемых для лечения острого тонзиллофарингита.
Ошибки и необоснованные назначения
Ошибками антибактериальной терапии являются:
Неправильный выбор антибиотика. Применение тетрациклинов, сульфаниламидов, ко-тримоксазола и хлорамфеникола при тонзиллите, вызванном бета-гемолитическим стрептококком группы А, не оправданно по причине высокой частоты резистентности и, следовательно, низких показателей эффективности терапии.
Отсутствие показаний к назначению антибиотика (острого тонзиллофарингита вирусного происхождения).
Сокращение курса антибиотикотерапии при клиническом улучшении.
Позднее назначение антибиотиков.
Ошибочным является назначение антибиотиков с профилактической целью.
ПРОГНОЗ
Острый вирусный тонзиллофарингит как заболевание, склонное к саморазрешению у иммунокомпетентных лиц, в подавляющем большинстве случаев заканчивается самостоятельным выздоровлением независимо от проводимого лечения.
Благоприятный исход при остром стрептококковом тонзиллофарингите, который также может разрешиться самостоятельно, определяется отсутствием негнойных осложнений, что достигается назначением системной антибактериальной терапии. При этом задержка начала системной антибактериальной терапии на несколько дней (например, при ожидании результатов бактериологического исследования) не повышает риска развития острой ревматической лихорадки.
Особого внимания заслуживают пациенты с первичными и вторичными иммунодефицитами (в т.ч. ВИЧ-инфекцией), сахарным диабетом, что обусловлено относительно большим риском развития гнойно-некротических осложнений с фульминантным и иногда фатальным течением.