Введение
Сахарный диабет 2 типа (СД2) – метаболическое заболевание, развивающееся вследствие нарушения секреции инсулина или сниженной чувствительности тканей к действию инсулина (инсулинорезистентности) [1]. Пациенты с СД2 часто имеют сопуствующие заболевания сердечно-сосудистой, нервной систем и др., которые также требуют обязательного медикаментозного лечения. Например, наличие у пациента с СД2 артериальной гипертензии и дислипидемии в качестве сопутствующих заболеваний значительно повышает риск развития тяжелых макрососудистых осложнений и смертность [2]. Вследствие этого пациенты с СД2 имеют высокий риск полипрагмазии, которая в свою очередь также является неблагоприятным прогностическим фактором и может стать причиной возникновения осложнений (нежелательных побочных реакций) вследствие лекарственных взаимодействий, коррекция которых также потребует дополнительного назначения лекарственных средств (ЛС) и лишь ухудшит ситуацию. Одним из самых грозных осложнений терапии СД2, нередко возникающих вследствие лекарственных взаимодействий, является гипогликемия и ее крайняя степень – гипогликемическая кома. Гипогликемия – уровень глюкозы плазмы <2,8 ммоль/л, сопровождающийся клинической симптоматикой (сердцебиение, дрожь, бледность кожи, потливость, мидриаз, тошнота, сильный голод, беспокойство, тревога, агрессивность, слабость, нарушение концентрации, головная боль, головокружение, сонливость, парестезии, нарушения зрения, растерянность, дезориентация, дизартрия, нарушение координации движений, спутанность сознания, кома, судороги) или <2,2 ммоль/л независимо от симптомов. Мероприятия по купированию гипогликемии у больных СД, получающих сахароснижающую терапию, следует начинать при уровне глюкозы плазмы <3,9 ммоль/л. Основная причина гипогликемии – избыток инсулина в организме по отношению к поступлению углеводов извне (с пищей) или из эндогенных источников (продукция глюкозы печенью), а также при ускоренной утилизации углеводов (мышечная работа). Частыми провоцирующими факторами развития гипогликемии являются передозировка сахароснижающих препаратов (ССП), переход с одной группы СПП на другую или погрешности в диете (пропуск приема или недостаточное количество ХЕ, алкоголь, ограничение питания для снижения массы тела без соответствующего уменьшения дозы ССП и др.) [3].
Следует особо отметить, что риски гипогликемии могут повышать не только ЛС, но и продукты питания, а также биологически активные добавки к пище (БАД).
В данной статье представлен краткий обзор некоторых фармакокинетических и фармакодинамических взаимодействий ССП, которые могут приводить к гипогликемии.
Фармакокинетические взаимодействия
Фармакокинетические взаимодействия включают взаимодействия на уровне всасывания (абсорбции), распределения, метаболизма и выведения лекарств [2]. Все это так или иначе изменяет концентрацию препарата в плазме крови, а значит, и его терапевтическую эффективность, под которой в фармакологии понимают величину фармакологического эффекта.
На этапе абсорбции важную роль играет одновременный прием препарата с пищей, который может приводить к замедлению/ускорению всасывания ЛС или снижать/повышать его биодоступность и тем самым становиться причиной недостаточной/избыточной терапевтической эффективности. Клиническим примером, иллюстрирующим данный тип взаимодействия, является снижение и замедление скорости абсорбции метформина при его одновременном приеме с пищей [4].
Другой важный фактор, играющий роль на этапе всасывания – Р-гликопротеин (син. белок множественной лекарственной устойчивости-1) – мембранный белок из семейства ABC-переносчиков, обеспечивающий перенос многих веществ, в т.ч. некоторых ЛС, через мембрану клетки [5–6]. Если ЛС является его субстратом, то ингибирование/потенцирование активности Р-гликопротеина будет повышать или снижать биодоступность такого препарата.
Также частым механизмом фармакокинетических взаимодействий является ингибирование или индукция ферментов цитохрома-Р450 печени, ответственных за метаболизм ЛС [2]. В качестве примера можно привести линаглиптин, который является одновременно субстратом CYP3A4 и Р-гликопротеина. В эксперименте было показано, что одновременное применение линаглиптина с ингибитором P-гликопротеина и CYP3A4 ритонавиром приводило к увеличению AUC и Cmax линаглиптина в 2 и 3 раза соответственно [7].
Хотя в инструкции по медицинскому применению линаглиптина данные эффекты были расценены как клинически незначимые, потенциально при некоторых клинических обстоятельствах это может приводить к возникновению у пациента гипогликемии.
В этом контексте генетические различия также имеют клиническое значение, т.к. ЛС, метаболизируемые ферментами CYP, могут существенно различаться по скорости их элиминации в зависимости от генетически определяемой активности фермента [8]. Более того, в метаболизме препаратов играет роль в т.ч. и пол пациента: для мужчин, как правило, требуются более высокие дозы ЛС ввиду более активного метаболизма печеночными ферментами [9, 10].
Важно, что не только ЛС, но и продукты питания и БАД к пище могут взаимодействовать с ЛС, включая ССП. Продукты питания, БАД, препараты растительного происхождения часто представляют собой сложную смесь биологически активных веществ, которые могут взаимодействовать с фармакологическими препаратами разнообразным и непредсказуемым образом.
Проблема усугубляется тем обстоятельством, что в большинстве случаев у врача имеется недостаточно информации о потребляемых пациентом БАД и рационе питания. Примером данного типа взаимодействия, которое потенциально может приводить к повышению риска гипогликемии, является взаимодействие алоэ вера (ингибитор CYP3A4 и 2D6) и ингибиторов дипептидилпептидазы-4 (ДПП-4) [11, 12].
Фармакодинамические взаимодействия
Фармакодинамические взаимодействия возникают на уровне рецепторов или фармакологических эффектов и, как правило, не затрагивают концентрации ЛС в крови. Взаимодействие может быть синергетическим, аддитивным, антагонистическим и иногда приводить к повышению риска нежелательных явлений. Примером желаемого фармакодинамического взаимодействия является аддитивный эффект снижения уровня глюкозы в крови путем комбинации двух или более ССП, например метформина (снижает инсулинорезистентность) и ЛС, стимулирующего выделение инсулина поджелудочной железой (ингибиторы ДПП-4, агонисты глюкагоно-подобного полипептида-1[ГПП-1] и др.). К сожалению, комбинированная сахароснижающая терапия может приводить к развитию гипогликемии, что также можно рассматривать как фармакодинамическое взаимодействие. Риск существенно повышается, когда комбинированная терапия включает производные сульфонилмочевины [13]. Пациентам, которым для достижения целевых значений гликемии необходимо проведение комбинированной терапии, рекомендуется подбирать комбинации из препаратов с низким риском гипогликемии (агонисты ГПП-1, ингибиторы ДПП-4, метформин, ингибиторы SGLT-2 белка, ингибиторы α-гликозидаз) [3].
Клинически значимые фармакодинамические взаимодействия ССП и ЛС других фармакологических групп, возникает когда используются препараты, влияющие на метаболизм глюкозы. Особое клиническое значение имеет сопутствующая терапия β-адреноблокаторами, которые могут усиливать гипогликемический эффект, например, производных сульфонилмочевины [14].
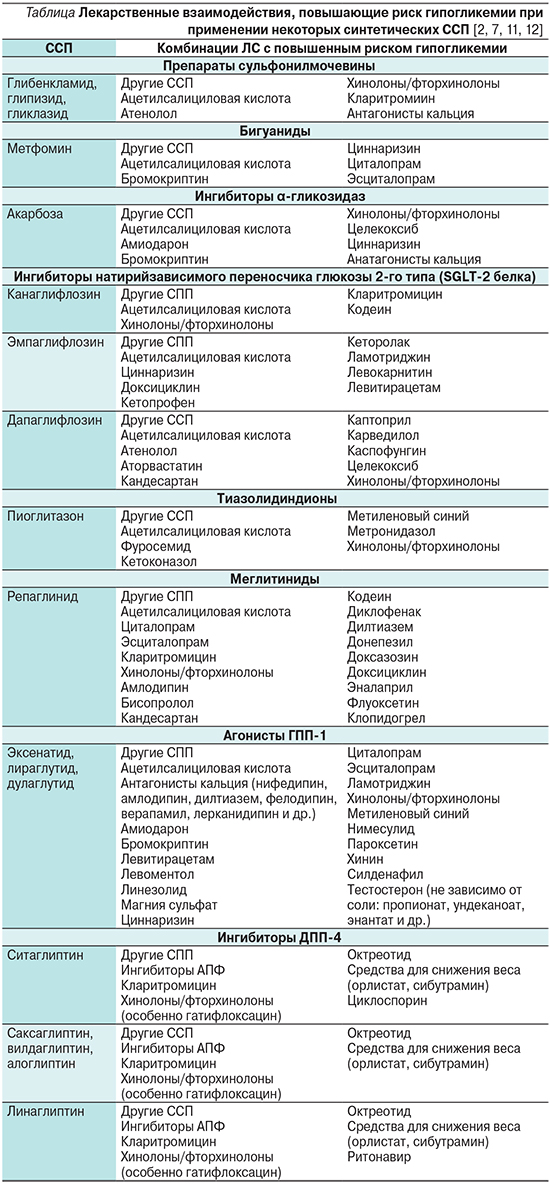
Краткий перечень потенциальных лекарственных взаимодействий между некоторыми ССП, которые повышают риск развития гипогликемии, представлены в таблице.
Заключение
Таким образом, коморбидные пациенты с СД2 требуют особого пристального внимания и дополнительного гликемического мониторинга на предмет развития гипогликемии как следствия взаимодействия междуССП и ЛС, назначаемыми для лечения сопутствующих заболеваний, а также БАД и продуктов питания.



