Распространенность нефролитиаза в развитых странах составляет до 5%. Большинство мочевых камней состоит из оксалата кальция (60%), фосфата кальция (20%), мочевой кислоты (10%), цистина (3%), трипельфосфата (7%). Существует несколько причин образования камней. Это низкий диурез, повышение экскреции кальция с мочой – гиперкальциурия. Гиперурикозурию, повышенный уровень мочевой кислоты сыворотки крови, обнаруживают примерно у 10% больных с камнями из оксалата кальция. Причинами гиперурикозурии может быть подагра, употребление продуктов, богатых пуринами, гемобластозы, злоупотребление алкоголем, прием урикозурических средств. При гиперурикозурии образуются кристаллы или коллоидные частицы мочевой кислоты, способствующие образованию кальциевых камней.
Низкий рН мочи – причина образования уратных камней. В кислой среде мочевая кислота находится в недиссоциированной форме и легко кристаллизуется, образует уратные или смешанные камни или способствует образованию кальциевых камней. При почечном дистальном канальцевом ацидозе, вторичной оксалурии, гипокалиемии, тяжелой физической нагрузке, повышенном потреблении животного белка и избытке натрия наблюдается гипоцитратурия. Цитрат образует с кальцием растворимые комплексы, уменьшая насыщение мочи солями кальция. Снижение экскреции цитрата с мочой – еще одна причина образования камней в мочевой системе. Гипоцитратурия является единственным нарушением для 10% больных мочекаменной болезнью, а для 50% больных она сочетается с другими причинами образования камней. При обследовании больных нефролитиазом уточняют рН мочи и ее динамику. При рН более 7,2 образуются трипельфосфатные камни, а при рН менее 5,5 – уратные камни. Показана обратная связь между потреблением большого количества жидкости и образованием камней в почках. Общей рекомендацией пациентам, у которых образуются мочевые камни, может быть поддержание высокого объема диуреза (не менее 2 литров) путем приема значительных объемов жидкостей.
Адекватное обучение пациентов в отношении приема жидкостей и диеты оказывается более значимым, поскольку исход лечения будет в значительной мере определяться соблюдением пациентом режима лечения. Идеальный лекарственный препарат должен предотвращать образование кальциевых камней, не вызывать побочных эффектов и допускать несложные схемы приема. Особенно эти аспекты важны для достижения достаточно хорошей степени соблюдения режима лечения. Низкая экскреция цитрата – одно из хорошо изученных и часто встречающихся нарушений при кальциевом типе камнеобразования. Цитрат играет важную роль с учетом возможности образования его комплексов с кальцием. Более того, цитрат подавляет рост и агрегацию этих кристаллов. Назначение щелочной соли приводит к повышению рН и повышению экскреции цитрата. Прием препаратов, создающих условия для растворения конкрементов, может быть эффективной терапией первой линии лечения [11]. Этот метод лечения применяется в дополнение к дистанционной ударно-волновой литотрипсии (ДЛТ), чрескожной литотрипсии, уретролитотрипсии или открытому оперативному вмешательству для облегчения выведения небольших резидуальных фрагментов.
Клиническая эффективность дистанционной литотрипсии связана с физико-химическими характеристиками камня [12, 14, 17, 18]. Одним из значимых прогностических факторов служит структурная плотность камня, определяемая спиральной рентгеновской компьютерной томографией (КТ-плотность) [8, 13].
Исследования, проведенные в клинике урологии Первого МГМУ им. И.М. Сеченова с целью выявления зависимости кратности ДЛТ от структурной плотности, показали, что при структурной плотности более 800–1000 по шкале Нounsfield (HU) повышается частота (2–3) повторных сеансов ДЛТ и возникает необходимость использовать высокоэнергетические режимы дезинтеграции [13]. Ввиду этого предоперационная медикаментозная подготовка к ДЛТ означает необходимость использования препаратов, изменяющих структуру, плотность и размеры (объем) камня [13]. Достижение данного клинического результата возможно при проведении цитратной терапии: калий-натрий цитратными препаратами (Блемарен), цитратом калия и калий-магниевым цитратом.
Особенно возрастает значение цитратной терапии после ДЛТ камней чашечек, в частности, у больных с рецидивными и резидуальными камнями нижней чашечки. По данным рандомизированного исследования (110 пациентов), проведенного больным с полным отхождением конкрементов после ДЛТ и лечением цитратом калия, через 12 месяцев отсутствовали рецидивные камни, а в контрольной группе последние встречались в 28,1% случаев [9]. Похожие результаты наблюдались в группе больных с резидуальными камнями. При лечении цитратом калия период ремиссии был значительно выше по сравнению с группой, в которой больные не получали лечения (44,5 и 12,5% соответственно). Как считают авторы, терапия цитратом калия важна в профилактическом лечении кальций-оксалатного уролитиаза после ДЛТ камней нижней чашечки.
Комбинированное применение ДЛТ и хемолиз – самый малоинвазивный способ лечения пациентов с коралловидными конкрементами, которым не показана чрескожная нефролитотрипсия. Дробление конкремента приводит к увеличению его поверхности, что повышает эффективность хемолиза. Прием препаратов, предназначенных для хемолиза, эффективен только при конкрементах из мочевой кислоты.
Высокую эффективность цитратной терапии в профилактике рецидивного кальций-оксалатного камнеобразования отмечает ряд авторов [1, 2, 10, 15, 16]. Проведение цитратной терапии после ДЛТ способствует уменьшению частоты рецидивного и резидуального кальций-оксалатного камнеобразования в 2 раза [3]. Эффективность профилактической цитратной терапии (калий-магниевый цитрат) при кальций-оксалатных камнях составляет 85% [5]. Наиболее эффективна профилактика цитратными препаратами при камнях из мочевой кислоты (100%), оксалата кальция (86,7%) [16], а также при комбинированных камнях из оксалата кальция и фосфата (96,7%). Авторы подчеркивают актуальность профилактики кальций-оксалатного камнеобразования с использованием цитрата при гиперкальциурии с гиперурикозурией, при наличии в составе камня дигидрата оксалата кальция (ведделлит) и риска рецидивного камнеобразования в единственной почке.
Принципиальное преимущество препарата Блемарен («Esparma GmbH», Германия) перед другими цитратными препаратами заключается в преобладании в нем лимонной кислоты над ее солью, значительную же часть буферной функции выполняет гидрогенкарбонат калия. Пониженное содержание натрия в препарате способствует ускоренному растворению мочевой кислоты в почечных канальцах и предотвращает их дальнейшую кристаллизацию. Ограниченное количество калия в препарате позволяет расширять показания к его применению в случаях, где содержание калия в организме имеет клиническое значение [19, 20]. Пероральный прием Блемарена обеспечивает дозозависимое смещение рН мочи от кислого до нейтрального или щелочного, не изменяя кислотно-основного баланса крови; суточная доза калий-натрий цитрата в 66–110 ммоль не оказывает влияния на уровень калия, натрия, кислорода, углекислоты и гидрогенкарбоната в крови. Цитрат связывает ионы кальция на всем своем пути – от желудочно-кишечного тракта, где он снижает всасывание кальция, до мочевых путей, где этот эффект наиболее активен в связи с наибольшей концентрацией цитрата. Кроме того, стабилизируя растворы, цитрат препятствует процессам кристаллизации в моче. Комплексное влияние цитрата на физико-химическое состояние мочи приводит к повышению растворимости уратов, кальцинатов и в первую очередь оксалатов, комплексных магний-аммониевых фосфатов и некоторых других солей, способствуя торможению камнеобразования и растворению уже сформировавшихся конкрементов, тем самым повышая ингибирующую активность мочи [1, 2, 4, 6, 7, 15]. Доза Блемарена устанавливается индивидуально в зависимости от достигнутой кислотности мочи, которая должна поддерживаться на оптимальном для каждого вида камней уровне. Контроль рН мочи проводится с помощью индикаторной бумаги перед каждым приемом препарата. При уратных, кальций-оксалатных или смешанных уратно-оксалатных камнях рН в течение суток следует поддерживать в пределах 6,2–6,8. Средние суточные дозы колеблются в пределах 6–18 г, равномерно распределенные в течение дня на 2–3 приема.
В основе лечения лежит ощелачивание мочи с помощью приема цитратных смесей или двууглекислого натрия. Разрушение кальций-оксалатных камней с помощью калий-натрий цитрата основано на связывании иона кальция цитрат ионом и переходом в растворимое соединение. На основании полученных данных считаем, что действие Блемарена in vitro приводит к уменьшению твердости кальций-оксалатных камней (от 1400 до 900 Нu), возможно, за счет увеличения их «пористости».
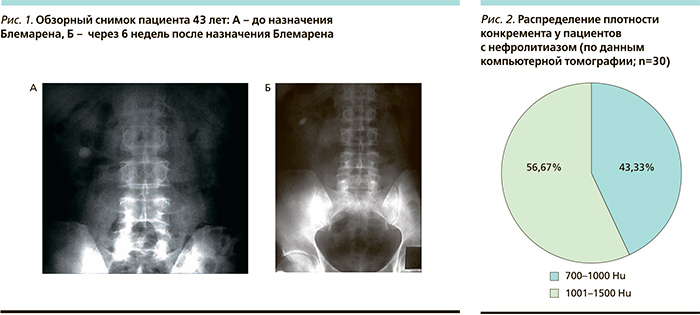
При динамическом контроле литолитической цитратной терапии Блемареном in vivo методом спиральной рентгеновской компьютерной томографии с денситометрией в течение 3–6 недель мы также отметили уменьшение характеристик смешанных камней (размер, объем, структурность, плотность). Изменения характеристик камня на фоне цитратной терапии представлены на обзорных рентгенограммах и денситометрических гистограммах (рис. 1). В данном клиническом наблюдении проведение цитратной терапии позволило снизить среднюю структурную плотность камня почки на 254 HU, что позволило фрагментировать камень за один сеанс ДЛТ.
Нами проанализированы результаты клинического применения препарата Блемарен в виде водорастворимой шипучей таблетки 30 пациентами в возрасте от 33 до 62 лет в 2000–2001 гг. Распределение плотности конкремента по данным компьютерной томографии представлено на рис. 2.
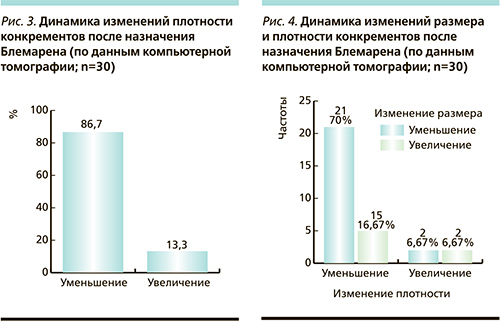
У 13 (43,3%) пациентов плотность конкремента до лечения составила от 700 до 1000 HU, а у 17 (56,7%) плотность составила от 1001 до 1500 HU. Динамика плотности конкремента по данным компьютерной томографии представлена на рис. 3. После применения Блемарена у 26 (86,7%) отмечено уменьшение плотности конкремента, а у 4 (13,3%) – увеличение. Изменение размера конкремента в зависимости от изменения плотности представлено на рис. 4. Отмечено значимое преобладание числа пациентов с уменьшением размеров конкремента на фоне снижения его плотности (р=0,176). Таким образом, проведение литолитической цитратной терапии позволило уменьшить среднюю плотность у 26 (86,7%).
Однако у 4 (13,3%) пациентов средняя плотность увеличилась. При этом у 2 (6,67%) пациентов было отмечено увеличение плотности конкремента вместе с увеличением размера. Проведенный анализ показал, что причины отрицательного результата (увеличение объема и плотности камня) цитратной терапии 4 (13,3%) пациентов заключаются в следующем:
- Использование препарата при преобладающем в составе камня фаз (более 50%) с плотностью более 800 НU.
- Невозможность стабилизации рН мочи в пределах 6,2–6,8.
Таким образом, проведение цитратной терапии препаратом Блемарен перед дистанционной литотрипсией позволяет:
- уменьшать структурную плотность камня;
- изменять макро- и микроструктуру камня;
- за счет стабилизации рН-мочи изменять кристализационные процессы.
Клиническая оценка результатов цитратной терапии позволила нам детализировать показания к назначению цитратных препаратов перед дистанционной литотрипсией:
- смешанные камни (рентген-неоднородные, рН<6);
- средняя плотность по данным компьютерной томографии более 800–1000 НU;
- объем структур (вокселей) камня с плотностью до 800 НU более 45–50%.
Обязательным условием цитратной терапии при подготовке к ДЛТ должна быть комплексная противовоспалительная и антибактериальная терапия, т.к. возможен эффект «бактериальной гипоцитратурии» ввиду способности бактерий метаболизировать цитрат мочи [1, 2]. Повторные сеансы ДЛТ были выполнены 4 (13,3%) пациентам при средней плотности камней более 1100 Нu ввиду частичной дезинтеграции камня или формирования протяженной «каменной дорожки».
Таким образом, проведение цитратной терапии препаратом Блемарен при смешанных (рентген-неоднородных) камнях перед ДЛТ повышает эффективность дистанционной нефролитотрипсии и снижает кратность повторных сеансов. Длительность цитратной терапии с целью подготовки к ДЛТ должна составлять не менее трех недель. При планировании хемолиза следует отрегулировать уровень рН до 7,0–7,2. При обструкции мочевых путей конкрементом из мочевой кислоты назначается пероральный хемолиз в сочетании с дренированием мочевых путей. Дозировка препарата определяется уровнем рН мочи. С целью профилактики оптимальный уровень рН составляет 6,2–6,8. При проведении хемолиза – 7,0–7,2.



