Актуальность
Достижение адекватного гликемического контроля при сахарном диабете (СД) является безусловной целью всех терапевтических мероприятий [1], направленных на снижение риска развития поздних осложнений СД и улучшение качества жизни больных. На фоне более глубокого понимания патогенеза развития СД и его осложнений менялись как критерии и показатели контроля гликемии, так и средства достижения этого контроля.
Так, появилось понимание важности вариабельности гликемии, контроля постпрандиальной гликемии, их вклада в достижение контроля СД. Были предложены новые критерии оценки контроля заболевания: коэффициент вариабельности, время в целевом диапазоне [2]. Эти показатели все шире входят в повседневную практику врачей-эндокринологов.
С другой стороны, появилось новое поколение аналогов инсулина, профиль действия которых наиболее близко имитирует профиль действия собственного инсулина в режиме прандиальной и базальной секреций.
Гипогликемизирующие эффекты прандиального аналога последнего поколения — сверхбыстродействующего инсулина аспарт (СБИАсп; Фиасп®) и прандиального аналога предыдущего поколения — инсулина аспарт в целом сопоставимы. Однако СБИАсп начинает действовать на 5 минут быстрее, а максимальный уровень инфузии глюкозы достигается на 11 минут раньше по сравнению с прандиальным аналогом предыдущего поколения. Концентрация глюкозы в крови в течение первых 30 минут (AUCGIR, 0-30 мин) после введения СБИАсп снижается на 51 мг/кг, тогда как после введения инсулина аспарт — на 29 мг/кг. Продолжительность действия СБИАсп короче, поздний гипогликемический эффект на 10% меньше, чем у инсулина аспарт. Все эти свойства приводят к тому, что СБИАсп начинает действовать раньше и со значительно большим гипогликемическим эффектом после стандартизированного приема пищи по сравнению с прандиальным аналогом предыдущего поколения [3], тем самым становясь ближе к профилю действия собственного инсулина в постпрандиальном периоде [4]. А это приводит к статистически значимому улучшению гликемического контроля у пациентов с СД 1 типа по сравнению с аналогами инсулина предыдущего поколения без увеличения количества эпизодов гипогликемии [5].
Другим представителем инсулиновых аналогов нового поколения является базальный аналог инсулина сверхдлительного действия — инсулин деглудек (Тресиба®). Отличительной особенностью данного базального аналога инсулина является практически плоский, беспиковый профиль с длительностью действия более 42 часов [6]. Профиль действия инсулина деглудек позволяет значительно, в т.ч. и статистически достоверно, снижать общее количество гипогликемий, а также число тяжелых и ночных эпизодов гипогликемии. Всего одна инъекция в сутки и гибкий режим введения способствуют повышению комплаентности пациентов [7].
В представленном ниже клиническом случае показана эффективность терапии аналогами инсулина последнего поколения у пациентки с СД 1 типа.
Клинический случай
Пациентка В. 47 лет предъявляет жалобы на частые гипогликемические состояния через 3-4 часа после еды, снижение чувствительности к гипогликемиям, слабость, онемение нижних конечностей на уровне стопы, головные боли.
Анамнез заболевания: сахарный диабет 1 типа с 12 лет в течение 35 лет.
Вводит детемир 11 ЕД перед завтраком и сном, аспарт по 8 ЕД перед основными приемами пищи. Потребность в инсулине на 1 ХЕ (хлебную единицу) в завтрак, обед и ужин составляет 2 ЕД инсулина. Фактор чувствительности - 3. Инсулин продленного действия вводит в предплечье, в участки липогипертрофии, ультракороткого действия - в подкожно-жировую клетчатку передней брюшной стенки, в липогипертрофию. Использует иглы длиной 4 мм. Одной иглой вводит инсулин до 2 дней.
Поздние осложнения СД: диабетические микроангиопатии: непролиферативная диабетическая ретинопатия обоих глаз, диабетическая нефропатия, ХБП (хроническая болезнь почек) С3а А1, диабетическая нейропатия, сенсорная форма, автономная нейропатия, нарушение распознавания гипогликемий.
Сопутствующие заболевания: артериальная гипертензия 1-й ст., риск - 4; первичный гипотиреоз в исходе аутоимунного тиреоидита, медикаментозная компенсация; возрастная макулярная дегенерация, начальная катаракта, миопический астигматизм; контрактура плечевого сустава справа; интрамуральная лейомиома матки; железодефицитная анемия легкой степени.
Гипотиреоз выявлен 25 лет назад. Проводит заместительную гормональную терапию левотироксином 88 мкг/сут. Тиреотропный гормон - 2,6 мМЕ/л.
Общий осмотр: рост - 162 см, вес - 52 кг, ИМТ (индекс массы тела) - 19,8 кг/м2, объем талии - 68 см, объем бедер - 88 см, число дыхательных движений (ЧДД) -16/мин, пульс - 69/мин, артериальное давление (АД) - 130/90 мм рт.ст. Щитовидная железа не увеличена. При аускультации сердца патологии не выявлено. Аускультация легких: дыхание везикулярное. Живот: патологии не выявлено.
Пациентке рекомендована смена мест инъекций инсулина, все инъекции следует проводить в подкожножировую клетчатку передней брюшной стенки, не вводить инсулин в липогипертрофию. Использовать иглы длиной 4 мм. Одной иглой вводить инсулин строго 1 раз.
Результаты исследований: НЬА1с — 8,2%, уровень креатинина - 118,5 (норма - 44,2-97,2) мкмоль/л, скорость клубочковой фильтрации (СКФ) - 47 мл/мин/1,73 м2, уровень витамина D - 36,4 (30,0-69,9) нг/мл, уровень липопротеидов низкой плотности - 1,35 (до 3,3) ммоль/л.
Для контроля уровня сахара крови использует систему для флэшмониторинга. Если пациент использует датчик в течение более чем 70% времени оценки, объем данных считается достаточным для анализа. В данном случае 50% времени датчик находился в активном состоянии, пациентка редко проводила сканирование своего датчика. В связи с этим пациентке рекомендовано чаще сканировать датчик. Целевой диапазон: 3,9-10,0 ммоль/л. В целевом диапазоне пациентка находилась 54% времени (норма - более 70%), в гипогликемическом диапазоне - 3% , в гипергликемическом диапазоне - 43%, вариабельность уровня глюкозы (коэффициент вариации) - 35,8% времени (рис.1, 2).
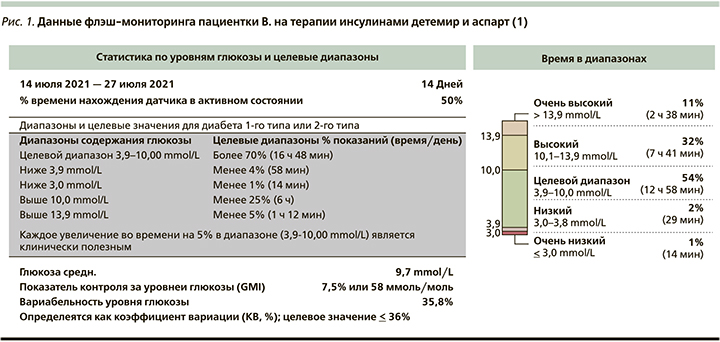
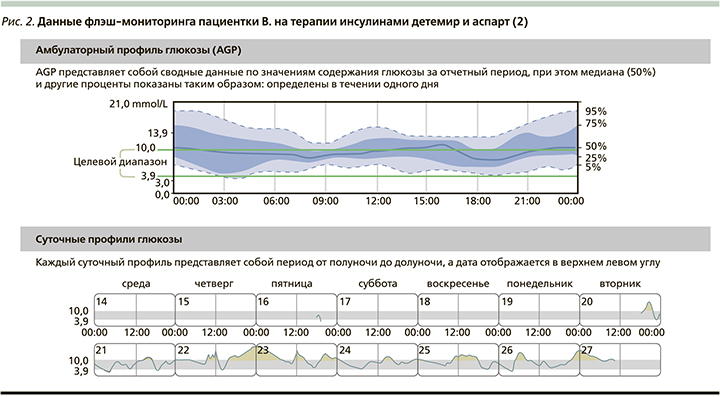
Представленные данные указывают на наличие ночной и постпрандиальной гипергликемии. При попытке увеличения дозы инсулина аспарт (из расчета 1 ХЕ=2,5 ЕД инсулина) регистрировались гипогликемические эпизоды через 3-4 часа после введения. В связи с этим принято решение перевести пациентку на аналог инсулина сверхбыстрого действия аспарт+никотинамид.
Была назначена стартовая доза препарата из расчета 2 ЕД инсулина на 1 ХЕ в завтрак, 1,5 ЕД - в обед, 2 ЕД - в ужин.
При повторном исследовании 95% времени датчик находился в активном состоянии, пациентка увеличила число сканирований до 10-12 в день. В целевом диапазоне (3,9-10,0 ммоль/л) пациентка находилась 80% времени, в гипогликемическом диапазоне (<3,9 ммоль/л) - 10% , в гипергликемическом диапазоне (10,1-13,9 ммоль/л) - 10% времени, коэффициент вариации уровня глюкозы - 34,8% (рис. 3-5).
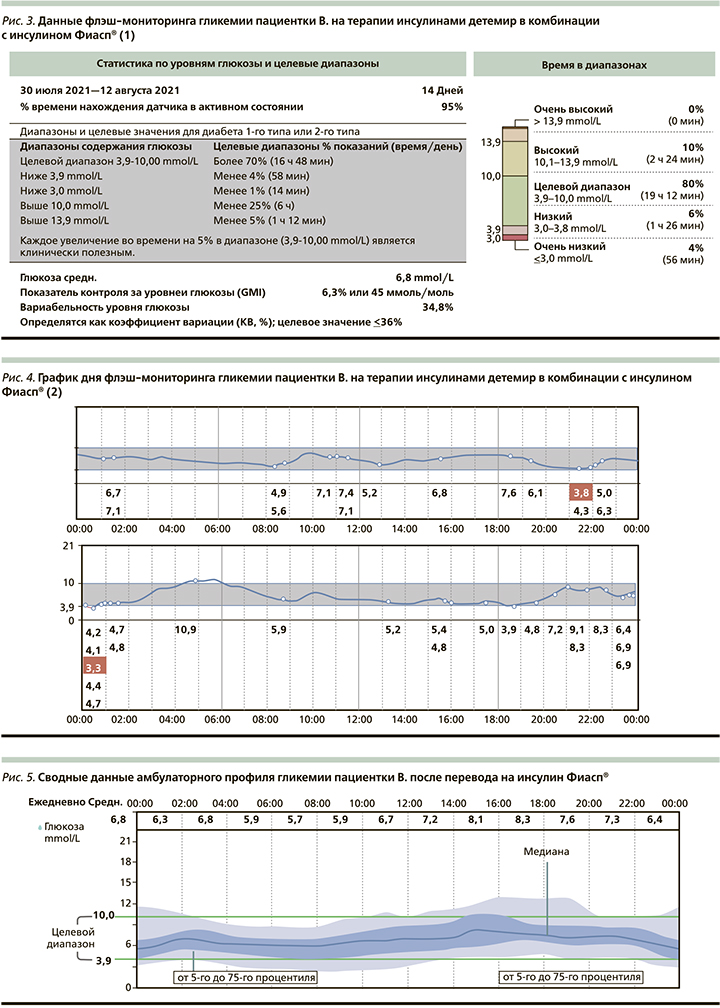
При контрольном осмотре через 3 месяца: вес - 52 кг, ИМТ - 19,8 кг/м2, объем талии - 68 см, объем бедер - 88 см, ЧДД — 16/мин, пульс 72/мин, АД - 120/80 мм рт.ст.
Результаты исследований: НЬА1с — 7,1%, уровень креатинина - 115 (норма - 44,2-97,2) мкмоль/л, СКФ - 47 мл/мин/1,73 м2.
Периодически пациентка регистрировала гипогликемические состояния ночью. В связи с этим переведена на инсулин деглудек в дозе 20 ЕД перед сном. Была поставлена система непрерывного мониторинга гликемии система мониторирования глюкозы iPro 2 для более точного подбора дозы инсулина (рис. 6).
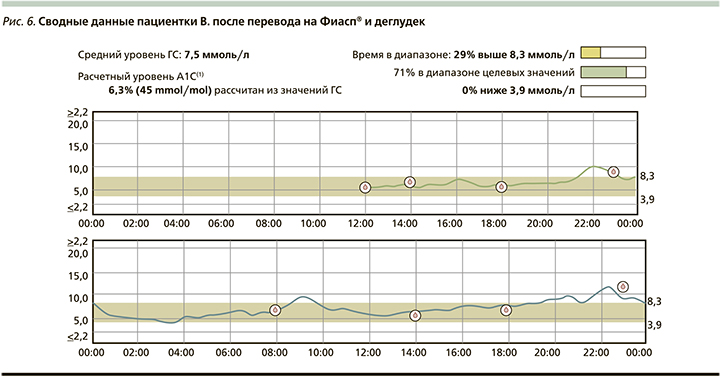
Результаты исследований через 6 месяцев после смены инсулинов: НЬА1с — 6,3%, время нахождения в целевом диапазоне - 71%; в гипогликемическом диапазоне — 0%, в гипергликемическом диапазоне — 24% времени. Была скорректирована доза сверхбыстродействующего аналога инсулина из расчета 2,2 ЕД инсулина на 1 ХЕ в завтрак, 1,5 ЕД — в обед, 2,5 ЕД — в ужин. Инсулин деглудек — 20 ЕД на ночь. На данной терапии достигнута нормогликемия без гипогликемических эпизодов.
Обсуждение
Причиной для назначения прандиального инсулинового аналога послужили частые эпизоды постпрандиальной гипогликемии, которые в свою очередь свидетельствовали о более позднем пике действия применявшегося прандиального инсулина. Перевод больного на сверхбыстродействующий аналог инсулина с более низким пиком действия позволил решить эту проблему. Также удалось повысить комплаентность пациентки к назначенной терапии, поскольку более удобный режим применения — непосредственно перед приемом пищи, позволил ей избегать отклонений от рекомендаций.
Применение же базального инсулинового аналога последнего поколения позволило избегать ночных гипогликемий.
Совместное использование этих препаратов способствовало достижению нормогликемии без эпизодов гипогликемии с показателем НЬА, 1с 6,3%, временем пребывания в целевом диапазоне 71% и снижению времени пребывания в диапазоне гипогликемии до 0%.
Заключение
Таким образом, сверхбыстродействующий прандиальный инсулин Фиасп® (аспарт+никотинамид) в условиях реальной амбулаторной практики действительно показал себя более быстродействующим по сравнению с другими прандиальными аналогами. Этот факт подтверждается не только приведенным клиническим примером, но и многими другими историями болезни пациентов.
Это свойство позволяет наиболее близко имитировать профиль действия инсулина, выделяемого поджелудочной железой здоровых людей и тем самым лучше контролировать постпрандиальную гликемию и нивелировать такие проблемы, как постпрандиальные гипогликемии.
Совместное применение сверхбыстродействующего аналога инсулина Фиасп® (аспарт+никотинамид) и базального аналога последнего поколения деглудек позволяет добиваться самых строгих целевых показателей контроля гликемии даже у коморбидных пациентов с длительным анамнезом СД.
Финансирование. Написание статьи выполнено по инициативе авторов без привлечения финансирования.
Вклад авторов. Котешкова О.М., Демидов Н.А., Духарева О.В. - анализ и интерпретация результатов исследования, написание текста статьи; Анциферов М.Б. - финальный анализ результатов и редактирование текста рукописи. Все авторы внесли существенный вклад в проведение исследования и подготовку статьи, прочли и одобрили финальную версию перед публикацией.



