Известно, что любое хирургическое вмешательство ассоциируется с определенным риском для больного. Как избежать осложнений и свести риск к возможному минимуму? Таким вопросом задаются кардиологи и терапевты, когда их пациенты, страдающие сердечно-сосудистыми заболеваниями, нуждаются в плановой внесердечной операции (ВСО).
Более 30 лет назад Goldman L. и соавт. впервые предложили клинический индекс оценки периоперационного риска кардиальных осложнений, а в 1996 г. были опубликованы первые Рекомендации по периоперационному кардиологическому обследованию и помощи при ВСО, разработанные Американским колледжем кардиологов и Американской ассоциацией сердца (АСС/АНА), где все действия были разделены на этапы и на каждом из них решался вопрос о возможности проведения операции, выделялись группы риска, пошагово проводились диагностические мероприятия в каждой из выделенных подгрупп. За первые 5 лет использования этого алгоритма удалось снизить не только количество сердечно-сосудистых осложнений, но и число операций, необоснованно проводившихся по неотложным показаниям, а также количество предоперационных диагностических процедур. Данная тенденция наблюдалась и в последующие годы.
При дальнейшем изучении информативности индекса Goldman L. и его модификации, предложенной Detsky A.S., не было установлено четкой зависимости количества неблагоприятных исходов от вида операции. Особенно большие колебания в частоте осложнений наблюдались при проведении вмешательств на аорте и магистральных артериях. Был сделан вывод, что у части больных данные индексы завышают риск возможных кардиологических осложнений и способствуют увеличению числа необоснованных дополнительных обследований до хирургического вмешательства. Были предложены другие методы оценки риска возникновения сердечно-сосудистых осложнений. Индекс, предложенный Lee T.H. и соавт. в 1999 г., и тактика ведения больных с его использованием (табл. 1 и 2) были приняты в последних рекомендациях ACC/AHA [1]. В 2009 г. впервые появились Европейские рекомендации по оценке кардиального риска и периоперационному ведению кардиологических больных при ВСО [2]. С практической точки зрения большой интерес представляет сравнение этих рекомендаций.
Таблица 1. Индекс риска сердечных осложнений (Lee T.H. и соавт., 1999).
Таблица 2. Тактика ведения больного перед ВСО в зависимости от количества набранных баллов (Lee T.H. и соавт., 1999).
В рекомендациях АСС/АНА выделяют шесть важных этапов обследования, которым должен следовать врач-консультант при подготовке больного к операции, в Европейских рекомендациях – их семь. Вначале действия в обоих руководствах идентичны (см. рисунок). На первом этапе хирургами решается вопрос о возможных сроках проведения данной операции. Если вмешательство не является срочным и его можно отложить на некоторое время, терапевт или кардиолог, консультируя больного, исключает наличие у него ряда кардиологических заболеваний или состояний, требующих проведения неотложного медикаментозного и/или хирургического лечения до проведения плановой внесердечной операции (табл. 3). Периоперационная летальность и риск развития сердечно-сосудистых осложнений при этих заболеваниях велики, поэтому оперативное вмешательство следует отложить до стабилизации состояния больного, что может занять довольно длительное время. Лечение этой группы пациентов проводится в соответствии с принятыми рекомендациями (в отношении, например, пароксизмальной тахикардии, острого коронарного синдрома).
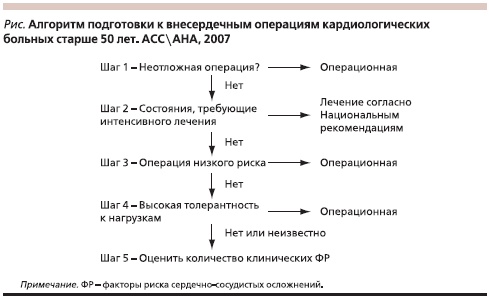
Таблица 3. Состояния, требующие интенсивного лечения и частого переноса сроков операции.
В обеих рекомендациях содержится оценка риска возникновения ИМ в результате хирургического вмешательства, причем существуют некоторые различия по видам операций, относящихся к группам среднего и низкого риска, также в Европейских рекомендациях более подробно представлены виды вмешательств, включая эндоваскулярные методы лечения [2].
В рекомендациях подчеркивается важность информации о переносимости больным физических нагрузок, что оценивается с помощью т. н. метаболического эквивалента (МЕТ). У лиц с удовлетворительной толерантностью (более 4 МЕТ) имеется возможность оперировать без дальнейшего обследования. У больных с низкой толерантностью (менее 4 МЕТ), которым предстоит операция с высоким риском сердечно-сосудистых осложнений, необходимо определить наличие кардиальных факторов риска и провести дополнительное тестирование с помощью неинвазивных методов. Толерантность к физическим нагрузкам определяется с помощью нагрузочных проб (велоэргометрия, тредмил-тест), а также косвенно – на основании оценки переносимости бытовых нагрузок и расчета их величины с помощью специальных таблиц, например, приведенных в рекомендациях АСС/АНА по лечению ИМ со стойким подъемом сегмента ST.
Многие больные, которым предстоит хирургическое вмешательство, постоянно принимают дезагреганты. В Европейских рекомендациях в особый раздел выделены показания к продолжению приема аспирина. Отменяется препарат лишь в случае, когда во время вмешательства трудно обеспечить контроль кровотечения, а также когда риск кровотечения может превысить таковой кардиальных осложнений. Одновременно с этим определяется наличие у больного кардиальных факторов риска: ИБС, систолической СН, сахарного диабета типа 2, почечной недостаточности, перенесенного инсульта или транзиторного нарушения мозгового кровообращения; оцениваются результаты, полученные во время нагрузочных проб. Если во время тестирования ишемия миокарда не возникла или развивалась лишь при высоком уровне нагрузки, перед операцией назначаются статины и β-адреноблокаторы (БАБ) в индивидуально подобранных дозах, а у больных со снижением фракции выброса левого желудочка < 40 % еще и ингибиторы ангиотензинпревращающего фермента (ИАПФ). У пациентов со значимой ишемией миокарда необходимо обеспечить ее лечение. Выбор метода определяется индивидуально, с учетом пользы и возможных осложнений при хирургическом вмешательстве на коронарных артериях.
При операциях на сосудах у больных с одним или двумя факторами риска или при операциях среднего риска развития ИМ у пациентов с любым количеством факторов в рекомендациях ACC/AHA обязательным условием является назначение БАБ в дозе, обеспечивающей снижение частоты сердечных сокращений (ЧСС) до 65 ударов в 1 минуту с последующей оценкой эффективности терапии при помощи нагрузочных проб. Полученные результаты определяют дальнейшую тактику ведения больного.
При операциях на периферических артериях у больных, имеющих ≥ 3 фактора риска, обязательно проведение как неинвазивных, так и инвазивных обследований, после чего у части пациентов решается вопрос о вмешательстве на коронарных артериях, остальных готовят к плановой ВСО. В отсутствие противопоказаний статины и БАБ назначают всем больным до операции на сосудах и не отменяют, если они применялись ранее, а ИАПФ – при наличии показаний к ним.
Особое внимание уделяется подготовке к операциям больных, у которых имеются некоторые нижеприведенные заболевания. В Европейских рекомендациях обсуждается лечение пациентов с систолической формой СН, пороками клапанов сердца, артериальной гипертензией (АГ), аритмиями. В рекомендациях ACC/AHA представлен более детальный перечень заболеваний сердца, к которому относятся ИБС, АГ, кардиомиопатия, систолическая СН, аритмия, нарушения проводимости, имплантированный электрокардиостимулятор или кардиовертер-дефибриллятор, приобретенный порок клапанов сердца, легочная гипертензия, врожденный порок сердца.
Основными вопросами, требующими уточнения до операции у больных ИБС, являются определение функции левого желудочка; уровня нагрузки, провоцирующей ишемию миокарда; насколько оптимально подобрано медикаментозное лечение. Все это позволяет правильно выбрать объем обследований и лечебных мероприятий перед операцией и оценить возможный риск осложнений.
Нагрузочный тест позволяет выделить группу больных с высоким риском осложнений, к которой относятся пациенты с ишемией миокарда, возникающей при низком уровне нагрузки (менее 4 МЕТ), а также при ЧСС менее 100 в минуту или менее 70 % от рассчитанной максимальной частоты для этого возраста, сопровождающейся хотя бы одним из следующих симптомов:
- горизонтальная или косонисходящая депрессия ST более чем на 0,1 мА;
- подъем ST более чем на 0,1 мА в отведениях без зубца Q;
- изменения в пяти и более отведениях;
- преходящие ишемические изменения на ЭКГ, возникшие после 3 минут отдыха;
- типичный приступ стенокардии;
- снижение артериального давления (АД) более чем на 10 мм рт. ст. при увеличении нагрузки.
Реваскуляризация миокарда у таких больных улучшает прогноз как во время проведения ВСО, так и в последующем.
Пожилой возраст является важным фактором риска внесердечных операций не только из-за большой распространенности ИБС, но и из-за возрастных изменений миокарда. Смертность от периоперационного ИМ выше у пожилых, что требует тщательного мониторирования ЭКГ во время и после операции, а при изменениях на ней – определения содержания в крови маркеров некроза миокарда. Так как смертность от ИМ выше у женщин, особенно при наличии у них сахарного диабета, требуется особое наблюдение за этой категорией больных во время внесердечных операций.
У больных АГ 3-й степени (АД выше 180/110 мм рт. ст.) оперативное вмешательство необходимо отложить до снижения АД с помощью антигипертензивных препаратов до нормального уровня. Предпочтение отдается БАБ, которые не только контролируют АД, но и уменьшают риск возникновения ишемии миокарда. Больным АГ 1-й и 2-й степеней переносить сроки операции не следует. Если повышение АД зарегистрировано непосредственно перед операцией как реакция на стрессовую ситуацию, назначать антигипертензивные препараты не нужно, т. к. во время анестезии может развиваться гипотония. У больных, постоянно принимающих ИАПФ или антагонисты рецепторов ангиотензина II, из-за снижения во время наркоза общего периферического сопротивления возможно падение АД. Поэтому не рекомендуется принимать эти препараты утром в день операции, а после нее они назначаются, лишь когда достигается полное восстановление объема циркулирующей крови, что позволяет избежать нарушения функции почек.
Всем больным с пороком сердца или даже только с подозрением на него до внесердечной операции показано проведение эхокардиографического исследования. При тяжелом стенозе аортального клапана необходимо провести его протезирование до ВСО, а при неотложных ВСО должен проводиться непрерывный инвазивный контроль показателей гемодинамики (как во время операции, так и в послеоперационном периоде). У таких больных возможно экстренное выполнение баллонной вальвулопластики или транскатетерной имплантации клапана. При критическом митральном стенозе с высокой легочной гипертензией показано проведение чрескожной митральной комиссуротомии или протезирование клапана до ВСО. Больные с недостаточностью митрального и аортального клапанов обычно хорошо переносят ВСО, и только при тяжелой степени митральной и аортальной регургитации риск осложнений очень высок, поэтому ВСО должна проводиться только в крайнем случае.
У всех больных с пороками клапанов необходимо проведение профилактики инфекционного эндокардита с помощью антибиотиков, а у пациентов с протезированными клапанами помимо этого показана отмена постоянно принимаемого варфарина до операции с переводом больного на терапию гепарином.
Отсутствуют определенные данные о том, как переносят ВСО пациенты с легочной гипертензией. Однако можно предположить, что такие больные будут плохо переносить увеличение гипоксии, возникающей во время и после операций на грудной клетке и брюшной полости. К тому же они часто имеют сниженную толерантность к физическим нагрузкам, что также ассоциируется с повышением риска развития кардиальных осложнений.
Мало информации и о том, как готовить к ВСО больных с кардиомиопатиями. Имеющиеся рекомендации основываются на знании патофизиологических изменений, возникающих при данных заболеваниях. До ВСО необходимо с помощью эхокардиографического исследования оценить тяжесть нарушения функции левого желудочка (систолической или диастолической). В частности, у пациентов с гипертрофической кардиомиопатией и обструкцией выносящего тракта независимыми предикторами кардиальных осложнений оказались не сам уровень градиента давления в выносящем тракте левого желудочка, а объем хирургической травмы и продолжительность операции, которые необходимо по возможности уменьшить. Этим больным противопоказано назначение симпатомиметиков для контроля сниженного АД из-за опасности нарастания градиента давления и ухудшения диастолической функции левого желудочка вплоть до развития неуправляемой гипотонии и отека легких.
Наличие систолической СН значительно увеличивает риск осложнений. Lee T.H. подчеркивает, что наличие хотя бы одного из ее проявлений (указания на СН в анамнезе, отек легких или приступы удушья по ночам, хрипы в нижних отделах легких с двух сторон, ритм галопа, застойные явления в легких при рентгенологическом обследовании) ухудшает прогноз. Обращается внимание на необходимость тщательного обследования и расспроса больного для выявления бессимптомно протекающей СН. Кроме того, перед операцией рекомендовано использовать эхокардиографическое исследование или другие неинвазивные методы определения фракции выброса левого желудочка у пациентов с одышкой неизвестной этиологии, застойными явлениями в легких или при указании на их наличие в анамнезе (класс доказательности IIА). В Европейских рекомендациях подробно описывается терапия больных систолической СН с помощью ИАПФ или антагонистов рецепторов ангиотензина II, указано на необходимость титрования дозы БАБ заблаговременно до операции и целесообразность назначения антагонистов альдостерона и диуретиков у больных с отеками. Оба руководства рекомендуют достижение полной компенсации до операции с последующим мониторингом показателей гемодинамики.
Ведение и лечение больных с аритмиями перед оперативным вмешательством не имеют особенностей и проводятся согласно единым для данной группы больных рекомендациям. Прием БАБ во время операции снижает количество кардиальных осложнений, в т. ч. эпизодов нарушений ритма сердца.
Атриовентрикулярная блокада, особенно 3-й степени, во время операции может увеличивать риск осложнений и требует временной электрокардиостимуляции. При блокаде левой или правой ножки пучка Гиса этого не требуется, т. к. при отсутствии в анамнезе указаний на потерю сознания крайне редко происходит увеличение степени блокады до дистальной атриовентрикулярной блокады 3-й степени.
Если у больного осуществляется постоянная электрокардиостимуляция, до операции необходимо провести проверку искусственного водителя ритма, оценить степень зависимости больного от его работы и при необходимости перепрограммировать водитель ритма на асинхронный режим VOO или DOO. У больных с имплантированным кардиовертером-дефибриллятором перед началом хирургического вмешательства следует отключить функцию дефибрилляции и вновь включить ее после наложения швов.
Новым является раздел в Европейских рекомендациях, посвященный ведению больных с сопутствующими заболеваниями. Перед ВСО пациенту нужно определить показатели функции почек. Ее снижение до операции – предиктор неблагоприятных исходов. Таким больным перед применением контраста с целью обследования следует предварительно ввести раствор плазмозаменителя для профилактики развития нефропатии и прогрессирования хронической почечной недостаточности.
При наличии стеноза сонных артерий, превышающего 70 %, до хирургического вмешательства рекомендуется назначать аспирин и, если это возможно, выполнить каротидную эндартерэктомию. Нет единого мнения о необходимости хирургической коррекции стеноза сонной артерии до ВСО, как это предлагается перед операцией на сердце. Нет согласия и по вопросу обязательного скринингового обследования состояния сонных артерий у всех пожилых больных перед операцией.
У больных легочной гипертензией или хронической обструктивной болезнью легких, осложненных развитием легочного сердца, особое внимание уделяется тщательному подбору и коррекции терапии как до, так и после ВСО. При хронических обструктивных заболеваниях легких число осложнений в послеоперационном периоде увеличивается за счет возникновения во время анестезии ателектазов легких. Поэтому терапия должна быть направленной на улучшение функции легких и профилактику возникновения инфекционных осложнений. В отсутствие у пациента сопутствующих заболеваний сердца специального обследования перед операцией не требуется.
В руководствах подчеркивается необходимость постоянного контроля над различными показателями жизнедеятельности во время операции, а у больных СН или ИБС – и после операции в течение от 24 до 72 часов. Впервые предлагается определять в динамике уровень гликемии во время операции не только у больных диабетом, особенно получающих инсулин, но и при внезапном повышении уровня сахара крови только перед операцией, а также у всех пациентов при больших операциях с высоким риском развития периоперационного ИМ. Кроме того, в рекомендациях ACC/AHA указано на необходимость мониторинга температуры тела при большинстве проводимых операций для выявления гипотермии, являющейся независимым предиктором развития острого коронарного синдрома и блокады сердца.
В разделе, посвященном стратегиям снижения риска кардиальных осложнений, содержатся показания к аортокоронарному шунтированию (АКШ), баллонной ангиопластике и стентированию коронарных артерий до ВСО.
Проведение АКШ для снижения риска осложнений перед ВСО высокого риска в Европейских рекомендациях предлагается лишь для части больных со стабильной ИБС, плохо поддающихся медикаментозной коррекции, однако у тех же пациентов перед операциями низкого и среднего риска осложнений она не требуется. В рекомендациях АСС/АНА показания к АКШ не зависят от планируемой ВСО и полностью повторяют последние национальные рекомендации по его проведению. При необходимости имплантации коронарного стента перед выполнением ВСО сроки ее осуществления зависят от вида стента и необходимой продолжительности приема комбинации дезагрегантов (табл. 4).
Таблица 4. Сроки проведения плановой внесердечной операции после установки стента.
В разделе медикаментозной терапии до выполнения ВСО обсуждаются показания к назначению α2-адреноагонистов, антагонистов кальция, ИАПФ, аспирина, диуретиков, антагонистов витамина К, а также БАБ и статинов.
В настоящее время нет убедительных доказательств необходимости применения α2-адреноагонистов (клонитидина и мивазерола) для контроля АГ, а также их использования у больных ИБС или лиц с одним или большим числом клинических факторов риска развития сердечно-сосудистых осложнений после ВСО, в т. ч. операций на сосудах.
Антагонисты кальция, использованные у больных перед ВСО, приводили к уменьшению числа эпизодов ишемии миокарда и суправентрикулярных аритмий, но при этом отмечалась лишь тенденция к уменьшению летальности и числа ИМ. Зарегистрированные положительные эффекты в основном наблюдались при терапии дилтиаземом. По-видимому, их использование следует обсуждать у больных со стенокардией Принцметала. В случае применения пульсурежающих антагонистов кальция рекомендуется заблаговременно подобрать их дозу под контролем ЧСС.
Результаты применения ИАПФ противоречивы. В части исследований было отмечено увеличение риска осложнений из-за развития гипотонии во время анестезии, особенно если вместе с ИАПФ больной принимал БАБ. Поэтому в настоящее время рекомендуется продолжать прием ИАПФ вплоть до дня операции лишь пациентам с систолической СН, причем во время операции необходимо проведение постоянного контроля гемодинамики. У больных АГ ИАПФ отменяются за 24 часа до операции и вновь назначаются лишь после восстановления объема циркулирующей крови (в течение 24–72 часов в зависимости от вида операции). Все эти рекомендации относятся и к назначению антагонистов рецепторов ангиотензина II.
У больного, получающего диуретик, необходимо до проведения операции восстановить электролитный баланс крови. Только больные с систолической СН могут принимать их вплоть до дня операции, а во время операции при необходимости их вводят внутривенно. В других случаях диуретики отменяют в день операции и назначают вновь, когда будет разрешен прием пищи.
Особое внимание при подготовке больных к хирургическому вмешательству уделяется показаниям к назначению БАБ, подчеркивается важность титрования их дозы с целью снижения ЧСС < 65 ударов в минуту, т. к. именно при такой частоте ритма желудочков отмечено наименьшее число кардиальных осложнений [1]. ЧСС от 50 до 60 ударов в минуту является оптимальной для больных, которые получают препарат из этой группы.
В 2008 г. было опубликовано исследование POISE, в котором была оценена эффективность метопролола при пероральном назначении в очень большой дозе с целью достижения быстрого насыщения больных. Пациентам с систолическим АД ≥ 100 мм рт. ст. назначалась стандартная доза 100 мг за 2 или 4 часа до ВСО, затем повторно 100 мг через 6 часов после операции при ЧСС > 80 в минуту и систолическом АД > 100 мм рт. ст., а при нормальных показателях ЧСС и АД – 200 мг через 12 часов после операции и в той же дозе 1 раз в день в последующие 30 дней. Таким образом, часть больных за первые 24 часа получили 400 мг, а остальные – 300 мг метопролола сукцината. В результате были получены данные, свидетельствовавшие об увеличении риска развития брадикардии и артериальной гипотонии, возрастании общей смертности и частоты развития инсульта. Отмечено также увеличение летальности у больных с сепсисом, принимавших БАБ.
Эти данные, вероятно, и стали основанием для подготовки ACC/AHA в 2009 г. новых рекомендаций [3], в которых подчеркивается, что для БАБ имеются доказательства пользы класса I, особенно у больных, получавших их ранее, а также класса IIа – у больных ИБС, с провоцируемой ишемией миокарда или с несколькими клиническими факторами риска, при назначении их перед планируемой операцией на сосудах или операцией со средним риском. Особое внимание уделяется тому, что во время операции у больных при применении БАБ нужно избегать развития брадикардии и гипотонии. Поэтому подбор дозы препарата должен начинаться заблаговременно до ВСО с постепенным достижением целевой дозы и прием БАБ должен продолжаться, включая день операции и после нее. После хирургического вмешательства необходимо тщательное наблюдение за больным для выявления вторичных причин тахикардии, не требующих назначения БАБ.
Таким образом, несмотря на наличие в представленных рекомендациях некоторых различий в подготовке больных к ВСО, основные подходы в большинстве случаев едины, однако в Европейских рекомендациях более подробно регламентируются действия терапевта и кардиолога.
Информация об авторах:
Мазур Николай Алексеевич – доктор медицинских наук, профессор, заведующий кафедрой кардиологии ГОУ ДПО РМАПО МЗиСР.
Тел. (495) 414-63-26;
Чигинева Виктория Васильевна – кандидат медицинских наук, ассистент кафедры кардиологии ГОУ ДПО РМАПО МЗиСР.
Тел. (495) 414-60-58, e-mail: vitachi@pochta.ru



