Введение
Раннее начало половой жизни и поздняя менопауза, характерные для современных женщин, свидетельствуют о потребности в контрацепции около 30 лет и диктуют необходимость в создании препаратов, которые обладают хорошей переносимостью при использовании на протяжении длительного времени [1]. Кроме того, длительность использования гормональных препаратов определяется возможностью предложить самый широкий выбор методов и средств планирования семьи («метод-микс», обеспечить их использование гарантированными информационными услугами и консультированием [2]. Во-первых, больший выбор ведет к увеличению числа потребителей, а во-вторых, «метод-микс» отвечает на изменяющиеся потребности населения на различных этапах жизненного репродуктивного цикла. Этот подход может предложить обратимые методы для тех, кто планирует беременность в будущем, и пролонгированные или постоянные методы – для тех, кто достиг желаемого размера семьи. Консультирование может помочь женщинам и супружеским парам выбрать метод контрацепции, удовлетворяющий их репродуктивным установкам в конкретный период жизни, помочь сделать выбор среди обратимых или необратимых методов [3].
С целью оценки соответствия комбинированного орального контрацептива (КОК) Бонадэ потребностям и ожиданиям женщин (эффективность, безопасность, контроль цикла, экономическая доступность) и его дополнительных неконтрацептивных преимуществ был проведен поиск и анализ публикаций в Кохрейновской библиотеке, базах данных EMBASE, PUBMED, MEDLINE, eLIBRARY. RU и электронных базах данных свободного доступа по ключевым словам. Глубина поиска: для исследований фармакологических свойств эстрадиола и диеногеста 20 лет, клинических – 5 лет.
Характеристика фармакологических свойств
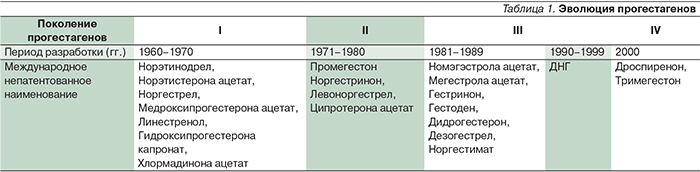
Бонадэ является низкодозированным монофазным КОК, в состав которого входит 30 мкг этинилэстрадиола (ЭЭ) и 2 мг диеногеста (ДНГ). Исторически ДНГ относится к третьему поколению гестагенов (табл. 1).
Препарат был выпущен в Германии в 1995 г. и в настоящее время является наиболее часто назначаемым КОК в этой стране [4]. По данным M. Ziller et al. [5] среди девочек-подростков 12–18 лет КОК с ДНГ входит в первую тройку препаратов наиболее часто используемых в этой возрастной группе. Доза 2 мг ДНГ достаточна для подавления овуляции, а доза 30 мкг ЭЭ обеспечивает удовлетворительный контроль цикла, в то же время обеспечивая минимум эстрогензависимых побочных явлений [6–8].
Фармакологическое действие ЭЭ – эстрогенное, анаболическое, гиполипидемическое. Взаимодействует со специализированными эстрогенными рецепторами в клетках-мишенях. Быстро абсорбируется через слизистые оболочки и кожу. Подвергается гепатоэнтеральной рециркуляции, сопровождающейся эффектом «первого прохождения» через печень. Эстрадиол (Е2) является наиболее мощным природным эстрогеном, который секретируется яичниками, однако Е2 обладает низкой активностью при пероральном приеме. Добавление этиниловой группы в положении 17 делает молекулу ЭЭ высокоактивной, а также изменяет ее свойства, что препятствует связыванию с глобулином, связывающим половые гормоны, делает ее устойчивой к ферментативному расщеплению с помощью 17-бета-гидроксилазы и придает более высокое сродство к рецептору эстрогена [9].
Без присутствия гестагенов ЭЭ оказывает эстрогенное влияние и вызывает пролиферацию эндометрия, стимулирует развитие матки и вторичных женских половых признаков. Будучи в составе КОК, ЭЭ поддерживает пролиферацию эндометрия и обеспечивает контроль цикла (отсутствие промежуточных кровотечений при приеме КОК). Кроме того, ЭЭ необходим для замещения эндогенного эстрадиола, поскольку при приеме КОК нет роста фолликула и, следовательно, эстрадиол в яичниках не вырабатывается.
Основные клинические различия между современными КОК, к которым можно отнести индивидуальную переносимость, частоту побочных реакций, особенности влияния на метаболизм, лечебные эффекты и прочее, обусловлены свойствами входящих в их состав прогестагенов.
Фармакология ДНГ
Характеристика 30ЭЭ/ДНГ в значительной степени основана на свойствах прогестагенного компонента. Это единственное производное нортестостерона, которое имеет цианометиловую группу вместо этиниловой группы в положении C-17 с добавлением двойной связи между C-9 и C-10 в отличие от норгестрела [10–12]. ДНГ имеет высокую биодоступность (96,2%) и довольно короткий период полувыведения (11,6 часа) [11]. ДНГ является «гибридным» гестагеном, особенность которого заключается в том, что он объединил преимущества 19-норстероидов и производных прогестерона, что характеризуется высокой степенью подавления овуляции, сильным прогестагенным эффектом на эндометрий, но менее выраженным антигонадотропным действием и отсутствием эстрогенных и андрогенных влияний [13–15]. Суточная доза ДНГ, необходимая для подавления овуляции без присутствия ЭЭ, составляет 1 мг и сравнима с производными прогестерона [8].
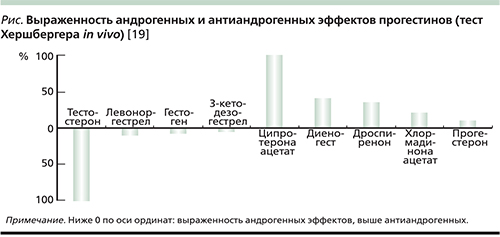
ДНГ имеет слабую аффинность к андрогенным рецепторам, поэтому не обладает андрогенной активностью, но демонстрирует антиандрогенное действие [15–17], что представляет его специфический фармакодинамический профиль. Тест оценки антиандрогенного влияния различных прогестинов Хершбергера указывает, что ДНГ имеет около 40% от активности ципротерона ацетата – наиболее сильного антиандрогенного прогестина (см. рисунок) [18, 19] (однако следует учитывать, что в сочетании с ЭЭ антиандрогенное действие усиливается и клинически оно может быть сопоставимым).
ДНГ не обладает сродством к глобулину, связывающему половые гормоны или кортикостероиды [15], и не связывается с ними. В свободном виде в сыворотке крови находится около 10% от общей концентрации; около 90% неспецифически связаны с сывороточным альбумином. Индукция ЭЭ синтеза глобулина, связывающего половые гормоны, не влияет на связывание ДНГ с этим белком.
Контрацептивная эффективность
Подавляющий эффект 30ЭЭ/ДНГ на функцию яичников и развитие фолликулов показан в нескольких исследованиях с участием большого количества женщин. В трех европейских клинических исследованиях [8, 20, 21], проанализировавших в общей сложности 3278 пациенток и 38 242 цикла лечения, установлен индекс Перля 0,55 (с учетом ошибок при применении). Скорректированный индекс Перля составил 0,19 беременности на 100 женщин-лет. Исследование с участием 16 087 женщин и 92 146 циклов сообщает о нескорректированном индексе Перля, равном 0,14. Скорректированный индекс Перля составил 0,09 беременности на 100 женщин-лет [22].
Для КОК, содержащих левоноргестрел, индекс Перля составляет 0,50 [23]. В совокупности объединенная эффективность всех КОК оценивается от 0,3 до 1,25 беременностей на 100 женщин-лет при «идеальном использовании» и от 2,15 до 8,0 – при «типичном» [24]. Таким образом, 30ЭЭ/ДНГ является надежным ингибитором овуляции, противозачаточная эффективность которого сопоставима с другими низкодозированными КОК [25, 26].
Контроль цикла
Возникновение межменструальных кровотечений или отсутствие менструации при использовании низких доз КОК являются одной из самых распространенных причин для прекращения их использования. Многоцентровое клиническое, а также наблюдательные исследования [8, 20–22] продемонстрировали хороший контроль цикла при использовании 30ЭЭ/ДНГ [26–28]: межменструальные кровотечения характеризовались прорывными кровотечениями, незначительными по объему в циклах 1–3 (3–5% женщин), после чего их частота быстро уменьшалась до <1% женщин; продолжительность цикла в целом оставалась неизменной на уровне 28 дней; продолжительность менструального кровотечения сокращалась с 5 дней в начале исследования до около 4 дней после 6 циклов лечения. В среднем снижались интенсивность кровотечения, частота дисменореи; отсутствие кровотечений отмены составляло примерно 3% циклов.
Безопасность ДНГ
В метаболизме липидов 30ЭЭ/ ДНГ может приводить [8, 29, 30] к значительному увеличению уровня триглицеридов; несущественному росту липопротеидов низкой плотности (с тенденцией к снижению в дальнейшем), без изменений в уровне липопротеидов высокой плотности. Возможны значительный рост аполипопротеина А1 и небольшое увеличение аполипопротеина В; значительное снижение липопротеина (а); отсутствие существенных изменений общего холестерина.
Влияние на липидный обмен 30ЭЭ/ ДНГ свидетельствует о преобладании эффекта эстрогенного компонента. Увеличение холестерина липопротеидов высокой плотности, незначительное уменьшение уровней липопротеидов низкой плотности и значительное снижение липопротеина (а), которые соответствуют изменениям, описанным для других низкодозированных КОК [31–32], считается более благоприятным, чем неблагоприятный эффект ЭЭ. I. Wiegratz еt al. [29] изучали влияние 30ЭЭ/ДНГ и комбинации 30ЭЭ/левоноргестрела. Изменения в метаболизме липидов в группе 30ЭЭ/ДНГ оказались более благоприятными из-за разницы в андрогенности прогестина.
По данным ряда клинических исследований, в конце 3 циклов ЭЭ/ДНГ может вызывать следующие изменения в углеводном обмене [33]: небольшое увеличение концентрации инсулина и С-пептида в сыворотке крови; незначительное увеличение концентрации глюкозы и HbA1c, а также отношения инсулин/глюкоза. Через 12 месяцев эти изменения были возвращены к норме. Никакой разницы в эффекте на углеводный обмен не наблюдалось между 30ЭЭ/ДНГ по сравнению с левоноргестрел-содержащим КОК. Небольшая гиперинсулинемия и инсулинорезистентность, вызванные 30ЭЭ/ДНГ, аналогичны вызванными другими низкодозированными КОК [31, 34]. Эти изменения находились в пределах нормального диапазона, но необходимо иметь в виду, что у предрасположенных женщин они могут приводить к патологическим изменениям толерантности к глюкозе.
В двойном слепом плацебоконтролируемом исследовании по сравнению с плацебо применение 30ЭЭ/ДНГ способствовало повышению уровня активности фибриногена (20%), фактора VII (45%) и фактора VIII (10–20%); снижению уровня и активности антитромбина (20–25%), общего и свободного белка S, а также росту уровня и активности протеина С (15–20%). Со стороны фибринолитических параметров значительно возрастал только плазминоген (на 50%), в то время как значительно снижался тканевой активатор плазминогена (на 30%) и ингибитор активатора плазминогена-1 (на 40–60%). Уровни плазмин–антиплазмин комплекса выросли на 30–40%, а D-димера – на 20–55%. Протромбиновое время слегка увеличивалось, немного снижалось активированное частичное тромбопластиновое время. Все выявленные изменения находились в пределах нормы и поэтому не имели клинического значения [35]. Лечение 30ЭЭ/ДНГ (n=20) по сравнению с препаратом ЭЭ/дезогестрел (n=20) продемонстрировало аналогичные изменения параметров коагуляции и фибринолиза [8].
Подобные изменения наблюдаются при использовании других КОК с низкими дозами [36]. Они отражают увеличение внутрисосудистой коагуляционной и фибринолитической активности, главным образом вследствие воздействия ЭЭ на печень и синтеза факторов коагуляции и фибринолиза. В отношении здоровых женщин эффект 30ЭЭ/ДНГ не способствует повышению риска тромботических осложнений, но у пациенток с предрасположенностью риск может быть увеличен, как сообщалось в исследованиях с другими низкодозированными КОК. Риск венозной тромбоэмболии при применении комбинации 30ЭЭ/ ДНГ против других КОК с низкой дозой ЭЭ составляет 0,9 (95% ДИ: 0,6– 1,3) [37].
На массу тела 30ЭЭ/ДНГ оказывает минимальное влияние. В некоторых клинических исследованиях сообщается о небольшом увеличении веса (в среднем на 0,5 кг) во время лечения с использованием 30ЭЭ/ДНГ [8, 21]. Аналогичные изменения встречаются и в других клинических исследованиях с низкими дозами КОК [38].
По данным ряда авторов, никаких существенных изменений в диастолическом или систолическом артериальном давлении не наблюдается во время лечения 30ЭЭ/ДНГ [8, 20, 21]. Другие исследователи сообщают о развитии гипертонии у небольшого количества женщин (2,5%) во время приема КОК [38, 39].
В открытом неконтролируемом многоцентровом клиническом исследовании III фазы (n= 2290) наиболее часто наблюдаемыми побочными эффектами в конце 3-го цикла были головная боль (12,3%), напряжение молочных желез (8,8%), тошнота и рвота (3,9%), депрессия (1,5%), отеки (0,5%). В конце 18-го цикла частота побочных эффектов уменьшилась, например, головная боль до 3,5%, напряжение молочных желез до 1,8% [40]. Только 7,7% из 557 здоровых женщин прекратили использование препарата из-за побочных реакций [21].
В другом наблюдательном исследовании (n=16267) 5,7% женщин сообщили о побочных реакциях. Наиболее часто отмечаемыми были боли в груди (1,5%), увеличение веса (1,1%), головная боль (1,1%), тошнота и рвота (1,0%), дисменорея (0,35%), снижение либидо (0,32%), депрессия (0,29%), и неспецифические боли в животе (0,14%). Из общего количества зарегистрированных побочных реакций только 6 были классифицированы как серьезные [22].
Фармакоэкономическая эффективность
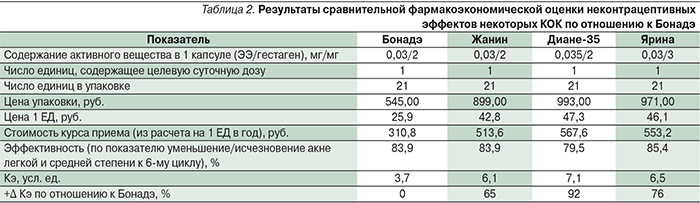
Определение затрат на 1 год использования предполагало оценку прямых затрат на приобретение КОК с одинаковым составом (30ЭЭ/ДНГ, Жанин) и КОК с разным составом для получения дополнительных преимуществ, связанных с неконтрацептивными эффектами (35ЭЭ/ципротерона ацетат, Диане-35 и 30ЭЭ/дроспиренона, Ярина). Оценка эффективности выполнялась по критерию «улучшение/исчезновение акне легкой и средней степени» с учетом типа гестагена, содержащегося в препарате, по данным сравнительного клинического исследования [41]. Средняя эффективность вычислялась по разнице суммы элементов акне (закрытые и открытые камедоны, папулы, пустулы) до и после лечения и выражалась в процентах. Для оценки затрат на лекарства были использованы данные о ценах Государственного реестра лекарственных средств РФ. Косвенные медицинские затраты (обслуживание) пациентов были одинаковыми и не учитывались. В результате проведенного исследования был выполнен анализ минимизации затрат при использовании указанных вариантов КОК (табл. 2). Расчеты соотношения затраты/эффективность для каждого из вариантов проведены по формуле: Кэ=C/Эф; где Кэ – коэффициент затратной эффективности, C – стоимость всех затрат при пользовании конкретным препаратом; Эф – количественное выражение эффективности лекарственного средства.
Как показывают результаты, Кэ оказался меньше у препарата Бонадэ по сравнению с оригинальным препаратом аналогичного состава на 65% и на 76–92% – по отношению к другим сравниваемым средствам антиандрогенного действия.
Неконтрацептивные эффекты
Воздействие на андрогензависимые заболевания кожи
В двойном слепом исследовании пациентов с акне (n=20) назначение 30ЭЭ/ДНГ привело к улучшению проявлений заболевания в 87% случаев после 6 циклов использования. Что касается выраженности акне, то ее степень уменьшилась на 50%. Площадь сальных желез значительно снизилась с 14,4 до 7,4% в 6-м цикле, что было сопоставимо с препаратом, содержащим 35 мкг ЭЭ и 2 мг ципротерона ацетата [17]. Улучшение клинических симптомов сопровождалось существенным снижением сывороточных концентраций общего и свободного тестостерона и значительным увеличением глобулина, связывающего половые гормоны [17].
В проспективном открытом многоцентровом неконтролируемом клиническом исследовании III фазы среди 108 женщин с акне у 57% было отмечено улучшение и у 15% излечение после 6-го цикла [20]. В другом исследовании улучшение отмечено у 80% пациентов [21]. В исследовании с участием 11 104 женщин с акне легкой и умеренной степеней проявления улучшились или исчезли после 6 циклов [4]. В сравнительном исследовании клиническая эффективность 30ЭЭ/ДНГ была сопоставимой с 35ЭЭ/ципротерона ацетата. Воспалительные поражения уменьшились на 65,6 и 64,6% соответственно. Общие проявления акне сократились на 54,7 и 53,6% соответственно. Процент пациентов с улучшением акне составил 91,9 и 90,2 соответственно (р<0,05) [42]. В двух многоцентровых клинических исследованиях было показано значительное уменьшение сальности кожи и волос [20, 21]. В наблюдательном исследовании с участием 11 104 женщин 70% из них сообщили о снижении сальности волос и 81% – об улучшении кожных заболеваний после 6 циклов ЭЭ/ДНГ использования [43].
Таким образом, антиандрогенное действие ДНГ делает 30ЭЭ/ДНГ особенно подходящим препаратом для лечения женщин с андрогензависимыми заболеваниями кожи, а также для женщин, обеспокоенных появлением акне при использовании других КОК [44].
Сексуальность и либидо
Оценка влияния КОК в целом на показатели сексуальности и либидо показывают, что отсутствие озабоченности риском наступления нежеланной беременности, улучшение внешности в связи с исчезновением акне и уменьшение болевого синдрома при дисменорее оказывают положительное влияние на сексуальную функцию женщин [45].
Эндометриоз
Согласно рекомендациям ведущих гинекологических обществ, КОК относят к препаратам первого выбора (хотя и без одобренных показаний), которые применяют для купирования связанной с эндометриозом тазовой боли у женщин, не имеющих противопоказаний и не планирующих беременность на данный момент времени.
Исследования по применению ДНГ в дозе 2 мг для лечения больных эндометриозом продемонстрировали его эффективность, сопоставимую с агонистами гонадотропин-рилизинггормона [46]. Было доказано, что назначение ДНГ позволяет статистически значимо уменьшать болевой синдром, что оценивается различием с плацебо по визуальной аналоговой шкале в 12,3 мм в пользу ДНГ (р<0,0001) [47]. Концентрация эстрадиола в сыворотке крови стабилизируется на уровне 37,4 пг/мл при лечении ДНГ в дозе 2 мг, что удовлетворяет требованиям порогового уровня эстрогена (в пределах 30–50 пг/мл) [48], при котором подавляются в достаточной степени эндометриоидные очаги, при этом уровень достаточен для предотвращения гипоэстрогенных побочных эффектов, таких как снижение минеральной плотности костной ткани. Без ЭЭ ДНГ можно рассматривать в качестве лечебного средства для долгосрочного ведения женщин с эндометриозом. Он эффективен и менее дорогостоящ, чем агонисты гонадотропин-рилизинг-гормона. Однако нерегулярные кровотечения являются самым распространенным осложнением у пациенток, получающих ДНГ (61,6 против 25,4% при использовании агонистов гонадотропинрилизинг-гормона) [49, 50].
L. Del Pup отмечает, что эндометриоидная ткань самостоятельно синтезирует эстрадиол, в то время как 30ЭЭ/ ДНГ поддерживает стабильно низкий уровень E2, который не может существенно стимулировать рост очагов эндометриоза [51]. Эндометриоидные ткани обладают устойчивостью к действию прогестерона, и ЭЭ, содержащийся в КОК, может поддерживать благотворное действие ДНГ, регулируя рецепторы прогестерона и тем самым повышая их чувствительность к прогестину. Существует длительный опыт применения ЭЭ/ДНГ в целях подавления эндометриоза, сокращения рецидивов и контроля над болью, связанной с эндометриозом. Кроме того, ЭЭ/ ДНГ уменьшает риск рака яичников у больных эндометриозом значительнее, чем только ДНГ. Когда цель лечения эндометриоза состоит в уменьшении болевого синдрома, улучшении качества жизни, профилактики рака и получении эстроген-опосредованных благоприятных (неконтрацептивных) эффектов и контрацепции, то ЭЭ/ДНГ представляет собой лучший выбор, чем только ДНГ. Кроме того, назначение ЭЭ/ДНГ в послеоперационном периоде снижает вероятность рецидива симптомов заболевания и появление повторных эндометриом [52].
Заключение
ДНГ является уникальным прогестагеном и сочетает типичные эффекты производных прогестерона (низкое влияние на печеночные функции, антиандрогенное действие, низкая антигонадотропная активность, высокая эффективность подавления овуляции), что сравнимо с другими современными производными 19-нортестостерона (короткий период полувыведения, высокая биодоступность при пероральном приеме). Доказано, что ДНГ надежно ингибирует овуляцию. Значения индекса Перля показывают, что контрацептивная эффективность 30ЭЭ/ ДНГ сравнима с другими низкодозированными КОК. Хороший контроль цикла обеспечивается благодаря содержанию ЭЭ в дозе 30 мкг, что снижает интенсивность и продолжительность менструального кровотечения и частоту дисменореи. 30ЭЭ/ДНГ относится к безопасным препаратам и хорошо переносится большинством женщин.
ДНГ оказывает антиандрогенное действие вместо андрогенных эффектов и особенно хорошо подходит для лечения акне и других проявлений гиперандрогенемии. Сильные гестагенные свойства ДНГ обеспечивают его действие на эндометриоидные очаги, эффективно снижая болевой синдром, обусловленный эндометриозом, и способствуют повышению качества жизни больных, обеспечивая надежный контроль цикла. Эти два обстоятельства определяют потребность пациенток в использовании неконтрацептивных эффектов Бонадэ, обеспечивая более высокую рентабельность на протяжении одного года применения.



