Введение
При оперативных вмешательствах на сосудах конечностей вне зависимости от их локализации, как правило, развиваются как местные, так и системные изменения коагуляционного потенциала крови в сторону ее гиперкоагуляции. Это происходит за счет повышения агрегационной и адгезивной активности тромбоцитов и эритроцитов, активации плазменных коагуляционных факторов (фибриногена, фибринстабилизирующего фактора, появление фибрин-мономерных комплексов), что ведет к истощению активности антикоагулянтных компонентов крови и угнетению фибринолиза [1–4].
Гиперкоагуляция, кровопотеря, нарушения системной и региональной гемодинамики, расстройство микроциркуляторного русла в посттравматическом периоде вызывают развитие тканевой гипоксии, приводящей не только к специфическим расстройствам функций поврежденных органов, но и к развитию токсемии, отеков, болевого синдрома, а в дальнейшем – иммунных нарушений и т. д. [5–7].
В химическом отношении гепарин является представителем кислых сульфатированных мукосахаридов – гликозаминогликанов. Уникальное химическое строение гепарина обусловливает его высокую растворимость как в водных, так и в жировых средах. В организме гепарин синтезируется в тучных клетках и хранится в секреторных гранулах, в которых гепарин находится в ковалентно связанном состоянии с белками [8]. При его высвобождении из тучных клеток происходит деградация связи гепарин–белок, и в кровоток поступает смесь гепариновых фрагментов различной молекулярной массы, которые не только проявляют антикоагулянтные свойства, но и оказывают противовоспалительное, противоотечное и гиполипидемическое, хотя и менее выраженные, действия [1, 9].
Обнаружение других помимо антикоагулянтных свойств физиологических эффектов от действия гепарина способствовало расширению спектра применения антитромботических средств на его основе, используемых, в частности, местно для наружного применения. К таким препаратам направленного действия относится гель для наружного применения Лавенум, содержащий активное вещество гепарин натрия с активностью 1000 МЕ/г, а также вспомогательные вещества (этанол, масло лаванды эфирное, воду очищенную, троламин, карбомер, метилпарагидроксибензоат) (регистрационный номер ЛСР-003344/07, ОАО “Синтез”, Курган, Россия).
Материал и методы
На проведение исследований было получено разрешение комитета по этике при ФГУ РНЦ ВТО им. акад. Г.А. Илизарова Минздрава РФ. Нами были обследованы 24 пациента, которым была выполнена флебэктомия по поводу первично-клапанной формы варикозной болезни нижних конечностей (ВБНК). Из них 12 пациентам (40–63 года, средний возраст – 50,5 ± 7,5 года) на 2-й день после операции на область пораженной вены накожно наносили гель Лавенум® в течение 14 дней с периодичностью 2–3 раза в сутки. Двенадцать пациентов (49–75 лет, средний возраст – 58,5 ± 8,9 года) составили группу контроля. До начала исследований всем больным были проведены необходимые клинические и лабораторные исследования. Согласно критериям включения в группу пациентов, проходящих обследование, были включены испытуемые с нормальной функцией экскреторных органов. По критериям исключения в исследования не включены лица с аллергическими заболеваниями, тучные и истощенные люди.

Всем пациентам произведены общеклиническое исследование, осмотр конечности, ультразвуковое исследование (УЗИ) вен нижних конечностей на аппарате VOLUSON-730 PRO (Швеция). Субъективную симптоматику оценили с помощью анкеты, куда были включены следующие вопросы: возникновение спонтанных болей, болезненность при пальпации по ходу вен, наличие отека, ограничение функции конечности, ощущение тяжести в пораженной конечности, парестезии и судороги, наличие эритемы, общее состояние кожных покровов, кожный зуд. Каждый параметр оценен по 10-балльной шкале. Кроме того, всем больным до и после применения средства Лавенум® выполнены в динамике клинический и биохимический анализы крови. Биохимическое исследование сыворотки крови включило определение активности маркеров мышечного повреждения – лактатдегидрогеназы (ЛДГ) и креатинфосфокиназы (КК), а также определение концентрации недоокисленных продуктов энергообмена – молочной (МК) и пировиноградной (ПВК) кислот. Активность ферментов, концентрация МК определены на автоматическом анализаторе BM/Hitachi 902 (Австрия) с использованием наборы реактивов фирмы “Vital Diagnostic” (Россия). Содержание ПВК в сыворотке определено по реакции с 2,4-динитрофенилгидразином. Исследование коагуляционного звена гемостаза проведено на коагулометре STart 4 (Diagnostica Stago, фирма “Roche”, Германия). Для контроля активности реактивов ежедневно использовалась донорская контрольная плазма. Определение физиологических антикоагулянтов произведено с использованием хромогенного субстрата (Хромотех-антитромбин, ТехнологияСтандарт, Барнаул, Россия) на биохимическом фотометре Stat Fax® 1904 Plus (США). В качестве маркеров активации процесса свертывания крови определены растворимые фибрин-мономерные комплексы (РФМК) – ортофенантролиновый тест (по Елыкомову и Момоту, 1996). Использованы наборы фирмы "Технология-Стандарт" (Барнаул, Россия). Гематологические исследования показателей периферическойкрови проведены в соответствии с требованиями клинико-гематологического обследования (Й. Тодоров, 1969).
Для определения значимости различий между группами использован непараметрический W-критерии Вилкоксона для связанных выборок. Достоверность межгрупповых различий (множественное сравнение) определена с помощью непараметрического H-критерия Крускала– Уоллиса с последующим применением Q-критерия Данна. Результаты в таблицах представлены в виде средней, ошибки средней, медианы, 25-го и 75-го процентилей.
Результаты исследования и обсуждение
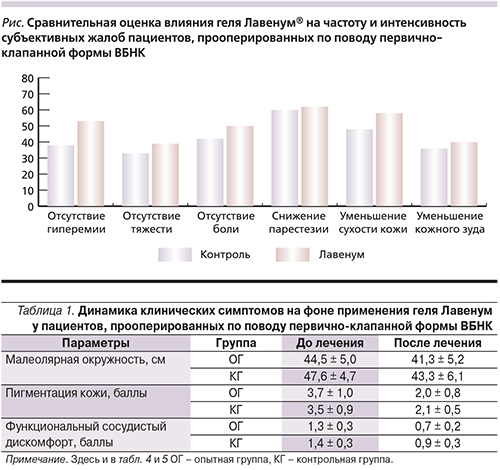
После венэктомии у пациентов в первые сутки и далее на оперированном сегменте конечности наблюдались подкожные кровоизлияния, при этом обширных отеков и выраженных гематом не наблюдалось. Клинически значимые отличия в опытной и контрольной группах имели место только в отношении уменьшения гиперемии (см. рисунок, табл. 1).
Результаты определения показателей красной крови и лейкоцитарной формулы пациентов, прооперированных по поводу первично-клапанной формы ВБНК, в опытной и контрольной группах достоверно не различались (табл. 2 и 3).
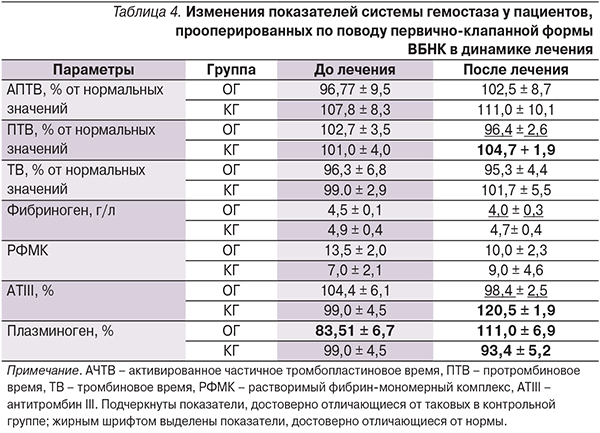
Однако на фоне проводимой терапии изменились показатели гемостаза. Так, в контрольной группе статистически значимых различий в показателях системы гемостаза в процессе лечения не наблюдалось. В опытной группе два показателя – количество фибриногена и активность антитромбина III – статистически значимо снизились в процессе лечения, что связано с механизмом действия гепарина, который входит в состав геля Лавенум (табл. 4). Гепарин при введении в организм соединяется с антитромбином III, образуя комплекс гепарин–антитромбин III, обладающий антикоагулянтным действием, при этом происходит потребление антитромбина III и снижается его активность. Однако значение уровня антитромбина III после лечения не вышло за пределы физиологической нормы. Фибриноген как белок острой фазы в процессе лечения нормализовался, что связано с противовоспалительным действием гепарина.
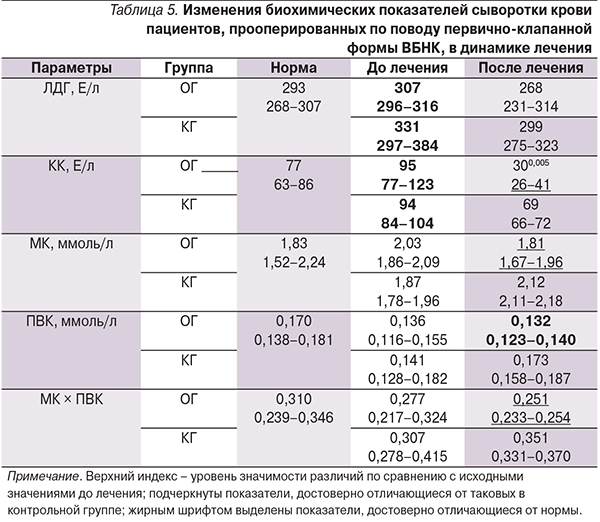
Результаты клинико-лабораторных исследований выявили, что перед началом применения препарата у пациентов обеих групп в сыворотке крови обнаружены достоверно высокие значения активности ЛДГ и КК (табл. 5). После окончания исследования активность ЛДГ у пациентов обеих групп находилась в границах нормы.В свою очередь активность КК у пациентов, которые использовали гель, к концу лечения была достоверно снижена относительно как исходных значений, так и показателей пациентов, которым препарат не назначали (р = 0,02). Кроме того, статистически значимые отличия между группами на момент окончания испытания отмечены для уровня МК в сыворотке крови: его значения у пациентов контрольной группы были выше, чем у пациентов опытной группы (р = 0,04). Помимо этого к концу лечения статистически значимо относительно нормы снижалась и концентрация ПВК в крови пациентов, применявших препарат; к концу лечения у пациентов опытаной подгруппы было достоверно ниже относительно контроля произведение МК × ПВК, отражающее суммарное содержание недоокисленных продуктов в сыворотке крови.
Применение геля Лавенум пациентами отделения сосудистой хирургии предупреждало развитие гипоксии мягких тканей (снижение уровня ПВК, отсутствие роста уровня МК) оперированного сегмента, а также способствовало раннему восстановлению целостности скелетных мышц пациентов, использовавших гель, на что указывало достоверное снижение у них активности КК к окончанию исследования.
Динамическое наблюдение за структурным состоянием подкожно-жировой клетчатки через 1–2 дня непосредственно после операции и через 5 и 10 суток после применения препарата установило, что у пациентов опытной группы происходило снижение показателя эхоплотности зоны интереса на 5–8 % и выравнивание контура дермы уже через 5 дней после применения препарата.
Таким образом, использование геля Лавенум больными в восстановительном периоде после операции флебэктомии по поводу ВБНК достоверно улучшило показатели гемостаза, энергообмена, уменьшило выраженность гиперемии и отека нижних конечностей, не вызвало побочных эффектов, хорошо переносилось больными.



