Введение
Функциональные заболевания желудочно-кишечного тракта (ФЗ ЖКТ) – наиболее распространенные гастроэнтерологические болезни, имеющие не только медицинскую, но и социальную значимость, так как часто манифестируют в молодом трудоспособном возрасте. В основе данной патологии лежат как физиологические, так и морфологические нарушения, которые часто встречаются в сочетании и включают нарушения моторики, висцеральную гиперчувствительность, альтерацию слизистой оболочки и нарушение локальной иммунной функции, изменение микробиоты кишечника, расстройства восприятия и обработки сигналов, поступающих в центральную нервную систему (ЦНС), и другие патогенетические аспекты [1, 2].
Хотя описания симптомов ФЗ ЖКТ исторически встречались на протяжении многих веков, данный термин появился только в течение последних нескольких десятилетий. Данный факт был обусловлен тем, что только в начале XX в. были проведены основополагающие исследования, демонстрирующие влияние деятельности ЦНС на ЖКТ.
Одними из наиболее известных считаются работы академика Ивана Петровича Павлова, которые продемонстрировали наличие двух фаз желудочного сокоотделения – нервнорефлекторной и гуморально-химической – и привели к пониманию роли блуждающего нерва в регуляции нервнорефлекторной фазы желудочного сокоотделения [1, 3].
Развитие медицинских технологий после 1960 г. дало новый толчок исследованиям ФЗ ЖКТ. Так, были разработаны исследовательские системы оценки моторной и электрической активности ЖКТ, с помощью которых были определены механизмы многих двигательных расстройств. Например, было продемонстрировано, что у пациентов с синдромом раздраженной кишки (СРК) наблюдается повышенный моторный ответ на различные раздражители окружающей среды, такие как психологический стресс, прием жирной пищи и т.д., по сравнению с пациентами без данной патологии [1].
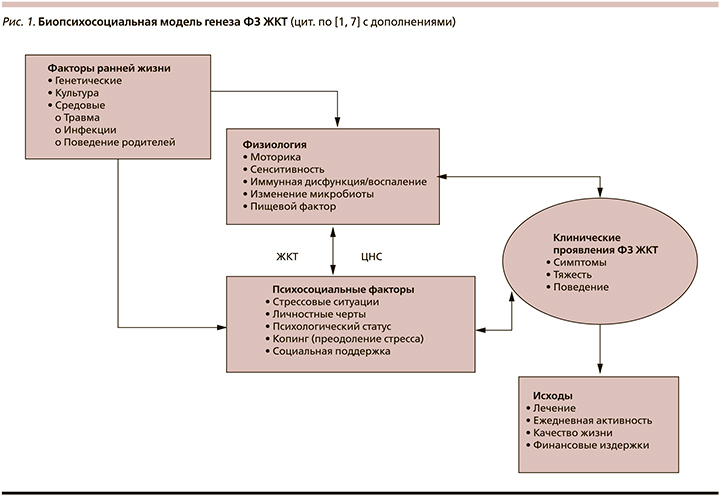
В 1980-х гг. начался период ключевых изменений в понимании психосоциальных аспектов болезней ЖКТ. В 1977 г. были опубликованы работы Джорджа Энгеля (Engel G.L.), которые вдохновили многих исследователей и клиницистов на поиск более интегрированной, биопсихосоциальной модели болезни (рис. 1). Engel G.L., терапевт и психоаналитик, предположил, что болезнь есть продукт биологических, психологических и социальных подсистем, взаимодействующих на разных уровнях, и именно комбинация этих взаимодействующих подсистем определяет болезнь. Таким образом, новая модель понимания психосоциальных аспектов заболеваний ЖКТ была основана на системном подходе и развитии биологии в течение XX в. [1, 4].
В конце 1980-x гг. усилиями ведущих гастроэнтерологов мира была создана общественная организация «Rome Foundation» (Римский Фонд), в основную цель которой вошло изучение ФЗ ЖКТ. Итогом работы организации стала разработка четырех версий т.н. Римских критериев диагностики ФЗ ЖКТ (редакции 1994, 1999–2000, 2006 и 2016 гг.). К концу 1990-х гг. новые клинические и диагностические методы улучшили понимание взаимодействий между ЦНС и кишечником и это привело к формированию концепции оси «мозг–кишка», что нашло отражение в Римских критериях II пересмотра, в которых впервые было представлено новое научное направление в гастроэнтерологии, получившее название «нейрогастроэнтерология». В рамках данного научного направления рассматривается взаимодействие ЦНС и энтеральной нервной системы, которая в свою очередь состоит из сенсорных нейронов, мотонейронов и интернейров, синаптически связанных в нейронные сети, которые обрабатывают информацию о состоянии кишечника и контролируют его работу. В рамках данного направления за последнее десятилетие был достигнут значительный прогресс в понимании того, как изменяется функционирование энтеральной нервной системы при различных патофизиологических условиях, каковы механизмы этих изменений и влияние нейропластичности на моторику кишки [5–7].
Основные изменения в Римских критериях IV пересмотра
Согласно последним Римским критериям IV пересмотра, изданным в 2016 г., ФЗ ЖКТ – это расстройства взаимодействия кишечника и мозга. Это группа расстройств, классифицированных по симптомам со стороны ЖКТ, связанных с любой комбинацией следующих аспектов: нарушения моторики, висцеральная гиперчувствительность, альтерация слизистой оболочки и нарушение локальной иммунной функции, изменение микробиоты кишечника, нарушение восприятия и обработки сигналов, поступающих в ЦНС [1, 5, 8]. Ниже представлена классификация ФЗ ЖКТ, предложенная Римским консенсусом IV пересмотра (2016), цит. по [7] (см. таблицу).

Именно в последнем пересмотре Римских критериев было впервые предложено заменить термин «функциональные» в отношении ФЗ ЖКТ на новую дефиницию этой группы заболеваний – «расстройства взаимодействия головного мозга и ЖКТ». Термин «синдром функциональной абдоминальной боли» предыдущей классификации ФЗ ЖКТ предложено заменить термином «болевой абдоминальный синдром центрального генеза» как более корректно отражающий патогенез рассматриваемой патологии. Тем не менее некоторые клинические расстройства (такие, как, например, функциональная диарея, функциональная изжога) сохранили свою терминологию, чтобы обеспечить их отличие от расстройств, имеющих сходные симптомы, но с четкой органической этиологией. В перечень ФЗ ЖКТ были включены новые нозологические единицы с известной этиологией: опиоидиндуцированная гастроинтестинальная гипералгезия, опиоидиндуцированный запор, каннабиноидиндуцированный рвотный синдром. Включение этих нозологий в обновленную классификацию было обусловлено тем, что данные заболевания в своей основе имеют нарушение взаимодействия головного мозга и ЖКТ, что соответствует новому определению ФЗ ЖКТ, кроме того, эти заболевания схожи в клинических проявлениях с ФЗ ЖКТ. Также экспертным советом Римского консенсуса IV пересмотра в обновленную классификацию ФЗ ЖКТ была внесена новая нозологическая единица – «синдром тошноты и рвоты», которая объединяет ранее выделявшиеся заболевания – хроническую идиопатическую тошноту и функциональную рвоту. Также были пересмотрены диагностические критерии дисфункции сфинктера Одди (ДСО), так как прежние рекомендации проведения папиллосфинктеротомии при III типе ДСО (расширение холедоха, повышение уровня трансаминаз и панкреатических ферментов) не получили убедительного подтверждения и сопровождались повышением риска развития панкреатита, прободения и кровотечения. Именно поэтому прежний III тип ДСО (согласно Милуокской классификации) из новых критериев был удален и было указано, что пациентам без убедительных доказательств обструкции желчного протока не следует проводить эндоскопическую ретроградную холангиопанкреатографию с манометрией и сфинктеротомию, а рекомендуется назначать симптоматическое лечение. При лечении ДСО билиарного типа с умеренными доказательствами билиарной обструкции до проведения сфинктеротомии должны рассматриваться другие диагностические возможности [1, 7].
Дифференциальная диагностика функциональной изжоги и гиперсенситивного рефлюксного синдрома
Одними из наиболее широко встречающихся в рутинной практике среди ФЗ ЖКТ являются функциональная изжога и гиперсенситивный рефлюксный синдром (ГСРС).
ГСРС был включен экспертным советом Римского консенсуса IV в раздел «расстройства функции пищевода», ранее рассматривавшийся как вариант неэрозивной рефлюксной болезни (НЭРБ). Диагностика данного заболевания базируется на следующих критериях [9]:
- Характерные симптомы: изжога или боль в загрудинной области (ответ на антисекреторную терапию не исключает данный диагноз).
- Связь возникновения симптомов с физиологическими кислыми или некислыми гастроэзофагеальными рефлюксами (при проведении рН-метрии или рН-импедансометрии верхних отделов ЖКТ) на фоне нормальных показателей экспозиции кислоты в пищеводе.
- Обнаружение нормальной эндоскопической картины слизистой оболочки пищевода.
- Отсутствие структурных изменений слизистой оболочки пищевода, характерных для эозинофильного эзофагита (по данным гистологического исследования биоптатов).
- Отсутствие основных заболеваний пищевода, протекающих с нарушением его двигательной функции (ахалазия кардии, диффузный эзофагоспазм, нарушения моторики по типу отбойного молотка, гиперкинезия грудного отдела пищевода, гипокинезия и др.).
- Клинические симптомы должны отмечаться по меньшей мере 2 раза в неделю на протяжении последних 3 месяцев при их общей продолжительности не менее 6 месяцев.
В отличие от ГСРС к диагностическим критериям функциональной изжоги относятся [9]:
- Ощущение жжения, дискомфорта или боли в загрудинной области.
- Симптомы сохраняются, несмотря на оптимальную терапию с использованием ингибиторов протонной помпы (ИПП; двойная доза, регулярный прием препаратов перед едой).
- Установлено отсутствие связи возникновения симптомов с патологическими или физиологическими гастроэзофагеальными рефлюксами.
- Подтверждено отсутствие структурных изменений слизистой оболочки пищевода, характерных для эозинофильного эзофагита (гистологическое исследование биоптатов).
- Доказано отсутствие заболеваний пищевода, связанных с нарушением моторики и перистальтики пищевода (ахалазия кардии, диффузный эзофагоспазм, расстройства моторики по типу «отбойного молотка», гиперкинезия грудного отдела пищевода, гипокинезия и др.).
- Клинические симптомы должны отмечаться по меньшей мере 2 раза в неделю на протяжении последних 3 месяцев при их общей продолжительности не менее 6 месяцев.
В связи со схожестью симптоматики вышеуказанных заболеваний закономерно возникает необходимость диагностического поиска у пациента, предъявляющего жалобы на изжогу. Так, в отсутствие изменений слизистой оболочки пищевода по результатам фиброгастродуоденоскопии и гистологического исследования и если у пациента нет ранее установленного диагноза гастроэзофагеальной рефлюксной болезни (ГЭРБ), рекомендовано проведение суточной внутрипищеводной рН-импедансометрии на фоне отмены ИПП или до их назначения. У пациентов с нормальными показателями экспозиции кислоты в пищеводе и отсутствием связи между возникновением симптомов и эпизодами рефлюкса устанавливается диагноз функциональной изжоги, в то время как в случае выявления повышения экспозиции кислоты в пищеводе по результатам рН-импедансометрии диагностируется НЭРБ, а у пациентов с нормальными показателями экспозиции кислоты в пищеводе и наличием связи между возникновением симптомов и эпизодами физиологического рефлюкса диагностируется ГСРС (рис. 2).
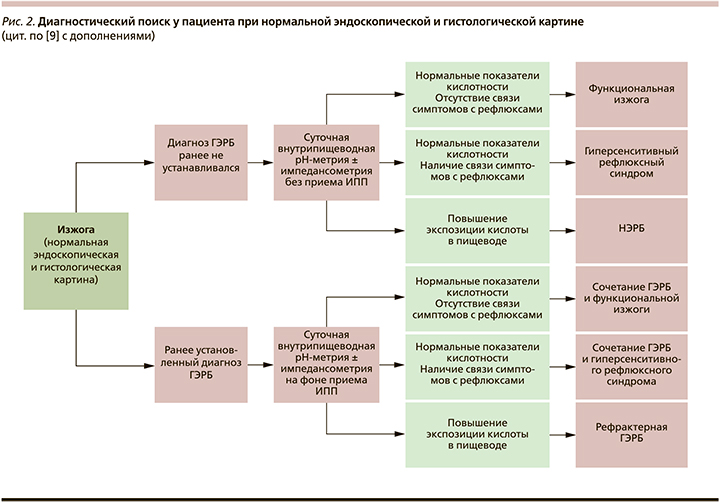
В том случае если у пациента ранее был установлен диагноз ГЭРБ, внутрипищеводная рН-импедансометрия выполняется на фоне приема ИПП. Тем же пациентам, у которых по результатам рН-импедансометрии нормальные показатели экспозиции кислоты в пищеводе и нет связи симптомов с рефлюксом, ставится диагноз ГЭРБ в сочетании с функциональной изжогой. В случае если показатели экспозиции кислоты в пищеводе соответствуют норме, но есть связь между симптомами и рефлюксом, у пациента диагностируется синдром перекреста ГЭРБ и гиперсенситивности пищевода. Если же по результатам рН-импедансометрии выявляется повышение экспозиции кислоты в пищеводе, то в таком случае диагностируется рефрактерная ГЭРБ.
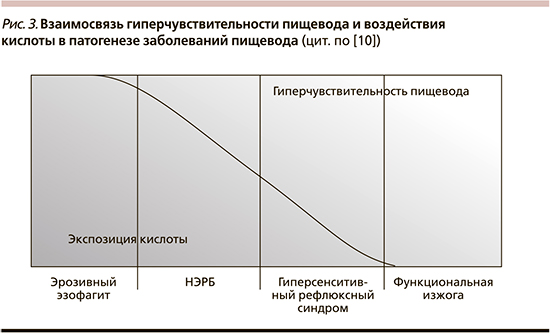
Симптомы ГСРС связаны с сочетанием воздействия кислоты и гиперчувствительности пищевода (рис. 3), причем разделительная кривая отражает более выраженный эффект воздействия кислоты для НЭРБ и более выраженный эффект гиперчувствительности пищевода для ГСРС, в то время как симптомы эрозивного эзофагита обусловлены аномальным воздействием кислоты, а симптомы функциональной изжоги – гиперчувствительностью [10].
Дифференциальная диагностика ФЗ ЖКТ и соматоформной дисфункции вегетативной нервной системы
Определенный интерес, особенно в свете нового представления о ФЗ ЖКТ как о нарушении взаимодействия кишечника и ЦНС, представляет собой вопрос о выявлении взаимосвязи и при необходимости проведении дифференциальной диагностики между ФЗ ЖКТ и соматоформной дисфункцией вегетативной нервной системы (СДВНС).
Соматоформные расстройства
(F45) – группа психических расстройств невротической природы, отличительным признаком которых являются многочисленные признаки соматических заболеваний, не подтвержденные объективными клиническими исследованиями. В Международной классификации болезней 10-го пересмотра (МКБ-10) в группе соматоформных расстройств выделяют СДВНС («органные неврозы»; F45.3), в составе которой выделяют также СДВНС верхней части ЖКТ (F45.31) и СДВНС нижней части ЖКТ (F45.32). Считается, что частным проявлением СДВНС нижней части желудочно-кишечного тракта может являться СРК, а СДВНС верхней части ЖКТ в своих клинических проявлениях соответствует ФЗ верхнего отдела ЖКТ [11].
Диагностические критерии СДВНС по МКБ-10:
- симптомы вегетативного возбуждения (сердцебиение, потение, тремор, покраснение), которые имеют хронический характер и причиняют беспокойство;
- наличие дополнительных субъективных симптомов, которые относятся к определенному органу или системе;
- озабоченность больного по поводу возможного серьезного, но, как правило, неопределенного заболевания этого органа или системы, причем повторные объяснения и разуверения врачей остаются бесплодными;
- сведений о существенном структурном или функциональном расстройстве данного органа или системы нет.
Следует отметить, что для постановки данного диагноза необходимо наличие всех критериев. Таким образом, СДВНС имеет диагностические критерии, отличающиеся от таковых у ФЗ ЖКТ, кроме того, такой диагноз может ставиться только профильным специалистом. При этом следует отметить, что в американском аналоге классификации соматоформных расстройств «Diagnostic and Statistical Manual of mental disorders, fifth edition» («Диагностическое и статистическое руководство по психическим расстройствам 5-го издания») диагноз «соматоформная дисфункция вегетативной нервной системы» отсутствует [12].
Вместе с тем тревожность и депрессия часто встречается у пациентов с ФЗ ЖКТ и до конца не ясно, являются ли эти состояния причиной возникновения ФЗ ЖКТ, или же они вторичны по отношению к ним, но в целом общепризнанно, что депрессия и тревожность, как и соматизация, влияют на симптоматику и частоту обострений заболевания у таких пациентов. Например, у пациентов с СРК «соматизация» встречается чаще, чем у здоровых людей, но реже, чем у пациентов с соматоформными расстройствами, и связана с тяжестью симптомов и ухудшением качества жизни. В ряде исследований было продемонстрировано, что те пациенты, у кого выраженность изжога слабо коррелирует с явлениями кислотного рефлюкса при pH-метрии, демонстрируют более высокие показатели тревоги и «соматизации», чем те, у кого симптомы спровоцированы рефлюксом [13–18].
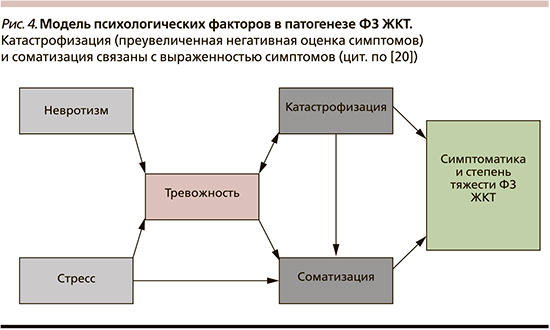
Кроме того, «соматизация» связана с частотой обращения за медицинской помощью и недостаточным ответом на лечение, в т.ч. в связи с прекращением приема лекарств из-за предполагаемых пациентом побочных эффектов (рис. 4). Поэтому оценка «соматизации», определение количества соматических симптомов и их тяжести являются клинически обоснованными [19–24].
Римские критерии IV пересмотра: нерешенные вопросы
Несмотря на то что Римские критерии достаточно полезны в рамках клинических исследований, они имеют и свои ограничения в клинической практике, поскольку многие из пациентов не соответствуют всем критериям или указанным в критериях количественным временным рамкам, необходимым для постановки диагноза. Например, пациенты с абдоминальной болью и кишечной дисфункцией в течение менее чем 6 месяцев или с частотой менее 1 эпизода в неделю не отвечают Римским критериям-IV для постановки диагноза СРК, хотя, возможно, эти пациенты будут получать схожую эмпирическую терапию. Кроме того, диагноз, установленный на основании Римских критериев-IV, не всегда позволяет полностью отражать состояние пациента и подбирать ему оптимальную терапию. Так, пациент с функциональной диспепсией, имеющий умеренные симптомы без снижения качества жизни, может и не нуждаться в специальном лечении. Аналогичный пациент с выраженной болью, депрессией и похуданием из-за ограничений в питании требует соответствующего лечения [5, 25, 26].
Заключение
Таким образом, если ранее ФЗ ЖКТ определялись более-менее специфическими симптомами и отсутствием структурных или биохимических нарушений, которые вызывают эти симптомы, то в настоящее время эта концепция считается устаревшей, ведь при тщательном обследовании у многих пациентов могут быть обнаружены патоморфологические изменения, которые объясняют или вызывают симптомы. Следовательно, термин «функциональные» в отношении ФЗ ЖКТ не отражает современных представлений о патогенезе этих заболеваний как о нарушении работы оси «кишечник–мозг» вследствие воздействия различных факторов. Тем не менее в настоящее время создать единую патофизиологическую модель для всех ФЗ ЖКТ не представляется возможным, поскольку даже наиболее изученные нозологические единицы могут иметь многофакторную природу [27].
Другой ключевой особенностью ФЗ ЖКТ является широкая распространенность среди таких пациентов депрессии, тревожности и соматизации, что требует разработки системного подхода к диагностике и лечению этих состояний с привлечением специалистов не только гастроэнтерологического профиля.



