Введение
Хроническая болезнь почек (ХБП) у пожилых пациентов является серьезной медицинской и социально-экономической проблемой. За последние 3 десятилетия число пациентов, находящихся на поддерживающем диализе во всем мире, резко возросло, и данные моделирования показывают, что к 2030 г. это число увеличится более чем в 2 раза [1]. При этом растет доля пожилых пациентов, требующих лечения с использованием различных методов заместительной почечной терапии (ЗПТ) [2].
По данным когортных исследований, у пациентов с тяжелой сопутствующей патологией диализ не обеспечивает значимого продления жизни, но при этом может приводить к ухудшению ее качества, снижению функционального статуса, ухудшению когнитивных функций и увеличению числа госпитализаций [3]. Целью исследования была оценка выживаемости и изучение влияния общеклинических и лабораторных факторов на продолжительность жизни пациентов от 60 лет и старше, получавших лечение хроническим диализом (ХД) в Минске.
Материал и методы
Работа представляет собой историческое когортное одноцентровое исследование, которое проведено в отделении гемодиализа УЗ «1-я городская клиническая больница» («1-я ГКБ»), являющемся самым крупным диализным центром в Минске: число прикрепленного населения к данному диализному центру составляет около 1 250 000 человек. Критериями включения в исследование были возраст ≥60 лет, наличие 5-й стадии хронической болезни почек (ХБП), требующей лечения ХД.
Критерии исключения включали возраст менее 60 лет, наличие острого почечного повреждения, отказ от лечения методами ЗПТ в пользу консервативного лечения.
Объектами исследования явились 199 (98 мужчин и 101 женщина) пациентов, взятых на лечение ХД: программным гемодиализом (ПГД) – 183 (92%), или постоянным амбулаторным перитонеальным диализом (ПАПД) –14 (8%) человек в 2017–2021 гг., при этом группа ПАПД также включила одного пациента, взятого на ПАПД в 2014 г. и одного, взятого на ПАПД в 2016 г. (ввиду малого числа наблюдений в группе ПАПД). Дизайн исследования представлен на рис. 1.

Во время исследования учитывали половозрастную структуру когорты, клинический диагноз заболевания, которое послужило причиной ХБП, метод лечения (ПГД или ПАПД), суточный диурез, наличие гипергидратации на момент начала диализа, уровни Кр и мочевины в сыворотке крови до начала диализа. Гипергидратацию оценивали по данным клинического осмотра на момент начала диализа (наличие периферических отеков) и по данным рентгенографического обследования легких (наличие застоя по малому кругу кровообращения, наличие гидроторакса). Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI [4], индекс массы тела (ИМТ) – по индексу Кетле [5].
Продолжительность наблюдений определяли как промежуток времени от момента начала диализа до достижения клинического исхода (летальный исход) или окончания периода наблюдения 18.01.2023. Пациенты, которым была проведена трансплантация донорской почки, считались цензурированными с момента трансплантации, как и пациенты, переведенные на ЗПТ в другое УЗ, с момента их перевода.
На первоначальном этапе проводили анализ соответствия вида распределения количественных показателей закону нормального распределения, который выполняли с использованием критерия Шапиро–Уилка. Поскольку все показатели, полученные в данном исследовании, имели отклонения от нормального распределения, количественные показатели исследования представлены медианой и квартилями в виде Me (Q25; Q75), а для анализа количественных данных использовались методы непараметрической статистики. Для сравнения количественных показателей в группах использовали критерий Манна–Уитни–Вилкоксона.
Качественные показатели в группе представлены в виде абсолютных (n) и относительных (%) значений. Для сравнения качественных данных более чем в двух группах использовался χ2-критерий.
Анализ выживаемости осуществляли с помощью оценки Каплан–Майера, определяли кумулятивную вероятность дожития. Однолетняя и двулетняя выживаемости представлены в виде %±стандартная ошибка (SE). Сравнение групп по выживаемости проводилось по критерию Гехана–Бреслоу (Gehan-Breslow).
Факторы риска оценивали на основании отношения рисков (ОР) и представлены как ОР (95% доверительный интервал – ДИ). Предположение о пропорциональности рисков проверяли с помощью критерия остатков Шоенфельда. При нарушении предположения о пропорциональности использовали стратифицированную модель Кокса для изучения влияния предикторов при различном времени наблюдения в многофакторном анализе. Для установления уровня количественного показателя, ассоциированного с риском неблагоприятного исхода, использовали метод максимальной ранговой статистики.
Статистическую обработку данных проводили с использованием статистического пакета R, версия 4.1.3, и библиотек survival, survminer, maxstat.
Для статистических выводов ошибка первого рода была принята как α=0,05.
Результаты
Распределение пациентов по группам ЗПТ было несбалансированным: 183 (92%) пациента находились на лечении ПГД и 16 (8%) – на лечении ПАПД. Распределение исходных клинико-лабораторных показателей в группах ЗПТ представлено в табл. 1.
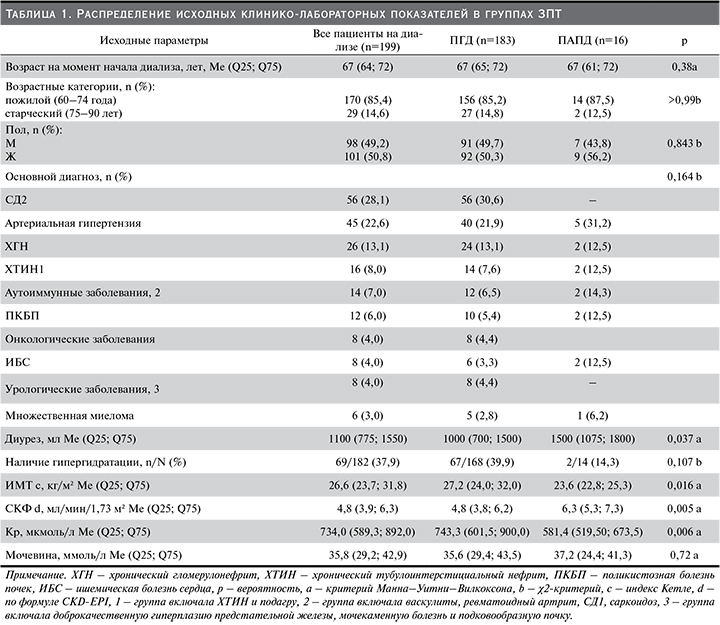
Медиана возраста на момент начала диализа составила 67 (64; 72) лет, при этом самому возрастному пациенту было 82 года. В соответствии с классификацией Всемирной организации здравоохранения (ВОЗ) были выделены следующие группы: 1-я – пациенты пожилого возраста (60–74 года), 2-я группа – пациенты старческого возраста (75–90 лет).
Не было различий в группах ЗПТ по возрасту на момент начала диализа. В обеих группах наиболее представительной была группа лиц пожилого возраста (85,2 и 87,5% соответственно). В группах ЗПТ было сопоставимое число мужчин и женщин (49,7% мужчин в группе ПГД и 43,8% в группе ПАПД). Основные причины проведения гемодиализа на 5-й стадии ХБП: СД2 (28,1%), артериальная гипертензия (22,6%) и ХГН (13,1%). На момент начала диализа группы статистически значимо различались по диурезу (p=0,037), ИМТ (p=0,016), СКФ (p=0,005), уровню Кр в сыворотке крови (p=0,006). Диурез, СКФ были выше в группе ПАПД, тогда как ИМТ, Кр были выше в группе ПГД. По уровню мочевины статистически значимых различий зарегистрировано не было (p=0,72), как и по наличию гипергидратации на момент начала диализа (p=0,107).
Медиана наблюдений в исследовании отдаленных результатов лечения составила 869 дней.
Кумулятивная выживаемость в группах ЗПТ представлена на рис. 2.
Выявлены различия в выживаемости у групп ЗПТ (p=0,011) по критерию Гехана–Бреслоу, который акцентирует различия в раннем периоде наблюдения (рис. 2).
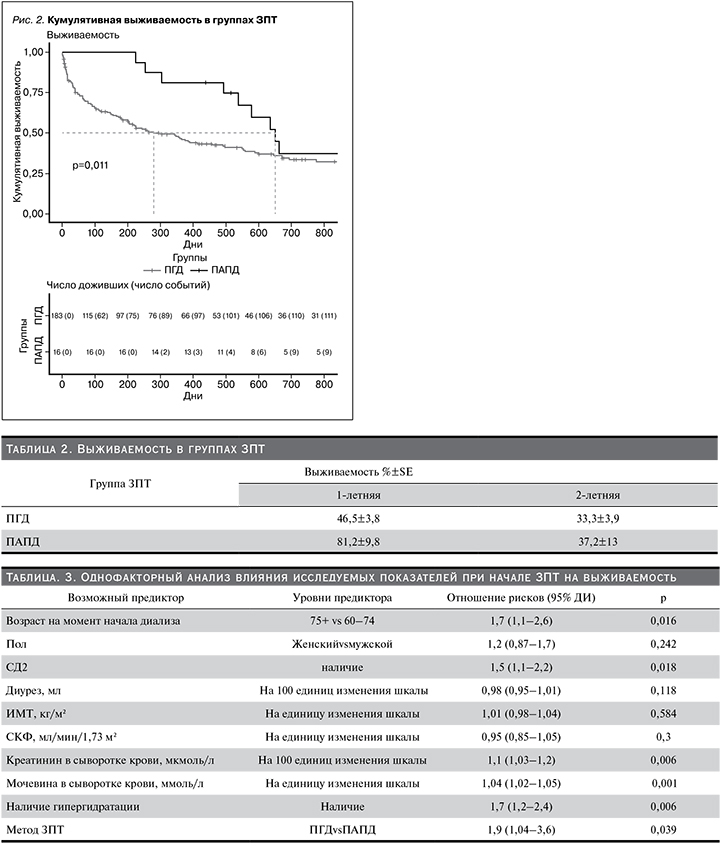
Медиана выживаемости на ПГД составила 279 дней, на ПАПД – 650 дней. Выживаемость различалась в первый год лечения (табл. 2): 1-летняя выживаемость пациентов на ПГД составила 46,5±3,8%, на ПАПД – 81,2±9,8%, далее статистически значимых различий в снижении выживаемости зарегистрировано не было: ПГДvsПАПД – 33,3±3,9vs37,2±13% соответственно (рис. 2).
Проведен однофакторный анализ влияния исследуемых показателей при начале ЗПТ на выживаемость (табл. 3).
Выявлены следующие ПЛИ у пациентов пожилого и старческого возраста на момент начала диализа (табл. 3):
- метод ЗПТ (ОР= 1,9, 95% ДИ: 1,04–3,6);
- возраст (ОР = 1,7, 95% ДИ: 1,1–2,6);
- наличие СД2 (ОР= 1,5, 95% ДИ: 1,1–2,2);
- наличие гипергидратации (ОР = 1,7, 95% ДИ: 1,2–2,4);
- додиализные уровни Кр (ОР= 1,1, 95% ДИ: 1,03–1,2);
- мочевины (ОР = 1,04, 95% ДИ: 1,02–1,05).
Согласно полученным данным, ПГД является фактором риска летального исхода у пациентов пожилого и старческого возраста (ОР = 1,9, 95% ДИ: 1,04–3,6). При этом отсутствие возможности проведения рандомизированных клинических испытаний у пожилых пациентов обусловило варьирование данных об исходах и продолжительности жизни в зависимости от метода ЗПТ. Ряд проведенных исследований в последнее время позволяет предполагать, что выживаемость на ПГД выше у пациентов с СД, а также через 1–3 года от начала диализа [6]. В нашем исследовании группа ПАПД была более сохранной в плане остаточной функции почек (табл. 1), что могло обусловить преимущества в выживании на первом году от начала диализа.
Старческий возраст на момент начала диализа является фактором риска летального исхода у пациентов на диализе (ОР = 1,7, 95% ДИ: 1,1–2,6). По данным мета-анализа 2020 г. [7], включившего 28 исследований, возраст служил фактором риска летального исхода в пожилой гемодиализной популяции (отношение шансов [ОШ] = 1,43, 95% ДИ: 1,22–1,68).
Наличие СД2 повышает риск смерти на диализе у пациентов ≥60 лет (ОР = 1,5; 95% ДИ: 1,1–2,2). Согласно данным мета-анализа 2020 г. [7], сердечно-сосудистые заболевания не являются фактором риска летального исхода, тогда как наличие СД2 увеличивает риск смерти в пожилой гемодиализной популяции (ОШ=1,19; 95% ДИ 1,06–1,33).
Гипергидратация на момент начала диализа повышает риск летального исхода у диализных пациентов ≥60 лет (ОР = 1,7; 95% ДИ: 1,2–2,4). По данным мета-анализа 2018 г. [8], включившего 29 исследований, имеется прямая зависимость между гипергидратацией и смертностью при различных заболеваниях взрослых (ОШ=4,38; 95% ДИ: 2,76–6,94). Более высокие уровни Кр и мочевины до начала диализа повышают риск летального исхода. В отсутствие лечения пациенты в уремии имеют неблагоприятный прогноз [9].
В нашем исследовании не было отмечено влияния пола (p=0,242), диуреза (p=0,118), ИМТ (p=0,584) и СКФ (p=0,292) на выживаемость на ЗПТ у пациентов пожилого и старческого возраста. Однако, согласно данным литературы, такие различия существуют. Пол влияет на продолжительность жизни на диализе: женщины на диализе, как правило, живут меньше и имеют худший прогноз в отношении сердечно-сосудистой смертности [10], у женщин, как правило, большее число госпитализаций в год по разным причинам (2,08 у женщин против 1,68 у мужчин) [11].
Диурез влияет на продолжительность жизни на диализе: согласно литературным данным, остаточный диурез обусловливает лучшую выживаемость и лучшее качество жизни у диализных пациентов [12].
ИМТ влияет на продолжительность жизни на диализе: по данным мета-анализа 2020 г. [7], ИМТ≥25 кг/м² ассоциирован с лучшей выживаемостью в пожилой гемодиализной популяции (ОШ=0,94, 95% ДИ: 0,92–0,96).
СКФ как фактор риска летального исхода лучше использовать на додиализных стадиях ХБП, т.к. варьирование Кр от 400 до 1000 мкмоль/л обусловливает лишь небольшое изменение СКФ по формуле CKD-EPI: для пациента женского пола в возрасте 65 лет и Кр 400 мкмоль/л СКФ будет равна 10 мл/мин/1,73 м², а при уровне Кр 1000 мкмоль/л – 3 мл/мин/1,73 м². Обе СКФ являются показанием к началу диализа, однако остаточная функция почек у данных пациентов будет разной.
Дальнейшее исследование ПЛИ показало, что для таких показателей, как мочевина и Кр, а также метод ЗПТ, нарушается предположение о пропорциональности рисков (p<0,05). При многофакторном анализе использована модель Кокса, стратифицированная по первому и второму годам наблюдения для вышеуказанных показателей. В многофакторную модель были включены предикторы, показавшие статистическую значимость в однофакторном анализе (табл. 4).
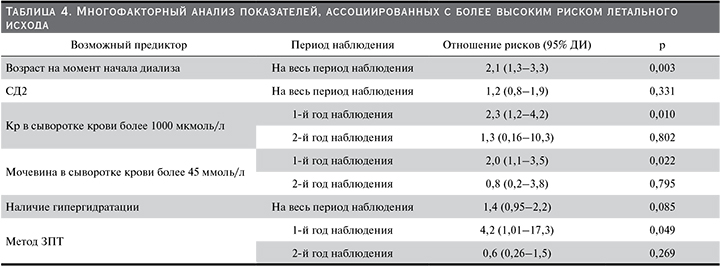
Многофакторный анализ (табл. 4) показал, что ПЛИ у пациентов пожилого и старческого возраста являются возраст на момент начала диализа и в первый год ЗПТ – уровень Кр в сыворотке крови более 1000 мкмоль/л, а мочевины более 45 ммоль/л и использование ПГД, как первого метода ЗПТ.
Обсуждение
В данном исследовании представлен анализ данных 199 пациентов пожилого и старческого возраста, находившихся на лечении методом ПГД (183 [92%]) или ПАПД (16 [8%]). Выявлен высокий уровень смертности пациентов пожилого и старческого возраста, получавших лечение ХД (табл. 2).
При этом наивысший пик смертности отмечен на первом году лечения ПГД, когда 1-летняя выживаемость пациентов на ПГД составила 46,5±3,8%, на ПАПД – 81,2±9,8%. При последующем анализе 2-летняя выживаемость составила на ПГД 33,3±3,9%, на ПАПД – 37,2±13%. Полученные данные совпадают с результатами исследования 391 пациента в возрасте от 65 лет и старше из североамериканской базы Medicare, в котором 88 (23%) пациентов умерли в течение первого месяца лечения, 173 (45%) – в течение 6 месяцев и 213 (55%) – в течение года лечения диализом [13].
Выявленная закономерность высокого риска смерти в первый год лечения ПГД, вероятно, связана с низкой адаптивной способностью пожилых пациентов к новым условиям существования при снижении общих резервных возможностей организма, что по сути является синдромом старческой слабости или немощности (frailty) [14] и приводит к необходимости оценки функционального статуса пожилых пациентов на диализе.
Имеющиеся на первом году лечения статистически значимые различия выживаемости пациентов пожилого и старческого возраста в зависимости от выбора метода ЗПТ (p=0,011) при дальнейшем наблюдении исчезают (рис. 2).
Различия в выживаемости на первом году ЗПТ могут быть обусловлены следующими факторами:
- несбалансированностью групп ЗПТ с небольшим числом наблюдений в группе ПАПД;
- различием групп ЗПТ по остаточной функции почек (в группу ПАПД входили пациенты с лучшей остаточной функцией почек);
- отсутствием в группе ПАПД пациентов с СД2 (согласно данным литературы, пациенты с СД на ПАПД живут меньше [6]);
Тем не менее, несмотря на дискутабельность полученных результатов, проведенный статистический анализ показал, что ПАПД достоверно не ухудшает выживаемость пациентов пожилого и старческого возраста.
Принимая во внимание социальные преимущества ПАПД в виде меньшего влияния на повседневную жизнь пациента с отсутствием дискомфорта, связанного с транспортировкой в и из гемодиализного центра, а также физиологические и медицинские преимущества – наличие медленной непрерывной ультрафильтрации, обеспечивающей кардиоваскулярную стабильность и отсутствие необходимости формирования сосудистого доступа для проведения сеансов гемодиализа [6], данный метод можно считать более подходящим для пациентов пожилого и старческого возраста, особенно на начальном этапе лечения.
Поскольку в проведенном многофакторном анализе показатели, ассоциированные с более высоким риском летального исхода, за исключением возраста, влияли на продолжительность жизни на диализе только в первый год лечения диализом, требуется поиск новых ПЛИ, определяющих продолжительность жизни на втором и последующих годах лечения диализом. Поиск данных ПЛИ поможет оптимизировать оказание медицинской помощи пациентам пожилого и старческого возраста с 5-й стадией ХБП.
Заключение
Старение населения и улучшение качества оказываемой медицинской помощи обусловило рост доли пожилых пациентов в нефрологической популяции, что значительно увеличило число пожилых пациентов в диализных центрах. При этом диализ у пациентов пожилого и старческого возраста имеет свои особенности ввиду имеющейся коморбидной патологии, снижения резервных возможностей организма и способности отвечать на стресс. Непредсказуемая переносимость сеанса гемодиализа и снижение функционального статуса обусловливают снижение качества жизни и высокий риск неблагоприятного исхода.
При этом ввиду наличия социальных и ряда физиологических преимуществ ПАПД может рассматриваться как ЗПТ 1-й линии у пациентов пожилого и старческого возраста.
Таким образом, поиск факторов, определяющих развитие неблагоприятного клинического исхода, с целью создания алгоритма выбора метода лечения пациентов пожилой возрастной группы с пятой стадией ХБП остается важной задачей современной нефрологии.



