Введение
Международное общество по изучению заболеваний вульвы и влагалища (International Society for the Study of Vulvar and Vaginal Diseases) трактует бактериальный вагиноз (БВ) как полимикробный клинический синдром [1–4], характеризующийся нарушением баланса микрофлоры влагалища. В норме во влагалище преобладают лактобациллы, продуцирующие молочную кислоту и перекись водорода, что создает кислую среду (pH 3,8–4,5), благодаря которой рост патогенных и условно-патогенных микроорганизмов затормаживается. Известно, что при БВ происходит снижение количества лактобацилл [5] и увеличение количества анаэробных бактерий, таких как Gardnerella vaginalis, Mobiluncus, Prevotella, Bacteroides и Mycoplasma hominis и множество других [6–8].
Бактериальная ассоциация условно-патогенных микроорганизмов влагалища продуцирует амины, повышая влагалищный pH (выше 4,5), что и вызывает характерную клиническую симптоматику у женщин [9].
БВ является наиболее частой причиной аномальных выделений из влагалища [10, 11]. На прием к гинекологу женщины обращаются с жалобами на патологические выделения из половых путей, неприятный запах из влагалища, дискомфорт в области вульвы и преддверия влагалища, некоторых также беспокоит вагинальный зуд [2, 10–12]. Практикующие специалисты всегда ссылаются на авторитетные источники информации и гайдлайны для подтверждения диагноза, определения тактики ведения и лечения пациентки. В клинических рекомендациях по БВ, утвержденных Минздравом РФ в 2024 г. [13], четко выделены основные диагностические симптомы БВ.
Клиническую картину БВ составляет ряд субъективных симптомов:
- выделения из влагалища обильного характера, серого или белого цвета;
- аминный («рыбный») неприятный запах выделений, усиливающийся после коитуса, менструации и чрезмерной гигиены с использованием моющих средств с щелочным pH, зачастую не предназначенных для интимной гигиены;
- дискомфорт в области наружных половых органов;
- диспареуния;
- редко – зуд и/или жжение в области половых органов.
Объективные симптомы БВ:
- гомогенные беловато-серые вагинальные выделения густой консистенции, равномерно распределяющиеся по слизистой оболочке влагалища и вульвы.
У пациенток симптомы воспалительной реакции со стороны половых органов отсутствуют, и это один из главных диагностических критериев, отличающих БВ от других заболеваний половых путей преимущественно воспалительной этиологии, встречающихся у женщин.
Диагностика БВ и существующие стандартные схемы терапии невоспалительного синдрома, характеризующегося вагинальным дисбиозом, четко прописаны в стандартных клинических рекомендациях МЗ РФ [13] и не вызывают каких-либо трудностей у врачей-клиницистов.
Процесс доминирования облигатных и факультативных анаэробных условно-патогенных микроорганизмов над лактобактериями во влагалище представляет огромную проблему для значимой категории пациенток с раком шейки и тела матки в анамнезе.
Согласно отчету GLOBOCAN за 2020 г. [14], рак шейки матки (РШМ) оставался самым распространенным злокачественным новообразованием женских половых органов во всем мире. В большинстве случаев причиной рака шейки матки является инфекция, вызванная вирусом папилломы человека высокого риска [15]. В последние годы было доказано, что изменения состава микрофлоры в кишечнике и влагалище повышают риск развития РШМ за счет воспаления, а также метаболических и иммунных изменений [16, 17], хотя сообщений о взаимосвязи между внутриопухолевой микробиотой и микробиотой других органов и РШМ немного.
Рак эндометрия занимает 6-е место по распространенности среди онкологических заболеваний у женщин и 15-е место по распространенности в мире (в соответствии с данными, представленными Международным фондом исследований рака) [18]. В 2020 г. было зарегистрировано более 417 000 новых случаев рака эндометрия.
Неутешительная статистика по заболеваемости онкологическими заболеваниями женских половых органов делает значимой проблему не только терапии рака органов малого таза, но и заболеваний, возникающих на фоне течения онкологических процессов, ассоциированных с ними и являющихся последствиями химио- и лучевой терапии.
Принимая во внимание фон, при котором развиваются онкологические процессы у женщин (нарушенная микрофлора влагалища с формированием БВ и изменения в кишечном микробиоме), для специалистов практического здравоохранения важно иметь возможность помочь такой категории пациенток.
БВ представляет особую значимость для пациенток, перенесших лечение по поводу рака шейки и тела матки, по следующим причинам.
- Нарушение микробиома. По мнению ряда исследователей, хроническое воспаление, вызванное дисбиозом, может быть фактором риска развития опухолей [19], а противоопухолевое лечение (химио- и лучевая терапия), само по себе значительно нарушает микробиоту влагалища, что впоследствии повышает риск развития БВ [19, 20].
- Иммуносупрессия. Получая противоопухолевое лечение, которое ослабляет иммунную систему, пациентки становятся более уязвимы по отношению к инфекциям, включая и БВ. Представленные в литературе данные свидетельствуют о том, что возможные механизмы канцерогенеза еще до начала лечения, вызывающего иммуносупрессию, включают дисбиоз мочеполового тракта и кишечника, который нарушает физиологический иммунный барьер, формируемый естественной бактериальной флорой и иммунной системой, что приводит к устойчивым воспалительным реакциям и повреждению ДНК [21, 22]. Связь между разнообразием микробиома кишечника, мочевого пузыря и злокачественными новообразованиями неоднозначна. В некоторых случаях у онкологических пациенток наблюдалось повышенное бактериальное разнообразие по сравнению с контрольной группой [22], что отразили Wu P. и соавт. в своей статье.
- Осложнения и рецидивы. Вагинальные инфекции, безусловно, осложняют процесс восстановления после лечения рака и потенциально увеличивают риск рецидива. Существует ряд гипотез, подтверждающих взаимосвязь между воспалительным процессом и канцерогенезом, который существует как до, так и после терапии. Возможным механизмом, ответственным за связь между микробиотой полости матки и раком эндометрия, является взаимодействие бактериальных токсинов с метаболитами, способствующими развитию опухоли, что может привести к хроническому бактериальному воспалению с высвобождением цитокинов [23]. Такие данные продемонстрировала группа ученых под руководством Schwabe R.F. и соавт. Другими авторскими коллективами исследователей была установлена решающая роль воспаления в инициации, развитии и рецидиве злокачественной дегенерации, инвазии и метастазировании различных типов рака, но важность этого процесса для развития и прогрессирования рака эндометрия до сих пор не до конца изучена и требует дальнейших тщательных исследований [24, 25].
- Влияние на качество жизни. Неоспоримый факт, что симптомы БВ негативно влияют на качество жизни пациенток, вызывая дискомфорт и тревогу [26]. К сожалению, в разных странах мира ни одна система здравоохранения обычно не учитывает влияние урогенитальных инфекций и наличие БВ на психическое здоровье. Между тем, нарушения в психоэмоциональной сфере, тем более на фоне перенесенного рака шейки или тела матки, встречаются достаточно часто. Пациентки испытывают стресс, тревожность и различного рода депрессивные состояния. Психические проблемы и страдания женщин после химио- и лучевой терапии могут дать старт или привести к рецидиву БВ и другим неспецифическим генитальным инфекциям [27].
Воздействие химиотерапевтического лечения на микрофлору вагинального тракта. Химиотерапевтическое лечение оказывает системное воздействие на организм, влияя на быстро делящиеся клетки, в том числе и клетки эпителия, выстилающие слизистые оболочки влагалища. Это приводит к нарушению целостности слизистой влагалища и изменению микробиома. Химиотерапевтические препараты вызывают мукозит – воспаление слизистых оболочек, включая вульву и влагалище, создавая благоприятную среду для развития БВ. Возникающий впоследствии процесс иммуносупрессии приводит к снижению уровня лейкоцитов, что ведет к развитию иммунодефицитных состояний, повышая восприимчивость к различным инфекциям, включая бактериальные. Вышеперечисленные патологические изменения, безусловно, меняют pH влагалища: создаются благоприятные условия для нарушений в нормальной микробиоте влагалища [28], что способствует росту условно-патогенных микроорганизмов и снижению числа лактобактерий [4, 7, 9, 22].
Влияние лучевой терапии на микрофлору влагалища. Лучевая терапия также оказывает негативное воздействие на микрофлору, несомненно меняя ее спектр и влияя на выявляемый микробиом вульвы и влагалища, особенно при облучении областей и структур малого таза. Радиационное воздействие вызывает повреждение тканей: в процесс вовлекаются слои эпителиальных клеток слизистой влагалища, что приводит к воспалению и нарушению целостности слизистой. Клинически женщины сталкиваются с проблемой сухости во влагалище по причине снижения выработки слизи. Пациентки испытывают дискомфорт. Изменение видового состава микробиома нарушает баланс микрофлоры влагалища, и при лабораторной диагностике специалисты выявляют признаки БВ и возможных фоновых микст-инфекций [8, 11, 13, 29, 30].
Таким образом, рано или поздно, перенеся лечение по поводу рака шейки или тела матки, пациентки сталкиваются с отдаленными последствиями противоопухолевой терапии, которые могут оказывать долгосрочное негативное влияние на видовой спектр флоры влагалища и вульвы.
Другие негативные эффекты у пациенток после противоопухолевого лечения – почва для развития БВ. Данная категория пациенток сталкивается и с рядом иных отрицательных эффектов после перенесенного противоопухолевого лечения, таких как гормональные изменения: ранняя менопауза, вызванная химиотерапией или хирургическим вмешательством, приводит к снижению уровня эстрогенов и андрогенов, что вызывает истончение слизистой вульвы и влагалища и снижение выработки слизистых выделений. Гормональные изменения, ассоциированные с последствиями терапии рака, оказывают значительное влияние на микробиом влагалища. Снижение уровня эстрогена приводит к уменьшению содержания гликогена в клетках эпителия влагалища, который является питательной средой для лактобацилл. Ятрогенная менопауза – последствие противоопухолевого лечения – усугубляет эти изменения, увеличивая риск развития БВ, и не оставляет шанса на сдвиг микробиологического равновесия влагалища в сторону физиологических значений [31].
На фоне имеющихся хронических воспалительных заболеваний, предшествующих развитию рака, почти у ста процентов женщин возникает длительный хронический воспалительный процесс, способствующий развитию дисбиоза и БВ и препятствующий восстановлению нормальной микрофлоры влагалища.
В клинической практике гинекологи и онкологи сталкиваются с наличием рубцовых изменений слизистой влагалища после хирургического лечения и/или лучевой терапии. Перенесенная операция и лучевое лечение меняют кровоснабжение и трофику тканей влагалища, повреждая защитный иммунный барьер и создавая условия для БВ [31].
Местная иммуносупрессия, вызванная как самой злокачественной опухолью, так и последствиями от ее лечения, играет ключевую роль в развитии БВ [16, 19, 20, 23]. Снижение активности иммунной системы приводит к снижению местного иммунитета: уменьшению количества лейкоцитов и иммунных клеток другого спектра во влагалище, что снижает способность организма к борьбе с патогенной и условно-патогенной флорой. Создается фон повышенной восприимчивости к инфекции: пациентки становятся более уязвимыми к различным патогенам, запускается процесс смещения равновесия между лактобактериями и условно-патогенными бактериями, развивается БВ. Нарушению баланса микрофлоры способствует локальная иммуносупрессия на фоне упомянутой гипоэстрогении ятрогенного характера [17, 20, 23, 25, 32].
Таким образом, факт, что противоопухолевое лечение (химио- и лучевая терапия) приводит к дисбиозу влагалища, нарушая равновесие между нормальной и патогенной микрофлорой, можно считать неоспоримым [23, 25, 28]. Количество и рост лактобацилл, являющихся основными представителями нормальной микрофлоры, подавляется, что приводит к активации роста условно-патогенных микроорганизмов, таких как Gardnerella vaginalis и Fannyhessea vaginae. Данная микрофлора, в свою очередь, и вызывает развитие БВ [2, 7, 9, 11].
Несомненно, большая часть женщин с перенесенным РШМ и раком тела матки, прошедших курсы химио- и лучевой терапии, имеют большой спектр сопутствующих заболеваний: эндокринная (сахарный диабет), кардиологическая, общетерапевтическая патология, заболевания желудочно-кишечного тракта (ЖКТ), которые оказывают негативное влияние на системный иммунитет и вторично – на спектр вагинальной микрофлоры. В ряде клинических случаев пациентки вынуждены получать курсы антибактериальной терапии. Назначаемые антибиотики показаны для лечения других возможных инфекционных процессов и могут также нарушать баланс микробиоты влагалища. Заболевания ЖКТ, возникающие после приема антибактериальных препаратов, способствуют развитию дисбактериоза кишечника и, несомненно, усугубляют ситуацию. Прямая кишка находится в непосредственной близости от входа во влагалище, и бактериальная масса легко проникает из анального отверстия в половые пути. Поэтому из влагалища часто высеваются представители кишечной микрофлоры, такие как кишечная палочка или энтерококк.
Еще один печальный факт – в XXI в. все еще есть женщины, практикующие спринцевания, а также использующие для интимной гигиены агрессивные моющие средства, которые усугубляют дисбиоз.
Таким образом, все вышеперечисленные неблагоприятные эффекты, включая последствия от противоопухолевого лечения, будут культивировать почву для формирования БВ и косвенно ухудшать прогноз основного заболевания.
Вопросы терапии БВ. Возможности применения деквалиния хлорида. Вне сомнений, у врачей практического здравоохранения остро стоит вопрос помощи таким пациенткам. Из протокола клинических рекомендаций по БВ [13] следует, что стандартными методами лечения БВ являются препараты группы нитроимидазола и клиндамицин. Указанные лекарственные препараты могут применяться в различных формах. Схемы стандартной терапии представлены в табл. 1 [33–40].
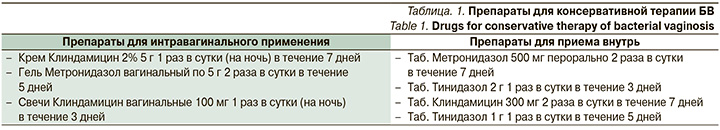
Российские исследователи отмечают, что в 55–90% случаев в течение 1–4 недель возможны рецидивы БВ. Несмотря на стандартные и показавшие свою эффективность схемы терапии, частота рецидивирования БВ остается высокой, достигая 30–70% в течение 6 месяцев [41]. Это связано с несколькими факторами, включая неполное уничтожение патогенных микроорганизмов и недостаточное снижение количества условно-патогенных бактерий, нарушение баланса микрофлоры и резистентность к антибиотикам [42].
Альтернативным вариантом терапии БВ у пациенток с перенесенным противоопухолевым лечением в анамнезе может стать применение антисептика деквалиния хлорида (ЛС Септофемин®), обладающего широким спектром действия и хорошей переносимостью [2, 43–45]. Это четвертичное аммониевое соединение с антисептическими свойствами. Его механизм действия заключается в нарушении целостности клеточной мембраны бактерий, что приводит к их гибели. Деквалиния хлорид обладает широким спектром антимикробной активности, эффективен против бактериального спектра, провоцирующего БВ, а также имеет эффективность против грибковой инфекции влагалища. Таким образом, эффективной альтернативой лечения БВ у таких пациенток является применение деквалиния хлорида [46, 47]. Антимикробная активность деквалиния хлорида представлена в табл. 2 [48].
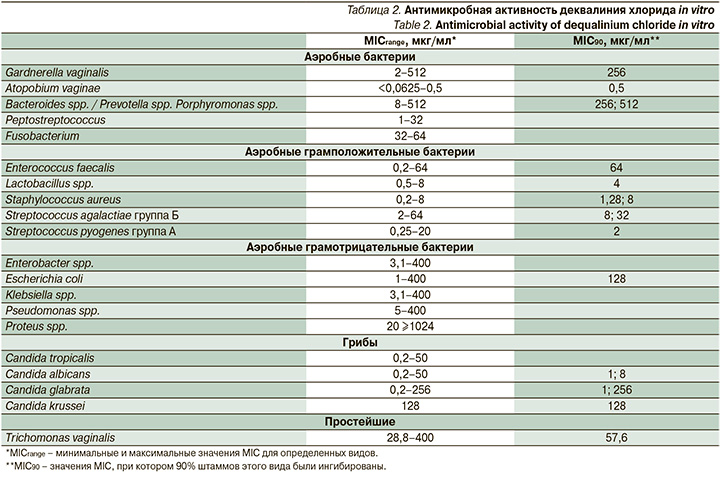
Антимикробная активность широкого спектра, охватывающая все соответствующие возможные патогены вагинальной флоры, и невыраженная системная абсорбция препарата являются основными доводами в пользу предпочтительного применения именно деквалиния хлорида для терапии всего спектра вагинальных инфекций, в той или иной степени встречающихся у пациенток с РШМ и раком тела матки в анамнезе.
Деквалиния хлорид имеет ряд преимуществ по сравнению со стандартными методами лечения. Он назначается в качестве местной санации и применяется в виде вагинальных таблеток, обеспечивает топическое воздействие, минимизируя системное действие и побочные эффекты [45, 46, 48]. Препарат обладает широким спектром активности: эффективен против различных бактерий, способствующих развитию БВ [48], обладает низким риском развития резистентности. Механизм действия деквалиния хлорида делает маловероятным развитие резистентности к препарату [45], учитывая мультифакториальность фармакодинамики данного лекарственного средства [49, 50]. Удобство применения препарата не подлежит сомнению, поэтому в ходе лечения достигается высокий уровень комплаентности. Режим дозирования состоит в применении одной вагинальной таблетки в течение 6 дней [2, 45, 47, 48, 51].
Несмотря на очевидные преимущества, применение деквалиния хлорида имеет и ограничения. Например, возможность развития резистентности: хотя риск ниже, чем у антибиотиков, но такая вероятность существует, особенно у пациенток с перенесенным противоопухолевым лечением в анамнезе, учитывая выраженную как системную, так и местного характера иммуносупрессию. Поэтому для достижения устойчивого результата важен комплексный подход. Целесообразно учитывать сопутствующие факторы и проводить мероприятия по восстановлению нормальной микробиоты влагалища уже после топической санации для достижения оптимального и эффективного результата терапии ВБ.
Учитывая большое разнообразие препаратов на фармакологическом рынке в мире, существует огромный пласт клинических исследований, как случаи case-control с небольшими выборками, так и масштабные рандомизированные исследования. В работе, опубликованной в журнале JAMA Network Open в 2024 г., Raba G. и соавт. [2], описано рандомизированное клиническое исследование, целью которого была сравнительная оценка эффективности деквалиния хлорида и метронидазола в лечении БВ. В исследование были включены женщины в пременопаузе с диагностированным БВ. По результатам исследования деквалиния хлорид был сопоставим по эффективности терапии БВ с метронидазолом. Обозначена высокая приверженность к лечению и среднее время до разрешения симптомов было также сопоставимо в обеих группах. Авторы отмечали хорошую переносимость препарата и единичные побочные эффекты. Поэтому именно деквалиния хлорид может быть приемлемым вариантом для пациенток, которые являются более чувствительными к побочным эффектам вследствие проведенного противоопухолевого лечения. На основании вышеизложенного авторы рекомендуют деквалиния хлорид как перспективную альтернативу метронидазолу и клиндамицину для терапии БВ. Важный факт – деквалиния хлорид может помочь снизить тенденцию к назначению антибактериальных препаратов, что существенно для минимизации риска развития антибиотикорезистентности, особенно у пациенток с онкологическим анамнезом органов малого таза.
Назначение деквалиния хлорида женщинам, перенесшим лечение РШМ и рака тела матки, несомненно имеет определенные преимущества: эффективное лечение БВ; минимизация системного воздействия, учитывая местное применение препарата, что особенно важно для данной категории пациенток; улучшение качества жизни путем устранения клинических симптомов БВ (неприятный запах, выделения), уменьшения тревожности и косвенной нормализации общего психологического состояния.
Безусловно, несмотря на потенциальные преимущества данной лекарственной формы, необходимы дальнейшие исследования для подтверждения эффективности и безопасности деквалиния хлорида у данной категории пациенток. Исследования должны учитывать специфическую выборку пациенток, долгосрочные результаты, влияние на микробиом влагалища, взаимодействие с другими препаратами, которые могут получать пациентки по основному заболеванию и сопутствующим патологиям. Значимый вопрос – определение оптимальной дозы и продолжительность курса лечения для данной группы пациенток.
С целью профилактики БВ у пациенток, перенесших лечение РШМ и рака тела матки, практикующими специалистами должны проводиться беседы информационного характера, включающие вопросы по соблюдению правил личной гигиены (необходимо избегать спринцеваний влагалища и использования агрессивных средств гигиены) [52–54]; поддержанию иммунитета (здоровое питание, физическая активность, по показаниям – иммуностимулирующие препараты); коррекции сопутствующих состояний; ранней диагностике и лечению БВ и других возможных гинекологических проблем; а также о необходимости восстановления микрофлоры влагалища (применение пробиотиков и пребиотиков после лечения БВ по назначению врача) [55]. При наличии симптомов БВ необходимо избегать самолечения и своевременно обращаться к врачу, такая информация важна, и необходимо доносить ее до каждой пациентки.
В настоящее время импортозамещение является одним из главных трендов для отечественной фармакоэкономики. На российском фармацевтическом рынке появился препарат, заслуживающий внимания – Септофемин® (деквалиния хлорид), производимый в России, который будет эффективной заменой существующих импортных вариантов.
Заключение
Противоопухолевая терапия, особенно химиотерапия, оказывает значительное негативное влияние на микробиом влагалища, способствуя развитию БВ в отдаленные сроки у пациенток, перенесших лечение по поводу рака шейки и тела матки. Деквалиния хлорид (ЛС Септофемин®) может рассматриваться как один из вариантов терапии БВ, однако необходимы дальнейшие исследования для оценки его эффективности и безопасности у данной категории пациенток для накопления большего опыта ведения подобных клинических кейсов. Важно подчеркнуть необходимость комплексного подхода к терапии и профилактике БВ у таких женщин, включающего коррекцию сопутствующих факторов, поддержание иммунитета и восстановление нормальной микрофлоры влагалища в обязательном порядке. К сожалению, в настоящее время не накоплена большая доказательная база по терапии БВ у описываемой в данной статье категории пациенток, и это будет большой пласт дальнейшей работы для врачей-исследователей по этому направлению.
Рекомендации
Пациенткам, перенесшим противоопухолевую терапию по поводу рака шейки и тела матки, рекомендуется регулярное наблюдение у гинеколога для ранней диагностики и своевременного лечения БВ. Проводя диагностику БВ, помимо комплексного обследования, включающего бактериоскопию с оценкой флоры и уровня лейкоцитов, будет актуальным провести исследование флороценоза (Фемофлор-16), ПЦР-диагностику половых инфекций, посев выделений из влагалища на чувствительность к антибиотикам.
При назначении терапии БВ следует учитывать анамнез противоопухолевого лечения и индивидуальные особенности конкретной пациентки, а также рассмотреть возможность применения пробиотиков и пребиотиков для восстановления микрофлоры влагалища после лечения БВ, после консультации с врачом. Врачам следует информировать пациенток о риске развития БВ после противоопухолевой терапии и о важности профилактических мероприятий.
Из всего сказанного следует вывод, что применение деквалиния хлорида (ЛС Септофемин®) может быть рассмотрено в качестве одного из вариантов терапии БВ, но оно требует дальнейшего изучения и проведения клинических исследований на большой выборке с различными группами пациенток. Курс ЛС Септофемин® в форме вагинальных таблеток в качестве терапии БВ с широким антимикробным спектром и высоким уровнем переносимости является надежным и рациональным вариантом эмпирической терапии внушительной совокупности известных вагинальных инфекций в ежедневной клинической работе врача гинеколога.



