Введение
Ишемическая болезнь сердца (ИБС) в течение длительного времени остается ведущей проблемой здравоохранения, поскольку этот синдром является одной из основных причин заболеваемости и смертности населения трудоспособного возраста [9].
Хроническая ишемия миокарда индуцирует процессы ремоделирования миокарда левого желудочка (ЛЖ), с течением времени приводя к развитию и усугублению хронической сердечной недостаточности [10].
В процессе ишемического ремоделирования миокарда происходит развитие дисфункции эндотелия интрамиокардиальных сосудов. Активация гуморальных факторов системного воспаления (С-реактивный белок, фибриноген, интерлейкины и др.), нарушение процессов деградации коллагена при эндотелиальной дисфункции (ЭД) способствуют фиброзированию миокарда, увеличению его жесткости и как следствие – развитию диастолической дисфункции и расширению полостей, снижению сократительной способности [5, 6].
Для купирования и профилактики симптомов стенокардии помимо нитратов и их производных, β-адреноблокаторов, блокаторов кальциевых каналов к лечению ИБС могут быть добавлены средства с различным механизмом действия (ивабрадин, триметазидин, ранолазин, никорандил) в качестве препаратов второго ряда в соответствии с частотой сердечных сокращений (ЧСС), артериальным давлением, сопутствующей патологией/толерантностью у определенных пациентов [8].
Препарат группы модуляторов калиевых каналов никорандил обладает двойным механизмом действия благодаря наличию в его структуре активной нитратной группы и остатка амидной части никотиновой кислоты [2]. Вазодилатация запускается высвобождающимся оксидом азота, за которым через накопление внутриклеточного гуанидилмонофосфата следует увеличение продукции эндотелий-зависимого фактора релаксации и расширение крупных коронарных сосудов. Второй механизм, связанный с активацией АТФ-зависимых калиевых каналов, приводит к гиперполяризации мембран, ингибированию притока ионов кальция в клетки гладкой мускулатуры сосудов и последующей периферической вазодилатации (непрямое блокирование кальциевых каналов). Никорандил обеспечивает одновременное снижение пред- и постнагрузки на миокард, но приводит лишь к минимальному влиянию на гемодинамику [1]. В исходе долгосрочной терапии никорандил стабилизировал атеросклеротические бляшки у пациентов со стенокардией, а в исследовании на мышиной модели атеросклероза способствовал уменьшению выраженности маркеров оксидативного стресса и провоспалительных цитокинов [4].
В отличие от β-адреноблокаторов, блокаторов кальциевых каналов и нитратов он также способен влиять на прогноз больных ИБС, уменьшая число сердечно-сосудистых осложнений [3].
Полноценный контроль симптомов стенокардии зачастую требует сочетания нескольких антиангинальных средств. В связи с этим изучение препаратов, которые могут быть использованы и для купирования, и для профилактики ишемии, способные к тому же снижать риск смерти от сердечно-сосудистых заболеваний, представляет особый интерес. Настоящее исследование посвящено оценке антиангинальной, антиишемической эффективности применения активатора калиевых каналов никорандила при долгосрочном приеме пациентов со стабильной стенокардией на фоне стандартной терапии по сравнению со стандартной терапией и пролонгированной формой нитратов, а также исследованию кардиопротективных свойств никорандила.
Материал и методы
В исследование были отобраны 107 пациентов, из которых после скрининга, первичного сбора анамнеза и жалоб в три группы были рандомизированы 93 пациента со стабильной стенокардией II и III функциональных классов (ФК). Средний возраст больных составил 69,9±8,1 года (от 48 до 86 лет), из них 38 мужчин и 55 женщин.
В группу I был рандомизирован 31 человек, в группу II – 30, в группу III – 32 человека. Пациенты всех трех групп получали стандартную терапию ИБС, включившую β-адреноблокаторы в виде бисопролола 5–10 мг/сут, ацетилсалициловую кислоту (аспирин), антагонисты рецепторов ангиотензина II (АРА II) в виде валсартана 40–160 мг/сут и розувастатин в дозе 10 мг/сут с коррекцией дозы от 5 до 20 мг/сут через 6 и 12 недель терапии.
Больные группы I принимали бисопролол, аспирин, валсартан и розувастатин, а для купирования приступов стенокардии пользовались таблетками нитроглицерина. Пациенты группы II в дополнение к стандартной терапии получали препарат группы пролонгированных нитратов – изосорбида динитрат в дозе 20–40 мг 2 раза в сутки. К основной терапии пациентам группы III был добавлен никорандил в дозе 20–40 мг 2 раза в сутки.
Пациенты должны были соответствовать следующим критериям: длительности стенокардии напряжения более 3 месяцев до включения в исследование, клинической стабильностью, строгому соблюдению режима терапии, подтвержденному диагнозу ИБС (на основании данных тестов с физической нагрузкой, наличия перенесенного инфаркта миокарда давностью более 6 месяцев и проведенной реваскуляризации, наличия клинических проявлений коронарной недостаточности). Критерием исключения во всех группах стало наличие сопутствующих хронических заболеваний в стадии обострения, инфекционной патологии, нестабильной стенокардии, фибрилляции предсердий, острого инфаркта или инсульта, непереносимость любого из шести препаратов, включенных в исследование.
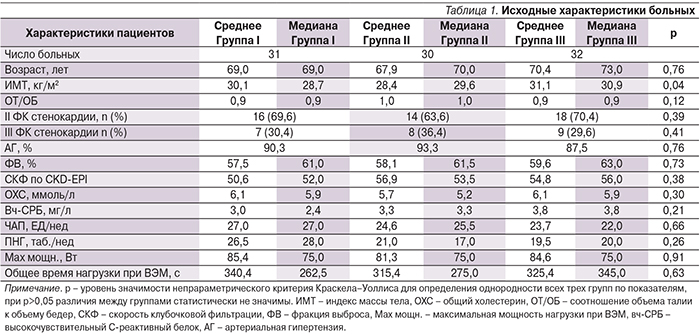
По основным антропометрическим, возрастным и клиническим критериям группы были сбалансированы (табл. 1).
В ходе исследования регистрировались «конечные точки», включавшие эпизоды нестабильной стенокардии, первичные и повторные ИМ, смерть от сердечно-сосудистых заболеваний. Общая продолжительность исследования составила 24 недели.
Для выявления отличия между группами по совокупности количественных показателей был использован дискриминантный анализ и применен метод последовательного исключения переменных (показателей) из модели. Статистика лямбда Уилкса (λ) нашего анализа, являющаяся основным показателем адекватности модели дискриминации, составила 0,658. Полученный результат свидетельствовал в пользу однородности групп (p<0,0001).
Исследование пациентов включило проведение Эхо-КГ с определением параметров ремоделирования сердца и оценкой диастолической дисфункции левого желудочка (ЛЖ); Холтеровское мониторирование электрокардиограммы (ХМ ЭКГ) с определением числа эпизодов ишемии миокарда (ЧЭИМ), продолжительности суточной ишемии миокарда (ПСИМ), ЧСС, средней глубины смещения сегмента ST (СМГИС); велоэргометрии (ВЭМ, определение максимальной мощности нагрузки и общего времени нагрузки), а также определение уровней Вч-СРБ, фибриногена, показателей липидного спектра – общего холестерина (ОХС), липопротеидов низкой плотности (ЛПНП), триглицеридов (ТГ) до и после 24 недель лечения.
Статистическая обработка материала проведена с помощью пакета прикладных программ Statistica 10.1 Windows, StatSoft, Inc. с использованием параметрических и непараметрических методов (однофакторного дисперсионного анализа, критериев Краскера–Уоллиса, критериев знаков и Вилкоксона, коэффициенты корреляции Пирсона и Спирмена, дискриминантного анализа степени однородности). Статистически значимыми считали результаты при р<0,05.
Результаты исследования и обсуждение
За 24 недели наблюдения летальные исходы среди больных отсутствовали. Значимое улучшение клинического состояния на фоне рекомендованной терапии было отмечено у пациентов всех трех групп: наблюдалось сопоставимое улучшение самочувствия, уменьшение числа и интенсивности приступов ангинозных болей, потребности в нитроглицерине, повышение работоспособности.
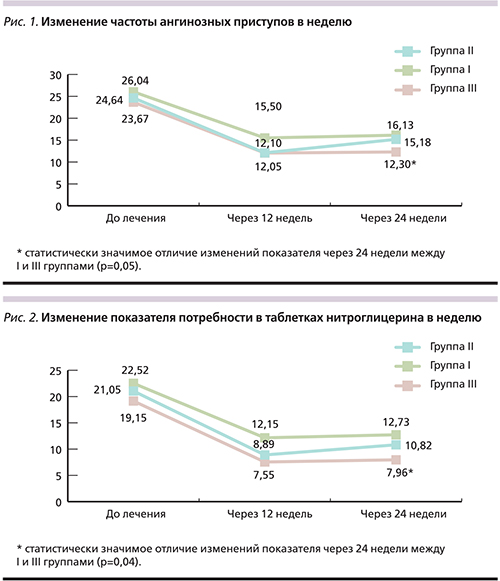
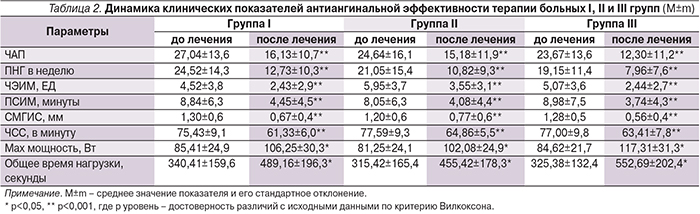
Через 12 недель в трех группах исследования было отмечено значительное снижение средней частоты ангинозных приступов в неделю (ЧАП) и потребности в приеме нитроглицерина (ПНГ): ЧАП снизилась в группе I с 26,04±13,6 до 15,5±7,1 (на 48,8%, p<0,001), в группе II – с 24,64±16,1 до 12,1±8,1 (на 61,1%, p<0,001), в группе III – с 23,67±13,6 до 11,85±5,8 (на 60,9%, p<0,001). ПНГ за 3 месяца терапии уменьшилась в группе I с 22,52±16,6 до 12,15±7,1 (на -50,91%, p<0,001), в группе II – с 21,05±15,5 до 8,89±5,1 (на 68,3%, p<0,001), в группе III – с 19,15±10,9 до 7,55±4,2 (на 70,4%, p<0,001). По прошествии еще 12 недель (рис. 1, 2) клинические показатели несколько изменились по сравнению с промежуточными данными: через 24 недели ЧАП группы I составила 16,13±10,7 (-45,73% по сравнению с исходными данными, р<0,001), в группе II – 15,18±11,9 -47,95%, р<0,001), в группе III – 12,30±11,2 (-59,45%, р<0,001). Также по показателю потребности в нитроглицерине через 24 недели в группе I наблюдали результат 12,73±10,3 (-50,77% по сравнению с исходными данными, р<0,001), в группе II – 10,82±9,3(-54,61%, р<0,001), в группе III – 7,96±7,6 (-69,04%, р<0,001). По данным однофакторного дисперсионного анализа, в группе III (с никорандилом) удалось достичь достоверно значимой разницы клинических показателей ЧАП и ПНГ по сравнению с группой пациентов, получавших только стандартную терапию (р=0,05 и 0,04 соответственно). Эффективность β-адреноблокатора в сочетании с пролонгированным нитратом была сравнимой и статистически не отличалась от таковой приема никорандила в комплексе со стандартной терапией. Однако при регулярном приеме изосорбида динитрата в течение 6 месяцев 4 (13,3%) больных группы II прекратили прием препарата из-за развития головной боли, а по антиангинальной эффективности показатели группы II практически сравнялись с таковыми группы I, из чего можно сделать выводы о возможной резвившейся потери эффективности изосорбида динитрата для части больных стабильной стенокардией.
По данным ХМ ЭКГ, в конце периода наблюдения (табл. 2) у пациентов I, II и III групп отмечено сопоставимо достоверное снижение среднесуточной ЧСС, ЧЭИМ, ПСИМ и глубины ишемического смещения сегмента ST (ГИС ST). Необходимо отметить более выраженное снижение ПСИМ и ГИС ST у пациентов, принимавших никорандил, которое, по данным однофакторного дисперсионного анализа, достигло значимой разницы по сравнению со стандартной терапией по показателю ПСИМ (-50,82% и -68,17%, р=0,026) и по сравнению с группой пролонгированных нитратов по показателю СМГИС (-35,00% и -59,26%, р=0,0259).
Аналогичная динамика сохранилась и при проведении нагрузочных проб. Показатели ВЭМ: максимальная мощность нагрузки (Max мощн.) и общее время нагрузки до возникновения клинических и ЭКГ-признаков ишемии миокарда достоверно значимо увеличились к концу 24-й недели терапии во всех трех группах. При сравнении групп увеличение физической работоспособности пациентов было более выражено у пациентов группы III по сравнению с группой I (ΔMax мощн. – 40,25 против 24,86% при р=0,05, ΔОбщее время нагрузки – 74,57 против 48,14% при р=0,02), между II и III группами достоверность различий не была достигнута.
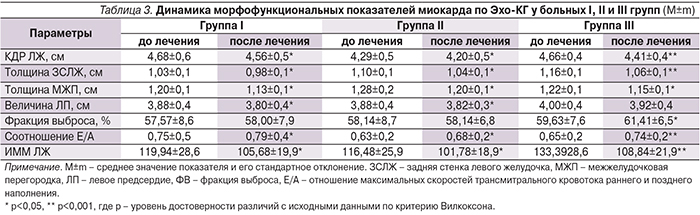
Через 24 недели наблюдения, по данным Эхо-КГ, у больных трех групп было отмечено достоверное снижение индекса массы миокарда ЛЖ (ИММЛЖ), конечно-диастолического размера ЛЖ (КДРЛЖ), увеличение показателя диастолического кровенаполнения (Е/А), а также тенденция к возрастанию фракции выброса ЛЖ (табл. 3). Изменения показателей в процессе лечения группы никорандила превосходили таковые по сравнению с остальными группами, однако в связи с большой дисперсией в группах и относительно небольшим числом пациентов в выборке значимость различий была достигнута только по показателю КДРЛЖ (р1-3=0,0017 и р2-3=0,051) и ИММЛЖ (р1-3=0,044). Динамика основных морфофункциональных показателей миокарда ЛЖ по Эхо-КГ у пациентов III группы по сравнению с двумя другими группами говорит о дополняющем влиянии никорандила на процессы улучшения адаптации кардиомиоцитов в условиях хронической ишемии, проявляющемся в уменьшении размеров дилатированных полостей и гипертрофированных стенок, уменьшении выраженности диастолической дисфункции и как следствие – замедлении ремоделирования миокарда.
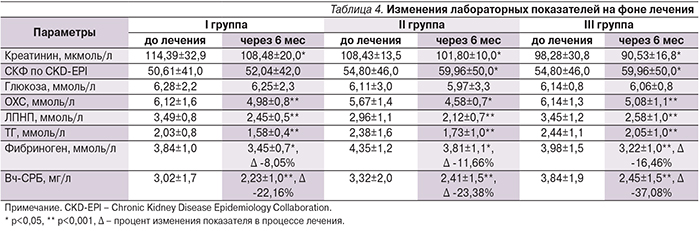
Необходимо указать, что длительная терапия препаратами всех трех групп не приводила к негативным изменениям лабораторных показателей (табл. 4).
Наблюдалось статистически достоверное снижение всех показателей липидного спектра (ОХС, ЛПНП, ТГ) без значимых различий между группами. Данный результат был обеспечен в значительной мере гиполипидемическим действием розувастатина, обладающего также рядом плейотропных эффектов [7], таких как снижение выраженности свободно-радикального окисления, ЭД, воспалительные процессы стенки сосудов. Эти «нелипидные» свойства сыграли свою роль в процессе снижения показателей Вч-СРБ и фибриногена, отражающих процессы хронического системного воспаления, сопровождающего ИБС. Однако в группе никорандила уровень фибриногена снизился более чем в 2 раза по сравнению с показателями группы стандартной терапии (-8,05% и -16,46%, р=0,042), а концентрация Вч-СРБ значимо снизилась в группе III по сравнению как с таковой в группе I (-37,08% и -22,16%, р=0,003), так и в группе II (-37,08% и -23,38%, р=0,04), что может являться подтверждением его положительного влияния на процессы редуцирования оксидативного повреждения и системного воспаления.
Выводы
Полученные нами данные свидетельствуют о высокой антиангинальной и антиишемической активности никорандила у пациентов со стабильной стенокардией. Частота ангинозных приступов, продолжительность суточной ишемии миокарда, по данным ХМ ЭКГ, максимальная мощность и общее время нагрузки при выполнении ВЭМ достоверно более значимо улучшились в группе III с добавлением никорандила по сравнению с группой I, получавшей только бисопролол, аспирин и статины (стандартную терапию), и были сопоставимыми с показателями группы II (с добавлением изосорбида динитрата). Прием никорандила не оказал влияния на липидный спектр и уровень глюкозы крови, но уменьшил концентрацию Вч-СРБ и фибриногена. Кроме того, в группе III по сравнению с остальными группами, по данным ЭХО-КГ, произошло более выраженное уменьшение размеров и толщины стенок ЛЖ, увеличение показателя диастолического кровенаполнения ЛЖ, отражающих выраженность ремоделирования миокарда и диастолической дисфункции.
Таким образом, сочетая свойства агониста АТФзависимымых калиевых каналов и нитратоподобное вазодилатирующее действие, активируя процессы ишемического прекондиционирования, никорандил способен значимо снижать частоту и выраженность болевой и безболевой ишемии миокарда, потребность в нитропрепаратах, обладающих рядом побочных эффектов, которые ограничивают их прием. Стимуляция никорандилом адаптационных процессов в клетках миокарда и эндотелии, уменьшение активности провоспалительных маркеров приводят к замедлению процессов ремоделирования миокарда, обеспечивая долгосрочную кардиопротекцию.



