Актуальность
Акне – одно из наиболее часто встречающихся заболеваний кожи. По статистике, пораженность данным дерматозом составляет 65,0–93,3% молодых людей и подростков, в среднем – 85,0%, что занимает 12,0% амбулаторного приема дерматологов. За последние годы наблюдается тенденция персистенции или позднего начала заболевания более чем у 50% пациентов. В свете рассмотрения акне как хронического рецидивирующего дерматоза, дебютирующего в подростковом возрасте или позже, подход к лечению взрослых женщин должен быть комплексным [1–3].
Согласно последним рекомендациям Глобального альянса по лечению пациентов с акне и Европейского дерматологического сообщества, при легком, среднетяжелом и тяжелом течении папулопустулезных акне второй линией выбора в сочетании с топической терапией помимо оральных антиандрогенов применяют комбинированные оральные контрацептивы (КОК).
Для женщин они служат альтернативой приему системных ретиноидов. При нодулокистозных акне КОК могут применяться как в виде монотерапии, так и в комбинации с оральными антиандогенами, антибактериальными препаратами либо системными ретиноидами [4–5].
Целесообразность назначения гормональной терапии обусловлена ключевым значением половых стероидов в патогенезе акне. Количество и чувствительность сальных желез к гормонам у женщин можно скорректировать. С целью минимизации дозозависимых побочных эффектов антиандрогенов наиболее оптимальным являются их фиксированные комбинации в форме КОК, содержащих этинилэстрадиол (ЭЭ) и различные гестагены. Препараты, включающие ципротерона ацетат (ЦПА), являются более результативными по сравнению с другими прогестинами, однако могут способствовать увеличению массы тела, задержке жидкости, снижению настроения.
Это в свою очередь снижает приверженность терапии и может усугубить психосоциальную дезадаптацию пациенток. Хлормадинона ацетат (ХМА) по эффективности сопоставим с ЦПА, но не обладает вышеперечисленными побочными эффектами. При сравнении КОК, содержащих фиксированные дозы ЦПА и ХМА, и препарата Белара, следует отметить, что последний в 4,5 раза безопаснее по риску развития тромбозов [6–7].

В ФГБУ «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» Минздрава РФ в 2014 г. проведено открытое сравнительное рандомизированное контролируемое исследование эффективности и безопасности применения препарата Белара (ЭЭ+ХМА; Гедеон Рихтер, Венгрия) в сочетании с традиционной топической терапией женщин с папулопустулезной формой акне средней степени тяжести.
Целью исследования стало оценить клиническую эффективность и безопасность терапии препаратом Белара в составе комплексной терапии пациентов, страдающих папулопустулезной формой акне средней степени тяжести по сравнению со стандартным топическим лечением.
Материал и методы
В исследование были включены 40 пациенток, рандомизированных в 2 группы – 1-ю (основную, n=20) и 2-ю (сравнения, n=20). Группы больных формировались параллельно в соотношении 1:1; рандомизированный список был составлен координатором исследования (методом случайных чисел).
Критерии включения: женщины в возрасте 25–39 лет включительно, находящиеся на амбулаторном лечении с клинически установленным диагнозом акне, папулопустулезная форма средней степени тяжести (характерная картина при визуальном осмотре); подписание информированного согласия на участие в исследовании; строгое соблюдение указаний врача относительно применения назначенных препаратов.
Критерии исключения: индивидуальная непереносимость препарата Белара в таблетках и/или компонентов топической терапии; применение КОК и/или топических ретиноидов, в т.ч. препаратов адапалена менее чем за 3 месяца до включения в исследование; беременность и лактация; прием препаратов, способных влиять на результаты исследования (антибактериальные, системные ретиноиды и другие лекарственные препараты системного действия); ВИЧ-инфекция, вирусные гепатиты В и С, онкологические заболевания, в т.ч. в анамнезе, наркомания, алкоголизм, никотиновая зависимость, варикозная болезнь, предрасположенность к тромбозам и тромбообразованию, в т.ч. у родственников 1-й линии родства, дислипопротеинемия, артериальная гипертензия, заболевания печени, мигрень; отсутствие готовности к сотрудничеству со стороны пациента.

Во 2-й группе из исследования выбыла 1 (2,5%) пациентка в связи с непереносимостью топической терапии адапаленом: постоянно рецидивирующими проявлениями тяжелого течения ретиноидного дерматита. Никто из пациенток 1-й группы не был исключен из исследования в соответствии с критериями, утвержденными в программе исследования.
Пациенткам 1-й группы (n=20) врач-гинеколог после предварительной консультации назначил препарат Белара: циклически по схеме по 1 таблетке в сутки в течение 21 дня и последующим перерывом 7 дней. Белара-КОК, содержащий ЭЭ 0,03 мг и ХМА 2,0 мг, с антиандрогенными свойствами. Одновременно проведена топическая терапия препаратом, содержащим адапален+клиндамицин (Клензит С), в сочетании с увлажняющим средством и пенкой для умывания Сетафил дермаконтрол (1 месяц) и дальнейшим переходом на Клензит в сочетании с бензоила пероксидом (Базирон АС 5%). Пациенткам 2-й группы (n=19) для лечения акне назначена исключительно вышеуказанная топическая терапия.
До начала терапии каждой пациентке было проведено исследование показателей общего и биохимического анализов крови, уровней гормонов (пролактин, общий тестостерон, дегидроэпиандростерон-сульфат – ДГЭА, тиреотропный гормон – ТТГ), ультразвуковое исследование органов малого таза, щитовидной железы.
Клиническое обследование пациенток включало сбор жалоб, анализ анамнеза, объективное исследование, включающее подсчет индекса общей тяжести угрей (ОТУ) до и после терапии.
Для оценки влияния препарата Белара на дермоэпидермальные структуры кожи проведено ультрасонографическое исследование кожи сканером DUB-USB производства Taberna Pro Medicum (Германия) с датчиком 75 МГц и конфокальная лазерная микроскопия на аппарате Vivascope 1500 Multilaser (Lucid-Tech. Inc., Henrietta, NY; Mavig GmbH Munich, Germany). Стандартной была выбрана точка Макгрегора слева, которая находится на месте пересечения линии, соединяющей крыло носа и козелок уха, и линией, соединяющей латеральный угол глаза и угол рта. Для оценки функционального состояния кожи всем пациенткам до и после терапии проведена себу-, корнео-, вапо- и мексаметрия на аппарате Courage and Khazaka Electronic GmbH (страна производитель – Германия) в контрольных точках измерений при стандартизированных показателях увлажненности воздуха в помещении.
Статистический анализ данных показал ненормальный характер распределения генеральной совокупности, что обусловило применение непараметрических методов статистики. Результаты были представлены в виде среднего и ошибки среднего (M±m) или медианы и межквартильного интервала Ме (МКИ 25,0%; 75,0%). Для сравнения количественных и порядковых данных внутри группы до и после лечения использован парный критерий Вилкоксона, для сравнения независимых выборок – критерий Манна–Уитни. Для всех статистических критериев ошибка первого рода установлена равной 0,05. Нулевая гипотеза (отсутствие различий) отвергалась, если вероятность (p) не превышала ошибку первого рода.
Результаты исследования и обсуждение
В исследование вошли 39 женщин, возраст которых составил в 1-й группе 31 год (МКИ 28,8; 33,3), во 2-й – 30 лет (МКИ 27,0; 32,0). Возраст начала заболевания составил 16 лет (МКИ 14,0; 20,0), при этом статистически значимой разницы между группами не выявлено (p>0,05). У 25 (64,1%) женщин он составил 14 лет (МКИ 13,3; 15,0) и соответствовал персистенции высыпаний. У 14 (35,9 %) женщин выявлено позднее начало акне в 20,5 лет (МКИ 19,0; 24,0). В выборке в целом длительность течения дерматоза составила 10,1 года (МКИ 5,2; 16,0).
Ранее чем за 3 месяца до начала исследования пациентки получали в качестве терапии акне топические антибактериальные препараты (83,1% всех больных), препараты салициловой кислоты (53,8%), азелаиновой кислоты (51,3%), КОК (28,8% женщин). Топические ретиноиды как препараты первого выбора ранее назначались пациенткам, включенным в исследование, лишь в 28,2% случаев. Из процедур косметологического профиля пациенткам назначали механическую комедоэкстракцию (66,7%), токи Д’Арсонваля (25,6%), поверхностные пилинги фруктовыми кислотами (53,8%). Данная терапия приносила лишь временное улучшение в отношении динамики воспалительных и невоспалительных акне. Процесс носил постоянно рецидивирующее течение у всех пациенток.
У родственников 1-й линии родства 32 (82,1%) пациенток выявлено наличие акне. При этом рубцевание у них наблюдалось в 46,9% случаев.
Согласно данным лабораторного исследования, значимых отклонений показателей биохимического и общего анализов крови, свидетельствующих о выраженных изменениях функции печени и нарушении липидного обмена, в обеих группах не выявлено.

У пяти пациенток 1-й и четырех больных 2-й группы до начала терапии выявлено повышение уровня ДГЭА на 12,1 (МКИ 5,6; 13,1) и 5,2 (МКИ 3,1; 10,2) мкг/дл соответственно. Уровень общего тестостерона был повышен лишь у 1 пациентки 1-й группы на 3,1 нг/дл. Уровень ТТГ у всех пациенток не выходил за пределы референсных значений. Ультразвуковых признаков, которые являлись бы противопоказанием к назначению врачами-гинекологами КОК Белара, выявлено не было.
Жалобы пациенток обеих групп до начала терапии были сопоставимыми и выражались в наличии множественных воспалительных элементов, комедонов, неровности цвета кожи лица у 100,0% респондентов. Выраженная жирность кожи беспокоила часть пациенток (65,0 и 73,7% в 1-й и 2-й группах соответственно). Наиболее полный субъективно оцениваемый регресс воспалительных и невоспалительных элементов наблюдался в 1-й группе, где в комплексную терапию входил пероральный прием препарата Белара. Большинство женщин отметили наступление полной ремиссии акне (80,0%), лишь 2 (10,0%) пациенток беспокоило незначительное количество комедонов. Во 2-й группе после лечения у 1 (5,3%) пациентки сохранялись жалобы на множественные воспалительные элементы, 13 (68,4%) указали на их единичный характер и лишь 5 (26,3%) отметили полную ремиссию, при этом комедоны беспокоили 6 (31,6%) пациенток. Также в 1-й группе число пациенток с избыточной жирностью кожи лица значительно уменьшилось: с 13 (65,0%) до 1 (5,0%). Во 2-й группе эти показатели составили 14 (73,7%) и 8 (42,1%) женщин соответственно. Улучшение тона кожи в большей степени было отмечено пациентками 1-й группы: на 70,0 против 36,4% во 2-й группе.
При оценке клинической эффективности терапии проведен количественный подсчет воспалительных и невоспалительных элементов с определением индекса ОТУ (табл. 1).
До начала терапии индекс ОТУ был сопоставим в обеих группах (р>0,05). В конце лечения регресс клинической картины в 1-й группе на фоне приема препарата Белара составил 79,8% (МКИ 74,2%; 91,0%), во 2-й – 49,3% (МКИ 38,8%; 60,1%), что служит статистически значимым отличием в динамике терапии, а также при оценке показателя между группами после лечения (р<0,05).
При оценке функциональных показателей эффективности комбинированной терапии с использованием Белары и топического лечения установлено, что исходная жирность кожи в 1-й и 2-й группах была сопоставимой (p>0,05) и находилась в пределах рекомендованных удовлетворительных значений (табл. 2).
Для 2-й группы через 6 месяцев терапии не было выявлено значимой разницы в показателях себуметрии по сравнению с исходными данными. Включение Белары в комплексную терапию в течение 6 циклов привело к значимому снижению жирности кожи лица пациенток 1-й группы до оптимальных значений в целом на 42,3% (р<0,05) – с 40,7 до 21,7 у.е.

Исходные показатели корнеометрии кожи пациенток с папулопустулезной формой акне были сопоставимыми в обеих группах и соответствовали удовлетворительному уровню увлажненности (31,2±4,4 и 35,4±6,7 у.е.). В 1-й группе после терапии статистически значимое увеличение увлажненности кожи наблюдалось в среднем на 33,0±6,2% (p между группами <0,05). Показатели корнеометрии во 2-й группе не изменились.
Показатели вапометрии между группами до начала курса терапии были статистически неразличимы и составили 5,8±2,7 и 4,6±1,1 у.е., что соответствовало оптимальному рекомендованному уровню. Динамика показателей трансэпидермальной потери влаги на фоне проводимого лечения в 1-й и 2-й группах не показала статистически значимых изменений, что, возможно, связано с применением топического ретиноида в течение последних 3 месяцев в поддерживающем режиме терапии, а также с адекватной терапией сопровождения (p между группами > 0,05).
По данным мексаметрии, индексы меланина (IM) и эритемы (IE) в группах до начала лечения не различались. В динамике на фоне комплексной терапии с пероральным приемом препарата Белара в 1-й группе произошло статистически значимое снижение IM на 34,9±5,1% – с 20,3±4,2 до 13,1±2,1 у.е., что можно объяснить более быстрым регрессом воспалительных элементов и меньшим риском формирования поствоспалительной гиперпигментации. Отсутствие динамики IE, несмотря на регресс большинства воспалительных элементов, возможно, связано с часто наблюдаемой легкой гиперемией кожи лица, характерной для топического нанесения ретиноидов. Разницы между группами в динамике показателей IM и IE не выявлено (р>0,05).
В ходе ультрасонографического исследования кожи оценивали толщину и акустическую плотность эпидермиса (табл. 3). Толщина эпидермиса была сопоставимой в обеих группах и менялась в ходе терапии незначительно (р>0,05).
Акустическая плотность эпидермиса после курса лечения имела тенденцию к увеличению, особенно в 1-й группе, где изменение было статистически значимо и составило 27,2% (МКИ 19,1%; 33,5%) (р<0,05).
Акустическая плотность верхних слоев дермы в 1-й группе значимо увеличилась на 59,5% (МКИ 22,3; 34,1%) – с 18,5 (МКИ 12,3; 21,4) до 29,5 у.е. (МКИ 22,3; 34,1) (р<0,05) (табл. 4). Данное изменение было существенно выше показателей контрольной группы (р между группами <0,05), где динамика составила 24,4% (МКИ 15,2; 29,5) – показатель колебался от 20,5 (МКИ 13,2; 24,6) до 25,5 у.е. (МКИ 19,1; 28,7) (р>0,05).
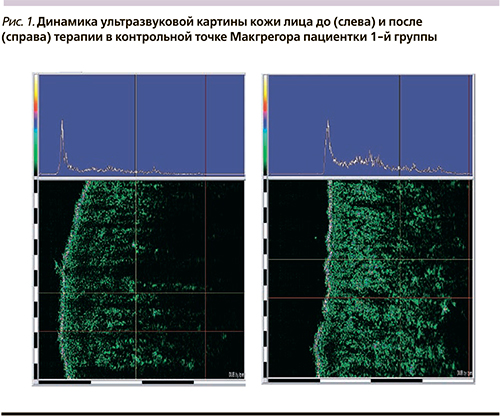
Ультрасонографическая картина кожи лица после лечения характеризовалась большей яркостью, четкостью и глубиной проникновения ультразвукового сигнала (рис. 1). Данные изменения были более выражены в 1-й группе пациенток, принимавших препарат Белара. Косвенно это свидетельствует в пользу структуризации белковых структур эпидермиса и процессов неоколлагеногенеза и улучшения качества каркасной матрицы преимущественно в верхних слоях ретикулярной дермы, что может быть обусловлено влиянием ЭЭ и гестагена ХМА на пластические процессы в коже за счет влияния на скорость и активность пролиферации фибробластов, усиления регенераторных процессов, подавления матриксных металлопротеиназ [8–9].
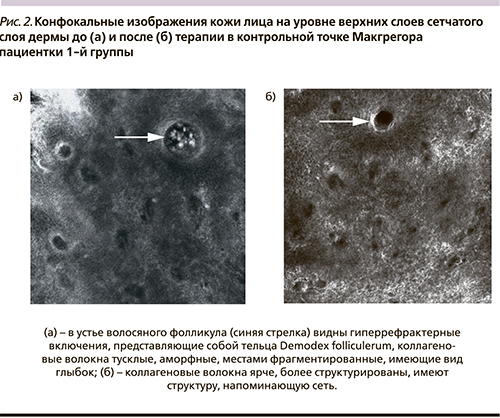
При проведении конфокальной микроскопии в 1-й группе на фоне приема препарата Белара было выявлено статистически значимое уменьшение диаметра просвета волосяного фолликула на 19,0% (МКИ 0; 50,0). В обеих группах отмечено уменьшение количества особей Demodex folliculerum: на 86,7% (МКИ 52,3; 94,7) и 84,3% (МКИ 35,3; 92,1) в 1-й и 2-й группах соответственно (p между группами >0,05). В 1-й группе также отмечена более яркая и равномерная структура коллагена, улучшение кровообращения в сосочках дермы (табл. 5, рис. 2).
Таким образом, сравнительный клинико-инструментальный анализ эффективности лечения показал, что терапия папулопустулезных акне у женщин с использованием только топической терапии привела к снижению индекса ОТУ лишь на 49,3% (МКИ 38,8; 60,1), а включение в комплекс лечения препарата Белара позволило добиться выраженного клинического эффекта со снижением индекса ОТУ на 79,8% (МКИ 74,2; 91,0). Кроме этого препарат Белара положительно повлиял на структуризацию белковых структур эпидермиса и дермы, способствуя увеличению и улучшению качества коллагеновых фибрилл, улучшению микроциркуляции папиллярной дермы, тем самым предупреждая и уменьшая первые признаки инволютивных изменений кожи.
Выводы
- Включение в комплексную терапию пациенток с папулопустулезной формой акне препарата Белара в сочетании с топической терапией позволяет добиваться высокой клинической эффективности для 90,0% пациентов, что подтверждается не только полным регрессом симптоматики у 80,0% больных, но и результатами объективных инструментальных методов диагностики – себу-, корнео-, вапо- и мексаметрии, ультрасонографического исследования и конфокальной лазерной микроскопии.
- Согласно данным функциональной диагностики, включение препарата Белара в комплексную терапию акне у взрослых женщин позволяет снижать жирность кожи на 42,3%, способствует увеличению показателя увлажненности на 33,0% (до оптимальных значений). Данный аспект не только позволяет нивелировать побочные эффекты топической терапии, но и способствует улучшению изначальных функциональных показателей кожи, способствуя нормализации водно-липидного баланса, что в свою очередь приводит к улучшению качества и эстетической привлекательности кожи и повышению приверженности пациенток данному виду комплексной терапии.
- По данным инструментальных методов исследования, препарат Белара влияет на количественное и качественное улучшение коллагенового каркаса дермы за счет сочетанного воздействия эстрогена (ЭЭ) и гестагена (ХМА): способствует увеличению и улучшению качества коллагеновых фибрилл, усиливает микроциркуляцию поверхностной сосудистой сети, тем самым улучшая регенерацию и влияя на процессы хроностарения кожи.
- Полученные данные о высокой эффективности и удовлетворенности пациенток результатами лечения, подтвержденные данными проведенного исследования, позволяют рекомендовать включение в комплексную терапию больных папулопустулезной формой акне средней степени тяжести препарат Белара одновременно с проведением топической терапии первого выбора.
- Полученные результаты предполагают рассмотрение препарат Белара не только как эффективный КОК, но и как действенный и безопасный компонент в комплексной терапии больных папулопустулезной формой акне средней степени тяжести, обладающий себорегулирующей, антикомедоногенной активностью, улучшающий морфофункциональные показатели эпидермиса и дермы, а также позволяющий достигаь лучших клинических результатов по сравнению с топическим лечением, и рекомендовать его широкое внедрение в практику дерматовенерологов и гинекологов.



