Начиная с 1940 г. внедрение в практику антимикробных препаратов привело к увеличению средней продолжительности жизни, принципиально изменив отношение к инфекционным болезням. На сегодняшний день сложно представить систему здравоохранения без доступных и эффективных антимикробных препаратов.
Рождение антимикробной химиотерапии принято связывать с созданием Паулем Эрлихом препарата сальварсан (1909 г.), успешно применявшегося для лечения сифилиса. Следующим важным шагом в развитии химиотерапии было открытие первого сульфаниламида пронтозила (Gerhard Domagk, 1932). В 1927 г. (за год до случайного открытия Флемингом пенициллина) Rene Dubos начал целенаправленный поиск почвенных микробов, способных разрушать полисахаридную капсулу пневмококков. В 1939 г. поиск увенчался открытием антибиотика грамицидина, оказавшегося токсичным при внутривенном введении, но долгие годы применявшегося как местный препарат.
Однако настоящий расцвет антимикробной химиотерапии, конечно же, связан с открытием первого β-лактамного антибиотика пенициллина. Для превращения некой субстанции «пенициллин», открытой Флемингом в 1928 г., в лекарственный препарат массового применения потребовалось 15 лет напряженного труда десятков, если не сотен, микробиологов и химиков, лишь двое из которых – Howard Florey и Ernst Chain – были удостоены в 1945 г. наряду непосредственно с Флемингом Нобелевской премии.
За пенициллином последовал ряд других β-лактамов, многие из которых полностью утратили клиническое значение и забыты из-за снижения эффективности, вызванного формированием бактериями резистентности. Всего в разных странах применялось или применяется более 100 β-лактамных антибиотиков, их классификация основана на химической структуре и спектре антимикробной активности [1].
В целом β-лактамы до сих пор не утратили своего лидирующего положения, на их долю приходится до 60% от всего объема антибиотиков, потребляемых в мире. История взаимоотношений β-лактамов и бактерий – наиболее яркий пример возможностей направленной химической модификации по получению новых β-лактамных структур с заданными свойствами, а также способности бактерий к использованию различных механизмов для быстрого формирования устойчивости к новым соединениям.
Механизмы антимикробной резистентности
Все разнообразие механизмов формирования антимикробной резистентности возможно объединить в несколько принципиальных направлений:
1. Модификация мишени. В случае с β-лактамным антибиотиком конкретный механизм устойчивости заключается в изменении структуры мишеней действия антибиотиков – пенициллинсвязывающих белков (ПСБ). Это в свою очередь приводит к уменьшению аффинности (родства) между ПСБ и молекулой антибиотика и как следствие – к увеличению значений минимальных подавляющих концентраций (МПК) антибиотиков. Возможно также приобретение бактериями новых для них низкоаффинных ПСБ. Устойчивость к β-лактамам, связанная с модификацией ПСБ, наиболее распространена среди грамположительных бактерий (Streptococcus spp. и Staphylococcus spp.) [2], среди грамотрицательных бактерий этот механизм встречается у Neisseria gonorrhoeae и Haemophilus spp.
2. Снижение проницаемости внешних структур. В случае грамотрицательных бактерий, для того чтобы добраться до своей мишени, молекула β-лактамного антибиотика должна преодолеть внешнюю мембрану – структуру, практически непроницаемую для водорастворимых соединений. В норме β-лактамы проникают внутрь грамотрицательных бактерий через пориновые каналы, формируемые пориновыми белками или поринами внешней мембраны (outer membrane porins – OMP). Модификация, снижение экспрессии или полная утрата ОМР приводят к увеличению МПК. Потерю OMP наблюдают у энтеробактерий, Pseudomonas aeruginosa и Acinetobacter baumannii [3, 4]. Но даже полная потеря поринов не всегда приводит к формированию резистентного фенотипа, в большинстве случаев это достигается при комбинации с увеличением экспрессии β-лактамаз [5].
3. Активное выведение (эффлюкс). Механизм устойчивости заключается в выведении различных веществ из периплазматического пространства бактерий во внешнюю среду. Если скорость выведения выше скорости проникновения препарата внутрь клетки, формируется устойчивый фенотип [6]. Эффлюксные насосы являются важным механизмом резистентности у многих грамотрицательных патогенов, в частности Acinetobacter spp. и P. aeruginosa. У P. aeruginosa система MexA-MexB-OprD в комбинации со снижением проницаемости мембраны может приводить к устойчивости ко многим антибиотикам (пенициллины, цефалоспорины, хинолоны, тетрациклин и хлорамфеникол) [7, 8].
4. Инактивация. Ферментативный гидролиз относится к основным механизмам устойчивости бактерий к β-лактамным антибиотикам. К настоящему времени описано более 1000 β-лактамаз, различающихся по субстратной специфичности, чувствительности к действию ингибиторов, локализации генов. Появление и распространение среди клинически значимых бактерий новых β-лактамаз во многом определяло весь ход развития этой группы антибиотиков.
Существует две классификации β-лактамаз. Первая – функциональная, основанная на субстратной специфичности и некоторых других свойствах этих ферментов [9], а вторая – молекулярная [10], основанная на аминокислотной и структурной гомологии ферментов. Все известные в настоящее время β-лактамазы по молекулярной классификации делят на 4 класса (А, В, С и D), в пределах которых ферменты характеризуются общностью свойств и определенной аминокислотной гомологией [9]. Бета-лактамазы классов А, С и D относятся к ферментам «серинового» типа (по аминокислоте, находящейся в активном центре фермента). В соответствии с современными представлениями считается, что β-лактамазы этих классов и ПСБ имеют общего предшественника. Ферменты, обладающие карбапенемазной активностью, описаны среди сериновых β-лактамаз классов А и D.
Ферменты класса В относятся к металло-β-лактамазам (МБЛ), поскольку в качестве ко-фермента в них присутствует атом цинка, по своему происхождению они не связаны с сериновыми β-лактамазами. От последних МБЛ отличаются и по механизму гидролитической активности. Ферменты класса В разделяют на три подкласса: В1, В2 и В3, при этом первые два подкласса, вероятно, имеют общего предшественника, а подкласс В3 относительно независим [11]. Выраженной в разной степени карбапенемазной активностью обладают все МБЛ.
Эволюция резистентности к β-лактамам
Негативные эффекты первых из получивших широкое распространение β-лактамаз класса А (стафилококковых и широкого спектра грамотрицательных бактерий) были достаточно легко преодолены в результате синтеза соединений, устойчивых к гидролизу этими энзимами (пенициллиназостабильных пенициллинов и цефлоспоринов), а также разработке суицидных ингибиторов (клавулановая кислота, сульбактам и тазобактам). С начала 1980-х гг. и до недавнего времени цефалоспорины III, а затем и IV поколения, а также защищенные пенициллины составляли основу этиотропной терапии подавляющего большинства инфекционных болезней человека.
Основной угрозой для перечисленных препаратов оказались появившиеся в 1983 г. β-лактамазы расширенного спектра (БЛРС) [12], отличавшиеся от своих предшественников способностью разрушать не только природные и полусинтетические пенициллины, но и цефалоспорины всех поколений. Несмотря на крайне широкое распространение термина БЛРС, единого определения этой группы ферментов нет. В строгом первоначальном смысле к БЛРС относят ферменты молекулярного класса А, разрушающие цефалоспорины всех поколений, чувствительные к действию ингибиторов (клавуланата, сульбактама и тазобактама).
В настоящее время к БЛРС иногда относят и некоторые ферменты классов D (оксациллиназы) и С, разрушающие цефалоспорины.
За 30 лет с момента их открытия БЛРС получили глобальное распространение. В отдельных странах Европейского Союза устойчивость к цефалоспоринам III поколения, связанную в основном с БЛРС, проявляют от 5,0 до 39,6% инвазивных изолятов Escherichia coli и до 70% Klebsiella pneumoniae. В стационарах России частота распространения БЛРС одна из самых высоких в мире, в ОРИТ среди представителей семейства Enterobacteriaceae этот показатель приближается к 90% или превышает его [13]. К крайне негативной глобальной тенденции следует отнести выход продуцентов БЛРС за пределы стационаров, такие бактерии обнаруживают не только у пациентов с внебольничными инфекциями, но и в окружающей среде. Продуценты БЛРС были обнаружены даже в сточных водах с полярной станции в Антарктиде [14].
Лечение инфекций, вызванных продуцентами БЛРС, оказалось крайне сложной задачей, поскольку такие бактерии не только были устойчивы к β-лактамам, но и проявляли ассоциированную устойчивость к антибиотикам других групп – фторхинолонам и аминогликозидам. В сложившейся ситуации единственными надежными средствами как эмпирической, так и целенаправленной терапии оказываются карбапенемы. Первый карбапенемный антибиотик – имипенем, характеризовавшийся не только очень широким спектром действия, но и устойчивостью к гидролизу, практически всеми известными на то время β-лактамазами был внедрен в медицинскую практику в начале 1980-х гг. – еще до широкого распространения БЛРС. В течение длительного времени карбапенемы рассматривали как антибиотики «резерва» и их применение было ограниченным как в связи с доступностью ряда эффективных препаратов (цефалоспоринов, фторхинолонов и аминогликозидов), так и из-за высокой стоимости. Однако параллельно с ростом частоты распространения БЛРС возрастал и объем потребления карбапенемов, что в конечном счете привело к формированию устойчивости и к этим антибиотикам.
В течение первых 20 лет клиниче-ского применения карбапенемов устойчивость к ним среди представителей семейства Enterobacteriaceae описывали крайне редко, но среди P. aeruginosa устойчивость выявляли уже в конце 1980-х гг. Чаще резистентность была связана со снижением проницаемости внешних структур бактериальной клетки, гиперпродукцией хромосомных β-лактамаз класса С и/или активацией систем выведения препаратов из бактериальной клетки.
Ситуация с резистентностью к карбапенемам принципиально изменилась после появления ферментов карбапенемаз, гены которых локализованы на мобильных элементах. Количество известных карбапенемаз лавинообразно нарастает, однако глобальное распространение в настоящее время получили немногие представители класса В (МБЛ) – VIM-тип, IMP-тип и NDM-тип; класса А – КРС-тип и класса D – ОХА-тип.
Карбапенемазы класса В
Первая карбапенемаза класса В с плазмидной локализацией гена была обнаружена в Японии в 1988 у P. aeruginosa [15]. В последующие годы в Японии аналогичные ферменты, идентифицированные как МБЛ IMP-типа, были описаны у многих видов бактерий. В 2000 г. вышло первое сообщение об обнаружении гена blaVIM-2 у Pseudomonas spp. во Фран-ции, а ретроспективные исследования зафиксировали первый случай в 1995 г. в Португалии [16, 17]. В дальнейшем количество описанных β-лактамаз, способных разрушать карбапенемы, начало быстро возрастать.
Переломным моментом в распространении устойчивости к карбапенемам стало появление МБЛ среди представителей семейства Enterobacteriaceae. Если в обзоре, опубликованном в 2005 г., T. Walsh охарактеризовал ситуацию с МБЛ как «затишье перед бурей» [18], то сегодня уже можно говорить о разразившейся буре. В настоящее время среди МБЛ выделяют 18 семейств из них 17 относятся к группе В1 (http://www.mbled.uni-stuttgart.de/). У представителей Enterobacteriaceae определенное значение имеют карбапенемазы VIM- и IMP-типа, других более редких типов, но наибольший общественный резонанс вызвало появление и необычайно быстрое глобальное распространение МБЛ, получивших название NDM (New Delhi Metallo-beta-lactamase – от названия города с которым связывают их появление). По данным ретроспективных исследований коллекций культур, эти ферменты появились на полуострове Индостан не позднее 2006 г., а в 2012 г. они уже обнаруживались в 40 странах на всех континентах, кроме Антарктиды и Южной Америки [19]. К концу 2014 г. число стран, где выявлен ген blaNDM-1, существенно возросло [20, 21]. Первоначально гены NDM-типа были обнаружены у K. pneumoniae, но к настоящему вре-мени они описаны у многих представителей Enterobacteriaceae (E. coli, Enterobacter spp., Citrobacter freundii, Morganella morganii, Providencia spp.), а также у P. aeruginosa и Acinetobacter spp.
В связи с быстрым распространением и эволюцией оценить относительную значимость отдельных карбапенемаз достаточно сложно, тем не менее МБЛ, вероятно, представляют наибольшую угрозу. Скорее всего, МБЛ являются эндогенными у многих свободно живущих грамположительных и грамотрицательных бактерий Chryseobacterium spp., Aeromonas spp., Legionella germanii., Bacillus spp., Stenotrophomonas maltophilia и др. Гены этих ферментов обнаружены также в составе генома бактерий, которые не удается культивировать и о свойствах которых известно крайне мало. МБЛ обнаруживаются также у единичных штаммов Bacteroides fragilis. Воссоздать эволюционную историю приобретения МБЛ клинически значимыми бактериями в настоящее время можно лишь гипотетически.
Клиническое значение МБЛ определяется их субстратной специфичностью. По этому показателю указанные ферменты не имеют себе равных среди всех β-лактамаз. МБЛ разрушают природные и полусинтетические пенициллины, цефалоспорины всех поколений и карбапенемы, но не гидролизуют азтреонам. Последнее свойство имеет ограниченное значение, поскольку из-за очень частого сочетания продукции МБЛ и БЛРС клинические штаммы, как правило, устойчивы и к азтреонаму. МБЛ не чувствительны к таким ингибиторам, как клавуланат, сульбактам и тазобактам. В то же время они ингибируются ЭДТА, что используют для фенотипической детекции МБЛ в лабораторной практике.
Карбапенемазы класса А
Гены большинства карбапенемаз класса А (NmcA, Sme, IMI-1, SFC-1) локализованы на хромосомах, для других (KPC, IMI-2, GES) характерна плазмидная локализация. Из всех перечисленных ферментов наибольшее значение имеют карбапенемазы группы КРС, впервые выделенные на востоке США в конце 1990-х гг. у K. pneumoniae [22], а к настоящему времени распространенные глобально [23]. Эти ферменты частично подавляются клавулановой кислотой, а также новым ингибитором – авибактамом (NXL104), который используют для создания защищенных препаратов [24].
Карбапенемазы класса D
Исторически β-лактамазы класса D получили название оксациллиназы благодаря большей способности гидролизовать оксациллин по сравнению с природными пенициллинами, в настоящее время известно более 100 вариантов β-лактамаз ОХА-типа, карбапенемазной активностью обладают лишь некоторые из них. Карбапенемазы ОХА-типа распространены в основном среди P. aeruginosa и Acinetobacter spp., среди представителей семейства Enterobacteriaceae распространены карбапенемазы ОХА-48 и ее производные [25].
Распространение карбапенемаз в России
Как отмечалось ранее, первые клинически значимые карбапенемазы были обнаружены у бактерий рода Pseudomonas, в настоящее время в различных регионах мира среди этих бактерий доминируют различные карбапенемазы. В России первые МБЛ также были выявлены у P. aeruginosa. С 2002 г. и до настоящего времени на территории России (от Хабаровска до Санкт-Петербурга), Казахстана и Белоруссии циркулирует доминирующая генетическая линия P. aeruginosa (сиквенс тип – ST235), продуцентов VIM-2 карбапенемазы [26]. В 2008–2010 гг. частота продукции МБЛ среди P. aeruginosa в указанном регионе достигла 28,7%, из которых 99,6% относились к VIM-2. Среди продуцентов МБЛ более 96% были устойчивы ко всем антибиотикам, кроме колистина [26].
В 2013 г. наиболее распространенными среди Enterobacteriaceae карбапенемазами в Европе были KPC-тип, VIM-тип, IMP-тип, NDM-тип и OXA-48-тип [27, 28]. Центр профилактики и контроля болезней (European Centre for Disease Prevention and Control http://www.ecdc.europa.eu/en/Pages/home.aspx) характеризует распространение карбапенемаз в Европе следующим образом: эндемичными регионами являются Италия и Греция, внутрибольничное распространение карбапенемаз зафиксировано в Израиле, Ирландии, Венгрии (4-я группа). Всего в 26 странах Европы ситуация характеризуется регулярными вспышками и эндемичными очагами, в девяти странах обнаружены единичные случаи и только в трех странах (Исландии, Черногории и Македонии) инфекций, вызванных продуцентами карбапенемаз, не выявлено.
Среди энтеробактерий в Российской Федерации до 2011 г. выявляли лишь единичные изоляты, продуцирующие карбапенемазы VIM-4 и ОХА-48.
С конца 2011 г. в стационарах Санкт-Петербурга энтеробактерии, продуцирующие карбапенемазы, начали выделять в значительном количестве. Результаты этих наблюдений были суммированы в нашей работе [29]. Наиболее распространенной карбапенемазой в Санкт-Петербурге оказалась NDM-1, выявлявшаяся в основном у K. pneumonia сиквенс-типа ST340, единичных изолятах K. pneumonia ST101 и Acinetobacter nosocomialis. Кроме того, были обнаружены единичные энтеробактерии, продуцирующие VIM-4, KPC-2 и OXA-48 карбапенемазы. Выявление продуцентов карбапенемаз во множестве стационаров, зафиксированные внутрибольничные вспышки и разнообразие генов карбапенемаз, а также видов и генетических групп бактерий, их продуцирующих, отсутствие данных о поездках пациентов за границу свидетельствуют о том, что первые случаи импорта карбапенемаз в Санкт-Петербург были пропущены.
По нашим данным, ситуация с распространением карбапенемаз в Санкт-Петербурге быстро ухудшается, что обосновывает целесообразность представить некоторые неопубликованные данные. На сегодняшний день продуценты NDM-1 обнаружены в семи стационарах, при этом в шести были зафиксированы внутрибольничные вспышки, некоторые из которых как минимум два года остаются нелокализованными, что приводит к постоянному появлению новых случаев инфекций. К особенностям распространения NDM-1 в Санкт-Петербурге относится следующее: подавляющее большинство случаев связано с одной генетической линией – K. pneumoniae сиквенс-типа ST340. Гипотетический сценарий распространения продуцентов NDM-1 в Санкт-Петербурге предполагает ограниченное число случаев импорта продуцента, после чего произошло распространение данного гена по нескольким стационарам.
Продуцентов карбапенемазы KPC-типа на сегодняшний день можно условно поставить на второе место по степени угрозы для здравоохранения в Санкт-Петербурге. Они выделены в пяти стационарах, в трех из которых были зафиксированы внутрибольничные вспышки. В отличие от продуцентов генов blaNDM-1 продуценты KPC демонстрируют разнообразие по сиквенс-типам, а также по вариантам самого гена (выявлены гены blaKPC-2 и blaKPC-3). Можно предположить, что это связано с несколькими независимыми случаями импорта. Аналогично продуцентам NDM продуценты KPC обычно имеют массу детерминант устойчивости. Анализ данных полногеномного секвенирования выявил у изолята K. pneumoniae, относящегося к ST273, 18 приобретенных генов резистентности. Также данный изолят имеет значение МПК полимиксина B 16 мкг/мл, сохраняя чувствительность только к тигециклину, что хорошо иллюстрирует проблему, связанную с распространением подобных изолятов.
K. pneumoniae, продуцирующие карбапенемазы ОХА-48, были выделены в 5 стационарах Санкт-Петербурга, их клональное родство в настоящее время еще не оценено. В течение последних нескольких лет в нашу лабораторию в инициативном порядке из ряда медицинских учреждений Москвы и других городов России направляли изоляты энтеробактерий, проявляющие устойчивость к карбапенемам. В Москве K. pneumonia, продуцирующие карбапенемазы ОХА-48, были обнаружены в четырех стационарах. В Москве же K. pneumoniae, продуцирующая ОХА-48, была выделена от ребенка в возрасте 3 месяцев, обследованного по поводу «дисбактериоза».
В настоящее время дать общую оценку распространения в России энтеробактерий, продуцирующих карбапенемазы, достаточно сложно. Очевидно, что в Санкт-Петербурге сформировались множественные эндемичные очаги распространения энтеробактерий – продуцентов карбапенемаз NDM-1, КРС-типа и ОХА-48. Есть основания подозревать, что в Москве также уже сформировались эндемичные очаги распространения продуцентов ОХА-48. Информация о распространении карбапенемаз среди энтеробактерий в других регионах России крайне ограничена. В недавно опубликованном исследовании 573 изолятов Enterobacteriaceae, выделенных в 25 стационарах 18 городов России, было обнаружено лишь 2 продуцента NDM-1 и 18 продуцентов ОХА-48[13].
Тот факт, что появление карбапенемаз на территории России было замечено на ранней стадии, позволяет надеяться, что при проведении адекватных мер инфекционного контроля дальнейшее распространение этого механизма резистентности удастся сдержать.
Сдерживание распространения карбапенемаз
В факте появления и распространения устойчивости к очередной группе антибиотиков нет ничего принципиально нового. В истории химиотерапии такие события происходили неоднократно.
Однако в случае с распространением карбапенемаз ситуация осложняется несколькими факторами.
Для продуцентов карбапенемаз кроме устойчивости практически ко всем β-лактамам характерна высокая частота устойчивости к антибиотикам других групп, прежде всего к аминогликозидам и фторхинолонам.
В силу ряда экономических и биологических причин появление в медицинской практике новых антибактериальных препаратов, преодолевающих множественную устойчивость грамотрицательных патогенов, в ближайшие 5–7 лет маловероятно.
Полученные к настоящему времени данные свидетельствуют, что по сравнению с другими детерминантами резистентности распространение наиболее успешных карбапенемаз происходит гораздо быстрее. Кроме того, уже сейчас появляются факты выхода карбапенемаз во внебольничную среду.
Таким образом, острая потребность в сдерживании распространения карбапенемаз вполне очевидна. О происхождении и резервуарах продуцентов карбапенемаз известно немного, но к настоящему времени установлена возможность формирования в медицинских учреждениях эндемичных очагов распространения таких бактерий. При этом кроме эпизодов клинически выраженных инфекций отмечают значительное количество случаев бессимптомного носительства в кишечнике. По современным представлениям, для сдерживания распространения карбапенемаз необходимо раннее выявление и изоляция как пациентов с клинически выраженными инфекциями, так и бессимптомных носителей. Для этого в свою очередь необходимо дифференцировать продукцию карбапенемаз от устойчивости к карбапенемам, связанной со снижением проницаемости и эффлюксом, а также проводить активный скрининг на выявление бессимптомных носителей.
Лабораторная детекция карбапенемаз
Методы детекции карбапенемаз можно разделить на фенотипические и генотипические. Фенотипические методы основаны на способности ряда соединений ингибировать активность указанных ферментов или на выявлении у исследуемых культур карбапенемазной активности.
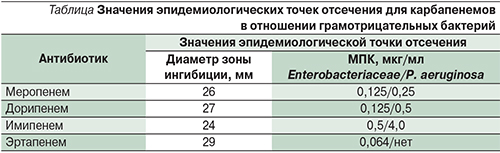
Первым этапом в поиске карбапенемаз является обнаружение подозрительных изолятов, к таковым следует относить все изоляты с МПК хотя бы одного карбапенемного антибиотика выше, чем значение эпидемиологической точки отсечения по определению EUCAST [30], возможно также использовать соответствующие значения диаметров зон задержки роста в случае применения диско-диффузионного анализа. Данные приведены в таблице.
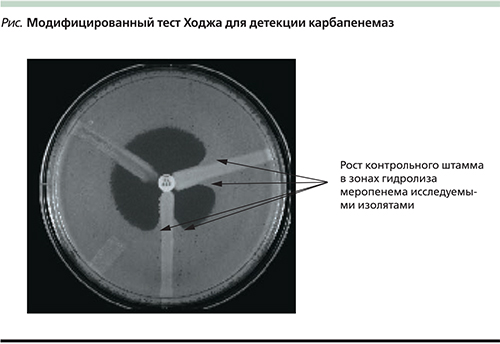
Наиболее простым и доступным методом выявления карбапенемазной активности у подозрительных изолятов является модифицированный тест Ходжа (modified Hodge test – MHT) [31]. Для постановки МНТ чашку Петри с агаром Мюллера–Хинтон засевают контрольным штаммом E. coli ATCC 25922, в середине чашки размещают диск с карбапенемным антибиотикам. Затем штрихом по направлению от диска к периферии засевают исследуемые изоляты. Если изоляты обладают карбапенемазной активностью, то в непосредственной близости от роста исследуемой культуры происходит гидролиз карбапенемного антибиотика и появляется рост контрольного штамма (см. рисунок).
К сожалению, иногда тест Ходжа может давать как ложноположительные, так и ложноотрицательные результаты. Более надежными методами выявления карбапенемазной активности являются масс-спектрометрия [32] и спектрофотомерия.
Ни МНТ, ни физико-химические методы детекции карбапенемазной активности не позволяют дифференцировать карбапенемазы. Для этой цели можно использовать метод двойных дисков с различными ингибиторами. Ингибиторами МБЛ являются этилендиамин тетраацетат (ЭДТА), дипиколиновая кислота, карбапенемаз КРС и AmpC β-лактамаз – бороновая кислота, AmpC β-лактамаз – клоксациллин. Диски, нагруженные ингибиторами β-лактамаз, а также комбинациями и ингибиторами, коммерчески доступны.
Наиболее чувствительными и надежными методами детекции МБЛ являются генотипические. Описанные β-лактамазы легко выявляются в полимеразной цепной реакции (ПЦР) с использованием специфических праймеров. Однако с помощью этого метода невозможно выявить новые МБЛ, для которых не определена нуклеотидная последовательность генов. При отрицательных результатах ПЦР и наличии фенотипических признаков продукции МБЛ необходимо использовать комплекс молекулярных методов клонирования.
Скрининг на носительство карбапенемаз
Выявление носительства карбапенемаз является необходимым этапом сдерживания их распространения. Аналогично детекции карбапенемаз применяются два подхода – фенотипический, основанный на высеве клинических образцов, чаще всего фекалий, на селективные питательные среды, обычно с добавлением одного из карбапенемных антибиотиков, а также методы на основе ПЦР с праймерами, специфичными к основным актуальным группам генов карбапенемаз. Чаще всего в практике используется комбинация этих методов. При этом возможно как применение коммерческих наборов, так и самостоятельное приготовление селективных сред и подбор праймеров с учетом региональных особенностей.
Возможности терапии инфекций, вызванных продуцентами карбапенемаз
Факт резкого снижения эффективности стандартных схем при лечении инфекций, вызванных энтеробактериями, продуцирующими карбапенемазы, хорошо документирован [33]. Как уже отмечалось, для продуцентов карбапенемаз характерна высокая частота ассоциированной устойчивости к антибиотикам наиболее распространенных групп (аминогликозидам и фторхинолонам), что существенно снижает возможности выбора терапии. Чаще всего, чувствительность in vitro сохраняется к тигециклину, полимиксину и фосфомицину. Следует также отметить, что уровень устойчивости к отдельным карбапенемам среди продуцентов различных карбапенемаз может существенно различаться. Так, для продуцентов ОХА-48 и карбапенемаз VIM-типа характерны невысокие значения МПК, в ряде случаев они могут даже оказываться в категории чувствительных.
Если проблема антибиотикочувствительности продуцентов карбапенемаз изучена достаточно хорошо, вопрос с обоснованием режимов терапии практически не решен. До настоящего времени по этой проблеме не было проведено ни одного рандомизированного плацебо-контролируемого клинического исследования. Опубликованы результаты ретроспективных исследований и мета-анализы, которые позволяют сделать несколько важных выводов. Практически все исследователи единодушны в том, что доступные на сегодняшний день антибиотики более эффективны при использовании в виде комбинаций, чем в виде монотерапии. Ряд авторов считают, что карбапенемы должны входить в схемы комбинированной терапии, несмотря на устойчивость к ним in vitro [34]. Такой подход полностью оправдан при невысоком уровне устойчивости к карбапенемам (МПК≤8,0 мкг/мл), указанный факт обосновывает необходимость внедрения в деятельность практических лабораторий методов количественной оценки чувствительности к антибиотикам. Следует также отметить целесообразность назначения максимальных доз карбапенемов в виде продленных инфузий. В качестве дополнений к карбапенемам в составе комбинированной терапии используют самые разнообразные антибиотики, но предпочтение отдают полимиксину и тигециклину, имеются сообщения об использовании комбинаций из двух, трех и даже четырех антибиотиков. Наибольший опыт использования комбинированных схем на основе карбапенемов накоплен при лечении инфекций, вызванных продуцентами VIM, KPC и OXA карбапенемаз [35]. Неизвестно, насколько это справедливо при инфекциях, вызванных продуцентами NDM.
Альтернативой режимам, основанным на карбапенемах, рассматриваются таковые, основанные на полимиксине или колистине (полимиксине Е), возможны комбинации с тигециклином, аминогликозидами и фосфомицином [36]. Обсуждается возможность тестирования in vitro различных комбинаций антибиотиков для выявления синергизма с последующим назначением наиболее активной; однако клинические данные, которые бы подтверждали перспективность такого подхода, ограничены.
Тигециклин, к которому in vitro большинство продуцентов карбапенемаз сохраняют чувствительность, в виде монотерапии назначать не рекомендуют. Обсуждается также целесообразность использования тигециклина в повышенной дозе (200 мг/сут), что является фармакодинамически вполне обоснованным [37].
К сожалению, ни один из альтернативных карбапенемам антибиотиков не лишен недостатков, и к полимиксину, и к тигециклину наблюдают незначительный, но устойчивый рост резистентности.
Заключение
Повышение уровня микробиологической диагностики, накопление информации о механизмах устойчивости бактерий позволили выявить ранние стадии распространения карбапенемаз, прежде всего МБЛ, на территории Российской Федерации. Составление прогноза скорости дальнейшего распространения этих ферментов вряд ли возможно, но наибольшая опасность связана с их межвидовой передачей и распространением среди таких важных бактерий, как E. coli, K. pneumoniae. Внедрение раннего выявления возбудителей инфекций, продуцирующих карбапенемазы, позволит осуществлять целенаправленные мероприятия по изоляции инфицированных и колонизованных пациентов и таким образом сдерживать распространение этого крайне опасного механизма устойчивости. Для реализации указанного подхода необходимо внедрение в практику бактериологических лабораторий фенотипических и генетических методов быстрой детекции продукции карбапенемаз.



