Алкогольная болезнь печени (АБП) – группа заболеваний, вызванных повреждающим действием этанола на клетки печени. В США под критерии, определяющие диагноз хронического алкоголизма, подпадают почти 14 млн человек. В России насчитывается более 10 млн больных алкоголизмом. Среди этой группы более 3 млн являются потенциальными пациентами гепатологов и около 14 тыс. ежегодно умирают от цирроза печени (ЦП). Точное число смертельных случаев вследствие злоупотребления алкоголем трудно определить из-за отсутствия подобной статистики.
АБП остается основной причиной осложненного течения заболеваний печени и высокой летальности во всем мире. Алкоголь – наиболее значимая причина заболеваний печени, вследствие которой развивается от 40 до 80 % всех случаев ЦП [7]. На долю летальности от ЦП вследствие АБП приходится около 44 % смертей среди больных с патологией печени. В последнее время АБП стала одной из основных причин смерти в возрастной группе от 45 до 64 лет [12]. Смертность от нее выше, чем от многих форм рака (молочной железы, толстой кишки, простаты).
В экономически развитых странах ЦП входит в число шести основных причин смерти в работоспособном возрасте. Приблизительно у 10–35 % больных этиологию ЦП установить не удается. Эти наблюдения относят к криптогенным циррозам. На самом деле причиной таких ЦП может быть алкоголь.
Следует отметить несоответствие понятий АБП и “алкоголизм”. У большинства больных АБП наблюдается слабовыраженная зависимость от алкоголя, редко возникает похмельный синдром, что и позволяет им употреблять спиртные напитки в больших количествах на протяжении многих лет. Стертое течение АБП вплоть до формирования ЦП очень характерно именно для таких пациентов, что препятствует оказанию им своевременной помощи и предотвращению ЦП.
Метаболизм этанола в печени
Печень представляет собой основной орган, где осуществляется метаболизм этанола. Однако выявление желудочной фракции алкогольдегидрогеназы (АДГ) дает основание считать желудок первым органом, в котором происходит окисление этанола. В желудке лимитируется количество алкоголя, проникающее в печень с портальным кровотоком, что потенциально предупреждает ее алкогольное повреждение. Известно, что активность желудочной АДГ у женщин в сравнении с мужчинами снижена, как и у лиц обоего пола, злоупотребляющих алкоголем. Некоторые лекарственные препараты (аспирин, антагонисты H2-гистаминовых рецепторов) также уменьшают активность желудочной фракции АДГ. Несмотря на эти факты, значение желудочной АДГ и самого желудка в метаболизме этанола находится в стадии исследования.
Основным ферментом, расщепляющим этанол в печени, является АДГ, которая трансформирует алкоголь до ацетальдегида – токсического метаболита этанола. Содержание АДГ в крови зависит от генетических особенностей, пола и расовой принадлежности. Дальнейшее расщепление ацетальдегида до ацетата происходит при помощи альдегиддегидрогеназы. Накопление ацетальдегида приводит к таким клиническим проявлениям, как прилив крови к лицу и шее, тахикардия, гипотензия и отвращение к алкоголю.
Когда концентрация этанола превышает возможности окисления АДГ, его метаболизм происходит в микросомальной системе окисления этанола с вовлечением изофермента цитохрома P450 CYP2Е1. Он является критическим изоферментом, появляющимся при хронической алкогольной интоксикации. Полиморфизм CYP2Е1 зависит от внешних причин и коррелирует с различными повреждениями печени. Кроме того, CYP2Е1 отвечает за метаболизм лекарств, например парацетамола. Это является объяснением тому, что пациенты с АБП имеют высокий риск повреждения печени при лечении парацетамолом в терапевтических дозах [13].
Патогенез АБП
Выделяют три основные стадии АБП: стеатоз, гепатит и цирроз. При длительном систематическом употреблении алкоголя образуются свободные радикалы, которые поддерживают воспалительный процесс и вызывают повреждение ткани печени через перекисное окисление липидов. Поступление алкоголя осуществляется через энтероциты тонкой кишки в портальную венозную систему, где он вызывает повышение эндотоксической абсорбции. Алкоголь в крови стимулирует купферовские клетки. Эндотоксины также стимулируют купферовские клетки, вырабатывающие цитокины и свободные радикалы [2]. Вследствие этого усиливается лейкоцитарная инфильтрация и активизируется процесс воспаления печени с возможным формированием гепатита (рис. 1).

Процесс повреждения печени начинается в зоне, расположенной вокруг центральной вены. Эта область отвечает за оксигенацию крови и имеет высокую концентрацию CYP2Е1. Важное значение имеет повышение концентраций интерлейкина-8 (ИЛ-8) и фактора некроза опухоли α (ФНО-α) в крови, коррелирующее с прогнозом заболевания. Эти медиаторы опосредуют повреждающее действие этанола, отвечают за активацию и адгезию лимфоцитов. Купферовские клетки (макрофаги в печени) также включены в процесс повреждения, продуцируя воспалительные и фиброгенетические цитокины, активизирующиеся алкоголем. Хроническая алкогольная интоксикация критически повышает всасываемость алкоголя в тонкой кишке и всасывание эндотоксинов в портальной крови. Это является проявлением действия цитокинов и свободных радикалов, высвобождающихся из стимулированных алкоголем купферовских клеток.
В формировании конечной стадии АБП – цирроза – принимают участие ацетальдегид, цитокины и звездчатые клетки, взаимодействующие друг с другом. В нормальных условиях такие клетки накапливают запасы витамина А. При активации цитокинами или ацетальдегидом они претерпевают ряд структурных изменений, теряют запасы витамина А и начинают продуцировать фиброзную ткань. Разрастание фиброзной ткани вокруг сосудов приводит к их констрикции и нарушению доставки кислорода к гепатоцитам.
Диагностика АБП
При диагностике АБП необходимо собрать полный анамнез, включающий данные о длительности и интенсивности злоупотребления алкоголем, провести полное физикальное и лабораторное обследование для выявления признаков болезни печени. При этом результаты физикальных и лабораторных исследований могут давать неопределенный результат или даже отсутствие проявлений болезни. Самое необходимое при диагностике АБП – точно определить, имеется ли злоупотребление алкоголем у пациента. В этом могут помочь различные анкеты и опросы, специальные теста.
В настоящее время установлены пороговые значения ежедневного количества и продолжительности потребления этанола, ассоциирующиеся с возможным развитием АБП. Показано, что ежедневное потребление алкоголя в течение 10–12 лет в дозах, превышающих 40–80 г для мужчин и 20–40 г для женщин, может быть причиной алкогольного гепатита/цирроза. Поскольку алкогольные напитки имеют различную крепость, необходимо учитывать содержание в них этанола в граммах.
Примерное содержание этанола в спиртных напитках составляет:
• 350 г пива (5 %) – 14 г;
• 100 г вина (12 %) – 10 г;
• 50 г крепленого вина (20 %) – 9 г;
• 30 г коктейля (40 %) – 9 г.
Следует подчеркнуть, что количество алкоголя, вызывающее АБП, индивидуально в каждом конкретном случае. В настоящее время существует множество споров вокруг безопасного количества алкоголя, т. к. риск развития болезни печени существует и при относительно низких ежедневных его дозах. Согласно современным представлениям, ежедневная пороговая доза составляет 30 г/день для мужчин и 20 г/день для женщин.
Среди пациентов, длительное время злоупотребляющих алкоголем, в 90–100 % случаев развивается стеатоз, но только у 10–35 % больных формируется алкогольный гепатит и у 8 % –ЦП.
Клинические признаки АБП варьируются от полного отсутствия каких-либо симптомов до классической картины тяжелых форм поражения печени с признаками печеночной недостаточности и портальной гипертензии. Пациенты часто предъявляют жалобы на слабость, отсутствие аппетита, тошноту и рвоту, нарушение ритма сна и бодрствования, снижение либидо, повышение температуры тела и т. д. Патогномоничных для АБП физикальных признаков нет. Наиболее часто при осмотре пациента можно выявить гинекомастию, гипогонадизм, контрактуру Дюпюитрена, белые ногти, периферическую полинейропатию, сосудистые звездочки (телеангиоэетазии), пальмарную эритему, асцит, спленомегалию, гипертрофию слюнных желез. Очевидно, что только по физикальным данным нельзя дифференцировать АБП от других форм повреждения печени.
Как уже отмечалось выше, АБП включает три отдельных патологических диагноза: алкогольное ожирение печени (стеатоз), алкогольный гепатит и алкогольный цирроз, которые могут встречаться в любой комбинации [4].
Алкогольный стеатоз печени обычно имеет бессимптомное течение, но у пациентов могут возникать неспецифичные жалобы, такие как усталость, тошнота или дискомфорт в верхнем правом квадранте живота. Приблизительно у 70 % госпитализированных пациентов со стеатозом выявляется гепатомегалия, у трети из них имелись изменения биохимических показателей крови.
Клинический синдром, связанный с алкогольным гепатитом, включает гепатомегалию, желтуху, лихорадку, асцит, печеночную энцефалопатию, мальабсорбцию, анорексию и недомогание. Возможно также наличие лейкемоидных реакций и гепаторенального синдрома. Портальная гипертензия может наблюдаться и в отсутствие цирроза. После выявления у пациента алкогольного гепатита вероятность развития цирроза повышается на 10–20 % ежегодно; в конечном итоге ЦП разовьется у 70 % таких больных. В группу с высоким риском формирования ЦП включают пациентов, продолжающих злоупотребление алкоголем, страдающих тяжелым алкогольным гепатитом, и женщин. Алкогольный ЦП обычно протекает бессимптомно или с наличием малых признаков, но в результате у большинства пациентов развиваются портальная гипертензия и печеночная недостаточность.
Биохимические исследования могут быть очень полезными в диагностике АБП, но на основании только этих показателей невозможно точно определить тяжесть печеночного процесса и его этиологию. Уровни аспарагиновой (АСТ) и аланиновой (АЛТ) трансаминаз редко превышают 300 ЕД/мл. При АБП соотношение АСТ/АЛТ часто превышает 2. Уровни трансаминаз, превышающие 300 ЕД/мл у пациента, злоупотребляющего алкоголем, позволяют предположить повреждение ткани печени другой этиологии.
Уровень щелочной фосфатазы у больных АБП часто находится в пределах нормы или незначительно повышен. В то же время уровень γ-глутамилтранспептидазы (ГГТП) у злоупотребляющих алкоголем обычно увеличен независимо от наличия болезни печени. Он также увеличен при большинстве неалкогольных заболеваний печени и применении ряда лекарственных средств, что делает специфичность ГГТП весьма ограниченной.
В целом к относительно типичным лабораторным признакам АБП можно отнести [2]:
• сывороточные трансаминазы: ACT > АЛТ;
• повышение уровней ГГТП и щелочной фосфатазы;
• метаболические нарушения: гипергликемию, гипертриглицеридемию, гиперурикемию;
• электролитные нарушения: низкие уровни калия, магния и фосфора в крови;
• изменение тестов, отражающих состояние функции печени – сывороточные альбумин, билирубин, протромбиновое время (ПВ; протромбиновый индекс) – обычно только при выраженном повреждении печени;
• гематологические показатели: макроцитарная анемия; количество тромбоцитов в пределах от нормального до низкого; лейкоцитоз; при алкогольном гепатите возможны лейкемоидные реакции.
Повышение уровня билирубина, удлиненное ПВ и гипоальбуминемия – маркеры тяжелого алкогольного гепатита и/или ЦП. Для прогноза болезни используется т. н. Maddrey’s Dis-criminant Function; а вычисления проводятся по следующему уравнению:
4,6 × (ПВпациент - ПВконтроль] + общий билирубин (мг/дл).
Если полученное значение превышает 32, летальность в течение месяца приближается к 50 %. Кроме того, имеются данные, что сывороточные концентрации ФНО-α, ИЛ-6 и ИЛ-8 коррелируют с летальностью больных алкогольным гепатитом, но определение этих цитокинов с указанной целью еще не получили распространения в рутинной клинической практике.
Биопсия печени – самый чувствительный и точный тест для оценки степени повреждения ткани этого органа и фиброза. А у пациентов с бессимптомным течением заболевания она остается единственным методом, позволяющим точно определять наличие стеатогепатита. Для выяснения этиологии болезни печени полезна также гистологическая оценка. На рис. 2 представлены примеры биопсии печени при различных стадиях АБП.

Терапия АБП
В последнее время достигнуты значительные успехи в понимании механизмов повреждений печени, вызванных приемом алкоголя, нашедшие свое применение в клинических исследованиях. Это позволило лучше понять принципы действия традиционных средств лечения АБП – от стероидов до антиоксидантов [9].
Несмотря на то что АБП остается основной причиной осложненного течения заболеваний печени и обусловленной ими смертности, сегодня нет общепринятой методики лечения алкогольных гепатита и ЦП. Тем не менее существует несколько препаратов, получивших широкое распространение при указанной патологии. Медикаментозная терапия АБП зависит от ее стадии. Первая линия лечения включает кортикостероиды и пентоксифилин.
Кортикостероиды – наиболее широко изученная группа лекарственных средств лечения алкогольного гепатита, однако их терапевтическое значение при указанной патологии до сих пор остается ограниченным. Основаниями для использования кортикостероидов в данном случае являются потенциальное нарушение иммунного ответа и повышение уровней провоспалительных цитокинов. Большинство промежуточных результатов исследований свидетельствует в пользу использования кортикостероидов при тяжелом остром алкогольном гепатите [13].
Пентоксифиллин – неселективный ингибитор фосфодиэстеразы, который увеличивает внутриклеточные концентрации аденозин-3,5-циклического монофосфата и гуанозин-3,5-циклического монофосфата, уменьшает продукцию способствующих воспалению хемокинов/цитокинов, включая ФНО-α. В некоторых центрах пентоксифиллин (400 мг перорально 3 раза ежедневно) используют в лечении алкогольных гепатита и ЦП, основываясь на его противовоспалительном эффекте, снижении риска возникновения гепаторенального синдрома и относительной безопасности.
Пристального внимания в плане лечения АБП заслуживает адеметионин (Гептрал), являющийся исключительно важной биологической субстанцией. Он присутствует во всех органах и тканях, но максимальное его содержание отмечено в печени и головном мозге. Известно, что адеметионин играет ключевую роль в реакциях детоксикации, происходящих в печени, определяет способность клеток этого органа к восстановлению и регенерации, участвует в антиоксидантной защите. Кроме того, адеметионин включается в реакции нейропротективной защиты и обладает антидепрессивным действием.
Гептрал восполняет недостаток адеметионина в организме, вызванный повышенным потреблением этого вещества при различных заболеваниях печени. Эквивалентность Гептрала эндогенному адеметионину определяет высокий уровень эффективности препарата и быстрое достижение лечебного эффекта за счет полного и быстрого включения в биохимические реакции, что позволяет не только восполнять дефицит адеметионина, но и стимулировать его синтез в гепатоцитах. Препарат оказывает многофункциональное действие и способен в короткие сроки уменьшать клинические проявления заболеваний печени, тревогу и проявления депрессии, восстанавливить работоспособность, улучшать функцию жизненно важных органов (печени, головного мозга).
Многофункциональность Гептрала проявляется в следующих его свойствах. Он стимулирует выработку и отток желчи, а также поступление желчных кислот из гепатоцитов в желчевыводящую систему, поскольку улучшает текучесть мембраны гепатоцита и работу внутриклеточных транспортных систем. Восстановление оттока желчи из гепатоцитов предотвращает ее избыточное скопление в клетках и повреждающее действие на мембрану. Гептрал нормализует, кроме того, моторику желчевыводящих путей, обеспечивает физиологическое продвижение желчи к желчному пузырю и далее – в двенадцатиперстную кишку. Это способствует улучшению пищеварения, разрешает внутрипеченочный холестаз и нормализует биохимические показатели крови.
Гептрал стимулирует регенерацию и пролиферацию гепатоцитов, что позволяет компенсировать функции печени и увеличивает выживаемость пациентов даже при выраженных изменениях, включая цирроз. Кроме того, препарат увеличивает синтез глутатиона и цистеина – естественных факторов антиоксидантной защиты в организме. Это предотвращает повреждающее действие свободных радикалов, желчных кислот и других токсических агентов на клетки печени. Адеметионин включается в основные биохимические реакции, которые быстро и эффективно обезвреживают токсины. Детоксикационное действие распространяется на вещества, поступающие в организм из внешней среды, а также продукты жизнедеятельности клеток и агрессивные компоненты желчи.
Гептрал стимулирует синтез нейромедиаторов, усиливающих синаптическую передачу, защищает клетки головного мозга от токсического действия продуктов метаболизма. Нарушение процессов биологического метилирования является одним из механизмов развития депрессии. Адеметионин является основным источником метильных групп в центральной и периферической нервной системе, благодаря чему активирует постсинаптические рецепторы и их взаимодействие с моноаминовыми нейромедиаторами. Кроме того, он непосредственно участвует в синтезе различных нейромедиаторов, в первую очередь серотонина. Антидепрессивный эффект Гептрала проявляется постепенно, начиная с 1-й недели, и стабилизируется в течение 2 недель лечения, способствуя быстрому улучшению настроения и самочувствия, уменьшая чувство тревоги. Эффективность и безопасность длительного применения Гептрала доказаны в многочисленных клинических рандомизированных исследованиях. Препарат хорошо переносится, при его использовании отсутствует лекарственная зависимость, не развивается синдром отмены.
Гептрал выпускается в двух лекарственных формах (лиофилизат для приготовления раствора для внутривенного и внутримышечного введения и таблетки, покрытые кишечно-растворимой оболочкой), что позволяет проводить ступенчатую терапию (в стационаре и амбулаторно). Схемы применения Гептрала представлены на рис. 3.
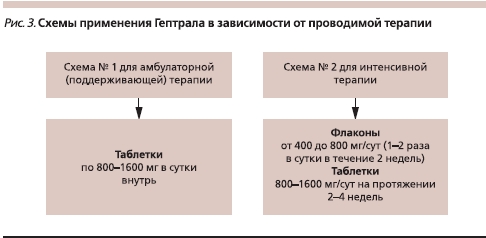
Синтез глутатиона при введении Гептрала в суточной дозе 400–800 мг в течение 14 дней внутривенно с переходом к приему в таблетированной форме по 800–1600 мг (1–2 таблетки) в течение 14 дней приводит к восстановлению функции печени и нормализации клинико-лабораторных признаков ее алкогольных повреждений.
Таким образом, благодаря включению адеметионина – активного компонента Гептрала, в каскад жизненно важных биохимических реакций стимулируется синтез глутатиона и таурина – ключевых компонентов детоксикации, что приводит к улучшению выделения токсинов и желчи, т. е. уменьшается внутрипеченочный холестаз; за счет реакции метилирования активируется синтез мембран и восстанавливаются структурные компоненты гепатоцита – митохондрии, органеллы, что препятствует прогрессированию заболевания; стимулируется синтез серотонина, ключевого фактора формирования позитивного эмоционального фона и повышения приверженности лечению.
Заключение
Суммируя все вышесказанное, можно заключить, что пациенты с АБП должны отказаться от алкоголя или резко снизить его потребление в сочетании с другими изменениями образа жизни. В частности, им необходимо соблюдать сбалансированную диету. Определенные препараты, такие как кортикостероиды и пентоксифиллин, могут быть эффективными при лечении некоторых больных алкогольным гепатитом.
Препаратом выбора при АБП является Гептрал (адеметионин), назначаемый внутримышечно или внутривенно по 400–800 мг/сут в течение 2–3 недель с последующим переходом на пероральный прием по 800–1600 мг/сут в течение 1–3 месяцев.
Крайне важным аспектом лечения АБП является терапия и профилактика осложнения, что повышает качество жизни больных и снижает летальность. К числу этих осложнений относятся асцит, гепаторенальный синдром, печеночная энцефалопатия, варикозное расширение вен пищевода. Терапия с применением Гептрала может уменьшить или полностью устранить риск подобных осложнений.



