Пациенты после трансплантации почки нуждаются в частом контакте с врачом. Особенно это актуально для пациентов первого года после операции, когда наблюдается максимально высокий риск развития осложнений, обусловленных прежде всего высокими дозами иммуносупрессивной терапии (ИСТ). Ряд симптомов и состояний у реципиентов почечного трансплантата (ПТ) требуют немедленного реагирования для предупреждения развития дисфункции ПТ. В отсутствие своевременной коррекции подобных состояний происходит развитие дисфункции ПТ и требуется госпитализация пациента.
Телемедицина, включающая варианты веб-приложений, видеоконференций и устройств удаленного мониторинга, была предложена для улучшения доступа к медицинской помощи и улучшения результатов пациентов с заболеваниями почек [1–3]. Важной составляющей пациент-ориентированного подхода при ведении пациента является использование информации, полученной напрямую от него самого. Поиск подходов к вовлечению пациентов с помощью цифровых технологий ведется более 15 лет, однако именно сейчас с учетом повсеместного использования смартфонов становится особенно актуальным.
В настоящее время активный опрос пациента широко применяют в рамках научных исследований [4, 5]. Так, небольшое рандомизированное контролируемое исследование, проведенное в Германии, сравнивавшее стандартную помощь со стандартной, плюс ведение пациентов с использованием телемедицины выявили более низкий уровень госпитализаций и меньшее число случаев несоблюдения режима лечения пациентами, использовавшими телемедицину [6].
Ведение пациентов с телемедицинской поддержкой может трансформировать наблюдение пациентов после трансплантации почки, если оно обеспечивает мгновенное предоставление специализированных услуг даже для более сложных клинических задач. Это потенциально может снижать риск острых осложнений или отторжения ПТ и связанную с этим потребность в использовании медицинских услуг. Предполагается, что этот подход будет поддерживать стабильную приверженность лечению с улучшением качества жизни, способствуя лучшим долгосрочным результатам.
Материал и методы
Исследование проводилось на базе Научно-практического центра нефрологии и патологии трансплантированной почки ГКБ № 52 с использованием специализированной цифровой платформы ТРАНСПЛАНТНЕТ (разработчик – ООО «Телепат»).
В исследование были включены 52 реципиента ПТ. Критерием включения был возраст старше 18 лет. Критерии исключения: некомплаентность, отсутствие доступа к компьютеру или неспособность его использования. Набор пациентов был начат в августе 2019 г. и закончен в августе 2021 г. Период наблюдения пациентов составил 28±7 месяцев. Среди пациентов были 28 (54%) пациентов мужского пола и 24 (46%) – женского. Средний возраст пациентов составил 46,5± 9,0 лет. Средний срок после трансплантации почки – 34 (1,2; 50,3) месяца.
Платформа ТРАНСПЛАНТНЕТ использовалась следующим образом: лечащий врач после физикального обследования и осмотра пациента, подписания пациентом информированного согласия на ведение дистанционного мониторинга в постгоспитальный период и обработку персональных данных, составлявших врачебную тайну, подключал своего пациента к системе дистанционного мониторинга, назначая ему набор специализированных опросников и периодичность (календарь) направления их пациенту. Всем реципиентам ПТ назначался опросник «Общий мониторинг после трансплантации почки», который включал контроль мочеиспускания, контроль отеков, контроль работы сердца, тошноту, диарею, одышку, кашель, запор, изменения слизистой оболочки рта, кожные проявления, контроль слабости. Оценка наличия или отсутствия симптомов и степень их выраженности оценивались по шкале от 0 до 3–5 баллов.
Кроме того, принимая во внимание риск развития нейротоксичности ИСТ, ряду пациентов (особенно раннего срока после аллотрансплантации почки – АТП) назначали опросники «Контроль нервной системы», «Контроль эмоционального фона» и «Контроль депрессии». «Контроль нервной системы» содержал следующие показатели: боль, нарушение сна, головокружение, нарушение равновесия и походки, головная боль, ощущение онемения (покалывания) в конечностях, ослабление памяти, дрожь в конечностях или во всем теле. Оценка проводилась по шкале от 0 до 10 баллов. В «Контроль эмоционального фона» входили тревожность, подавленность, раздражительность. Оценку проводили по шкале от 0 до 10 баллов. «Контроль депрессии» включал показатели: пессимизм, утрату удовольствия, беспокойство, плач, утрату интересов, раздражительность, изменения аппетита, потерю энергии, усталость, изменения сна, утрату интереса к сексу. Оценку проводили от 0 до 3–5 баллов.
Частота отправки опросников пациенту могла варьироваться от 1 до 30 дней. У большинства пациентов «Общий мониторинг после трансплантации почки» оценивали каждые 3 дня, «Контроль нервной системы» – каждые 7 дней, «Контроль эмоционального фона» и «Контроль депрессии» – каждые 30 дней.
Помимо опросников пациенту назначали расписание измерений артериального давления, температуры, некоторым пациентам – измерение массы тела и количества выпитого и выделенного. Контроль этих измерений проводили в режиме 1–2 раза в день, в некоторых случаях реже.
Пациентам также можно было отправлять расписание приема лекарств, чаще всего – пациентам раннего срока после АТП для контроля точности приема лекарственных препаратов и коррекции ИСТ, которая особенно часто проводится именно в раннем сроке после АТП.
Пациент получал по электронной почте ссылку на активацию и подключение к системе ТРАНСПЛАНТНЕТ. Затем ему на электронную почту приходили опросники и расписания измерений и приема лекарств в соответствии с графиком, установленным врачом. Пациент отвечал на вопросы, отмечал результаты измерений, подтверждал прием лекарственных препаратов.
Если пациент в процессе заполнения опросника указывал опасный или критический симптом, он сразу же получал уведомление «Немедленно вызовите скорую помощь!» или «Срочно обратитесь к лечащему врачу!». Кроме того, в системе ТРАНСПЛАНТНЕТ также есть возможность для пациента прикрепить дополнительные документы (например, анализ, выполненный в другой лаборатории) и написать врачу сообщение, описав симптом или проблему, не включенные в опросник.
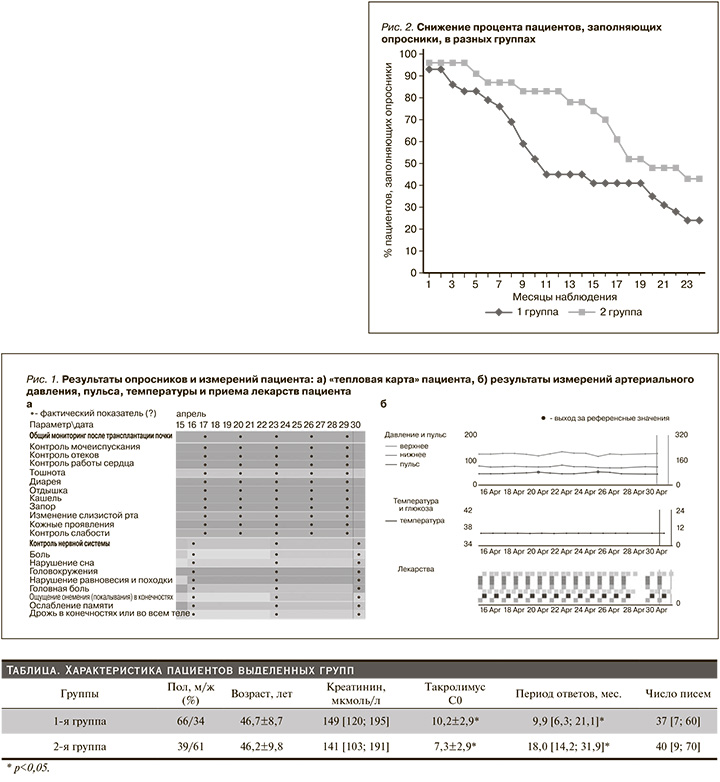
Результаты измерений и заполненных опросников сохранялись на закрытом сервере и периодически направлялись врачу в виде специальной «тепловой карты», демонстрирующей динамику симптомов пациента (рис. 1). Врач получал сводку по всем своим пациентам, состоявшим на дистанционном мониторинге. Сводка ранжировалась по общей тяжести отмеченных пациентом симптомов, чтобы врач мог оперативно оценивать состояние самых тяжелых пациентов и принимать соответствующие меры. При необходимости врач мог написать пациенту в системе ТРАНСПЛАНТНЕТ дополнительную рекомендацию, уточнить некоторые симптомы, пригласить на очный прием.
Результаты
Все пациенты были разделены на две группы в зависимости от срока после АТП. Первую группу составили пациенты со сроком до 12 месяцев после АТП, 2-ю – пациенты со сроком более 12 месяцев после АТП. В 1-ю группу вошли 29 человек, во 2-ю – 23. Пациенты выделенных групп не различались по возрасту, уровню креатинина крови на момент начала наблюдения и числу писем-обращений, написанных за период наблюдения (см. таблицу). Однако они различались по среднему уровню Такролимуса С0: у пациентов 1-й группы он был статистически значимо выше (р<0,05), т.к. у пациентов раннего срока после АТП целевые концентрации такролимуса были выше, чем у пациентов позднего срока.
При анализе данных пациентов в зависимости от периода ответов на присылаемые опросники обнаружено, что у пациентов раннего срока после АТП (1-я группа) период ответов был меньше и составил 9,9 [6,3; 21,1] месяца по сравнению с пациентами позднего срока после АТП (2-я группа) – 18,0 [14,2; 31,9] месяцев. Разница была статистически значимой (p<0,05).
При этом и скорость снижения процента пациентов, отвечавших на опросники, в представленных группах различалась (рис. 2). Пациенты раннего срока после АТП (1-я группа) быстрее прекращали отвечать на опросники – половина пациентов уже к 10-му месяцу наблюдения не заполняли опросники. У пациентов позднего срока после АТП (2-я группа) этот период был в 2 раза больше. только к 18-му месяцу наблюдения оставалось 50% пациентов, регулярно заполнявших опросники.
При анализе опросника «Общий мониторинг после трансплантации почки», максимальная сумма баллов которого составляла 38, у пациентов обеих групп сумма баллов была небольшой и статистически не различалась: в 1-й группе – 0,5 [0; 2], во 2-й группе – 1 [0; 7] балл (p>0,05). При анализе по группам каждого из симптомов было обнаружено, что большинство пациентов 1-й группы жаловались на отеки, тошноту и диарею. А у пациентов 2-й группы самыми распространенными симптомами были отеки, кашель, тошнота, нарушение мочеиспускания, диарея, одышка и слабость (рис. 3). Интересно, что число пациентов с жалобами на наличие симптомов из данного опросника было больше во 2-й группе, чем в 1-й. Но эта разница не достигала статистической значимости (р>0,05).
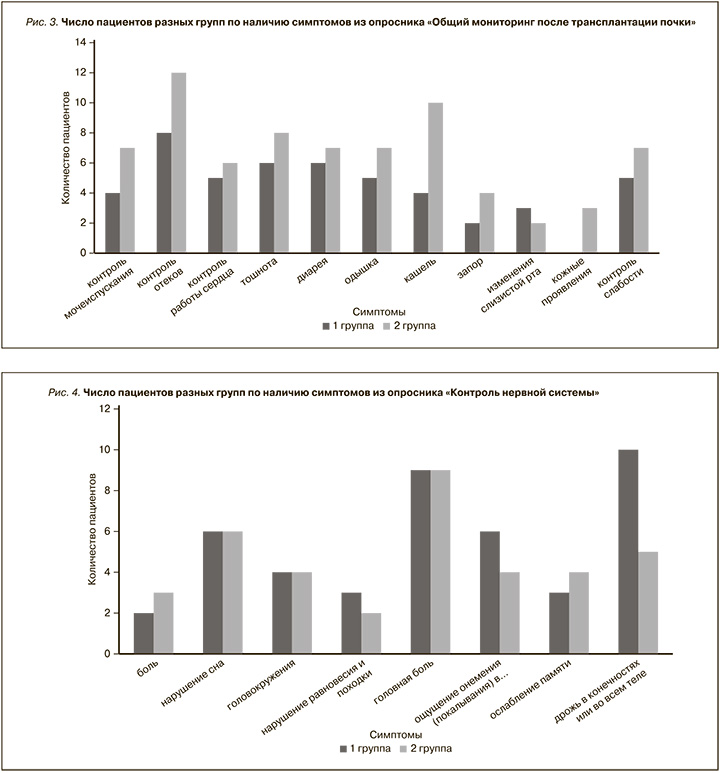
При оценке опросника «Контроль нервной системы» средняя сумма баллов в группах практически не различалась и составляла в 1-й группе – 3,0 [0; 6,0], во 2-й – 3,0 [0; 10,0] (р>0,05). Максимальная сумма баллов в этом опроснике была 80. Частота встречаемости разных симптомов данного опросника была практически одинаковой в обеих группах (рис. 4). Значимые различия наблюдались лишь при оценке дрожи в конечностях или во всем теле. Данный симптом в 2 раза чаще наблюдался у пациентов раннего срока после АТП.
Средняя сумма баллов опросника «Контроль эмоционального фона» у пациентов 1-й группы составила 2,4 [0; 4,0], 2-й группы – 3,2 [0; 4,8] при максимальном значении 30 (р>0,05). Среди симптомов данного опросника у пациентов раннего срока после АТП в 2 раза чаще наблюдались раздражительность и агрессия (рис. 5).

По результатам анализа опросника «Контроль депрессии» (максимальное число баллов – 36), в 1-й группе средняя сумма баллов составила 1,1 [0; 2,5], во 2-й – 2,7 [0; 5,0] (р>0,05). Интересно, что практически все симптомы данного опросника почти в 2 раза чаще наблюдались у пациентов позднего срока после АТП (рис. 6).
Кроме того, у пациентов выделенных групп обнаружена зависимость уровня Такролимуса С0 от наличия или отсутствия таких симптомов, как дрожь в конечностях или во всем теле и раздражительность/агрессивность (рис. 7). Так, при наличии дрожи в конечностях или во всем теле средний уровень Такролимуса С0 составлял 11,3±3,4 нг/мл, а в отсутствие этих симптомов – 7,8±2,5 нг/мл (р<0,05). Также статистически значимая была разница между уровнем Такролимуса С0 у пациентов с наличием раздражительности/агрессии (11,2±3,0 нг/мл) и пациентов без этих симптомов – 7,9±2,9 нг/мл (р<0,05).
Обсуждение
Мы провели ретроспективное наблюдательное исследование пациентов, которые использовали телемедицину как один из вариантов медицинской помощи. Анализ был проведен в группах пациентов раннего (до 12 месяцев) и позднего (более 12 месяцев) сроков после АТП. Такое выделение групп обусловлено различающейся ИСТ по целевым концентрациям такролимуса и циклоспорина, разной дозой глюкокортикостероидов (ГКС), необходимостью более частого лабораторного контроля (соответственно, и очного визита) у пациентов 1-й группы. Так, в нашем исследовании уровень Такролимуса С0 был значимо выше у пациентов 1-й группы. Как известно, на концентрацию такролимуса в крови влияет не только сам препарат, но и характеристика пациента, включая этническую принадлежность, возраст, пол, печеночную и почечную дисфункцию, а также генетические факторы, воздействующие на абсорбцию и метаболизм такролимуса [7]. У пациентов раннего срока после АТП целевые концентрации такролимуса в крови более высокие [8]. Кроме того, у этих пациентов наблюдаются частые колебания концентраций такролимуса, связанные с подбором ИСТ: повышение концентрации такролимуса за счет лекарственного взаимодействия на фоне постепенного снижения дозы ГКС, риска развития диареи на фоне приема препаратов микофеноловой кислоты, посттрансплантационных инфекционных процессов (клостридиальный колит, ЦМВ (цитомегаловирус)-колит и т.д.), погрешностей в диете [9].
Пациенты в раннем послеоперационном периоде еще только начинают привыкать к новому образу жизни после трансплантации, соответственно, у них могут чаще возникать вопросы по питанию, физической нагрузке и т.д. Однако, как мы видим, пациенты выделенных групп не различались по числу написанных писем с вопросами к лечащему вопросу: 37 [7; 60] писем в 1-й группе и 40 [9; 70] – во 2-й. Причина становится понятной при анализе периода ответов и оценки скорости снижения процента пациентов, отвечавших на опросники. Пациенты раннего срока после АТП в начале наблюдения задают много вопросов по разным проблемам и своему состоянию, регулярно отвечают на опросники. Однако с течением времени при благополучном течении послеоперационного периода и хорошем самочувствии они прекращают заполнять опросники (к 10-му месяцу наблюдения только половина пациентов продолжала отвечать на опросники). Ситуация с пациентами позднего срока после АТП несколько иная – они были более привержены отвечать на опросники (лишь к 18-му месяцу наблюдения оставалась половина регулярно отвечающих пациентов). А присылаемые им письма чаще содержали вопросы по возникновению новых симптомов либо обсуждению результатов анализов, выполненных в поликлинике по месту жительства.
Оценку и документирование состояния и самочувствия пациентов проводили с помощью «тепловой карты» ТРАНСПЛАНТНЕТ, формируемой автоматически на основе регулярно заполняемых пациентом опросников. Так, согласно нашим опросникам, можно было выделить пациентов с нарушением мочеиспускания, отеками, изменением работы сердца, тошнотой, диареей, одышкой, кашлем, изменениями слизистой оболочки рта, кожными проявлениями.
Изменения мочеиспускания могли быть обусловлены присоединением инфекции мочевых путей, развитием дисфункции ПТ. Инфекции мочевых путей возникают у 25% реципиентов ПТ в течение первого года после трансплантации почки и служат причиной 45% всех инфекционных осложнений [10]. Своевременное реагирование на данные симптомы с назначением пациенту очного визита для внеочередной сдачи анализа крови с определением уровня креатинина и мочевины, общего анализа мочи позволяло назначать соответствующее лечение.
При появлении отеков, согласно опросникам, проводилось уточнение по соблюдению пациентами бессолевой диеты, по динамике прибавки массы тела с последующим назначением или коррекцией диуретической терапии.
Желудочно-кишечные осложнения у реципиентов ПТ могут быть следствием типичных инфекций, встречающихся у пациентов данной группы, таких как ЦМВ-инфекция [11], а также опосредованного ИСТ повреждения слизистой оболочки желудочно-кишечного тракта [12]. Тяжелая диарея может приводить к потере массы тела, обезвоживанию, снижению качества жизни, повышению уровня креатинина в сыворотке крови и колебанию уровней иммунодепрессантов [13]. Требуются, во-первых, немедленное начало лечения этих симптомов, во-вторых, внеочередная сдача анализа крови на концентрацию такролимуса или циклоспорина в крови для проведения коррекции дозы препаратов в связи с высоким риском возникновения дисфункции ПТ вследствие нефротоксичности ИКН (в случае приема такролимуса) либо отторжения (в случае приема циклоспорина).
В случае появления кашля или одышки лечащий врач, как правило, связывался с пациентом для уточнения состояния с решением вопроса о назначении лечения (в случае нетяжелых форм респираторных инфекций или проявлений хронической сердечной недостаточности) или срочной госпитализации в стационар (при подозрении на пневмонию, декомпенсацию хронической сердечной недостаточности и других ургентных состояний). У пациентов в раннем сроке после АТП на фоне интенсивной ИСТ больше риск активации вирусных и оппортунистических инфекций [14].
Изменения слизистой оболочки полости рта у пациентов после АТП могут быть обусловлены развитием герпес-вирусной, грибковой инфекций, гиперплазией десен (на фоне приема циклоспорина), афтозными язвами, лейкоплакией [15]. Для уточнения диагноза пациенты присылали фотографии слизистой оболочки полости рта либо требовалась очная консультация с осмотром и решением вопроса о назначении лечения.
Кожными проявлениями у реципиентов ПТ чаще всего являются высыпания по типу акне на фоне приема ГКС (чаще у пациентов раннего срока после АТП в связи с приемом более высокой дозой ГКС). Но также известен онкогенный эффект ИСТ с повышенным риском развития базально-клеточного рака и плоскоклеточного рака кожи [16], а также саркомы Капоши [17]. Кроме того, изменения на коже могут быть аллергической реакцией, дерматитом, ксерозом и т.д. [18].
Оценка состояния нервной системы важна прежде всего для выявления нейротоксичности ИКН. Как известно, кальцинейрин экспрессируется в центральной нервной системе, особенно в нейронах, уязвимых к ишемическим и травматическим повреждениям [19], что обусловливает воздействие ИКН на центральную и периферическую нервную систему.
Тремор поражает примерно треть реципиентов ПТ с различной степенью тяжести симптомов – от легкой до тяжелой [20]. ИКН обусловливают развитие тремора из-за их влияния на истощение серотонина в нейронах [21]. У больных обычно развивается мелкий тремор покоя и тремор движений верхних конечностей, который может существенно влиять на повседневную активность. Хотя тремор может развиваться после воздействия любого ИКН, такролимус чаще ассоциируется с этим расстройством по сравнению с циклоспорином [22, 23].
Тремор, вызванный ИКН, обычно имеет дозозависимый эффект. Однако уровни в крови не всегда коррелируют с внутриклеточными концентрациями и фармакологическим эффектом [24]. Тремор, вызванный ИКН, также может развиваться у пациентов с уровнями такролимуса/циклоспорина в крови в «правильном» терапевтическом диапазоне, но чаще наблюдается именно при высоких концентрациях.
В нашем исследовании симптом «дрожь в конечностях или во всем теле» в 2 раза чаще наблюдался у пациентов раннего срока после АТП, что, видимо, обусловлено более высокими концентрациями такролимуса в крови пациентов данной группы. Была прослежена связь этого симптома со средним уровнем такролимуса в крови: при наличии симптомов средний уровень Такролимуса С0 составлял 11,3±3,4 нг/мл, а в отсутствие этих симптомов – 7,8±2,5 нг/мл (р<0,05). Это подтверждает нейротоксичный эффект высоких концентраций такролимуса в крови.
Риск побочных эффектов со стороны психики увеличивается с возрастом, наличием предшествовавших психических расстройств, дозой ГКС и продолжительностью лечения. Поведенческие расстройства также могут осложнять терапию ИКН. В исследованиях BENEFIT и BENEFIT-EXT сравнивали данные пациентов, получавших поддерживающую ИСТ с помощью белатацепта или циклоспорина, и обнаружили, что у пациентов в последней группе наблюдалась более высокая частота побочных эффектов, связанных с эмоциями, таких как депрессия, тревога или беспокойство [25]. В нашем исследовании практически все симптомы опросника «Контроль депрессии» почти в 2 раза чаще наблюдались у пациентов позднего срока после АТП, что, видимо, обусловлено продолжительностью лечения ГКС и ИКН.
Заключение
Проведенное исследование демонстрирует полезность и эффективность дистанционного мониторинга пациентов после трансплантации почки. Благодаря дистанционному мониторингу у пациентов удалось выявить серьезные симптомы, которые либо были проявлением дисфункции ПТ, либо могли приводить к развитию дисфункции ПТ в отсутствие своевременного лечения. Кроме того, дистанционный мониторинг помогает сокращать число очных приемов пациентов, что, с одной стороны, снизит риск инфекционных осложнений для пациента за счет уменьшения контактов друг с другом, с другой, увеличит экономическую эффективность проводимого лечения и уменьшит нагрузку на нефрологический стационар.



