Ингаляционная терапия (аэрозольтерапия) – метод лечения, заключающийся во введении аэрозолей лекарственных средств в дыхательные пути.
Согласно клиническим рекомендациям, основной путь введения лекарственных средств (ЛС) при бронхиальной астме (БА) и хронической обструктивной болезни легких (ХОБЛ) – ингаляционный [1, 2]. Ингаляционный путь введения лекарственных препаратов является основным при БА и ХОБЛ, поскольку создает высокие концентрации препарата в нижних дыхательных путях и позволяет сводить к минимуму системные побочные эффекты. Но при этом ингаляционный путь доставки является одним из самых сложных, т.к. неправильная техника ингаляции не только не обеспечит поступления адекватных доз препарата в легкие, но и может вызвать местные побочные эффекты за счет депозиции препарата в ротоглотке и трахее. Поэтому трудно не согласиться с утверждением J.B. Fink [3], что эффективность ингаляционной терапии больных хроническими заболеваниями легких на 10% определяется самим лекарственным препаратом, а на 90% – правильной техникой ингаляции.
Залогом успешной ингаляционной терапии служит не только правильный выбор препарата, но и такие факторы, как обучение пациента ингаляционной технике, выбор оптимальной системы доставки ЛС [4]. Идеальное устройство доставки предполагает достаточно высокую депозицию препарата в легких, надежность и простоту в использовании, возможность применения в любом возрасте и при тяжелых стадиях заболевания [5].
Преимущества и недостатки ингаляционной терапии
Преимущества ингаляционной терапии:
- непосредственное воздействие на орган-мишень – трахеобронхиальное дерево;
- высокая концентрация ЛС в легких;
- эффективность значительно меньшей (в 15–20 раз) дозы по сравнению с вводимой внутрь;
- отсутствие при местном применении побочных эффектов (неизбежны при системном действии препаратов);
- быстрый ответ на препарат;
- проникновение препарата в дистальные отделы дыхательных путей.
Наряду с преимуществами имеются и определенные недостатки:
- технологические сложности при изготовлении специальных лекарственных форм и ингаляционных устройств;
- необходимость обучения пациента технике выполнения ингаляции;
- зависимость эффективности лечения не только от самого препарата, но и от полноты его доставки к органу-мишени;
- возможность местного раздражающего действия;
- высокая доза депозиции препаратов в ротоглотке (около 80%);
- невозможность доставки больших доз ЛС;
- ошибки, допускаемые пациентами.
Правовой контроль применения ингаляционных устройств
В Европе ингаляционные устройства для аэрозольной терапии контролируются Европейским лекарственным агентством (ЕМА – European Medicines Agency,). В США контролирующим органом является Агентство по контролю пищевых продуктов и лекарственных препаратов (FDA – Food and Drug Administration).
Рекомендации Европейского респираторного общества (ERS – European Respiratory Society) и Международного общества по использованию аэрозолей в медицине (ISAM – International Society for Aerosols in Medicine) ERS/ISAM [6]
Врач, назначающий лечение, обязан:
- Знать типы устройств, доступных для доставки конкретных препаратов и классов препаратов.
- Оценить преимущества и недостатки каждого устройства.
- Выбрать устройства, которые пациент будет эффективно использовать.
- Выбрать устройства, одобренные законодательными органами.
- Научить пациентов правильному маневру вдоха, соответствующему назначенному устройству.
- Регулярно проверять технику ингаляций, применяемую пациентом.
- Во время каждого визита опрашивать пациента о соблюдении режима назначенной терапии.
- Не переводить больного на другое устройство без согласования с пациентом и без последовательного обучения технике использования нового устройства доставки [6].
Что должен знать специалист, назначающий аэрозольную терапию
Для ингаляций используют ЛС, разрешенные для применения в этих целях регуляторными органами.
Листок-вкладыш к препарату должен допускать или рекомендовать ингаляционный путь введения.
Независимо от личного опыта врача и рекомендаций т.н. старой школы в настоящее время для ингаляций не рекомендованы водорастворимые глюкокортикостероиды (преднизолон, гидрокортизон), аминофиллин, антигистаминные препараты, многие антибактериальные препараты.

Создание произвольных смесей препаратов для ингаляций, не оговоренных в листке-вкладыше или стандартах оказания медицинской помощи, недопустимо.
Для ингаляционной терапии используют следующие группы ЛС [6]:
Традиционные препараты для аэрозольной доставки:
- короткодействующие β2-агонисты (КДБА);
- длительнодействующие β2-агонисты (ДДБА);
- антихолинергические средства;
- ингаляционные глюкокортикостероиды (ИГКС);
- нестероидные противовоспалительные средства;
- антибиотики;
- муколитики.
Классификация ингаляционных устройств
Ингаляционные устройства можно разделить на пять групп [6]. Все типы ингаляционных устройств приведены в табл. 1.
Дозированные аэрозольные ингаляторы
ДАИ были введены в практику в 1956 г. как первые портативные многодозовые устройства для ингаляции бронходилататоров, и по сей день они остаются наиболее распространенными и часто назначаемыми [7]. При использовании ДАИ около 30–40% всех частиц аэрозоля, генерируемого ДАИ, находятся в пределах респирабельных размеров (<5 мкм). К преимуществам ДАИ относятся портативность, удобство в использовании, быстрота выполнения процедуры, низкая стоимость [8]. Однако проведение ингаляции с помощью ДАИ сопряжено с определенными трудностями, в частности с необходимостью синхронизировать вдох с нажатием на баллончик. Даже при адекватном применении ДАИ в легкие поступает только 10–15% от номинальной дозы [9]. Дети младше 7 лет, пожилые люди, а также пациенты, не способные производить адекватный маневр вдоха (при выраженной обструкции, заболеваниях, ограничивающих подвижность грудной клетки, и т.д.), не могут пользоваться ДАИ.
Спейсеры
Чтобы решить проблему координации вдоха с активацией ДАИ, было предложено использовать ДАИ с дополнительным устройством – спейсером. Это могут быть как простые приспособления, увеличивающие расстояние между ДАИ и ротоглоткой пациента, тем самым уменьшая депонирование ЛС в ротоглотке и снижая системную биодоступность, так и более сложные. Некоторые спейсеры снабжены односторонним клапаном (клапанные спейсеры), который позволяет пациенту ингалировать статичное облако аэрозоля. Клапанные спейсеры не требуют координации вдоха с активацией ингалятора и повышают депонирование ЛС в легких у тех пациентов, которые не могут добиться оптимальной координации при пользовании ДАИ [10].
Дозирующие аэрозольные ингаляторы, активируемые вдохом
В 1990 г. был создан ДАИ-АВ – Аутохалер (Easy Breathe). В России он зарегистрирован под названием «Легкое Дыхание». Такое ингаляционное устройство было разработано для того, чтобы решить проблему плохой координации вдоха с активацией ингалятора при использовании стандартных ДАИ [11]. Особенностью подобной ингаляционной системы является наличие пружинного механизма, который взводится при открытии колпачка. В ответ на вдох в течение 0,2 секунды происходит высвобождение фиксированной дозы препарата. Для активации ингалятора пациенту достаточно развить скорость вдоха около 10–25 л/мин. Эта характеристика устройства делает его доступным для большинства больных БА [12].
Порошковые ингаляторы
В 1889 г. в Великобритании F. Roe запатентовал устройство, предназначенное для ингаляции тонкодисперс-ного порошка фенола при БА и сенной лихорадке, а также для профилактики простудных заболеваний [13]. В 1940-е гг. были известны два ПИ со сходными названиями: Aerohalor применялся для ингаляции пенициллина, а Aerohaler — изопреналина. ПИ Спинхалер был разработан в 1971 г. для ингаляции высоких доз кромогликата натрия, содержащегося в капсулах [14].
Принцип действия ПИ заключается в том, что ингаляция ЛС осуществляется за счет силы вдоха пациента. Это исключает проблемы координации, характерные для ДАИ, и определяет широкое использование ПИ как средства доставки. Среди преимуществ ПИ можно отметить следующие:
- отсутствие пропеллентов (в отличие от ДАИ);
- отсутствие проблемы синхронизации;
- необходимая скорость вдоха 30–75 л/мин;
- низкая скорость выброса (фактически соответствует скорости вдоха);
- портативность, компактность;
- возможность использования у пациентов разных возрастных групп.
Бурному развитию новых ПИ способствовало принятие Монреальского протокола, направленного на ограничение производства и использования фреонов, поскольку ПИ справедливо рассматриваются как альтернатива фреонсодержащим ДАИ. Наконец, еще одним стимулом для развития ПИ стала новая стратегия ингаляционной доставки в организм некоторых препаратов для терапии внелегочных заболеваний – пептидов, протеинов, инсулина, наркотических и противоопухолевых препаратов [14].
В ПИ препарат находится в чистом виде или в соединении с носителем (лактозой, бензоатом натрия) и является крупнодисперсным (около 60 мкм). Во время вдоха часть ЛС вместе с турбулентным потоком, проходя через устройство ингалятора, измельчается до частиц респирабельных размеров. Эти частицы сухого вещества аэродинамически более стабильны, чем частицы ДАИ, поскольку транспортируются в легкие со скоростью потока воздуха, а не со скоростью струи пропеллента, не меняют своего размера и формы после высвобождения из устройства и обеспечивают большую депозицию ЛС в легких – до 40%.
Существует два основных типа ПИ: многодозовые и однодозовые.
В однодозовых ПИ активный препарат находится внутри желатиновой капсулы, которая перед каждой ингаляцией перфорируется специальными иглами. К однодозовым капсульным ПИ относятся как ранние модели (Ротахалер, Спинхалер), так и более современные ПИ (Аэролайзер, ХандиХалер). Достоинствами капсульных моделей ПИ являются точность дозирования, компактный размер устройств, защита лекарственной субстанции от влажности, возможность назначения большой разовой дозы препарата (до 20–30 мг) и низкая стоимость ингалятора.
К недостаткам можно отнести неудобство, связанное с частой заправкой ингалятора, и возможность технических проблем: неадекватного вскрытия капсулы, застревания ее в камере ингалятора, ингаляции частиц оболочки. При применении однодозовых ПИ довольно часто пациент недополучает дозу препарата [15]. Как правило, капсула вставляется в ингалятор перед каждой ингаляцией.
В новейших системах может находиться одновременно несколько капсул, что значительно упрощает использование ПИ.
Многодозовые ПИ в свою очередь подразделяются на резервуарные и блистерные. В многодозовых резервуарных ПИ препарат находится в едином контейнере, а каждая ингаляционная доза отмеряется при помощи специального дозирующего устройства. Данный тип ПИ отличается наибольшим удобством для больного: ингалятор содержит до 60–200 доз, требует минимальной подготовки перед использованием и может применяться в самых экстренных ситуациях. К резервуарным ПИ принадлежат Турбухалер, Циклохалер, Изихейлер, Новолайзер, Твистхейлер, Кликхалер и др. Условными недостатками резервуарных ПИ являются вариабельность дозы, ограничение дозы размером резервуара и более высокая стоимость, а также чувствительность к влаге. Абсорбция влаги из окружающей среды или во время использования ингалятора пациентом может повлиять на взаимодействие между частицами препарата или носителя и значительно уменьшить генерацию респирабельного аэрозоля.
Достоинства капсульных и резервуарных ПИ сочетают многодозовые блистерные ПИ, в которых несколько разовых доз упакованы в блистеры: в виде диска — Дискхалер (4 и 8 доз), полоски – Мультидиск (60 доз) или кассеты – Acu-Breathe (15 и 30 доз), Spiros (30 доз), Xcelovair (60 доз), Эллипта® (30доз). Блистерные ингаляторы успешно решают проблему защиты лекарственной субстанции от влаги и обеспечивают хорошую точность дозирования.
Ингаляторы, продуцирующие «мягкий» аэрозоль
В настоящее время выпускается только один ингалятор, продуцирующий «мягкий» аэрозоль, – Респимат Софт Мист. В основном он применяется в Германии для доставки комбинации фенотерола и ипратропия бромида (50 и 20 мкг в одной дозе соответственно). В России подобная форма доставки используется для ингаляций тиотропия бромида (2,5 мкг в одной дозе). Респимат расщепляет лекарственный раствор за счет механической энергии пружины. Пружина распрямляется, и раствор проталкивается через чрезвычайно тонкую форсунку. Это создает мельчайший туман. Минимальная скорость движения обеспечивает низкое депонирование во рту и глотке и относительно высокое в легких (~39%) [16].
Небулайзеры
Небулайзерная терапия – метод ингаляционной терапии, основанный на эффекте преобразования жидких форм лекарственных препаратов в мелкодисперсный аэрозоль.
Современные небулайзеры не похожи на своих предшественников, но надежно выполняют основную функцию – дозированную продукцию аэрозоля из раствора лекарственного препарата [17].
В настоящее время в зависимости от вида энергии, превращающей жидкость в аэрозоль, различают три основных типа небулайзеров:
- компрессорные (струйные) – использующие струю газа (воздух или кислород);
- ультразвуковые – использующие энергию колебаний пьезокристалла;
- мембранные (mesh) – использующие вибрирующую мембрану или пластину с множественными микроскопическими отверстиями (сито), через которую пропускается жидкая лекарственная субстанция [18].
Выбор ингаляционного устройства
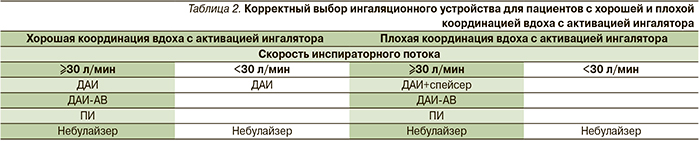
Выбор ингалятора для конкретного лекарственного препарата определяется устройствами, применяемыми для доставки данного препарата, а также способностью и желанием пациента использовать его правильно. ДАИ требуют хорошей координации вдоха с активацией ингалятора для оптимального депонирования лекарства, тогда как для ПИ необходим соответствующий инспираторный поток. В табл. 2 представлен порядок выбора ингаляционного устройства для больных с хорошей координацией вдоха и активацией ингалятора с достаточным инспираторным усилием [19]. К пациентам с плохой координацией вдоха и активацией ингалятора относятся дети и пожилые больные.
С целью создания практических рекомендаций по выбору устройства для ингаляционной доставки лекарств M.B. Dolovich и соавт. [20] провели систематический обзор отобранных рандомизированных контролируемых клинических исследований, в ходе которых сравнивалась эффективность применения различных типов ингаляционных устройств. В анализ было включено 131 исследование. Исследования были неоднородными по целям, дизайну и группам больных. Пациентов обучали правильно использовать ингаляционные устройства, что впоследствии строго контролировалось. Авторы приводят рекомендации по выбору ингаляционного устройства (ДАИ, ДАИ-АВ, ДАИ+спейсер/встроенный резервуар, ПИ, небулайзер малого размера) для различных препаратов (β2-агонистов, ИГКС, антихолинергических препаратов) в различных клинических ситуациях (отделении неотложной помощи, стационаре, амбулаторных условиях) при лечении БА и ХОБЛ.
Во всех клинических ситуациях выбор ингаляционного устройства зависит от следующих факторов:
- способности пациента правильно использовать ингалятор;
- предпочтений пациента;
- наличия необходимого ЛС в виде конкретных ингаляционных устройств;
- объемной скорости вдоха (скорость воздушного потока, которую демонстрирует больной на вдохе, в л/мин);
- внутреннего сопротивления (респираторного) устройства – скорость воздушного потока, необходимая для проведения ингалятора в действие или оптимальной ингаляции;
- возможности врача обучить больного правильному применению ингалятора и мониторировать приобретенные навыки впоследствии;
- стоимости терапии и возможности ее компенсации страховыми компаниями.
Был сделан важный вывод: в идеале пациент должен использовать только один тип ингалятора для всех назначенных ему ингаляционных ЛС. Это упрощает обучение больного и снижает вероятность ошибок [21]. Данное заключение соответствует рекомендациям Европейского респираторного общества и Международного общества по использованию аэрозолей в медицине при выборе ингаляционного устройства.
Заключение
Согласно клиническим рекомендациям, основной путь введения ЛС при БА и ХОБЛ – ингаляционный. Преимуществом ингаляционной терапии является создание высокой концентрации лекарства в дыхательных путях при минимальных системных побочных эффектах. Эффективность лечения ингаляционными препаратами во многом зависит от характеристики средства доставки и отношения пациента к ингалятору.
Выбор ингалятора для введения лекарственного препарата является ключевым фактором клинической эффективности любой ингаляционной терапии.



