В России у детей до настоящего времени ежегодно регистрируется более 40 млн случаев острых респираторных инфекций (ОРИ). Наиболее часто ОРИ болеют дети от 3 до 12 лет, особенно начинающие посещать дошкольные и школьные учреждения, что связано с массой контактов. Пик заболеваемости респираторными инфекциями у детей приходится на холодное время года (октябрь–апрель). Катаральный синдром в данном возрасте имеет более тяжелое течение, нередко вирусные инфекции осложняются присоединением вторичной бактериальной флоры или возникает обострение уже существующих хронических инфекций. Частые ОРИ способствуют снижению общей и местной резистентности организма, длительному рецидивирующему течению воспалительных заболеваний верхних и нижних дыхательных путей, предрасполагают к формированию гиперчувствительности к некоторым триггерам вирусной и бактериальной природы с последующим развитием аллергической патологии респираторного тракта, а также к задержке физического и психомоторного развития детей [1].
Склонность к частым респираторным заболеваниям у детей младших возрастных групп определяется незрелостью защитных реакций, утратой пассивного материнского и недостаточным уровнем приобретенного иммунитета, наличием высокого уровня контактов с многообразными инфекционными агентами. После перенесенной ОРИ у детей часто не формируется продолжительный стойкий иммунитет, отсутствует перекрестная защитная реакция к другим типам респираторных вирусов. В связи с этим ребенок может переболеть ОРИ до 8–12 и более раз в год, попадая в группу часто болеющих детей (ЧБД). Число детей, переносящих ОРИ, практически каждый месяц в детской популяции составляет от 15 до 50% [2, 6].
Возбудители ОРИ способны проникать в эпителиальные клетки слизистых оболочек верхних отделов дыхательного тракта и, размножаясь, вызывать в них дистрофические и воспалительные изменения. Разные виды респираторных вирусов обладают преимущественной тропностью к эпителию определенных участков дыхательных путей. Так, для вирусов парагриппа наиболее характерно поражение слизистой оболочки гортани; для аденовирусов – слизистой оболочки носоглотки с вовлечением в воспалительный процесс конъюнктивы глаз и лимфоидных образований; для респираторно-синцитиальных вирусов характерно воспаление слизистой оболочки мелких и средних бронхов и т.д.
До настоящего времени вопросы профилактики и лечения ОРИ у детей, особенно в отношении выбора эффективных и безопасных лекарственных средств, – одни из самых актуальных [4]. Современный фармакологический рынок предлагает огромный выбор средств лечения респираторных инфекций, но полипрагмазия при этом заболевании, к сожалению, является повседневной реальностью. Богатый ассортимент неспецифических лекарственных препаратов ставит нелегкую задачу выбора наиболее эффективного средства, при этом обладающего минимальным числом побочных эффектов. Ни одно из патологических состояний не может сравниться с ОРИ по числу осложнений, связанных с проводимой терапией [5, 7]. К другой серьезной проблеме относится неоправданное назначение антибактериальных препаратов (в среднем 52% детей с респираторными заболеваниями) [2]. Таким образом, применение лекарственных препаратов, обладающих комплексным клиническим действием, имеющих минимальный спектр побочных эффектов и доказанную эффективность, особенно актуально.
При решении данного вопроса неоценимую помощь врачу может оказывать разрешенный к применению в педиатрической практике препарат Тонзилгон Н (Бионорика). Это препарат растительного происхождения, в состав которого входят корень алтея, цветы ромашки, хвощ, тысячелистник, одуванчик, листья ореха и кора дуба. Тонзилгон Н выпускается в виде капель для приема внутрь и драже.
Целью нашего исследования стала сравнительная оценка эффективности применения препарата Тонзилгон Н в качестве монотерапии, комбинированной терапии с традиционно применяемой терапией боли в горле у детей на фоне ОРИ.
Материал и методы
Проведено рандомизированное проспективное клиническое исследование по сравнительной оценке эффективности монотерапии препаратом Тонзилгон Н, комбинированной терапии с включением данного препарата и традиционной симптоматической терапии детей, обратившихся в амбулаторных условиях к педиатру и/или врачу-оториноларингологу по поводу боли в горле на фоне клинических проявлений острой респираторной вирусной инфекции. Под наблюдением находился 71 ребенок в возрасте 2–12 лет. У 55 (88,7%) пациентов диагностировали явления острого фарингита, в 16 (11,3%) случаях регистрировали катаральный тонзиллофарингит. В исследование не включали детей с признаками острого бронхита, хроническими заболеваниями в стадии обострения, с наличием тяжелых сопутствующих заболеваний (язвенная болезнь желудка, 12-перстной кишки, сахарный диабет, хронические заболевания печени, почек и т.п.), с заболеваниями, нуждающимися в применении антибактериальных препаратов. После рандомизации и получения информированного согласия родителей на участие детей в наблюдения пациентов включали в одну из трех групп наблюдения.
 В основную группу исследования (1-я группа) вошел 31 ребенок, которому проводилась монотерапия Тонзилгоном Н. Из них мальчиков 18 (58%), девочек 13 (42%). Пациентов до 3 лет – 18,8%, детей дошкольного и школьного возраста – равномерно по 40,6%. Лекарственный препарат назначался согласно инструкции.
В основную группу исследования (1-я группа) вошел 31 ребенок, которому проводилась монотерапия Тонзилгоном Н. Из них мальчиков 18 (58%), девочек 13 (42%). Пациентов до 3 лет – 18,8%, детей дошкольного и школьного возраста – равномерно по 40,6%. Лекарственный препарат назначался согласно инструкции.
В острый период развития заболевания дети школьного возраста (6–12 лет) получали по 15 капель препарата 5–6 раз в сутки, дети 2–6 лет – по 10 капель 5–6 раз в сутки. После исчезновения острых симптомов заболевания (боль в горле) лечение препаратом продолжали в течение еще одной недели.
В этот период Тонзилгон Н назначался в возрастных дозировках 3 раза в сутки.
Во 2-ю группу (группа сравнения) были включены 20 детей, которым проводилась симптоматическая терапия ОРИ с применением муколитиков и местная терапия в виде промываний носа и ротоглотки растворами морской воды. Третья группа (20 детей) наряду с традиционной симптоматической терапией получала Тонзилгон Н (комбинированная терапия). Всем детям предписывался домашний полупостельный режим и обильное теплое питье.
Длительность наблюдения за пациентами составила 10 дней, в течение которых осмотр врачом проводился не менее 4 раз (1-й, 3, 6 и 10-й дни терапии). Для оценки клинического состояния каждого ребенка и динамики выраженности основных симптомов заболевания лечащим врачом использовалась 4-балльная шкала (0 баллов – симптом отсутствует, 1 – слабые проявления, 2 – умеренные, 3 – выраженная симптоматика, 4 балла – максимальная степень изменений).
В периоды между осмотрами педиатра родители самостоятельно вели дневники симптомов, в которых наряду со временем приема препаратов и его дозировкой отмечали наличие жалоб (нарушенное самочувствие, наличие симптомов интоксикации, боль в горле при глотании, головная боль, кашель, температура, осиплость голоса). Эффективность терапии оценивали на последнем визите на основании общепринятых методик (по первичным и вторичным критериям). К первичным критериям относили число пациентов, у которых уменьшились клинические проявления заболевания к исходу 3-х, 6 и 10-х суток болезни согласно балльной оценке. С помощью вторичных критериев оценивали среднюю длительность заболевания, среднюю продолжительность каждого симптома болезни, число пациентов, у которых отмечено развитие осложнений, требующих дополнительной терапии или госпитализации, общее число дней заболевания.
Статистически анализ результатов проводили по группам в отдельности для популяции всех пациентов, которые приняли хотя бы одну дозу исследуемого лекарственного средства и имели хотя бы одну оценку после исходной по параметрам эффективности и безопасности. Средние величины (М), стандартное отклонение (SD), медиану (Ме), а также различия между переменными рассчитывали с помощью программы «Биостат» (2009). Различия между сравниваемыми параметрами считали статистически значимыми при p<0,05.
Результаты исследования
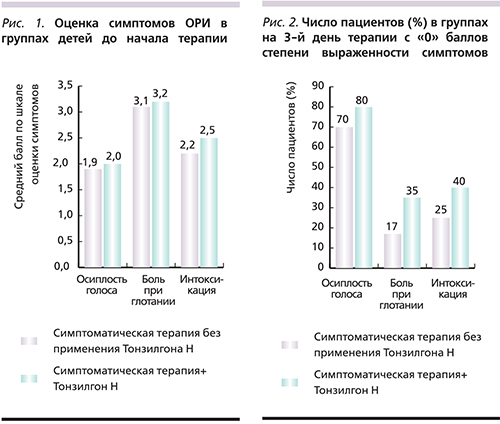
Степень и характер клинических проявлений респираторной инфекции у пациентов до начала терапии во всех трех исследуемых группах не имели достоверных различий (рис. 1). Проведенный анализ показал, что интенсивность симптома «боль в горле» определялась как «выраженная» у пациентов 1-й, 2 и 3-й групп и регистрировалась на уровне 3,3 балла, 3,1 и 3,2 балла соответственно. Симптомы интоксикации у детей оценивались в среднем как «умеренно выраженные» и равнялись 2,3 балла; 2,2 и 2,5 балла соответственно в трех исследуемых группах. Осиплость голоса была выражена слабо, ее оценка в баллах составила у детей 1-й группы 1,7 балла, 2-й – 1,9, 3-й группы – 2,0 балла. Интенсивность кашля у пациентов характеризовалась 1,8 балла, 1,9 и 1,8 балла соответственно в 1-й, 2 и 3-й группах исследования.
Редким симптомом была головная боль, балльная оценка которой у детей в наблюдаемых группах составила 1,1 балла, 1,2 и 1,1 балла соответственно. Степень повышения температуры у пациентов всех исследуемых групп была оценена как «слабая» и составила 1 балл (рис. 1)
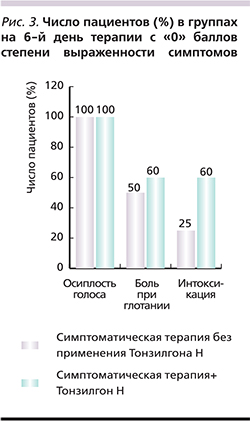
Анализ динамики клинической симптоматики, проведенный на третий день терапии в 1-й группе больных, получавших монотерапию Тонзилгоном Н, показал, что симптомы интоксикации (степень оценки 0) отсутствовали у 14 (45,0%) пациентов вне зависимости от половой принадлежности (рис. 2). У детей 2-й группы, которым проводилась симптоматическая терапия, только у 5 (25,0%) было зарегистрировано небольшое улучшение состояния, у остальных пациентов явления интоксикации сохранялись на прежнем уровне. В 3-й исследуемой группе больных на третий день терапии у 8 (40,0%) пациентов симптомы интоксикации отсутствовали.
Боль при глотании являлась одним из ведущих симптомов заболевания. При монотерапии Тонзилгоном Н у 5 (15,0%) пациентов 1-й группы к третьему дню терапии зарегистрирована положительная динамика и отсутствие данного проявления. Интенсивность боли в горле уменьшилась и оценивалась как «слабая степень» у 26 (85,0%) пациентов этой группы.
У 11 (55,0%) больных 2-й исследуемой группы отмечалось отсутствие улучшения самочувствия, сохранялась боль в горле прежней интенсивности, что потребовало дополнительной коррекции терапии и назначения лекарственных препаратов (Имудон, Лизобакт, Тантум Верде и др.). При комбинированной терапии ОРИ у детей с включением Тонзилгона Н (3-я группа) у 7 (35,0%) человек лечащий врач и родители отметили полное отсутствие данного симптома (0 баллов по шкале оценки). Головная боль у пациентов всех трех групп была слабой выраженности и разрешилась к 3-му дню вне зависимости от вида терапии (рис. 2).
Повышение температуры у пациентов 1-й, 2 и 3-й групп исследования регистрировалось до субфебрильного уровня и на 3-й день в 70,0% случаев во 2-й группе и 80,0% случаев – в 3-й группе. Осиплость голоса на 3-й день терапии отсутствовала у 70,0% пациентов в 1-й и 2-й группах и у 80% детей, получавших комбинированную терапию (3-я группа). Кашель сохранялся с одинаковой степенью интенсивности у всех исследуемых детей.
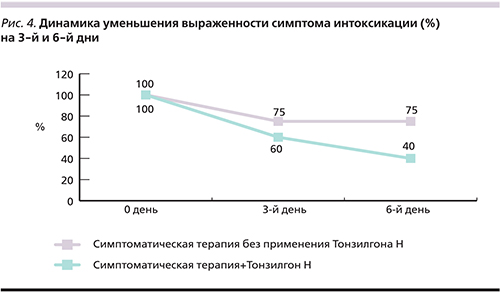
На 6-й день от начала терапии и наблюдения за больными слабовыраженные явления интоксикации и нарушение общего самочувствия сохранялись у 17 (55,0%) детей 1-й группы, во 2-й группе у 15 (75%) детей и у 8 (40%) пациентов 3-й группы, получавших комбинированную терапию ОРИ (рис. 3).
Боль в горле к 6-му дню монотерапии Тонзилгоном Н не регистрировали у 19 (61%) пациентов 1-й группы. У больных 2-й группы, получавших традиционную симптоматическую терапию, у 10 (50%) детей также не отмечали болевого симптома при глотании, однако слабовыраженный дискомфорт (боль) при глотании испытывали также 10 (50%) пациентов этой группы.
В 3-й группе, в которой больным проводилась комбинированная терапия с применением Тонзилгона Н, к 6-му дню 18 (90%) детей не имели боли в горле. У 2 пациентов этой группы на фоне положительной клинической динамики регистрировали слабовыраженный болевой симптом.
Осиплости голоса и повышения температуры к 6-му дню терапии не наблюдали во всех исследуемых группах пациентов. Кашель отсутствовал у 29 (94%) детей 1-й группы, у 16 (80%) 2-й. На 6-й день терапии кашель не регистрировали только у больных 3-й группы (рис. 3). При оценке состояния пациентов на 10-й день терапии врачом и согласно заполненным дневникам родителей основные симптомы респираторной инфекции, анализируемые в исследовании, были купированы у пациентов во всех группах. Побочных эффектов лекарственной терапии осложненного течения инфекций в группах наблюдения не зарегистрировали. Препарат Тонзилгон Н хорошо переносился детьми, на фоне его применения не было зарегистрировано ни одного побочного эффекта, благодаря чему отмечалась высокая приверженность лечению фитопрепаратом.
Обсуждение
Проведенный сравнительный анализ показал, что длительность и степень выраженности клинических проявлений ОРИ (интоксикация, температурная реакция, боль в горле, кашель и др.), не только приносящих страдания ребенку, но и оказывающих влияние на состояние его психоэмоционального тонуса, иммунологической резистентности, рост и развитие, напрямую зависят от характера проводимой терапии. Наше исследование установило, что использование в лечении респираторных инфекций у детей, протекающих с синдромом «боль в горле», только симптоматических средств, в большинстве случаев требует в дальнейшем дополнительных лекарственных назначений, что повышает лекарственную нагрузку на организм, увеличивает стоимость терапии. Включение в терапию ОРИ с синдромом «боль в горле» лекарственного препарата растительного происхождения (Тонзилгон Н) имеет клиническую эффективность в острый период инфекции, уменьшает степень выраженности основной симптоматики, избавляет врача от необходимости дальнейшего подбора и назначения других лекарственных препаратов. Наиболее выраженный клинический эффект получен нами у пациентов, в лечении которых с первого дня наряду с симптоматическими средствами использовали препарат Тонзилгон Н. При данной комбинированной терапии по сравнению с другими вариантами лечения отмечено более быстрое (p<0,05) купирование симптомов интоксикации, болей в горле и кашля (6-й день терапии), а головная боль и температурная реакция исчезали к 3-му дню заболевания.
Таким образом, сравнение эффективности препарата Тонзилгон Н при монотерапии и комбинированной терапии с традиционно проводимым симптоматическим лечением ОРИ у детей с синдромом «боль в горле» свидетельствует о целесообразности включения данного препарата в схему лечения. Применение препарата Тонзилгон Н клинически эффективно, во время исследования не было зарегистрировано ни одного побочного эффекта, связанного с применением препарата, что говорит о его высоком профиле безопасности. Тонзилгон Н хорошо переносится детьми, повышает приверженность терапии, позволяет минимализировать лекарственную нагрузку на организм ребенка и избегать полипрагмазии.



