Введение
Постинсультная реабилитация – совокупность мероприятий, направленных на продолжение лечения, начатого в остром периоде, а также начало мероприятий по компенсации любого повреждения, которое произошло в головном мозге. Основой служит раннее и безотлагательное начало специфических мероприятий еще в отделении неотложной терапии (реанимации) с целью скорейшего возвращения пациента к прежней жизни/социальной активности или его адаптации к личностному или социальному окружению. Данный подход позволяет пациенту быть вовлеченным в личную, семейную, профессиональную и социальную жизнь, что и характеризует процесс реабилитации [1]. Необходима ранняя вовлеченность пациента и родственников в реабилитационный процесс. Различают раннюю и позднюю (отсроченную во времени) реабилитацию. Данные понятия не имеют какого-то определенного биологического обоснования и используются по-разному. Однако они важны для формирования финансовых и социальных норм и правил.
С точки зрения научно-обоснованных рекомендаций по лечению, все большее значение приобретают понятия нейрорепарации, нейропластичности и нейровосстановления. Фаза нейропротекции почти полностью заканчивается в остром периоде инсульта, после чего начинается фаза нейрорепарации [2]. Поэтому задача предотвращения гибели нейронов в остром периоде инсульта постепенно замещается задачей реорганизации нейрональных систем [3]. Это подчеркивает непрерывность биологического процесса и клинического течения заболевания.
Многие эксперты, занимающиеся проблемой инсульта, уверены, что реабилитация отличается от интенсивной терапии не только с точки зрения времени, но и характером вовлеченности в нее пациента, причем за нее ответственны другие медицинские специальности и/или учреждения. Это не самая оптимальный форма организации с точки зрения продолжения лечения, однако в ежедневной практике ресурсы клиник неотложной помощи ограничены. Многие реаниматологи и неврологи до сих пор считают, что только они на «линии фронта», и уверены, что реабилитация находится далеко позади этой линии. Поэтому традиционно была оправданна идея отсроченной реабилитации инсульта, т.е. модель преемственной помощи. Тем не менее взгляд на биологический процесс течения постинсульного периода дает основание для очень ранней реабилитации (зачастую в первые 24 часа). Это создает некоторый диссонанс между фазами нейропротекции и нейровосстановления. Поэтому среди прочих мер важно начинать раннюю медикаментозную терапию (см. далее).
За последние 20 лет произошло два важных изменения:
- Появилась возможность более тщательной оценки репаративных процессов в головном мозге с улучшением параметров/качества нейровизуализации, показавших, что защита нейрососудистой структуры от ишемического повреждения имеет первостепенное значение. Пенумбра часто может сохраняться часами, иногда даже до 24 часов после инсульта, за счет реканализации сосудистых окклюзий, особенно в случаях хорошо развитых коллатералей. Пассивные (позиционирование, повышающее капиллярный кровоток благодаря временному увеличению тока крови) или активные методы (нейропротективные изменения в реканализированных артериях) должны быть пересмотрены. Появилась возможность применения репаративных лекарственных средств, и уже сейчас некоторые из них имеются в наличии. К их числу относят стволовые клетки, генную терапия, моноклональные антитела, экстракты из биологических тканей животных и другие ускорители восстановления [2]. В итоге с беспрецедентной точностью на молекулярном уровне мы можем визуализировать патофизиологические процессы в деталях и провести корреляцию с клинической картиной развития заболевания. Таким образом, обзор более чем 1000 исследований эффективности применения нейропротекторов при инсульте, показавший их безуспешность, должен быть пересмотрен и переоценен [2].
- В 2017 г. были подготовлены новые всемирные и европейские документы, определившие основные элементы реабилитации. Документ ВОЗ «Rehabilitation 2030» и «Report on Stroke in Europe» Европейского альянса по инсульту (SAFE), а также ESO SAFE – Программа действий по инсульту в Европе 2018–2030 (текущие и продолжающиеся конференции) определяют необходимость и важность реабилитации после инсульта. Документ ВОЗ «Global Stroke Bill of Rights» также предусматривает оценку, реабилитацию и социальную реинтеграцию как основное право пациента после инсульта [4].
Настоящие рекомендации по лечению пациентов после инсульта в подавляющем своем большинстве носят консенсус-ориентированный характер, т.к. большинство из них имеют небольшое или незначительное научное обоснование. Это связано с тем, что время начала вмешательства, его частота и интенсивность, а также продолжительность и сочетание с другими методами должны быть установлены отдельно в рамках контролируемых исследований, если кто-то требует, чтобы контролируемые исследования поддерживали эти рекомендации. Например, дискуссия по поводу возможных негативных эффектов слишком ранней мобилизации (менее чем через 24 часа) не ставит под сомнение раннюю мобилизацию (после первых 24 часов). Множество более детальных исследований проводится или планируется, многие уже завершены, но с небольшим количеством участников или без достаточной клинической достоверности в рамках первичных конечных точек. Поэтому сегодня существует необходимость в постепенном уходе от GRADE-концепции и других рекомендуемых принципов с учетом того, что большинство рассматриваемых рекомендаций имеют уровень доказательности III и класс рекомендаций С. Тем не менее есть данные с более высоким уровнем доказательности, которые будут рассмотрены далее. В других отношениях мы следуем Рекомендациям по наилучшей практике Канадского общества по борьбе с инсультом (Canadian Stroke Society) [5].
Инсультное отделение и ранняя реабилитация
Организация инсультного отделения позволяет снижать смертность и инвалидизацию. В хорошо оснащенном инсультном отделении осуществляются не только экстренная диагностика и терапия, но и целенаправленный уход и реабилитация.
Необходимо следующее:
- Наличие соответствующего персонала, включающего физиотерапевта, эрготерапевта, логопеда, а также психологов и социальных работников. В некоторых клиниках также внедрена музыкотерапия. Всем пациентам как можно раньше,должен быть проведен неврологический осмотр с использованием проверенных валидных шкал и опросников.
- Регулярные (как минимум еженедельные) консилиумы с ведущими неврологами и другими врачами для определения и документирования терапии, ее динамики. Важно принимать во внимание сопутствующие заболевания или предшествовавшие двигательные или другие ограничения. Обязателен скрининг на наличие депрессии, равно как и других психических расстройств.
- Когнитивный скрининг как важная часть диагностики и терапии.
- Строгое планирование процесса выписки с определением и упорядочиванием последующего наблюдения.
- Все обследования должны обсуждаться в самые ранние сроки госпитализации и, насколько это возможно, с родственниками, которые, по возможности, должны играть активную роль в реабилитации пациента.
- Пациенты с легкими и умеренными нарушениями также нуждаются в ранней реабилитации.
- Пациенты и родственники нуждаются в информации об инсульте, его причинах, лечении и профилактике. Это может происходить как индивидуально, так и в группах.
Поликлиника, дневной стационар и реабилитация в долгосрочном периоде
- Последующее наблюдение должно быть хорошо спланировано и быть максимально полным в соответствии с выписным эпикризом, проводиться не позже, чем через 3 месяца после выписки. Постинсультный проверочный лист является хорошо зарекомендованным способом достижения долгосрочных потребностей.
- Долгосрочное наблюдение и заполнение документации должны быть сделаны после 12 месяцев, а затем ежегодно в сроки более 3 лет.
- Ранняя выписка из стационара характерна в основном для Великобритании и Скандинавии. Восстановление после легких и умеренных нарушений достигается с помощью мобильной реабилитационной бригады в домашних условиях или в группе. Данная методика заменяет длительное нахождение в стационаре. Может быть показано, что чем раньше будет начата реабилитация в домашних условиях, тем большей вовлеченности пациента можно достичь, кроме того, такой подход, возможно, будет более экономически эффективным. Важно реально предложить необходимые лечебные ресурсы для эффективного проведения домашней реабилитации. В Австрии имеется небольшой подобный опыт за счет различных способов финансирования. Зарубежный опыт показывает, что госпитализацию можно сократить до 6 дней, при этом риск смертности и инвалидности снижается на 20% (уровень А). Пациенты с тяжелым инсультом, конечно же, имеют право на проведение реабилитационных мероприятий в стационаре.
Имеются данные, согласно которым выполнение упражнений по тренировке бытовых навыков в домашних условиях после выписки из стационара эффективно в течение года после перенесенного инсульта (уровень В). Различные виды реабилитации, включая занятия в поликлинике или дневном стационаре, также оказывают положительное влияние на независимость пациента в повседневной жизни в течение первого года после выписки.
Люди, перенесшие инсульт, часто страдают от мышечной слабости как пораженной, так и непораженной конечности, а также от снижения кардио-респираторной толерантности к физической активности. Физическая активность в постинсультном периоде способствует снижению инвалидизации, повышает толерантность к ходьбе, а также влияет на другие аспекты, связанные с инсультом (уровень В). Она в т.ч. улучшает когнитивные функции, настроение и уменьшает утомляемость. Программы физических упражнений должны разрабатываться и предлагаться всем перенесшим инсульт пациентам, кто физически способен ее выполнять совместно с программами по кардиореабилитации.
На данный момент уровень доступности реабилитационных отделений в разных странах различен, в некоторых из них пациенты после инсульта ограничены в получении направлений в реабилитационные отделения. В Австрии отделения реабилитации в настоящее время доступны для пациентов. По мнению экспертов неврологического сообщества, терапевтических отделений, специализирующихся на реабилитации, слишком мало, и они не функционируют надлежащим образом. В частности, это касается восстановления речевых нарушений, коммуникации, когнитивного статуса, настроения и мотивации. Различные способы логопедической коррекции, когнитивные тренинги должны чаще предлагаться пациентам в реабилитационных отделениях либо в структурах, ориентированных на домашнюю реабилитацию: терапевтические отделения, центры социального обслуживания. Следует отметить, что для многих пациентов требуется разработка индивидуального лечения вследствие коморбидности. Кроме того, каждый пациент должен получить письменный план последующего лечения сразу после выписки из стационара.
Поздняя реабилитация и реинтеграция
К наиболее распространенным проблемам пациентов относят в первую очередь нарушения когнитивных функций, настроения, психического состояния; отсутствие возможности получения регулярных реабилитационных мероприятий; занятия в основном являются результатом собственной инициативы пациентов и зависят от региональных особенностей. Как правило, пациенты уделяют больше внимания вторичной медикаментозной профилактике инсульта.
Спустя год после инсульта дальнейшая реабилитация недостаточно прописана. Стойкое нарушение жизнедеятельности, как правило, ведет к дальнейшему ухудшению и сопутствующим нарушениям. Поэтому лечение хронических нарушений должно быть продолжено под регулярным наблюдением невролога. Спастичность, болевой синдром, парестезии, изменения температурной чувствительности часто развиваются только на этапе хронизации. Именно в этих случаях Постинсультный проверочный лист играет важную роль как инструмент скрининга врача для выявления возможных/скрытых нарушений.
Несмотря на небольшое количество исследований, целевые специализированные тренировки, такие как упражнения на равновесие, обучение походке с использованием разных методов, тренировки для верхних конечностей, оказывали положительный эффект даже спустя год и более после инсульта. Хотя данные Кокрейновского обзора не убедительны, тем не менее в целом они показали положительный тренд [6]. Для многих молодых пациентов возвращение к работе служит фактором, определяющим качество жизни и необходимым источником дохода. Поэтому профессиональная реабилитация имеет решающее значение для многих больных.
Все пациенты и их родственники имеют право на неврологический осмотр через 6–12 месяцев, а затем регулярно минимум в течение 3 лет после инсульта.
Лечебные/реабилитационные мероприятия
Постинсультная реабилитация – это целенаправленный процесс, суть которого – помочь пациенту достичь наилучшего физического, когнитивного, эмоционального, социального и функционального уровней активности (уровень А).
Этот процесс начинается в ранний период (в течение 24–48 часов, уровень В) и осуществляется междисциплинарной, специально подготовленной командой в специализированном отделении (уровень А).
Оценка
Перед началом лечения проводится терапевтическая оценка (рекомендовано в течение 48 часов). Оцениваются конкретные функциональные ограничения каждого пациента по различным уровням – Международная классификация функционирования, жизнедеятельности и здоровья (МФК) [7]. Данная система позволяет классифицировать состояние пациента по отдельным системам организма и их функциональному состоянию, по уровню активности больного, его взаимодействия с социальной средой с учетом персональных и контекстуальных факторов. Выбор соответствующих стандартизованных инструментов зависит от основных повреждений, имеющихся у пациента, а также от удобства использования, релевантности и целей реабилитации (уровень B).
В табл. 1 представлены примеры стандартизированной методики оценки функциональных уровней, согласно МКФ.
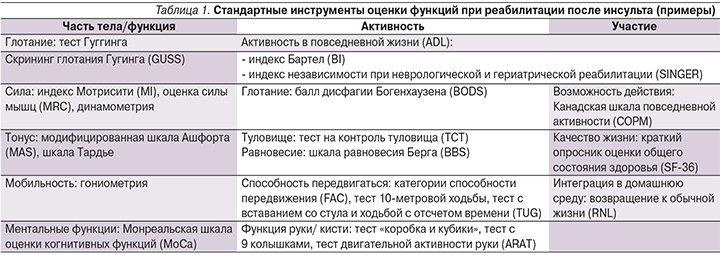
Постановка целей
По результатам оценки мультидисциплинарная бригада вместе с пациентом, учитывая окружающую его среду, определяют и согласовывают цели лечения, которые в дальнейшем могут регулярно пересматриваться. Хотя первоначальные реабилитационные назначения – в зависимости от возможностей пациента – выполняются на структурном и функциональном уровнях (например, мышечная силы, тонус, дыхание), цели по активности/ участию больного должны быть легко измеряемы и расписаны во времени, для возможности мотивации пациента, а также должны быть релевантными его состоянию (уровень A).
Реабилитационная оценка на ранних этапах может иметь прогностическое значение в отношении восстановления возможностей пациента (движение в пальцах/руке или возможность ходить – в течение первых 48 часов) или динамики восстановления активности в повседневной жизни (индекс Бартел – в течение 5 дней), что в дополнение к постановке реалистичной реабилитационной цели позволяет выбирать наилучший метод лечения для каждого отдельного случая.
Терапия в остром периоде/фаза мобилизации
Начало мобилизации зависит от различных факторов, таких как состояние жизненно важных функций, этиология инсульта и сопутствующие заболевания. Данные параметры индивидуально определяются реабилитационной командой. Очень ранняя мобилизация подразумевает активизацию пациента вне кровати в течение первых 24 часов [8]. Невозможно дать общих рекомендаций для каждого пациента, однако ранняя мобилизация, по-видимому, обеспечивает более короткое нахождение в отделении интенсивной терапии и лучший эффект по сравнению с длительной терапией (уровень В).
Восстановительный период / фаза реабилитации
За счет повышения активности нейропластичности в первые несколько недель или месяцев можно достичь наибольших функциональных изменений, поэтому интенсивная реабилитация может оказать наибольшее влияние в данный временной промежуток, но не всегда ограничивается лишь этим периодом. На практике, однако, пациенты проводят большую часть дня в одиночестве, в неактивном сидячем или лежачем положении в своей палате даже в специализированных учреждениях. Более высокая интенсивность тренировок с точки зрения их продолжительности в условиях стимулирующей (обогащенной) среды оказывает очевидные положительные эффекты на функциональное восстановление пациентов [9]. Рекомендуется несколько часов в день уделять занятиям в разных реабилитационных областях. Дополнительно следует предлагать пациентам самостоятельно проводить упражнения в мотивационной среде, предполагающей активное решение задач (уровень А).
Однако успех реабилитации зависит не только от интенсивности с точки зрения продолжительности, но и от ее содержания. Многие т.н. традиционные концепции, разрабатывавшиеся эмпирически, в большинстве случаев не показали полезности при индивидуальном подходе. Рекомендован комплексный подход, включающий индивидуально подобранные работающие методики, которые определены исходя из функциональных проблем пациента. Все чаще используются двигательные обучающие программы.
Данная концепция находит отражение во все бóльшем числе новых реабилитационных методик:
- Задания должны подразумевать активное решение проблем пациентом и регулярно возрастать по уровню сложности и интенсивности (уровень А).
- Необходимым условием обучения является достаточное количество повторений различных упражнений. К сожалению, требуемое количество повторений с трудом достигается в рутинной практике (уровень А).
- Задания должны быть релевантными (востребованными), понятными и мотивирующими пациента, а также подкрепляться обратной связью таким образом, чтобы пациент имел возможность планировать, выполнять и контролировать результаты своих действий (уровень А).
- Обучение – это задача и контекст-зависимый процесс, обладающий высокой специфичностью. Это означает, что задания хорошо выполняются и заучиваются, только когда они ориентированы на определенную окружающую среду. Переключение на другие задания или генерализованный подход не приемлемы. Занятия должны проходить в той среде, в которой потом эти навыки будут использоваться (уровень А).
Выводы
Нейрореабилитационные мероприятия эффективны, но убедительные данные о преимуществе какого-то конкретного метода (рекомендации) отсутствуют, что свидетельствует в пользу комплексного подхода [6].
Рекомендации
Огромное количество терапевтических методик могут быть применимы к широкому спектру синдромов, поэтому они должны использоваться в различных комбинациях для каждого конкретного пациента в зависимости от его физических, эмоциональных, двигательных и когнитивных способностей в широком разнообразии комбинаций (табл. 2).
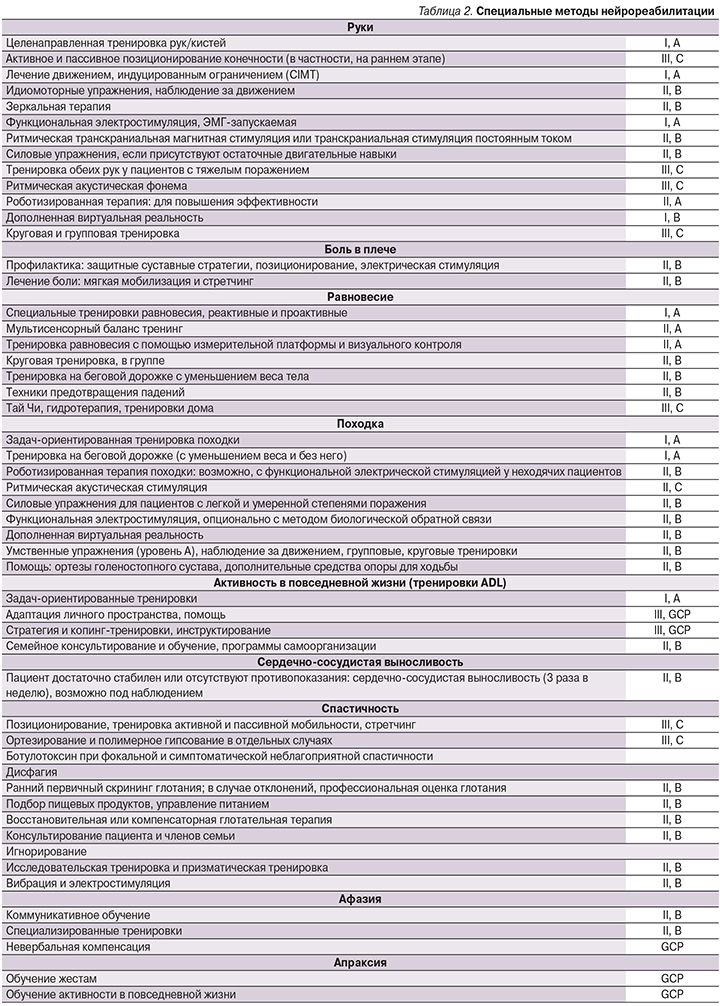
Лекарственные препараты
В некоторых случаях медикаментозное лечение может помочь и ускорить нейровосстановление. Например, есть данные о положительном влиянии леводопы [14] и антидепрессантов (селективных ингибиторов обратного захвата серотонина) [10] (класс II–III, уровень В–С).
В отношении специфических пептидных комплексов есть данные об успешном применении Церебролизина в дозе 30 мл курсом 3 недели и более (класс II, уровень В). Согласно этим данным, Церебролизин может улучшать восстановление функции верхних конечностей после инсульта [11–13].
Убедительных данных в отношении лечения больных после инсульта пищевыми добавками и витаминами нет. Терапия стволовыми клетками все еще находится на стадии изучения, исследования будут завершены в ближайшие годы.




