Острые и хронические цереброваскулярные заболевания (ЦВЗ) относятся к числу приоритетных проблем неврологии [1]. Хроническая ишемия головного мозга (ХИГМ) является наиболее частой формой ЦВЗ, имеющей тенденцию к нарастанию распространенности за последние 10 лет. Это связано с общей демографической ситуацией «постарения» населения, ростом в популяции лиц пожилого возраста и контингента населения с факторами риска ЦВЗ. По определению ВОЗ, в группу пожилого возраста входят лица 60–74 лет, старческого возраста – 75–89 лет, к долгожителям относятся лица ≥90 лет.
Старение – это генетически запрограммированный процесс, в котором основное значение придается состоянию сердечно-сосудистой системы. Этот период жизни характеризуется полиморфизмом патологических состояний у индивидуального пациента [2]. В структуре патологии лиц старшего возраста сердечно-сосудистые заболевания (ССЗ) оказывают наибольшее влияние на продолжи-тельность жизни и смертность. В рамках стратегии профилактики ССЗ большое значение придается определению суммарного сердечно-сосудистого риска (ССР). В последнее время активно развивается антивозрастная медицина (превентивная гериартрия), в задачу которой входит предупреждение развития заболеваний, связанных с возрастом и факторами ССР [2]. Среди этих факторов наибольшее значение имеет артериальная гипертензия (АГ), являющаяся чрезвычайно распространенным заболеванием, частота которого с возрастом повышается и достигает 80% среди лиц пожилого и старческого возраста. Ей принадлежит ведущая роль в этиопатогенезе ХИГМ, связанном с формированием эндотелиальной дисфункции и церебральной микроангиопатии, следствием которых становятся когнитивный дефицит и инсульт [6, 10, 11]. В старшей возрастной группе возрастает роль основных, дополнительных и независимых факторов риска развития инсульта [8, 9]. К их числу относятся сахарный диабет, дислипидемия, стенозирующий атеросклероз магистральных артерий головы (МАГ), кардиологическая патология, ожирение, курение [4, 9, 15]. Ишемическая болезнь сердца (ИБС), включая постинфарктный кардиосклероз (ПИКС), хроническая сердечная недостаточность, фибрилляция предсердий (ФП), патология клапанного аппарата сердца также тесно связаны с механизмами эндотелиальной дисфункции, мозговой гипоперфузии и церебральными микроэмболиями [14, 15]. На фоне имеющейся сосудистой неврологической патологии и соматических заболеваний в пожилом и старческом возрасте увеличивается роль хронического стресса и вероятность развития тревожно-депрессивных расстройств [3].
 Программы, проводимые в неврологии в аспекте превентивной гериартрии, должны включать своевременную диагностику факторов риска преждевременного старения и ССЗ, их коррекцию, разработку мер по первичной и вторичной профилактике инсульта, прогрессирования ХИГМ с учетом полиморфизма патологических состояний, характерного для старших возрастных групп, с целью увеличения численности активного населения и повышения качества жизни больных [2].
Программы, проводимые в неврологии в аспекте превентивной гериартрии, должны включать своевременную диагностику факторов риска преждевременного старения и ССЗ, их коррекцию, разработку мер по первичной и вторичной профилактике инсульта, прогрессирования ХИГМ с учетом полиморфизма патологических состояний, характерного для старших возрастных групп, с целью увеличения численности активного населения и повышения качества жизни больных [2].
Цель исследования состояла в изучении структуры факторов ССР у пациентов пожилого и старческого возраста.
Материал и методы
Проведен анализ 272 историй болезней неврологического отделения ГБУЗ ВГВ, в котором основной контингент больных составили лица пожилого возраста. Средний возраст больных – 67,8 (60–82) года. Среди госпитализированных пациентов значительно преобладали мужчины: 197 (72,4%) против 75 (27,6%) женщин. Эти данные подтверждают итоги территориально-популяционного регистра 2009–2014 гг. о преобладании заболеваемости инсультом в Республике Башкортостан среди лиц мужского пола – 3,2:1,6 (р<0,01). Все больные, находившиеся на лечении, имели подтвержденный диагноз ЦВЗ, ХИГМ II–III стадий. По данным анамнеза, 67 (24,6%) пациентов перенесли острое нарушение мозгового кровообращения, из них 15 (5,5%) повторно. Всем больным осуществлено комплексное клинико-инструментальное исследование соматического и неврологического статусов, анализировались данные их амбулаторных карт. При необходимости проводились консультации кардиолога, окулиста, эндокринолога. Пациентам с инсультом в анамнезе проведена оценка риска повторного инсульта по шкале ESRS (Essen Stroke Risk Score). По сумме баллов в диапазоне от 3 до 6 все постинсультные больные относились к группе высокого риска повторного инсульта, что учитывалось при планировании лечебно-профилактических мероприятий.
Результаты исследования
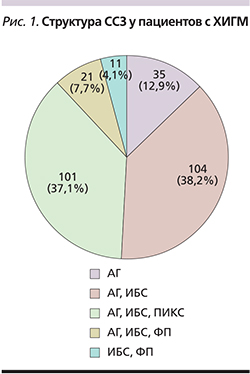
По совокупности заболеваний пациенты относились к группе высокого и очень высокого ССР (рис. 1).
Из приведенных данных видно, что лидирующим фактором ССР была АГ, которой страдал 261 (95,9%) госпитализированный больной, в т.ч. в сочетании с патологией сердца – 226 (86,5%) пациентов.
Среди 179 (65,8%) госпитализированных больных был проведен опрос об известных им факторах сосудистой патологии мозга, инсульта, инфаркта. Меньшая осведомленность в отношении указанной проблематики была у пациентов старшего возраста – от 78 до 82 лет. Только 23,5% из них смогли назвать 1–2 фактора риска, которыми оказались АГ и курение или употребление алкоголя. Нередко причиной инсульта пациенты называли стресс, «переживания», нарушения сна, головные боли.
 Как показал опрос, больные с диагнозом АГ систематически принимали антигипертензивные препараты – 38,3%. Монотерапию одним из антигипертензивных средств получали 28% больных, и по данным суточного мониторирования АД, она не позволяла достигать контроля АГ. При этом, по результатам суточного мониторирования АД, у 9 (6,03%) пациентов (в т.ч. с инсультом в анамнезе) на фоне антигипертензивной терапии отмечено снижение систолического артериального давления (САД) <110 мм рт.ст., что ассоциировано с риском ухудшения церебрального кровообращения и требовало коррекции лечения. В группе больных, перенесших острое нарушение мозгового кровообращения, частота регулярного приема антигипертензивных препаратов была выше – 72,6% пациентов, однако и здесь 16,4% больных получали лишь одно антигипертензивное средство, несмотря на рекомендации врачей, основанные на данных крупных международных исследований о влиянии антигипертензивной терапии на риск развития инсульта [1, 6, 12]. Как известно, оптимальная и адекватная коррекция АГ является одним из направлений первичной и вторичной профилактики ишемического и геморрагического инсульта. В частности, наиболее значительное снижение риска повторного инсульта (на 43%) в исследовании PROGRESS было достигнуто на фоне сочетанного приема периндоприла и индапамида, что послужило основанием рекомендовать эту комбинацию препаратов всем больным, перенесшим транзиторную ишемическую атаку или инсульт.
Как показал опрос, больные с диагнозом АГ систематически принимали антигипертензивные препараты – 38,3%. Монотерапию одним из антигипертензивных средств получали 28% больных, и по данным суточного мониторирования АД, она не позволяла достигать контроля АГ. При этом, по результатам суточного мониторирования АД, у 9 (6,03%) пациентов (в т.ч. с инсультом в анамнезе) на фоне антигипертензивной терапии отмечено снижение систолического артериального давления (САД) <110 мм рт.ст., что ассоциировано с риском ухудшения церебрального кровообращения и требовало коррекции лечения. В группе больных, перенесших острое нарушение мозгового кровообращения, частота регулярного приема антигипертензивных препаратов была выше – 72,6% пациентов, однако и здесь 16,4% больных получали лишь одно антигипертензивное средство, несмотря на рекомендации врачей, основанные на данных крупных международных исследований о влиянии антигипертензивной терапии на риск развития инсульта [1, 6, 12]. Как известно, оптимальная и адекватная коррекция АГ является одним из направлений первичной и вторичной профилактики ишемического и геморрагического инсульта. В частности, наиболее значительное снижение риска повторного инсульта (на 43%) в исследовании PROGRESS было достигнуто на фоне сочетанного приема периндоприла и индапамида, что послужило основанием рекомендовать эту комбинацию препаратов всем больным, перенесшим транзиторную ишемическую атаку или инсульт.
В отделении проведена необходимая коррекция антигипертензивной терапии, в основном с использованием комбинации диуретика (индапамид, гидрохлоротиазид) и ингибитора ангиотензинпревращающего фермента или блокатора рецепторов ангиотензина II, или блокатора кальциевых каналов. При назначении антигипертензивных средств учитывалось наличие у больных сопутствующей патологии МАГ, диабета и инсульта в анамнезе. При наличии стеноза МАГ ≥50% избыточное снижение САД <130–150 мм рт.ст. снижает перфузию головного мозга и повышает риск транзиторной ишемической атаки или инсульта [16, 17]. Клинически значимые стенозы прецеребральных каротидных артерий (50–63%), по данным ультразвуковых методов исследования, определены у 53 (20,4%) больных, в т.ч. у 12 пациентов, перенесших инсульт. Средние показатели уровня триглицеридов 2,8±0,7 ммоль/л и липопротеидов низкой плотности 4,2±0,4 ммоль/л у этих больных свидетельствовали о нарушении липидного обмена. Все они получали антитромбоцитарную терапию, преимущественно аспирином, и статины.
Сопутствующий АГ сахарный диабет 1 или 2 типов определен у 63 (23,2%) больных. Кроме того, за время нахождения в стационаре у 26 (9,5%) пациентов впервые была установлена гипергликемия натощак в среднем до 6,9±0,7 ммоль/л.
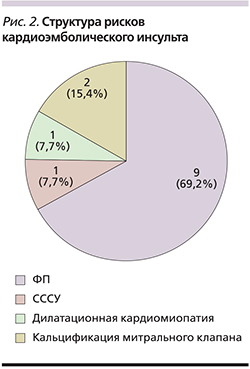
Значимым независимым фактором риска инсульта является ФП, которая чаще встречается среди лиц старше 60 лет [5, 13]. Из 237 пациентов с сопутствующей ЦВЗ-патологией сердца (32 [13,5%]) наблюдались у кардиолога по поводу ФП. Кардиогенная эмболия церебральных сосудов служит частой причиной ишемического инсульта (до 30–40% случаев), причем кардиоэмболический инсульт нередко осложняется геморрагической трансформацией очага ишемии с неблагоприятным жизненным и реабилитационным прогнозом, оставляет выраженный остаточный двигательный дефицит и имеет тенденцию к рецидивам [9]. Кардиоэмболический подтип ишемического инсульта на фоне ФП имел место у 9 (13,4%) постинсультных больных. Среди причин церебральной кардиоэмболии кроме ФП были также синдром слабости синусового узла (СССУ), дилатационная кардиомиопатия и кальцификация митрального клапана (рис. 2).
По данным литературы, инсульт нередко предшествует патологии сердца. До развития кардиоэмболического инсульта трое больных не наблюдались у кардиолога.
Приведенные данные обосновывают необходимость первичной и вторичной профилактики ишемического инсульта при наличии факторов риска кардиогенной эмболии, которые при ФП определяются шкалой вероятности развития тромбоэмболических осложнений CHA2DS2-VASc [5]. По результатам расчета суммарного балла рисков тромбоэмболии, определяется необходимость назначения антиагрегантной или антикоагулянтной терапии. Пациентам с ФП антикоагулянтная терапия рекомендуется при сумме баллов ≥1–2. В нашем исследовании результаты значений шкалы CHA2DS2-VASc у больных ФП находились в пределах 3–6 баллов: 23 (71,9%) – от 3 до 4 баллов; 5 (15,6%) – 6 и 4 (12,5%) – 2 балла. Итак, все пациенты с ФП имели риск тромбоэмболии, что обосновывало назначение антикоагулянтной терапии препаратами непрямого или прямого действия. Антикоагулянт непрямого действия варфарин в дозе от 2,5 до 3,5 мг до поступления в стационар принимали 8 (25%) пациентов с ФП, прямой антикоагулянт дабигатран (Прадакса) в дозе 300 мг/сут – 3 (9,4%) больных. Таким образом, антикоагулянтную терапию в качестве средства первичной и вторичной профилактики кардиоэмболического инсульта получали менее половины пациентов (34,4%) с ФП. Приверженность пациентов антикоагулянтной терапии остается низкой, в частности, из-за необходимости регулярного контроля международного нормализованного отношения (МНО) и ограничения потребления ряда пищевых продуктов при приеме варфарина. В связи с этим преимущество имеют современные антикоагулянты прямого действия – дабигатран, апиксабан. Эти препараты по эффективности сопоставимы с варфарином, минимально взаимодействуют с пищей и другими лекарствами, при их применении не требуется контроля МНО. При назначении антикоагулянтов учитывались риск кровотечений по шкале HAS–BLED, возраст больных, состояние функции почек. Пациентам старше 75 лет с потенциально высоким риском кровотечений (3 балла) Прадакса была рекомендована в сниженной дозе – 220 мг/сут [15].
При наличии многолетнего анамнеза АГ, дислипидемии, коронарной патологии, гипергликемии, избыточной массы тела большинство больных, находившихся на стационарном лечении, не придерживались рекомендаций по рациональному питанию и дозированным физическим нагрузкам, а 57 (24,6%) – продолжали курить. Курение отрицательно влияет на коагуляционный профиль крови и усиливает процессы атерогенеза, что повышает вероятность риска развития инсульта [7].
Заключение
Таким образом, ведущим фактором прогрессирования ХИГМ и риска развития инсульта в нашем исследовании стала АГ. Особенностью структуры факторов риска у больных пожилого и старческого возраста было наличие коморбидной сердечно-сосудистой патологии, дислипидемии, сахарного диабета. С целью предупреждения прогрессирования клинических проявлений ХИГМ, первичной и вторичной профилактики инсульта необходимо проводить адекватную рациональную антигипертензивную терапию с учетом возраста больных, сопутствующей патологии сердца, состояния МАГ и наличия диабета. Обоснован длительный прием антикоагулянтов, предпочтительно нового поколения, с индивидуальным подбором их дозировок при ФП. Отказ от курения, модификация образа жизни и питания наряду с проводимой терапией считаются одним из эффективных направлений профилактики ССЗ и инсульта в нейрогериартрии.



