Функциональная патология сегодня занимает ведущее место среди заболеваний желудочно-кишечного тракта (ЖКТ), практически вдвое превышая таковые органической природы. Безусловным лидером среди функциональных проблем со стороны ЖКТ является синдром раздраженного кишечника (СРК).
Согласно Римским критериям IV пересмотра (2016) [1, 2, 3], СРК определяется как функциональное расстройство, при котором периодические боли в животе наблюдаются в среднем по крайней мере 1 день в неделю за последние 3 месяца и связаны с двумя или более критериями: 1) дефекацией; 2) изменением частоты стула; 3) изменением формы стула. Критерии должны наблюдаться в последние 3 месяца после появления симптомов, не менее 6 месяцев перед диагностикой.
Однако настоящее исследование проводилось на основании Римских критериев III пересмотра (2006), определивших СРК как функциональное расстройство, при котором боль или дискомфорт в животе уменьшаются после дефекации, связаны с изменением частоты и консистенции стула, возникают не менее 3 дней в месяц на протяжении последних 3 месяцев при общей продолжительности жалоб не менее 6 месяцев [4]. Как видно из определения, последние Римские критерии конкретизируют временные рамки наличия симптомов у пациентов, не используют термин «дискомфорт», термин «уменьшается» заменен на «связано», т.к. часть пациентов не отмечают уменьшения болевого синдрома после дефекации, а наоборот, говорят об ухудшении, что, тем не менее, не исключает СРК.
Данные о распространенности СРК разнятся в зависимости от регионов земного шара с некоторым преобладанием в экономически развитых странах (9–48% населения), в среднем около 20% [5]. Анализ литературы выявляет закономерность ежегодного прироста заболеваемости СРК примерно на 1%.
Первые признаки болезни, как правило, появляются в молодом возрасте (24–41 год) [6], далее наблюдается стабилизация процесса без выраженного прогрессирования.
На сегодняшний день определено, что СРК является биопсихосоциальным функциональным кишечным расстройством, в основе которого лежит взаимодействие двух основных патогенетических механизмов: психосоциального воздействия и сенсорномоторной дисфункции, т.е. нарушения висцеральной чувствительности и двигательной активности кишечника [7–10]. Наличие болевого синдрома – отличительная черта СРК от функциональных запора и диареи. Ведущим аспектом, существенно снижающим качество жизни (КЖ) при любой патологии, в частности при СРК, является боль [10, 11]. Интересно, что именно СРК входит в число лидеров по снижению КЖ. Так, при сравнении КЖ пациентов с СРК, сахарным диабетом, острым инфарктом миокарда, артериальной гипертензией и депрессией (тест SF–36) установлено, что КЖ больных СРК сопоставимо с таковым у лиц с депрессивными расстройствами. Это послужило поводом для рассмотрения СРК как «маску» психосоматических заболеваний, результат личностной патологии и «болезненного поведения» [7].
В современной медицине используется постулат, говорящий о необходимости применения единого критерия для оценки состояний основных функций человека: физической, социальной, духовной. Этим критерием служит показатель КЖ [12]. По определению Всемирной организации здравоохранения (ВОЗ) качество жизни – это восприятие индивидами их положения в жизни в контексте культуры и системы ценностей, в которых они живут в соответствии с целями, ожиданиями, нормами и заботами. КЖ определяется физическими, социальными и эмоциональными факторами жизни человека, имеющими для него большое значение и влияющими на него. Качество жизни — это своеобразная степень комфортности человека как внутри себя, так и в рамках своего общества [13].
Согласно мнению Организации Объединенных Наций (ООН), социальная категория КЖ включает 12 параметров, из которых на первом месте стоит здоровье. Европейская экономическая комиссия систематизировала 8 групп социальных индикаторов КЖ, при этом здоровье также поставлено на первое место. Следовательно, КЖ, связанное со здоровьем, можно рассматривать как интегральную характеристику физического, психологического, эмоционального и социального функционирования больного, основанную на его субъективном восприятии [12, 14–16].
Таким образом, изучение показателей и коррекция сниженного КЖ пациентов через купирование болевого синдрома являются одной из важных составляющих ведения больных СРК [14].
 Арсенал лекарственных средств, используемых для лечения больных СРК, включает несколько классов препаратов, среди которых на первом месте находятся средства борьбы с абдоминальной болью – спазмолитики. Одним из препаратов, применяющихся при лечении функциональных расстройств ЖКТ, является тримебутин. Согласно инструкции по применению, тримебутин показан при болевом синдроме, явлениях запора и диареи. Тримебутин успешно применяется на протяжении ряда лет в терапии функциональных заболеваний органов пищеварения, в частности при СРК, о чем свидетельствуют результаты клинических исследований [17, 18].
Арсенал лекарственных средств, используемых для лечения больных СРК, включает несколько классов препаратов, среди которых на первом месте находятся средства борьбы с абдоминальной болью – спазмолитики. Одним из препаратов, применяющихся при лечении функциональных расстройств ЖКТ, является тримебутин. Согласно инструкции по применению, тримебутин показан при болевом синдроме, явлениях запора и диареи. Тримебутин успешно применяется на протяжении ряда лет в терапии функциональных заболеваний органов пищеварения, в частности при СРК, о чем свидетельствуют результаты клинических исследований [17, 18].
Кроме того, в медикаментозном комплексе имеются препараты, влияющие на моторную активность кишечника и сенситивность, средства для нормализации бактериальных взаимоотношений (антибиотики, про- и пребиотики), имеющие свой класс доказательности, свои преимущества и недостатки [19–21]. До недавнего времени в распоряжении врача отсутствовали комбинированные средства, способные корректировать основные патогенетические механизмы СРК и решать главную задачу лечения: купирование боли и диспепсических расстройств. Новый лекарственный препарат, Колофорт®, в состав которого входит комбинация релиз-активных антител к мозгоспецифическому белку S100 (РА АТ S100), гистамину (РА АТ к гистамину) и к фактору некроза опухоли α (РА АТ ФНО-α), создан для лечения функциональных расстройств ЖКТ [22]. Сочетание трех активных компонентов позволяет осуществлять комплексное воздействие на центральные и периферические звенья патогенеза функциональных нарушений кишечника, в частности СРК. Опубликованные результаты многоцентрового плацебо-контролируемого исследования Колофорта® на больных различными клиническими вариантами СРК свидетельствуют о достоверной клинической эффективности препарата по сравнению с плацебо [23].
Проведено сравнительное неинтервенционное исследование, целью которого было изучение клинической эффективности и показателей КЖ на фоне терапии СРК препаратом Колофорт® и тримебутином (Тримедат®).
Материал и методы
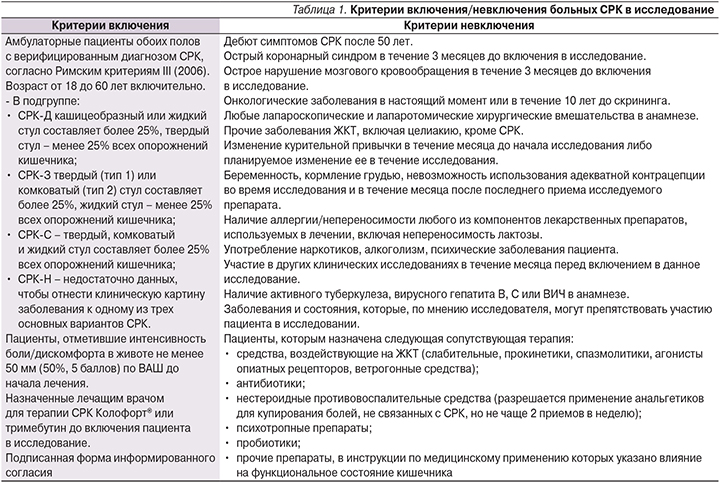
В исследовании приняли участие 149 пациентов обоего пола в возрасте от 18 до 60 лет включительно с установленным диагнозом СРК в соответствии с Римскими критериями III (2006), которые соответствовали критериям включения/невключения (табл. 1).
Помимо объективного обследования для оценки клинической динамики симптомов СРК использовались визуальная аналоговая шкала (ВАШ), Бристольская шкала формы стула, расчет суммарного индекса висцеральной чувствительности по шкале VSI (Visceral Sensitivity Index) и опросник для оценки КЖ при СРК (IBS-QoL – Irritable Bowel Syndrome – Qualityof Life).
Для оценки эффективности лечения использовались следующие критерии.
Первичные критерии:
- доля пациентов, у которых отмечено снижение выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5;
- доля пациентов, у которых отмечено снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5.
Вторичные критерии:
- доля пациентов в подгруппе СРК-Д с изменением типа стула по Бристольской шкале формы стула до 5 и менее (в среднем за неделю);
- динамика изменения типа стула по Бристольской шкале;
- доля пациентов в подгруппе СРК-З, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем;
- динамика числа актов дефекации у пациентов с СРК-З;
- динамика результатов оценки по ВАШ;
- динамика значений суммарного балла индекса висцеральной чувствительности по опроснику VSI;
- динамика значений суммарного балла опросника качества жизни IBS-QоL.
Наличие, характер и продолжительность побочных эффектов, их связь с приемом препарата и выраженность были отнесены к критериям безопасности.

В течение исследования пациенты осуществляли 5 визитов к врачу: визит 1 (день 0), визит 2 (день 14±3), визит 3 (день 28±3), визит 4 (день 56±3) и визит 5 (день 84±3). На каждом визите наряду с объективным обследованием пациента (измерение массы тела, артериального давления, частоты сердечных сокращений, температуры тела) и оценкой безопасности проводилось заполнение соответствующих опросников и шкал. Кроме того, на визите 1 все пациенты подписывали установленную форму информированного согласия при условии соответствия критериям включения. Первая выдача исследуемого препарата осуществлялась на визите 1. На визитах 2, 3 4 пациентам выдавалось количество препаратов, рассчитанное до следующего визита. Все пациенты получали инструктаж о необходимости принести неиспользованный препарат и/или пустую упаковку на следующий плановый визит.
Для обработки полученных данных использовались стандартные методы описательной статистики, включая дисперсионный анализ, метод Generalized estimating equations (GEE), расчеты t-критерия Стъюдента, точного критерия Фишера, χ2-критерия, критерия Кохрана–Мантеля–Хенсзеля (модификация χ2-критерия для множественных сравнений), критерия Фаррингтона–Мэннинга.
Результаты исследования
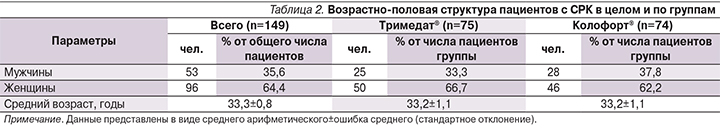
В соответствии с назначенной терапией пациенты были распределены в 2 группы: 74 пациента составили группу Колофорта®, 75 человек – группу Тримедата®. Возрастно-половая структура пациентов с СРК в целом и по группам представлена в табл. 2.
Согласно классификации СРК по типам в зависимости от преобладающих нарушений стула, пациенты в сравниваемых группах распределились таким образом, что отмечено доминирование больных СРК-Д и СРК-З – 53 и 31% в группе Колофорта®, 44 и 39% в группе Тримедата® соответственно.
В сравниваемых группах не было выявлено достоверных различий по выраженности болевого синдрома (ВАШ), индекса висцеральной чувствительности (VSI) и качества жизни (IBS-QoL), из чего следует, что по возрастному, половому составу и исходным клиническим характеристикам обе группы были сопоставимыми.
В качестве оценки эффективности лечения пациентов с СРК использовался анализ влияния сравниваемых препаратов на болевой синдром, паттерн стула, висцеральную гиперчувствительность и КЖ.
Боль при СРК – это ключевой симптом, традиционно рассматриваемый в качестве терапевтической мишени [24]. Поэтому в качестве первичных (снижение выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5) и вторичных (снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5) критериев эффективности лечения использовалась оценка влияния препаратов на болевой синдром.
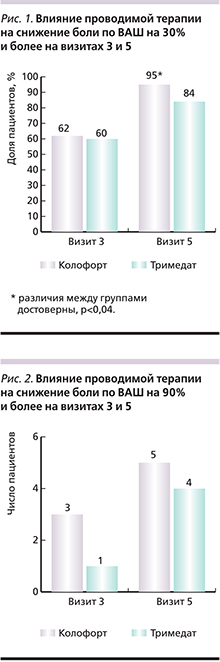
К визиту 3 доля пациентов со снижением боли по ВАШ на 30% и более была сопоставимой в группе Колофорта® (62%) и группе Тримедата® – 60% (χ2=0,07; p=0,7867; критерий Фаррингтона–Мэннинга (nonferiority test): z=1,53; p=0,0633). Однако к визиту 5 продемонстрировано статистически значимое превосходство терапии Колофортом® по сравнению с Тримедатом®: 95 против 84% пациентов соответственно (χ2=4,4; p=0,0368; критерий Фаррингтона–Мэннинга (nonferiority test): z=3,7; p=0,0001; рис. 1).
Для более детальной оценки эффективности Колофорта® и Тримедата® в отношении боли дополнительно был проведен анализ динамики снижения боли на 30% и более на визитах 3 и 5 с учетом типа СРК. Так, на визите 3 в обеих группах выявлена сопоставимая динамика – купирование боли более чем на 30% наблюдалось приблизительно у трети пациентов с СРК-Д (35% в группе Колофорта® против 31% в группе Тримедата®), у 16% пациентов с СРК-З в каждой группе и в 3–9% при других типах СРК (критерий Кохрана–Мантеля–Хенсзеля: χ2=0.0; p=0,9790). На визите 5 в группе Колофорта® снижение выраженности болевого синдрома на 30% и более наблюдалось у всех пациентов с СРК-З и СРК-С (у 31 из 31 пациента и у 8 из 8 пациентов соответственно) и у большинства пациентов с СРК-Н (7 из 8 пациентов), тогда как в группе Тримедата® – лишь в подгруппе СРК-Н (у 11 из 11 пациентов).
При оценке доли пациентов, у которых отмечено снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5, получены сопоставимые данные в обеих группах с тенденцией к лучшим показателям в группе Колофорта® (рис. 2).
Уменьшение боли на 90% и более было достигнуто 2 пациентами с СРК-Д в группе Колофорта® уже к визиту 3, а к визиту 5 – еще 2 пациентами с СРК-Н. В группе Тримедата® данный результат был достигнут лишь 1 пациентом с СРК-Н к визиту 3 и еще 2 пациентами с СРК-С к визиту 5. Таким образом, Колофорт® продемонстрировал как более выраженное влияние на уменьшение болевого синдрома в целом, так и стабильный эффект вне зависимости от типа СРК по сравнению с Тримедатом®.

Еще одним вторичным критерием эффективности терапии Колофортом® и Тримедатом® стал параметр, отражающий динамику паттерна стула на фоне лечения.
Анализ динамики изменений типа стула по Бристольской шкале формы кала у пациентов с СРК-Д свидетельствовал о превосходстве Колофорта® по сравнению с Тримедатом® уже к визиту 2, достигшем статистической значимости к визиту 5. Нормальный стул наблюдался у 90% пациентов группы Колофорта® против 58% пациентов группы Тримедата® (критерий Кохрана–Мантеля–Хенсзеля: χ2= 8,4; p=0,0038; точный критерий Фишера: p=0,0024). При исходно идентичных показателях в обеих группах иная динамика нормализации стула наблюдалась у пациентов с СРК-Д, получавших Тримедат®: к визиту 3 пациентов с нормальным типом стула было 48%, к визиту 4 их число достигло только уровня группы Колофорта® на визите 3 (64%) (рис. 3).
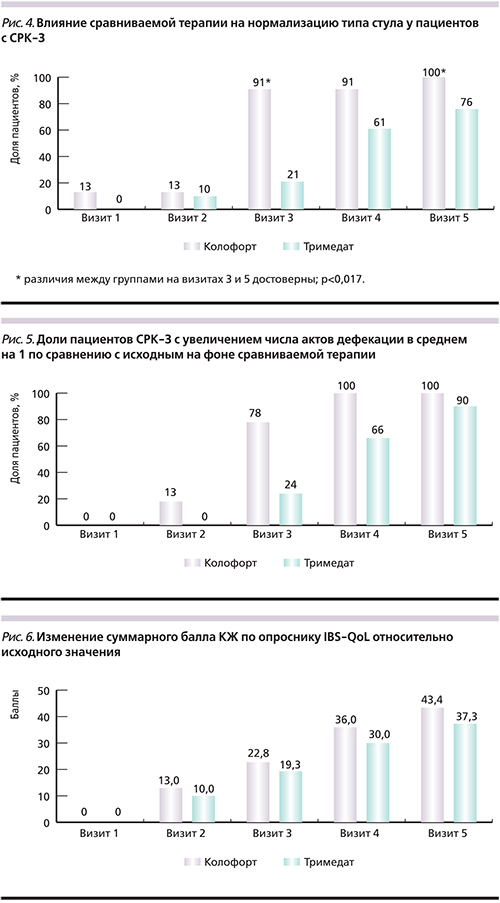
Оценка динамики типа стула по Бристольской шкале формы кала у пациентов с СРК-З также продемонстрировала статистически значимое преимущество Колофорта® по сравнению с Тримедатом® (критерий Кохрана–Мантеля–Хенсзеля: χ2=29,1; p=0,0001). Оба препарата показали положительную динамику, но уже к визиту 3 доля пациентов с нормальным стулом в группе Колофорта® была более чем в 4 раза больше, чем в группе Тримедата®. К визиту 5 нормальный тип стула отмечен у всех пациентов группы Колофорта®, тогда как в группе Тримедата® достиг значения лишь в 76% (точный критерий Фишера: визит 3, p=0,0001, визит 5, p=0,0135; рис. 4).
Таким образом, Колофорт® продемонстрировал достоверно превосходящую Тримедат® эффективность во влиянии на нормализацию типа стула по Бристольской шкале формы кала у пациентов с СРК-Д и СРК-З. К визиту 5 на фоне лечения Колофортом® нормальный тип стула отмечался у подавляющего большинства респондентов, тогда как в группе Тримедата® таковых было около половины. При этом эффективность Колофорта® была более выраженной как по срокам, так и по стабильности изменений [22, 25, 26].
При оценке динамики частоты дефекаций в подгруппе СРК-З определялась доля пациентов, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем. Оказалось, что результаты группы Колофорта® значимо превосходили таковые группы Тримедата®, начиная уже с визита 2 достигнув максимума к визиту 4 (метод GEE – Generalized estimating equations: Z=4,8; p=0,0001). В группе Тримедата® увеличение частоты стула при СРК-З происходило значительно медленнее начиная только с визита 3, а на визите 5 улучшения достигли 90% пациентов, тогда как в группе Колофорта® уже на визите 4 отмечалась его нормализация у 100% пациентов (рис. 5).
Динамика актов дефекации у пациентов с СРК-З также свидетельствовала в пользу большей эффективности Колофорта® (4,6±0,9 раза в неделю против 3,2±0,6 раза в неделю в группе Тримедата®). При этом прирост частоты дефекаций у пациентов с СРК-З на фоне Колофорта® начинался на 2 недели раньше и был более выраженным по сравнению с Тримедатом®, достигнув к окончанию исследования разницы между группами в 2 раза [22, 23, 27].
Таким образом, положительная динамика увеличения частоты стула при приеме Колофорта® отмечалась быстрее, а частота дефекаций превышала таковую при приеме Тримедата® в итоге почти в 1,5 и в 2 раза более интенсивном ее приросте относительно исходных параметров у пациентов с СРК-З.
В ходе данного исследования проводилась оценка влияния сравниваемых препаратов на патофизиологический механизм СРК, обусловливающий возникновение и интенсивность боли, выраженность моторных расстройств – висцеральную гиперчувствительность.
При анализе динамики значений висцеральной гиперчувствительности по шкале VSI была установлена статистически значимая тенденция к превосходству терапии Колофортом® по сравнению с Тримедатом® (фактор «Группа» F1/146=4,3; p=0,0411; фактор «Визит» F3/438=306; p=0,0001; фактор «Группа*Визит» F3/438=2,8; p=0,0725; ковариата «Визит 1» F1/146=263; p=0,0001). Таким образом, как Колофорт® так и Тримедат® способны нормализовывать висцеральную гиперчувствительность.
Положительные результаты влияния сравниваемой терапии на клиническую симптоматику и висцеральную гиперчувствительность нашли отражение в динамике суммарного балла опросника КЖ (IBS-QoL). При оценке его динамики в обеих группах выявлены сопоставимые результаты (фактор «Группа» F1/146=2,1; p=0,1459; фактор «Визит» F3/438=0,8; p=0,4409; фактор «Группа*Визит» F3/438=0,5; p=0,6112; ковариата «Визит 1» F1/146=223; p=0,0001; табл. 3).
Вместе с тем при сопоставимом в целом влиянии исследуемых препаратов на КЖ пациентов по изменению суммарного балла IBS-QoL относительно исходного значения было установлено, что изменения уровня КЖ при приеме Колофорта® были более выраженными, чем в группе Тримедата®, и статистически достоверными (фактор «Группа» F1/147=2,95; p=0,0880; фактор «Визит» F3/441=214; p=0,0001; фактор «Группа*Визит» F3/441=0,9; p=0,3934). Тогда как в группе Тримедата® улучшение КЖ, несмотря на положительный характер изменений, имело характер лишь статистически незначимой тенденции (рис. 6).
Заключение
Проведенное неинтервенционное сравнительное клиническое исследование в параллельных группах для оценки эффективности и безопасности применения Колофорта® в терапии СРК по сравнению с Тримедатом® продемонстрировало соответствие препаратов основным клиническим задачам, решаемым при терапии данного заболевания – необходимости купирования его ведущих проявлений, в частности болевого синдрома, что отражается на улучшении КЖ пациентов. В ходе исследования какого-либо неблагоприятного влияния на витальные функции и параметры, а также побочных эффектов в обеих группах зарегистрировано не было.
При сопоставимой в целом эффективности препаратов полученные результаты позволили сделать следующие выводы:
- Колофорт® более выраженно уменьшает интенсивность болевого синдрома у пациентов с СРК и проявляет стабильный эффект вне зависимости от типа СРК по сравнению с Тримедатом®.
- Колофорт® достоверно более эффективно как по срокам, так и по стабильности нормализует паттерн стула при доминирующих типах СРК (СРК-Д и СРК-З) по сравнению с Тримедатом®.
- Колофорт® достоверно быстрее Тримедата® увеличивает частоту стула при СРК-З.
- Терапия Колофортом® способствует нормализации висцеральной гиперчувствительности со статистически значимой тенденцией к превосходству по сравнению с Тримедатом®.
- Колофорт® статистически значимо улучшает КЖ пациентов с СРК по сравнению с Тримедатом®.
- Подтверждена высокая безопасность длительного использования Колофорта® в терапии СРК, что иллюстрируют отсутствие зарегистрированных в ходе исследования побочных эффектов и результаты мониторинга витальных функций пациентов.
Совокупность хорошей переносимости и продемонстрированной эффективности обеспечила высокий уровень приверженности пациентов назначенной терапии.
Таким образом, полученные данные позволяют рекомендовать Колофорт® к широкому применению в терапии СРК, что положительно отразится на качестве жизни пациентов.



