Введение
Аллергический ринит (АР) – иммуноопосредованное воспаление слизистой оболочки носа, вызванное контактом с аллергеном. Характеризуется зудом в полости носа, чиханием, передней или задней водянистой ринореей, заложенностью носа, которые периодически обостряются или могут наблюдаться постоянно. Такие симптомы, как боль, аносмия, кровотечение или рецидивирующая заложенность носа, встречаются редко.
АР является одним из самых распространенных заболеваний в мире, распространенность которого колеблется от 10 до 60% в зависимости от региона (табл. 1).
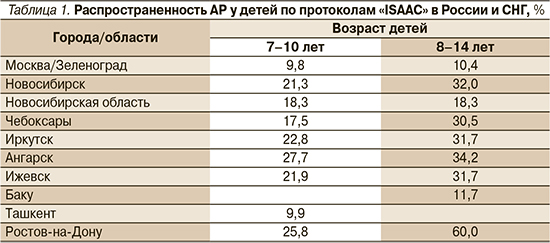
В международном исследовании астмы и аллергии у детей (ISAAC – International Study of Asthma and Allergies in Childhood) распространенность текущего АР была намного выше у детей старшего возраста по сравнению с младшими школьниками. Процент новых случаев АР у детей в возрасте от 3 до 12 лет увеличивается с постоянной скоростью примерно на 2% в год. У детей с наследственной предрасположенностью к аллергии в возрасте от 3 до 13 лет распространенность АР повышается с 13 до 44%.
У мальчиков АР возникает раньше, но девочки демонстрируют более высокие показатели заболеваемости в период полового созревания, достигая высоких показателей к 20 годам. В общей сложности 50–70% детей с персистирующим АР имеют тяжелое течение болезни, существенно влияющее на качество жизни [1–4].
АР распространен во всех возрастных группах, но это часто упускается из виду, поэтому он не диагностируется, особенно у детей дошкольного возраста. Все это служит причиной запоздалой диагностики и развития осложнений со стороны ЛОР-органов. Следует помнить, что дифференциальный диагноз АР довольно обширный и включает многочисленные воспалительные состояния в носовой области. В большинстве случаев клиническая диагностика АР затруднена, особенно при острой респираторной инфекции, инфекционном и неаллергическом рините, риносинусите.
Актуальность АР настолько высока, что данная проблема нашла отражение во многих отечественных и международных документах, таких как [5–7]:
- Международный консенсус по диагностике и лечению ринита – International Consensus Report on the Diagnosis and Management of Rhinitis (International Rhinitis Management Working Group, 1994).
- Консенсус по лечению аллергического ринита – Consensus statement on the treatment of allergic rhinitis (EAACI, 2000).
- Аллергический ринит и его влияние на астму (инициатива ВОЗ) – Allergic Rhinitis and its Impact on Asthma (ARIA, WHO, 2001–2008–2021).
- Аллергический ринит у детей. Научно-практическая программа. 2006 г.
- Pediatric rhinitis: position of European Academy of Allergy and Clinical Immunology, 2013 г.
- РАДАР (Рекомендации и алгоритм для детского аллергического ринита). Научно-практическая программа, 2015–2017–2020 гг.
Этиология АР
АР обычно классифицируют как сезонный или круглогодичный. Симптомы сезонного АР связаны с воздействием пыльцы растений или других аллергенов на открытом воздухе. К пыльцевым относятся аллергены пыльцы деревьев (береза, ольха, орешник, дуб и др.), луговых (тимофеевка, овсяница, мятлик, ежа и др.) и злаковых (подсолнечник, полынь, амброзия, лебеда) трав. На открытом воздухе преобладают споры грибов Alternaria и Cladosporium. Их концентрация в воздухе увеличивается в конце лета и начале осени. Они концентрируются в опавших листьях, гниющих растениях. Споры грибов Alternaria преобладают там, где сеют зерновые культуры. Из дрожжевых грибов наиболее выраженными сенсибилизирующими свойствами обладают Candida albicans, Saccaromyces cerevisiae и Saccaromyces minor и Pityrosporum. IgE (иммунглобулин Е)-опосредованная сенсибилизация к дрожжам продемонстрирована при атопическом дерматите, но может быть причиной развития АР и астмы. Большинство дрожжей не имеет перекрестно реагирующих антигенов.
За последние годы возросла роль пищевых аллергенов в этиологии АР у детей раннего возраста. К наиболее частыми продуктам, вызывающим аллергические реакции у них, относятся коровье молоко, злаки, яйцо, рыба, у детей старшего возраста – орехи, шоколад, соя, кунжут, морепродукты, киви, черная смородина. Аллергия может возникать на овощи, фрукты, пищевые добавки. В пищевых продуктах могут присутствовать клещи (мясной, сенной, бакалейный) или грибки рода Candida, Alternaria. Пищевые добавки и красители, широко используемые при изготовлении консервов и кондитерских изделий, способны провоцировать симптомы АР.
Круглогодичный ринит в большинстве случаев связан с бытовыми аллергенами, такими как клещи домашней пыли, домашние животные или тараканы.
Течение АР
В зависимости от продолжительности симптомов классифицирует АР как интермиттирующий и персиститрующий. По выраженности симптомов выделяют легкое течение АР, которое характеризуется ограниченным количеством симптомов, они не мешают каждый день вести нормальный образ жизни и/или не приводят к нарушению сна; при средней степени тяжести симптомы умеренно выражены, мешают привычной деятельности и/или нарушают сон; тяжелое течение характеризуется выраженными мучительными симптомами, из-за которых пациент не может справиться с повседневными обязанностями, у него существенно нарушен сон. Следует подчеркнуть, что интермитирующий АР в период обострения заболевания может иметь среднетяжелое/тяжелое течение, персистирующий ринит может протекать легко.
За последние годы отмечено увеличение случаев коморбидных состояний. В основе коморбидности лежат анатомическая близость вовлеченных в патологический процесс органов, общность этиологии, патогенетических механизмов, временнáя причинно-следственная связь между клинической манифестацией заболеваний [8].
У детей-атопиков коморбидность служит характерным признаком уже в первые годы жизни. У многих детей с АР в младенчестве развивается атопический дерматит, у 15–35% отмечаются свистящие хрипы. В более старшем возрасте у детей с тяжелым персистирующим АР наличие сухих хрипов выявляется в 52% случаев.
Сочетание АР с бронхиальной астмой
АР в раннем детском возрасте является сильным предиктором бронхиальной астмы (БА) у подростков и взрослых. Установлено, что АР у детей дошкольного возраста служит фактором высокого риска развития атопической БА. Эти данные согласуются с концепцией «единых дыхательных путей» и свидетельствуют о прогрессировании воспалительного процесса в слизистой оболочке верхних и нижних дыхательных путей. Считается, что нарушение барьера слизистых оболочек дыхательных путей может приводить к повышенному проникновению аллергена и усилению выработки IgE, антител, что в конечном итоге инициирует развитие иммунного (аллергического) воспаления и повышенной гиперреактивности в дыхательных путях. Высокая чувствительность к вирусным инфекциям со стороны нижних дыхательных путей могут усиливать аллергическую сенсибилизацию и тем самым увеличивать риск развития БА.
Из клинической практики и наблюдений известно, что большинство пациентов с БА имеют АР, а многие пациенты с АР имеют БА. Выделяют различные сочетания АР с БА (табл. 2).

АР может манифестировать одновременно с БА или существовать как самостоятельное аллергическое заболевание и при определенных условиях способствовать развитию БА. Среди факторов, содействующих развитию БА у пациентов с АР, выделяют запоздалую диагностику, длительный контакт с аллергенами, необоснованное назначение антибиотиков и хирургического лечения, полипрогмазию, стресс, курение (активное и пассивное).
В связи с этим у пациента с АР необходимо расспросить о случаях кашля, чихания, нехватки дыхания, бронхоспазма при физической нагрузке, провести аускультацию грудной клетки на предмет свистящих хрипов, оценить пиковую скорость выдоха у детей старшего возраста, провести пробу на обратимость с бронхоспазмолитиком. При сомнении провести провокационную пробу с физической нагрузкой или метахолином.
Лечение АР
Очень важно оценить все факторы риска развития БА у пациента с АР. Необходимо проводить адекватную терапию АР, которая включает:
- контроль окружающей среды для устранения или уменьшение контакта с триггером;
- терапию АР в острый период;
- терапию, направленную на достижение длительной ремиссии;
- реабилитацию.
Для терапии АР в острый период используют:
- антигистаминные препараты – АГП (интраназальные) и системные для приема внутрь и парентерального введения);
- препараты для ирригационно-элиминационной терапии;
- глюкокортикостероиды (интраназальные), системные по особым показаниям;
- антилейкотриеновые препараты;
- сосудосуживающие средства;
- симптоматические средства.
Ирригационно-элиминационная терапия используется для защиты, увлажнения и улучшения трофики слизистой оболочки носовых ходов, улучшения мукоцилиарного транспорта. Особое значение эти средства имеют для элиминации частиц, попадающих на слизистую оболочку и вызывающих воспаление (вирусов, бактерий, аллергенов, поллютантов, табачного дыма, токсинов). К положительным эффектам этого метода относятся уменьшение отека слизистой оболочки носа и количества медиаторов воспаления, механическое удаление густой слизи и аэроаллергенов, улучшение мукоцилиарного клиренса. В настоящее время получили распространение следующие виды: орошение полости носа, ретроназальный душ, назофарингеальное аспирационное промывание (промывание носа и носоглотки методом перемещения жидкости). При выборе препаратов для элиминационно-ирригационной терапии следует отдавать предпочтение средствам на основе морской воды, т.к. они содержат в своем составе соли и микроэлементы, обусловливающие терапевтический эффект. В настоящее время используются средства на основе солевых растворов различной концентрации: гипотонический – 0,65%, изотонический – 0,9 % и гипертонический – 2,3% NaCl.
Большинство фармакологических препаратов при АР используется как перорально, так и интраназально.
Преимущества интраназального применения лекарственных средств у детей и подростков с АР [9]:
- препараты в высоких концентрациях поступают непосредственно в органы-мишени, что позволяет избегать системных эффектов или сводить их к минимуму;
- некоторые препараты вызывают выраженные системные эффекты при пероральном применении (например, кортикостероиды и производные атропина);
- при интраназальном применении действие обычно начинается быстрее, чем при приеме внутрь (например, сосудосуживающие средства и, возможно, АГП).
У некоторых пациентов интраназальные кортикостероиды вызывают местные побочные эффекты, в частности кровотечение из носа и образование корок.
АГП (пероральные и интраназальные). Большое значение в лечении АР у детей имеет применение АГП, т.к. многие маленькие дети предпочитают пероральные препараты интраназальным. АГП первого поколения вызывают побочные эффекты со стороны центральной нервной системы, включая седацию и усталость. У новорожденных и маленьких детей могут наблюдаться парадоксальная гиперактивность, бессонница и раздражительность. Сезонный АР сам по себе влияет на способность к обучению и концентрацию внимания. Лечение АГП первого поколения часто приводит к дальнейшему ухудшению когнитивной функции. Однако новые АГП уменьшают недомогание, вызванное АР, и могут улучшать способность к обучению детей с АР.
H1-АГП блокируют гистамин на Н1-гистаминовых рецепторах, широко используются при лечении АР и конъюнктивита. Было показано, что пероральные H1-АГП уменьшают опосредованные гистамином такие симптомы, как чихание, зуд, ринорея и глазные симптомы, менее эффективны в облегчении заложенности носа. Они быстро всасываются после перорального приема и начинают свое действие в течение 1–2 часов. Было также показано, что пероральные H1-АГП безопасны и эффективны для детей и многие из них доступны в жидкой форме.
Прием АГП первого поколения при АР ограничен их седативным и антихолинергическим действиями. Длительность их применения составляет 7–14 дней из-за снижения терапевтической эффективности.
Новые АГП имеют низкую частоту седативного эффекта, а также минимальные или отсутствующие антихолинергические эффекты. H1-АГП также доступны для интраназального введения. Азеластина гидрохлорид и олопатадина гидрохлорид имеют более быстрое, чем пероральные АГП, начало действия – обычно в течение 15–30 минут, и приводят к значительному уменьшению заложенности носа, а также зуда, чихания и насморка. Эти лекарства могут вызывать изменение вкусовых ощущений и иногда сонливость.
Пероральные и интраназальные АГП второго поколения одинаково эффективны при АР. Пероральные препараты лучше переносятся пациентами, в то время как интраназальные действуют быстрее. Хотя у некоторых детей препараты второго поколения также могут вызывать седативный эффект.
АГП второго поколения не обладают побочными эффектами, характерными для АГП первого поколения. Они могут использоваться более длительными курсами (от 14 до 28 дней и более) из-за отсутствия тахифилаксии. Они действуют от 12 до 24 часов, что позволяет назначать их 1–2 раза в сутки. Препараты этой группы оказывают выраженное действие и на такие коморбидные заболевания, как конъюнктивит и кожные проявления аллергии.
Рекомендуемые дозы не должны превышаться!
Исследования фармакокинетики АГП второго поколения проводились на детях, однако имеются единичные исследования у новорожденных. Взаимодействие с цитохромом Р-450 может приводить к ухудшению метаболизма АГП в печени. Макролидные антибиотики, которые назначают детям, могут давать этот эффект. Цетиризин, фексофенадин и левоцетиризин не подвергаются биотрансформации. Более того, хотя многие АГП второго поколения эффективны и безопасны в лечении АР у детей, в длительных исследованиях подтверждены эффективность и безопасность только цетиризина, левоцетиризина и лоратадина.
Цетиризин
Среди АГП нового поколения цетиризин имеет 30-летнюю историю применения при аллергических заболеваниях.
Цетиризин (Зодак) сохраняет ведущую роль в лечении АР. Время наступления терапевтического эффекта – 20 минут, длительность эффекта – 24 часа. Зодак селективно блокирует Н1-гистаминовые рецепторы, у него низкая вероятность развития тахифилаксии и отсутствует зависимость от приема пищи. Выпускается в нескольких лекарственных формах (таблетки и капли).
Капли для приема внутрь в виде прозрачного раствора от бесцветного до светло-желтого цвета. В 1 мл содержится 10 мг цетиризина дигидрохлорида.
Вспомогательные вещества: метилпарагидроксибензоат, пропилпарагидроксибензоат, глицерол, пропиленгликоль, натрия сахаринат дигидрат, натрия ацетат тригидрат, уксусная кислота ледяная, вода очищенная.
Фармакологическое действие. Цетиризин (активное вещество препарата Зодак®) является метаболитом гидроксизина, блокирует гистаминовые H1-рецепторы с небольшим воздействием на другие рецепторы и практически не оказывает антихолинергического и антисеротонинового действий.
После приема внутрь препарат быст-ро абсорбируется из желудочно-ки-шечного тракта. Фармакокинетические параметры цетиризина при его применении в дозах от 5 до 60 мг изменяются линейно. Фармакокинетический профиль цетиризина аналогичен для взрослых и детей.
У детей после приема цетиризина в дозе 5 мг концентрация активной субстанции в организме такая же, как и у взрослых после приема 10 мг.
У взрослых после приема цетиризина в дозе 10 мг Cmax в плазме крови дос-тигается через 1–2 часа и составляет 350 нг/мл. У детей после приема цетиризина в дозе 5 мг Cmax в плазме крови достигается через 1 час и составляет 275 нг/мл.
При приеме цетиризина в форме капель Cmax в плазме крови достигаются с более высокой скоростью.
Распределение. Распределение после приема 10 мг составляет 35 л у взрослых, а связывание с белками плазмы крови – 93%. У детей Vd после приема 5 мг составляет примерно 17 л. Незначительное количество цетиризина выделяется с грудным молоком.
Выведение. У взрослых 60% дозы выводится из организма почками в неизмененном виде.
После приема 10 мг у взрослых общий клиренс цетиризина составля-ет 0,60 мл/мин/кг, Т1/2 – примерно 10 часов.
Прием нескольких доз не изменяет фармакокинетических параметров. При приеме препарата в суточной дозе 10 мг в течение 10 дней кумуляции цетиризина не наблюдалось. После окончания лечения уровень цетиризина в плазме крови быстро падает ниже определяемых пределов. Повторные аллергологические тесты можно возобновлять через 3 дня.
Показания к применению препарата Зодак®. Взрослым и детям в возрасте 6 месяцев и старше препарат показан для облегчения:
- назальных и глазных симптомов круглогодичного (персистирующего) и сезонного (интермиттирующего) АР и аллергического конъюнктивита (зуда, чихания, заложенности носа, ринореи, слезотечения, гиперемии конъюнктивы);
- симптомов хронической идиопатической крапивницы.
Применение у детей от 6 до 12 месяцев возможно только по назначению врача и под строгим медицинским контролем!
Заключение
Данные многолетнего клинического опыта подтверждают, что цетиризин обладает благоприятным профилем безопасности и способствует повышению эффективности терапии в лечении АР.



