Комбинация амоксициллина с клавуланатом используется в клинической практике для лечения респираторных инфекций уже более 30 лет. Широкий спектр антимикробной активности, включающий основные респираторные возбудители (Streptococcus pneumoniae, Haemophilus influenzae и Moraxella catarrhalis), благоприятные фармакокинетические и фармакодинамические (ФК/ФД) параметры при пероральном приеме обеспечивают высокую клиническую и микробиологическую эффективность амоксициллина/клавуланата (АМК). В то же время появление и распространение пенициллорезистентных штаммов пневмококков потребовали дальнейшей оптимизации ФК/ФД параметров АМК, что привело к созданию новой высокодозной лекарственной формы АМК с модифицированным высвобождением амоксициллина Аугментина СР, зарегистрированного в РФ в 2010 г. В обзоре обсуждаются характеристики данного препарата и перспективы его клинического применения при респираторных инфекциях у взрослых пациентов в амбулаторной практике.
Введение
Бактериальные инфекции дыхательных путей (ИДП; пневмония, инфекционное обострение хронической обструктивной болезни легких – ХОБЛ, острый бактериальный синусит – ОБС) являются одной из наиболее частых причин временной утраты трудоспособности среди взрослого населения. У пациентов старших возрастных групп с сопутствующими заболеваниями (застойной сердечной недостаточностью, сахарным диабетом, алкоголизмом) внебольничная пневмония (ВП) является одной из ведущих причин смерти от инфекционных болезней.
Данные официальной статистики, к сожалению, не отражают истинной распространенности бактериальных ИДП в Российской Федерации. Так, зарегистрированное число случаев ВП в России составляет менее 600 тыс., тогда как, по оценкам экспертов, число пациентов с ВП в РФ ежегодно превышает 1,5 млн [1]. Аналогично, по данным Министерства здравоохранения и социального развития РФ, в России зарегистрировано около 2,5 млн больных ХОБЛ, но эпидемиологические данные позволяют предположить, что их число может составлять около 16 млн человек [2], причем каждый пациент переносит от одного до четырех и более обострений ХОБЛ в течение года [3]. Частой проблемой в амбулаторной практике является и острый бактериальный риносинусит (ОБРС), который развивается как осложнение вирусного риносинусита в 0,5–2,0 % всех случаев острой респираторной вирусной инфекции [4]. Бактериальные ИДП являются показанием к назначению антибактериальной терапии (АБТ), которая купирует инфекционный процесс, предотвращает развитие осложнений
и неблагоприятных исходов, способствует быстрому улучшению состояния пациента.
Основные возбудители ИДП
Для всех перечисленных бактериальных ИДП характерна общность “типичных” возбудителей. Наиболее значимыми патогенами при ВП,инфекционных обострениях ХОБЛ и ОБРС являются пневмококки (Streptococcus pneumoniae) и гемофильная палочка (Haemophilus influenzae) [5]. При ВП этиологическое значение также имеют “атипичные” микроорганизмы – Mycoplasma pneumoniae и Chlamydophila pneumoniae, а при обострениях ХОБЛ и ОБРС – Moraxella catarrhalis [1, 2, 4]. В табл. 1 представлена структура основных бактериальных возбудителей перечисленных респираторных инфекций.
Таблица 1.
Основные бактериальные возбудители ВП, обострений ХОБЛ и ОБРС, %.
В ряде исследований установлено, что ИДП пневмококковой этиологии в наименьшей степени склонны к самоизлечению, поэтому при назначении АБТ особое внимание следует уделять активности антибиотика в отношении S. pneumoniae [6, 7].
Принципы выбора антимикробных препаратов при респираторных инфекциях
Выбор антимикробных препаратов (АМП) для лечения ИДП должен быть основан на знании природной активности антибиотиков в отношении основных респираторных возбудителей, эпидемиологических данных по антибиотикорезистентности (АБР) микроорганизмов в определенном регионе с учетом фармакокинетических (ФК) и фармакодинамических (ФД) характеристик АМП, риска развития нежелательных лекарственных реакций (НЛР), а также затрат на проведение терапии. Кроме того, в современных условиях при назначении АБТ следует обращать внимание не только на возможные неблагоприятные результаты применения антибиотика у отдельного пациента, но и на глобальные экологические последствия широкого применения различных классов АМП, а именно – на вероятность появления и распространения АБР.
Общеизвестно, что применение АМП служит основным фактором риска селекции резистентных штаммов микроорганизмов. В ряде исследований было убедительно показано, что уровень резистентности пневмококков к пенициллину в определенной степени зависит от потребления пенициллинов или β-лактамов в целом [8–10], а уровень резистентности к макролидам – от потребления макролидов [8]. При этом несомненный практический интерес для определения политики применения антибиотиков представляют работы, свидетельствующие о неравноценном потенциале различных АМП приводить к селекции резистентных штаммов. В исследованиях, организованных НИИ антимикробной химиотерапии (НИИАХ) Смоленской государственной медицинской академии в 12 детских домах 5 городов РФ, было продемонстрировано, что увеличение частоты назначения амоксициллина/клавуланата (АМК) в 2,4 раза не привело к росту резистентности назофарингеальных изолятов S. pneumoniae к пенициллину и амоксициллину, в то время как повышение потребления цефалоспоринов вызвало увеличение доли пневмококков, не чувствительных к данному классу АМП [11].
Кроме того, риск селекции резистентных штаммов возрастает при использовании субоптимальных доз АМП, недостаточных для надежной эрадикации возбудителя. Соответственно, для обеспечения максимальной “экологической” безопасности терапии необходимо использовать высокоэффективные АМП в довольно высоких дозах. Именно такой подход соответствует принципу “убитые бактерии не мутируют” [12].
Проблемы АбР респираторных возбудителей
Если сравнить данные по АБР респираторных возбудителей, полученные в ходе многоцентровых исследований ПеГАС в РФ [1, 13], и аналогичные показатели других стран мира, то на первый взгляд ситуация в России выглядит вполне благополучно. Так, по результатам исследования ПеГАС-III [1, 6] частота пенициллинорезистентности среди пневмококков в РФ составляет 11,2 % (из них 9,1 % – штаммы с промежуточной резистентностью и 2,1 % – с высоким уровнем резистентности к пенициллину).
Резистентность S. pneumoniae к эритромицину составляет менее 5 %; 99,6 и 100 % изолятов соответственно чувствительны к амоксициллину и респираторным фторхинолонам. Однако не может вызывать тревоги тот факт, что в некоторых федеральных округах РФ (Южном, Дальневосточном и Уральском) частота выделения пенициллонечувствительных пневмококков (ПНЧП) выше среднего показателя по РФ и составляет 14,3, 25 и 16,7 % соответственно [6].
В целом показатели резистентности пневмококков к пенициллину в России при сравнении со странами Европейского сообщества аналогичны таковым в Финляндии; существенно ниже, чем в Болгарии (37 %), Франции (26,8 %), Польше (29,8 %) и Испании (22 %), однако минимум вдвое выше, чем в Германии, Великобритании, Бельгии, Нидерландах, Дании, Швеции и Норвегии, где частота ПНЧП не превышает 5 % [14].
По данным глобального эпидемиологического исследования PROTECT, в 2003–2004 гг. нечувствительность к пенициллину была отмечена у 35,7 %, а к макролидам – у 36,0 % клинических штаммов S. pneumoniae; продукция β-лактамаз – у 12,3 % H. influenzae, еще 5,2 % изолятов гемофильной палочки были устойчивы к ампициллину за счет других механизмов резистентности [15].
По данным исследования ПеГАС-II, штаммы гемофильной палочки, продуцирующие β-лактамазы, в РФ не распространены и составляют 5,4 % среди всех изолятов в общей популяции [13]. В то же время можно предполагать, что у пациентов, ранее получавших АМП, частота выделения ПНЧП и ампициллинорезистентных штаммов H. influenzae окажется существенно выше, что обязательно следует учитывать при назначении терапии.
АМП для лечения респираторных инфекций в амбулаторной практике
В настоящее время в амбулаторной практике для лечения респираторных инфекций широко применяются два основных класса АМП – β-лактамы и макролиды. В последние годы отмечается относительное увеличение частоты назначений респираторных фторхинолонов (левофлоксацина). В то же время в РФ имеют место нерациональные назначения АМП для лечения респираторных инфекций в амбулаторной практике, а именно: терапияпарентеральными препаратами, назначение цефалоспоринов I–III поколений, ципрофлоксацина, ампициллина внутрь, линкозамидов при лечении нетяжелой ВП или ОБРС [1, 16].
Основное место в лечении респираторных инфекций в амбулаторной практике принадлежит амоксициллину, что обусловлено его мощным бактерицидным действием в отношении S. pneumoniae (включая штаммы со сниженной чувствительностью к пенициллину), низкой токсичностью, многолетним опытом эффективного и безопасного применения. У пациентов с факторами риска β-лактамазопродуцирующих штаммов (предшествующей АБТ, рецидивирующими или хроническими инфекциями) амоксициллин применяют в комбинации с ингибитором β-лактамаз клавуланатом в форме АМК. Амоксициллин и АМК при применении в высоких дозах (80–90 мг/кг/сут по амоксициллину) сохраняют активность в отношении пенициллинорезистентных пневмококков (ПРП).
Респираторные фторхинолоны (левофлоксацин, моксифлоксацин и гемифлоксацин) являются высокоэффективными препаратами для лечения респираторных инфекций. В то же время с позиций рационального применения АМП респираторные фторхинолоны не должны использоваться амбулаторно как препараты выбора для лечения нетяжелых инфекций у пациентов без факторов риска терапевтической неудачи [1]. “Классические” фторхинолоны (ципрофлоксацин) обладают недостаточной активностью в отношении S. pneumoniae и не должны назначаться для эмпирической терапии респираторных инфекций.
Возможности оптимизации терапии респираторных инфекций
аминопенициллинами
Принимая во внимание значение амоксициллина и АМК при лечении респираторных инфекций в амбулаторной практике, важно максимально полно использовать и сохранять терапевтический потенциал этих АМП. Для достижения этой цели следует на практике учитывать и использовать возможности оптимизации АБТ на основании знания взаимосвязи ФК- и ФД-свойств АМП. Применение ФК/ФД-принципов на практике позволяет улучшить исходы лечения пациентов с инфекциями и потенциально снизить риск АБР.
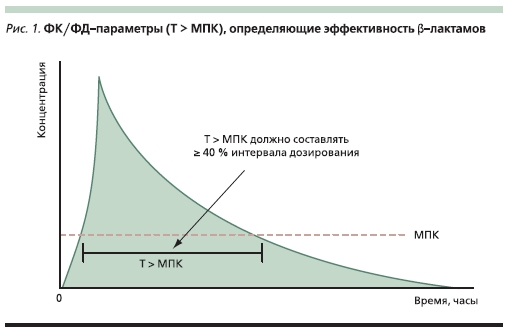
Установлено, что эффективность лечения β-лактамными антибиотиками зависит от времени поддержания концентрации препарата в очаге инфекции выше значения его минимальной подавляющей концентрации (МПК) в отношении возбудителя. Данный параметр обозначается как Т > МПК (рис. 1). Следует отметить, что приувеличении концентрации препарата более 4–5 МПК эффективность терапии не повышается, но может отмечаться возрастание риска НЛР [17]. Оптимальная эффективность терапии β-лактамами может быть достигнута при Т > МПК, составляющем минимум 40 %-ный интервал дозирования.
Для достижения этой цели теоретически можно использовать три способа:
1. повысить дозу препарата;
2. увеличить кратность приема АМП;
3. использовать особые лекарственные формы с модифицированным высвобождением антибиотика.
Однако необходимо учитывать, что повышение дозы препарата вдвое не обеспечивает эквивалентного увеличения показателя Т > МПК и, соответственно, не позволяет существенно повысить эффективность терапии в случае резистентных возбудителей. Увеличение кратности введения препарата до 3–4 раз в сутки сопровождается снижением приверженности пациентов лечению. Так, было показано, что при приеме препарата 2 раза в сутки пациенты соблюдают назначенный режим лечения в 80 % случаев, а при 3-кратном приеме – только в половине [18], что несомненно отражается на эффективности терапии. Таким образом, достижение оптимальных ФК/ФД-параметров пероральных β-лактамов возможно только при использовании особых лекарственных форм с модифицированным высвобождением активного вещества.
Эволюция аминопенициллинов при лечении ИДП
История разработки новых АМП в значительной степени определяется появлением и распространением АБР у бактерий. Типичным примером, подтверждающим данный тезис, является история применения аминопенициллинов в лечении ИДП. Ампициллин был внедрен в клиническую практику в 1963 г., и понадобилось еще 10 лет для создания амоксициллина – аминопенициллина с высокой биодоступностью при приеме внутрь и максимальной среди всех пероральных β-лактамов активностью в отношении S. pneumoniae [19]. Однако уже в 1974 г. были обнаружены первые штаммы H. influenzae, резистентные к аминопенициллинам, а в 1977 г. описаны первые штаммы ПРП и M. catarrhalis, проду-
цирующие β-лактамазы. Клавулановая кислота была открыта примерно в то же время (1976), однако комбинированный препарат АМК был зарегистрирован только в 1984 г. [19].
Таблица 2.
Лекарственные формы АМК для приема внутрь [20].
Таблица 3. ФД/ФК-параметры (Т > МПК, %) пероральных β-лактамов в отношении респираторных возбудителей [21, 22 с изменениями].
Появление АМК (первоначально в форме таблеток по 625 мг, содержащих 500 мг амоксициллина и 125 мг клавуланата) позволило решить проблему терапии респираторных инфекций у взрослых, кроме случаев, вызванных пневмококками со сниженной чувствительностью к пенициллину. Поэтому дальнейшая разработка пероральных лекарственных форм АМК была направлена на повышение содержания амоксициллина в препарате, сокращение кратности приема до 2 раз в сутки и наконец на создание формы с модифицированным высвобождением (Аугментин СР; табл. 2). Следует также подчеркнуть, что применение у взрослых пациентов таблеток АМК по 375 мг не обеспечивает адекватных ФК/ФД-параметров эффективности в отношении основных бактериальных возбудителей респираторных инфекций. ФД/ФК-параметры эффективности различных пероральных β-лактамов в отношении респираторных возбудителей приведены в табл. 3 [21, 22]. Из представленных данных следует, что при инфекциях, вызванных пенициллиночувствительными пневмококками, амоксициллин (в дозе от 1,5 г/сут), АМК и цефуроксим в рекомендованных дозах будут обеспечивать достаточную эффективность терапии. Необходимо отметить, что пероральные цефалоспорины III поколения (цефиксим и цефтибутен) существенно уступают аминопенициллинам по антипневмококковой активности – даже в отношении пенициллиночувствительных штаммов S. pneumoniae.
В отношении пневмококков с промежуточной резистентностью к пенициллину достаточную активность проявляют только амоксициллин в высокой дозе (90 мг/кг/сут) и АМК СР, “традиционные” лекарственные формы и режимы дозирования АМК (500/125 мг 3 раза/сут и 875/125 мг 2 раза/сут) обладают “пограничной” активностью в отношении таких изолятов, как S. pneumoniae. И наконец гарантированная фармакодинамическая активность в отношении ПРП отмечена только при использовании АМК СР – лекарственной формы с модифицированным высвобождением. В отличие от амоксициллина АМК также сохраняет активность в отношении штаммов H. influenzae и M. catarrhalis, продуцирующих β-лактамазы.
Таблица 4.
Чувствительность респираторных возбудителей в мире к пероральным АМП на основании ФД/ФК-критериев [23].
Таким образом, на сегодняшний день в мире АМК СР – наиболее активный препарат среди всех пероральных β-лактамов в отношении основных возбудителей респираторных инфекций (табл. 4) [23]. По показателям прогнозируемой фармакодинамической эффективности при респираторных инфекциях АМК СР практически эквивалентен респираторным фторхинолонам.
АМК СР – новая лекарственная форма АМК с модифицированнымвысвобождением
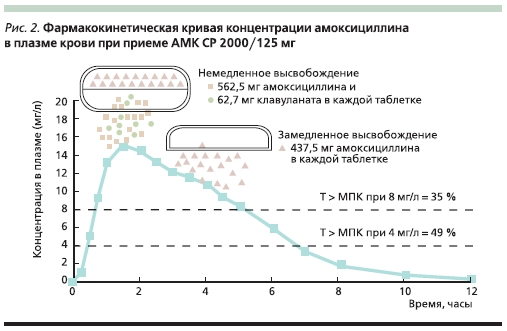
АМК СР представляет собой особую лекарственную форму АМК в видедвукомпонентных таблеток, содержащих 562,5 мг амоксициллина тригидрата и 62,5 мг клавулановой кислотыв слое немедленного высвобожденияи еще 437,5 мг амоксициллина в виденатриевой соли в слое замедленного высвобождения. Таким образом, вкаждой таблетке содержится 1000 мгамоксициллина и 62,5 мг клавуланата, а суточная доза составляет 4 такиетаблетки: по 2 таблетки (2000/125 мг)2 раза в сутки [24].
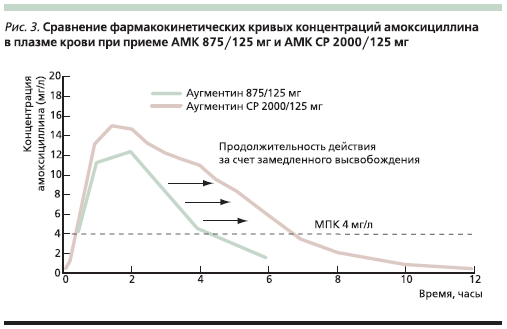
За счет такого строения таблетки и наличия слоев с немедленным изамедленным высвобождением амоксициллина пиковая концентрация действующего вещества достигается в теже сроки, что и при приеме обычногоамоксициллина или АМК. Однако засчет слоя с замедленным высвобождением концентрация амоксициллинав сыворотке крови снижается болеемедленно, чем при приеме “традиционных” препаратов, что обеспечиваетувеличение параметра Т > МПК (рис.2, 3 и 4).
Для АМК СР по сравнению с АМК875/125 мг характерна более высокаяпиковая концентрация амоксициллина в крови (17,0 против 11,6 мг/л), аза счет более медленного ее снижения параметр T > МПК для штаммовс МПК 4 мг/л для указанных лекарственных форм АМК составляет 49 и< 35 % от интервала дозирования соответственно (рис. 3) [20].
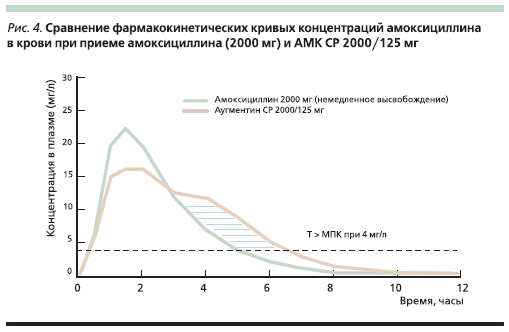
При приеме 2000 мг амоксициллина в виде обычной лекарственной формыс немедленным высвобождениемпиковая концентрация антибиотикадостигает > 20 мг/л, однако за счет еебыстрого снижения T > МПК в данномслучае меньше, чем при приеме АМКСР 2000/125 мг, и для штаммов с МПК 4 мг/л составляет 5 и 7 часов соответственно (рис. 4) [24].
Таким образом, новая лекарственная форма АМК – АМК СР – позволяет обеспечивать эффективное лечение инфекций даже при наличииПРП с МПК 4 мг/л. Помимо теоретического обоснования данный факт подтвержден результатами анализаэффективности АМК СР у пациентов с инфекциями дыхательных путей,вызванными ПРП [25]. Эрадикациявозбудителя отмечена в 96,2 % случаев респираторных инфекций, вызванныхПРП (у 51 из 53 больных). Успешнаяэрадикация возбудителя также отмечена в 14 из 15 случаев инфекций, вызванных S. pneumoniae с высокимизначениями МПК амоксициллина(4–8 мг/л) [25].
Безопасность и переносимость
АМК СР по сравнению с обычными формами АМК АМК является одним из наиболее хорошо изученных АМП в отношении профиля безопасности и переносимости, апробированного в процессе широкого клинического примененияданного препарата в мире более чем у819 млн пациентов [20].
При изучении новой высокодозной лекарственной формы АМК СР оказалось, что профили ее безопасности ипереносимости существенно не отличаются от таковых традиционных лекарственных форм АМК с более низкимсодержанием амоксициллина [26–28].
В клинических исследованиях IIIфазы безопасность и переносимостьАМК СР изучены у 4144 пациентов.Частота НЛР, отмеченных при приемеАМК СР, была эквивалентной таковойпри приеме АМК 875/125 мг 2 раза всутки. Большинство НЛР были легкойстепени и транзиторными, не требовали отмены препарата и дополнительного лечения. Наиболее частыми НЛР,зарегистрированными на фоне терапииАМК СР были: диарея (15,6 %), тошнота (2,2 %), вагинальный кандидоз (2,1 %) и боль в животе (1,6 %) [22].
АМК в стандартах лечения респираторных инфекций
С учетом высокой клиническойэффективности АМК при леченииИДП данный препарат включен в национальные и международные руководства по лечению ОБС, инфекционных обострений ХОБЛ и ВП (табл. 5).
Таблица 5.
АМК в национальных и международных руководствах по лечению респираторных инфекций [20 с изменениями].
В тех странах, где высокодозные лекарственные формы АМК (детская суспензия с дозировкой АМК 90/6,4 мгна 1 кг массы тела и АМК СР) зарегистрированы и применяются напрактике уже в течение почти 10 лет,отмечается замена обычных формАМК в стандартах лечения респираторных инфекций на высокодозныелекарственные формы, особенно упациентов с факторами риска наличиярезистентных возбудителей (предшествующее применение антибиотиков, сопутствующая патология, неэффективность стартовой АБТ) [29, 31, 32].
Эффективность АМК СРпри респираторныхинфекциях по данным КИ
При объединенном анализе 10 клинических исследований эффективности и безопасности АМК СР у пациентов с респираторными инфекциями (ОБС, инфекционное обострение ХОБЛ и ВП) оказалось, что общаяклиническая эффективность АМК СРпри ИДП, вызванных S. pneumoniae, всравнительных исследованиях составила 94,4 %, а в несравнительных – 94,6 %. Общая клиническая эффективность препаратов сравнения составила82,9 % [25].
Таблица 6.
Результаты основных клинических исследований АМК СР при респираторных инфекциях [23, 25 с изменениями].
Результаты клинических исследований АМК СР у пациентов с ОБС(табл. 6) свидетельствуют о том, что по показателям клинической и бактериологической эффективности приданной нозологии АМК СР не уступает респираторным фторхинолонам [33,34]. Таким образом, результаты клинических исследований АМК СР приОБС полностью соответствуют прогнозируемым показателям эффективности данного препарата на основанииФК/ФД-моделирования [35].
В клиническом исследовании у пациентов с ВП АМК СР продемонстрировал по меньшей мере эквивалентнуюклиническую, рентгенологическую ибактериологическую эффективностьпо сравнению с АМК 875/125 мг, принимаемым 2 или 3 раза в сутки, и АМК1000/125 мг, принимаемым 3 раза всутки. В целом эффективность 7-дневного курса терапии АМК СР в дозе 2000/125 мг 2 раза в сутки в отношении нормализации клинических и рентгенологических симптомов ВП, а также эрадикации возбудителя составляет > 85 % [23].
В клиническом исследовании у пациентов с инфекционными обострениями ХОБЛ АМК СР обеспечивал бактериологическую эффективность терапии у 86,2 % пациентов с обострениями, предположительно вызванными H. influenzae, в то время как при лечении АМК 875/125 мг данный показатель составил только 75 % [26].
Тенденции применения АМК при респираторных инфекциях в клинической практикеДля обеспечения эффективной терапии респираторных инфекций, обусловленных ПРП, дозы амоксициллина, содержащейся в “традиционных” лекарственных формах АМК (500 или 875 мг), может быть недостаточно. При этом увеличение кратности приема таких форм, например применение АМК 875/125 мг 3 раза в сутки, не позволяет обеспечивать адекватную дозу амоксициилина (4 г/сут) и сопряжено с повышением риска НЛР (в частности, диареи), развитие которой обусловлено преимущественно клавуланатом.
В связи с этим некоторые руководства по лечению ИДП советуют назначать АМК в комбинации с амоксициллином [38] для достижения высокой эффективности терапии в отношении как ПРП, так и β-лактамазопродуцирующих штаммов H. Influenzae, а также M. catarrhalis. Появление высокодозных форм АМК, в частности АМК СР, позволило не только воплотить указанную идею, но и улучшить ФК/ФД-характеристики за счет технологии замедленного высвобождения амоксициллина.
Таким образом, появление АМК СР в клинической практике является своевременным дополнением к существующему арсеналу пероральных АМП для эффективного лечения респираторных инфекций. Оптимизация ФК/ФД-параметров, которой удалось достичь при создании АМК СР, позволила “сделать хороший антибиотик еще лучше” [39]. Использование АМК СР позволяет не только успешно лечить инфекции, вызванные возбудителями со сниженной чувствительностью к традиционным препаратам, но и надеяться на уменьшение риска селекции и распространения резистентных штаммов. Наибольшее значение новая лекарственная форма с модифицированным высвобождением имеет для терапии респираторных инфекций у пациентов с высоким риском резистентных возбудителей при наличии тяжелых сопутствующих заболеваний, таких как сахарный диабет, ХОБЛ, застойная сердечная недостаточность, новообразования и др.; ранее получавших антибиотики; у пациентов с более тяжелыми, хроническими и рецидивирующими формами инфекций. Для лечения респираторных инфекций у пациентов “без отягощенного анамнеза” в амбулаторной практике можно с успехом использовать амоксициллин в дозах от 1,5 до 4,0/сут, а также “традиционные” формы АМК (по 875/125 мг 2 раза в сутки).
1. Чучалин А.Г., Синопальников А.И., Козлов Р.С.и др. Внебольничная пневмония у взрослых.Практические рекомендации по диагностике,лечению и профилактике. Пособие для
врачей. МАКМАХ, 2010.
2. Синопальников А.И., Козлов Р.С., Романовских А.Г. и др. Инфекционное обострениехронической обструктивной болезни легких.Практические рекомендации по диагностике,лечению, профилактике // Рос. мед. вести.2006. № 11(1). C. 4–18.
3. Snider GL. Nosology for our day: its applicationto chronic obstructive pulmonary disease. Am JRespir Crit Care Med 2003;167(5):678–83.
4. Янов Ю.К., Рязанцев С.В., Страчунский Л.С.и др. Практические рекомендации поантибактериальной терапии синусита.Пособие для врачей // Клин. микробиол.антимикроб. химиотер. 2003. № 5(2).C. 167–74.
5. Козлов Р.С. Пневмококки: уроки прошлого –взгляд в будущее. МАКМАХ. 2010.
6. Hadley JA, Pfaller MA. Oral beta-lactams in thetreatment of acute bacterial rhinosinusitis. Diagn
Microbiol Infect Dis 2007;57(3):47–54.
7. Dagan R, Leibovitz E. Bacterial eradication inthe treatment of otitis media. Lancet Infect Dis2002;2:593–604.
8. Bronzwaer SL, Cars O, Buchholz U, et al.European Antimicrobial Resistance SurveillanceSystem. A European study on the relationshipbetween antimicrobial use and antimicrobial resistance. Emerg Infect Dis 2002;8(3):278–82.
9. Granizo JJ, Aguilar L, Casal J, et al. Streptococcuspneumoniae resistance to erythromycin andpenicillin in relation to macrolide and b-lactamconsumption in Spain. J Antimicrob Chemother2000;46:767–73.
10. van de Sande-Bruinsma N, Grundmann H, Verloo D, et al. Antimicrobial drug use and resistance in Europe. Emerg Infect Dis 2008;14(11): 1722–30.
11. Stetsiouk OU, Kozlov RS, Poupard JA, et al. Curbing pneumococcal resistance in orphanages:interventions on the basis of prospectivesurveillance of nasopharyngeal isolates. Clin
Microbiol Infect 2006;12(S4):1484.
12. Stratton CW. Dead bugs don’t mutate: susceptibilityisues in the emergence of bacterial resistance. Emerg Infect Dis [serial online] 2003 Jan[date cited]. Available from: URL: http://www.cdc.gov/ncidod/EID/vol9no1/02-0175.htm
13. Решедько Г.К., Козлов Р.С. Состояние резистентности к антиинфекционным препаратам в России / Под редакцией Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова. Практическое руководство по антиинфекционной химиотерапии. Смоленск,2007. С. 32–46.
14. European Centre for Disease Prevention andControl. Antimicrobial resistance surveillance inEurope 2009. Annual Report of the EuropeanAntimicrobial Resistance Surveillance Network(EARS-Net). Stockholm: ECDC. 2010.
15. Blasi F, Farrell DJ, Dubreuil L. Antibacterial activityof telithromycin and comparators againstpathogens isolated from patients with community-acquired respiratory tract infections: theProspective Resistant Organism Tracking andEpidemiology for the Ketolide Telithromycinstudy year 5 (2003–004). Diagn Microbiol
Infect Dis 2009;63(3):302–10.
16. Анготоева И.Б. Острые риносинуситы. Как мыследуем стандартам. Материалы VII Конгрессароссийского общества ринологов “Актуальныевопросы ринологии на современном этапе”.
Таганрог, 2007.
17. Nicolau DP. Pharmacodynamic optimization of β-lactams in the patient care setting. Critical Care 2008;2(4):2.
18. Pavic-Sladoljev D. Patient compliance in the treatment of respiratory tract infections. K Lijec Vjesn 1997;119:193–200.
19. Medeiros AA. Evolution and dissemination of beta-lactamases accelerated by generations of beta-lactam antibiotics. Clin Infect Dis 1997;24(1):19–45.
20. White AR, Kaye C, Poupard J, et al. Augmentin (amoxicillin/clavulanate) in the treatment of community-acquired respiratory tract infection: a review of the continuing development of an innovative antimicrobial agent. J Antimicrob Chemother 2004;53(1):3–20.
21. Auckenthaler R. Pharmacokinetics and pharmacodynamics of oral beta-lactam antibiotics as a two-dimensional approach to their efficacy. J Antimicrob Chemother 2002;50:13–7.
22. Jacobs MR. How can we predict bacterial eradication? Int J Infect Dis 2003;7(1):13–20.
23. File TM Jr, Benninger MS, Jacobs MR. Evolution of amoxicillin/clavulanate in the treatment of adults with acute bacterial rhinosinusitis and community-acquired pneumonia in response to antimicrobial-resistance patterns. Clin Lab Med 2004;24(2):531–51.
24. Kaye CM, Allen A, Perry S, et al. The clinical pharmacokinetics of a new pharmacokinetically enhanced formulation of amoxicillin/clavulanate. Clin Ther 2001;23(4):578–84.
25. Garau J. Performance in practice: bacteriological efficacy in patients with drug-resistant Streptococcus pneumoniae. Clin Microbiol Infect 2003;9(1):28. Abstract S167.
26. Sethi S, Breton J, Wynne B. Efficacy and safety of pharmacokinetically enhanced amoxicillin/clavulanate (AMX/CA) 2000/125 mg b.i.d. for 5 days vs AMX/CA 875/125 mg b.i.d. for 7 days in the treatment of acute exacerbations of chronic bronchitis (AECB). 43rd Interscience Conference on Antimicrobial Agents and Chemotherapy, Chicago, IL, 2003. Abstract L-1592. P. 427.
27. Richard MP, Wynne B, et al. Clinical safety of pharmacokinetically enhanced amoxicillin/clavulanate compared with currently approved formulations of amoxicillin/clavulanate. 41st Interscience Conference on Antimicrobial Agents and Chemotherapy, Chicago, IL, 2001. Abstract 952. Р. 25.
28. File T, Lode H, Kurz H, et al. Comparative efficacy/safety of pharmacokinetically enhanced amoxicillin/clavulanate 2000/125 mg vs amoxicillin/clavulanate 875/125 mg in communityacquired pneumonia (CAP). 99th International Conference of the American Thoracic Society, Seattle, WA, 2003. Abstract B11. P. A370.
29. Rosenfeld RM, Andes D, Bhattacharyya N, et al. Clinical practice guideline: adult sinusitis. Otolaryngol Head Neck Surg 2007; 137 (3):1–31.
30. World Health Organization. WHO ModelPrescribing Information. Drugs used in Bacterial Infections. 2001. WHO, Geneva, Switzerland.
31. Mandell LA, Wunderink RG, Anzueto A, et al. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007;44(2):27–72.
32. American Academy of Pediatrics Subcommittee on Management of Acute Otitis Media. Diagnosis and management of acute otitis media. Pediatrics 2004;113(5):1451–65.
33. Augmentin XR, prescribing information. GlaxoSmithKline, Research Triangle Park, NC, USA, 2002.
34. File TM Jr, Jacobs MR, Poole MD, Wynne B. Outcome of treatment of respiratory tract infections due to Streptococcus pneumoniae, including drug-resistant strains, with pharmacokinetically enhanced amoxycillin/clavulanate. Int J Antimicrob Agents 2002;20(4): 235–47.
35. Anon JB, Berkowitz E, Breton J, et al. Efficacy/safety of amoxicillin/ clavulanate in adults with bacterial rhinosinusitis. Am J Otolaryngol 2006;27(4):248–54.
36. Garau J, Twynholm M, Garcia-Mendez E, et al. Comparative efficacy and safety of pharmacokinetically
enhanced amoxicillin/clavulanate 2000/125 mg b.d. versus amoxicillin/ clavulanate 875/125 mg t.d.s. in community-acquired pneumonia (CAP). 12th European Congress of Clinical Microbiology and Infectious Diseases. Milan, Italy, April 24–27, 2002.
37. Petitpretz P, Chidiac C, Soriano F, et al. The efficacy and safety of oral pharmacokinetically enhanced amoxycillin-clavulanate 2000/125 mg, twice daily, versus oral amoxycillin-clavulanate 1000/125 mg, three times daily, for the treatment of bacterial community-acquired pneumonia in adults. Int J Antimicrob Agents
2002;20(2):119–29.
38. Каманин Е.И., Стецюк О.У. Инфекции верхних дыхательных путей и ЛОР-органов / Под редакцией Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова. Антибактериальная терапия. Практическое руководство. М., 2000.
39. Andes D, Anon J, Jacobs MR, et al. Application of pharmacokinetics and pharmacodynamics to antimicrobial therapy of respiratory tract infections. Clin Lab Med 2004;24(2):477–502.