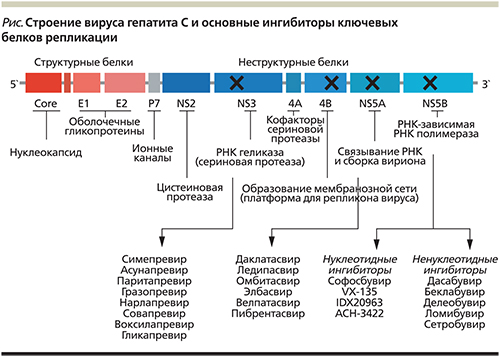
Рост частоты цирроза печени (ЦП) среди больных хроническим гепатитом С (ХГС) обусловлен высокой распространенностью и ежегодной заболеваемостью HCV-инфекцией пациентов с сопутствующими заболеваниями (ко-инфекция, ВИЧ, HBV, ожирение, алкогольный стеатоз и стеатогепатит и неалкогольный стеатогепатит в рамках распространенной в популяции жировой болезни печени, сахарный диабет, синдром перегрузки железом), приводящих к быстрому прогрессированию фиброза печени. Кроме того, естественное течение ХГС с пиком заболеваемости в России в 1990–1995 гг. привело к формированию ЦП в среднем у 20–30% больных в течение 20–30 лет хронической инфекции, а в группах риска вероятность развития ЦП повышается до 56% [1–3]. Число больных ЦП увеличивается также за счет использования неудачной в прошлом схемы лечения интерферонами (до 50% рецидива ХГС с исходом в дальнейшем в ЦП, до 85% рецидива инфекции при наличии ЦП) и сложных схем терапии иммунодепрессантами и генно-инженерными биологическими препаратами в ревматологии, онкологии, гематологии, трансплантологии инфицированных HCV пациентов. Бессимптомные варианты течения HCV-инфекции, в т.ч. на стадии ЦП, способствуют его позднему распознаванию и росту других глобальных проблем – декомпенсированного ЦП и гепатоцеллюлярного рака (ГЦР). Отсутствие настороженности со стороны врачей общей практики и «узких» специалистов также способствует увеличению числа больных ЦП. Достижения молекулярной биологии последних лет позволили изучить цикл вируса гепатита С в инфицированных гепатоцитах и уточнить основные белки вируса, обеспечивающие его выживание. В свою очередь высокотехнологичные терапевтические стратегии сделали доступными в реальной клинической практике последних трех лет прямые противовирусные препараты (ПВП), направленные на ингибирование ключевых белков репликации (см. рисунок): NS3/4 протеазы, NS5A белка, NS5B полимеразы вируса, и внедрить в клиническую практику безинтерфероновые режимы лечения ХГС, что значительно повысило эффективность противовирусной терапии (ПВТ). Комбинации ПВП, направленные на ингибирование различных белков вируса гепатита С, стали основой ПВТ последних трех лет в связи с высоким вирусологическим ответом, хорошей переносимостью, легкостью использования в реальной клинической практике, а также отсутствием нежелательных явлений лечения. В настоящее время основные усилия исследователей направлены на создание лекарственных средств, высокоэффективных и безопасных для больных компенсированным и декомпенсированным ЦП, а также трудной категории пациентов с ВИЧ-инфекцией, хронической болезнью почек, внепеченочными проявлениями, криоглобулинемическим васкулитом, HCV-ассоциированной В-клеточной лимфомой и рецидивом HCV-инфекции в трансплантате. Рекомендации по лечению ПВП после первого их применения в 2011 г. обновляются и уточняются дважды в год после конгрессов гепатологов в Европе (EASL) и США (AASLD) [6, 7]. Выбор терапии ЦП определяется генотипом вируса, т.к. большинство ПВП моногенотипные и направлены на 1-й или 2–3-й генотипы вируса. Если у пациента 1-й генотип HCV, исследуются субтипы 1а и 1b, которые могут изменить тактику лечения. Проводится оценка стадии фиброза неинвазивными методами (эластометрия печени) и степени компенсации цирроза по шкале Чайлд–Пью (класс А, В, С). Для больных декомпенсированным ЦП рассчитывается сумма баллов по шкале MELD. Необходимо также выявить сопутствующие заболевания (коморбидность) и уточнить их лечение, т.к. ряд лекарственных препаратов взаимодействует с ПВП и может резко снижать их эффективность [6, 7]. Межлекарственные взаимодействия при применении ПВП представлены на постоянно обновляемых информационных ресурсах в Интернете [6]. Следует помнить о правилах, выработанных еще при интерфероновых режимах ПВТ: пациенты с ЦП и F3-стадией фиброза подлежат «незамедлительной» терапии в связи с риском «печеночной» смерти и ГЦР, обязательной ПВТ подлежат также больные F2-стадией фиброза по шкале METAVIR [6, 7]. Всем пациентам c вирусным ЦП необходимо проводить тщательное динамическое наблюдение в ходе ПВТ, особенно в отношении анемии при дополнительном назначении рибавирина (РБВ), печеночно-клеточной функции (альбумин, холестерин, протромбин, холинэстераза, общий и прямой билирубин) при лечении декомпенсированного ЦП.
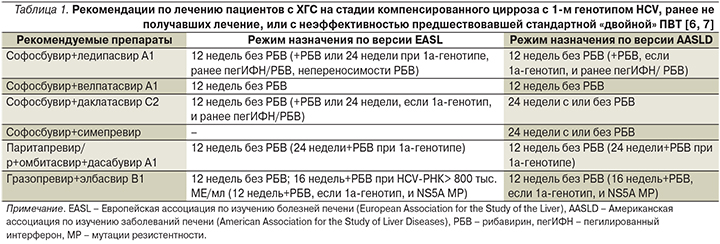
В июле и сентябре 2016 г. опубликованы последние рекомендации EASL и AASLD по лечению ЦП при ХГС, что легло в основу информации по выбору оптимального лечения вирусного цирроза печени в мире и в нашей стране (табл. 1–4).
Все рекомендуемые схемы лечения ПВП для 1-го генотипа вируса имеют высокую степень доказательности эффективности. Основной терапевтической схемой у первичных нелеченых пациентов с компенсированным ЦП при 1-м генотипе вируса является комбинация софосбувира (Соф) 400 мг и ледипасвира (Лед) 90 мг в одной таблетке 1 раз в день утром во время еды в течение 12 недель. При 1а-генотипе вируса лечение комбинацией Соф+Лед первичных пациентов в течение 12 недель комбинируют с РБВ, рассчитанным по весу пациента: <75 кг–1000 мг/сут, > 75 кг–1200 мг/сут (степень доказательности А1). При плохой переносимости РБВ или противопоказаниях к нему рекомендована терапия Соф+Лед при 1а-генотипе в течение 24 недель (степень доказательности В1). Комбинация Соф+Лед+РБВ на протяжении 12 недель показана также больным компенсированным ЦП с классом А по Чайлду–Пью, 1а-генотипом и наличием исходных мутаций резистентности (МР) NS5A (если они исследованы) к Лед в позициях M28A/G/T, Q30E/G/H/K/R, L31M/V, P32L/S, H58D и/или Y93C/H/N/S. Пациенты с 1а-генотипом без данных мутаций могут получать лечение Соф+Лед без РБВ с планируемым достижением устойчивого вирусологического ответа (УВО) на 12-й неделе (в 97% случаях) [6].
Наиболее оптимальным режимом лечения компенсированного ЦП при 1-м, 2-, 3-м генотипах HCV в настоящее время считается комбинация двух пангенотипных препаратов: Соф 400 мг и велпатасвира (Вел) 100 мг в одной таблетке 1 раз в день во время еды 12 недель без РБВ: УВО на 12-й неделе достигается в 99% случаев [6]. Лечение компенсированного ЦП с 1-м генотипом вируса Соф 400 мг+даклатасвиром (Дак) 60 мг в режиме 1 раз в день во время еды проводится в течение 24 недель в комбинации с РБВ, рассчитанным по весу <75/>75 кг 1000/1200 мг, или без РБВ на усмотрение врача, оценивающего факторы прогноза ответа на ПВТ. УВО на 12-й неделе у пациентов с 1а-генотипом HCV достигается в 76% случаев, получающих комбинированную терапию Соф+Дак+РБВ в течение 24 недель, и у 100% пациентов с 1в-генотипом вируса, однако долгосрочный прогноз не оценен. В любом случае риск появления резистентности к ингибитору неструктурного белка 5А (NS5A) может обусловить неудачу терапии, в связи с чем всем пациентам с 1а-генотипом и ЦП рекомендован 24-недельный курс ПВТ в комбинации с РБВ [7].
3D-терапия (Викейра Пак) фиксированными дозами паритапревира (Пар) 75 мг, усиленного ритонавиром (Р) 50 мг, в комбинации с омбитасвиром 12,5 мг в одной таблетке (2 таблетки утром) в комбинации с дасабувиром (Дас) 250 мг дважды в день во время еды (суточная доза – 150/100/50 мг и 500 мг соответственно) и РБВ по весу <75/>75 кг 1000/1200 мг 24 недели у пациентов с компенсированным ЦП и 1а-генотипом HCV позволяет достигать УВО на 12-й неделе 94% пациентов, 12-недельный курс лечения характеризовался УВО на 12-й неделе у 89% пациентов [8]. Рекомендации по лечению больных с 1-м генотипом вируса Викейрой Пак зависят от степени компенсации ЦП: при компенсированном ЦП, класс A по Чайлду–Пью 3D-терапия рекомендована; при декомпенсированном ЦП, класс В и С по Чайлду–Пью противопоказана. При 1-м генотипе HCV 3D-терапия в течение 12 недель без РБВ характеризуется достижением УВО на 12-й неделе у 89–96,7% пациентов [8, 9]. Пациенты с компенсированным ЦП должны быть информированы о редком нежелательном явлении (НЯ) – декомпенсации ЦП с быстрым нарастанием уровня билирубина и трансаминаз сыворотки и подлежат тщательному динамическому мониторингу ПВТ.
Гразопревир (Граз) 100 мг и элбасвир (Элб) 50 мг в одной таблетке 1 раз в день 12 недель без РБВ рекомендованы для пациентов с 1в-генотипом вируса. Если нет данных о мутациях резистентности к NS5A региону вируса, то при 1а-генотипе ориентируются на вирусную нагрузку (ВН): при ВН >800 тыс. МЕ/мл лечение проводят в течение 16 недель с РБВ по весу <75/>75 кг 1000/1200 мг, при виремии ≤800 тыс. МЕ/мл длительность терапии 12 недель без РБВ. При наличии исходных мутаций резистентности к Элб в зоне NS5A (М28А/G/T, Q30D/E/G/H/K/L/R, L31F/M/V, H58D и/или Y93C/H/N/S) пациенты ЦП с 1а-генотипом вируса и высокой ВН >800 тыс. МЕ/мл получают лечение 16 недель с РБВ по весу. Без мутаций резистентности и при низкой вирусной нагрузке <800 тыс. МЕ/мл – 12 недель без РБВ [7].

В Рекомендациях Американской ассоциации по изучению заболеваний печени (American Association for the Study of Liver Diseases, AASLD) для пациентов с компенсированным ЦП с 1-м генотипом вируса рекомендована также терапия симепревиром (Сим) 150 мг/сут и Соф 400 мг/сут с или без РБВ, рассчитанным по весу <75/>75 кг 1000/1200 мг, в течение 24 недель в отсутствие клинически значимой мутации резистентности Q80K. Эффективность ПВТ достигает 95–97% [7]. Не рекомендуется исследование мутаций резистентности до начала терапии ПВП. Встречаемость исходных мутаций NS5A составляет 10–15% при 1-м генотипе и обусловливает снижение активности NS5A ингибиторов более чем в 5 раз при 1а-генотипе вируса и наличии клинически значимых мутаций резистентности в позициях М28,Q30, L31и Y93, выявляемых у 5–10% пациентов [7]. Тестирование вариантов резистентности перед выбором схемы лечения обсуждается в отдельных группах: при наличии длительно существующих HCV-инфекции и ЦП, отсутствии эффекта от предшествовавшей ПВТ, в т.ч. с использованием ПВП 1-го поколения. Преодоление резистентности возможно комбинацией различных ПВП, в т.ч. с РБВ, и увеличением длительности терапии до 24 недель.
У пациентов с компенсированным ЦП С и генотипом-2 наиболее эффективной схемой ПВТ является комбинация Соф+Вел 12 недель без РБВ с достижением УВО на 12-й неделе в 99–100% случаев. Данная схема лечения не зависит от мутаций резистентности ключевых белков вируса NS5A и NS5B [6, 7]. Альтернативной схемой ПВТ при компенсированном ЦП является комбинация Соф+Дак без РБВ в течение 16 или 24 недель в зависимости от коморбидности.
ПВТ компенсированного ЦП с 3-м генотипом HCV у первичных (нелеченых) больных проводится комбинацией Соф+Вел +PБВ 12 недель, учитывая возможный риск Y93-мутаций резистентности в этой группе пациентов. УВО на 12-й неделе в клинических исследованиях достигается в 93% случаев. При непереносимости или наличии противопоказаний к назначению РБВ лечение Соф+Вел проводится в течение 24 недель [7]. Альтернативное лечение компенсированного ЦП с 3-м генотипом HCV Соф+Дак+РБВ по весу в течение 24 недель.
В России для лечения компенсированного ЦП при 1-м генотипе HCV зарегистрированы Соф+Дак, Соф+Сим, Дак+асунапревир (Асун), 3D-терапия Пар/р+омбитасвир+Дас. Доступными в реальной клинической практике в связи с трудностями, обусловленными поставками софосбувира в аптечную сеть, являются лишь две схемы лечения компенсированного ЦП в исходе ХГС: Дак 60 мг один раз в день+Асун 100 мг 2 раза в день во время еды 24 недели и 3D-терапия Викейрой Пак, применяемая согласно рекомендациям EASL и AASLD [10, 12–14]. Терапия Дак+Асун проводится 24 недели без РБВ при ЦП с 1b-генотипом HCV. Эффективность данной схемы лечения при компенсированном ЦП достигает 91% у ранее не леченных больных. Пациенты с неэффективностью предыдущей двойной ПВТ или имевшие в прошлом непереносимость и/или противопоказания к назначению терапии интерферонами имели УВО на 12-й неделе в 82 и 83% случаев соответственно. УВО на 12-й неделе в различных группах пациентов отмечен вне зависимости от таких исходных характеристик пациентов, как возраст, пол, раса, генотип ИЛ28В: эффективность у пожилых пациентов (старше 65 лет) составила 100% [12, 13]. В отсутствие клинически значимых исходных мутаций резистентности NS5A участка вируса в позиции Y93 и L31 УВО на 12-й неделе достигают 93,5–98% пациентов [12, 13]. Компенсированный ЦП не влияет на эффективность ПВТ, но при декомпенсированном ЦП, класс В и С по Чайлду–Пью, комбинация Дак+Асун противопоказана [14].
Доступных комбинаций ПВТ для лечения пациентов с ЦП и 3-м генотипом вируса С в настоящий момент в РФ нет в связи с отсутствием Соф в аптечной сети.
Лечение пациентов с декомпенсированным ЦП с наличием показаний к ортотопической трансплантации печени (ОТП) или без них без ГЦР представлено в табл. 4. Безынтерфероновый режим – единственно возможное лечение в этой группе больных печеночно-клеточной недостаточностью (менее 18–20 баллов по шкале MELD) и у пациентов после трансплантации печени. ПВТ проводится незамедлительно, доза РБВ первоначально может быть 600 мг с подбором переносимой дозы в последующем. При декомпенсированном ЦП не используются ингибиторы протеазы NS3/4A.
Пациентам с компенсированным ЦП и ГПЦ, находящимся в листе ожидания ОТП, показана незамедлительная ПВТ до проведения ОТП по общим рекомендациям для пациентов с компенсированным ЦП без ГЦР. Пациентам с рецидивом HCV-инфекции после ОТП и компенсированным или декомпенсированным ЦП (классы А, В, С по Чайлду–Пью) при 1-м и 2-м генотипах HCV рекомендована комбинация Соф+Вел+РБВ в течение 12 недель. При 3-м генотипе комбинация Соф+Вел+РБВ рекомендована к применению в течение 24 недель. Необходимость в РБВ для лечения рецидива HCV-инфекции после ОТП при компенсированном ЦП (класс А по Чайлду–Пью) не продемонстрирована и нуждается в дальнейшем изучении [6]. Стартовая доза РБВ при декомпенсированном ЦП может быть 600 мг в зависимости от уровня гемоглобина и степени тяжести ЦП с постепенным подбором переносимой дозы. При непереносимости РБВ или наличии противопоказаний к его применению в отношении пациентов с декомпенсированным ЦП рекомендованы Соф+Вел и Соф+Дак в течение 24 недель без РБВ.
Пациенты с декомпенсированным ЦП (классы В и С по Чайлду–Пью) в отсутствие показаний к ОТП должны наблюдаться в специализированных центрах. При ЦП с 1-м генотипом вируса рекомендованы Соф+Лед+РБВ, Соф+Вел+РБВ, Соф+Дак+РБВ в течение 12 недель. При 2-м генотипе HCV применяют Соф+Вел+РБВ или Соф+Дак+РБВ в течение 12 недель. При 3-м генотипе HC-терапию Соф+Вел+РБВ или Соф+Дак+РБВ продлевают до 24 недель как и при наличии противопоказаний к РБВ или при его непереносимости. Доза РБВ рассчитывается по весу <75/>75 кг 1000/1200 мг, но в связи с тяжестью состояния пациента и декомпенсацией ЦП может быть уменьшена до 600 мг с последующим подбором переносимой дозы.
Таким образом, лечение компенсированного и декомпенсированного ЦП в исходе ХГС широко практикуется в мире, но в Российской Федерации представляет значительные трудности, имеет ограниченные возможности и требует обсуждения необходимости незамедлительной регистрации генериков для лечения сложной и довольно многочисленной когорты больных ХГС.



