Несмотря на усилия ученых, врачей и органов управления здравоохранения, артериальная гипертензия (АГ) в Российской Федерации остается одной из наиболее значимых медико-социальных проблем. Это обусловлено как широким распространением данного заболевания (около 40 % взрослого населения РФ имеет повышенный уровень артериального давления [АД]), так и тем, что АГ является важнейшим фактором риска основных сердечно-сосудистых заболеваний – инфаркта миокарда и мозгового инсульта, главным образом определяющих высокую смертность в нашей стране [1].
Согласно современным представлениям, основной целью антигипертензивной терапии (АГТ) является снижение смертности и частоты осложнений. Поэтому в задачи лечения входит не только достижение целевого уровня АД, но и защита органов-мишеней (сердца, мозга, почек) [1]. Как показали крупные клинические исследования, для решения данной задачи большинству пациентов с АГ требовалось применение комбинации из двух и более препаратов [2]. В настоящее время комбинированная АГТ становится одним из основных направлений в терапии АГ. Современные подходы к лечению АГ значительно расширили показания к комбинированной АГТ: согласно российским рекомендациям по диагностике и лечению АГ 4-го пересмотра (2010), с нее рекомендуется начинать лечение, минуя стадию монотерапии, у больных АГ не только II–III, но даже и I степени при наличии высокого и очень высокого риска развития сердечно-сосудистых осложнений. При этом приоритет отдается применению фиксированных комбинаций, содержащих в одной таблетке два антигипертензивных препарата (АГП) [1]. При этом исследования, изучающие антигипертензивную эффективность и безопасность разных фиксированных комбинаций, малочисленны. В последнее десятилетие активно изучаются органопротективные эффекты разных АГП. Представлено множество работ, доказывающих способность практически всех групп АГП вызывать регресс поражений органов-мишеней (сердца, почек, головного мозга), в т. ч. коррекцию дисфункции эндотелия. Однако изучение органопротективного действия именно фиксированных комбинаций АГП только начинается. В табл. 1 приведены рациональные комбинации АГП и некоторые существующие в настоящее время фиксированные комбинации.
Таблица 1. Некоторые рациональные комбинации АГП и фиксированные комбинации АГП, применяемые в России.
Во всех имеющихся в настоящее время рекомендациях по лечению АГ (американских, европейских, российских) разработаны подходы к выбору группы АГП в разных клинических ситуациях, тогда как подходы к выбору рациональных комбинаций для разных подгрупп пациентов с АГ не разработаны вовсе [1, 3, 4]. И это при том, что во всех рекомендациях по лечению АГ приоритет отдается именно комбинированной терапии. В связи с этим в готовящейся 4-й редакции российских рекомендаций по диагностике и лечению АГ (2010) впервые в мире предпринимается попытка разработать показания к выбору двухкомпонентных антигипертензивных комбинаций в конкретных клинических ситуациях. Основные показания к назначению рациональных комбинаций АГП представлены в табл. 2 и 3.
Таблица 2. Преимущественные показания к назначению рациональных комбинаций АГП.
Рекомендации по выбору рациональных и возможных комбинаций АГП препаратов для лечения больных АГ в зависимости от клинической ситуации
Поражение органов-мишеней:
- ГЛЖ – АРА-II/ИАПФ с ТД или АК;
- бессимптомный атеросклероз – АРА-II/ИАПФ с АК;
- микроальбуминурия – АРА-II/ ИАПФ с ТД;
- поражение почек – АРА-II/ИАПФ с ТД;
Ассоциированные клинические состояния:
- предшествующий мозговой инсульт – любые рациональные комбинации АГП;
- предшествующий ИМ – β-АБ/АК с АРА-II/ИАПФ, β-АБ с АК;
- ИБС – β-АБ или АК с АРА-II или ИАПФ;
- ХСН – АРА-II/ИАПФ с β-АБ и ТД;
- почечная недостаточность/протеинурия – АРА-II/ИАПФ с петлевым диуретиком;
- заболевания периферических артерий – АК с АРА-II/ИАПФ;
Особые клинические ситуации:
- пожилые – АРА-II/ИАПФ с АК/ТД;
- ИСАГ – АК с ТД, АК или ТД с АРАII/ИАПФ;
- метаболический синдром – АРА-II/ ИАПФ с АК/ТД;
- сахарный диабет – АРА-II/ИАПФ с АК/ТД;
- беременность – метилдопа с АК/β-АБ.
В данной статье мы cфокусируем внимание на возможности применения наиболее часто используемой в нашей стране комбинации АГП– ИАПФ с ТД (тиазидным диуретиком).
В настоящее время комбинация ИАПФ и ТД по-прежнему является наиболее часто назначаемой из всех нефиксированных и фиксированных комбинаций АГП не только в нашей стране. Высокая эффективность и безопасность данной комбинации при лечении АГ отмечена в рекомендациях ВНОК, ЕОК-ЕОГ и JNC VII [1, 3, 4]. Рациональность комбинации ИАПФ с диуретиком для лечения больных АГ полностью обоснована. Так, антигипертензивное действие ИАПФ основано в первую очередь на уменьшении продукции ангиотензина II, поэтому наиболее выраженное антигипертензивное действие они оказывают на пациентов с повышенной активностью ренин-ангиотензин-альдостероновой системы (РААС), что было показано в ряде исследований [5]. При этом антигипертензивный эффект всех диуретиков ограничен неизбежно возникающими на фоне их применения реактивной гиперренинемией и вторичной гиперальдостеронемией, связанными с активацией РААС, выраженность которых значительно снижается при одновременном назначении ИАПФ. Совместное применение ИАПФ и диуретиков позволяет значительно повысить эффективность обоих препаратов, что ведет к расширению круга пациентов, отвечающих на терапию, позволяя чаще достигать целевого уровня АД [5]. У больных с нормои низкорениновой АГ эффективность ИАПФ невысока, но добавление диуретика помогает повысить активность ренина, восстановив чувствительность к ИАПФ. В результате эта комбинация эффективно снижает АД практически у всех пациентов независимо от исходной активности РААС, что позволяет использовать ее при нормо- и даже гипорениновой формах АГ [5]. Это крайне важно для лечения пожилых больных, поскольку у них нормо- и гипорениновые формы встречаются весьма часто.
Дополнительное снижение АД при комбинированной терапии диуретиком и ИАПФ также обусловлено тем, что последние потенцируют натрийуретический эффект мочегонных препаратов, повышая их эффективность. Совместное применение ИАПФ и диуретиков приводит к аддитивному антигипертензивному эффекту при использовании меньших доз обоих АГП [5].
ИАПФ предотвращают развитие гипокалиемии, возникающей в результате стимуляции выработки альдостерона под действием диуретиков, за счет уменьшения активности ангиотензина II и снижения концентрации альдостерона, что способствует обратному всасыванию калия, теряемого при назначении мочегонных препаратов. Одновременно совместное применение ИАПФ и диуретиков способствует усиленному выведению натрия из организма, тем самым уменьшая нагрузку объемом [5]. При проведении комбинированной терапии очень важны метаболические эффекты ТД и ИАПФ, особенно влияние на инсулинорезистентность, т. к. ее наличие связано с увеличением сердечно-сосудистого риска у больных АГ [2]. Применение диуретиков сопряжено с отрицательным влиянием на углеводный, липидный и пуриновый обмены, способствуя повышению уровней мочевой кислоты, глюкозы и холестерина в крови, что значительно ограничивается при совместном применении с ИАПФ, противодействующими неблагоприятному влиянию мочегонных препаратов [5].
При наличии множества положительных моментов существует несколько проблем, связанных с использованием комбинации ИАПФ и диуретика. Применяя данную комбинацию в качестве средства первого выбора, можно опасаться развития гипотонии из-за эффекта первой дозы. Добавление ИАПФ к мочегонному средству может ухудшить функцию почек у больных сердечной недостаточностью, однако эти проблемы возможно решить посредством тщательного контроля за пациентом в первые дни лечения и постепенного титрования дозы ИАПФ [5].
Снижение доз диуретика и ИАПФ в рациональной комбинации происходит не только без потери, но даже и с увеличением антигипертензивного эффекта, а также снижением риска побочных явлений при лечении этой комбинацией препаратов. Применение комбинации ИАПФ + диуретик позволяет достигать целевого уровня АД более чем у 80 % больных АГ: имея высокую антигипертензивную эффективность, эта комбинация доказала разноплановый органопротективный эффект в виде уменьшения выраженности гипертрофии миокарда левого желудочка (ГМЛЖ), нефропротекции и способности восстанавливать нарушенную эндотелиальную функцию [5]. Данная комбинация АГП предназначена в первую очередь пациентам с хронической сердечной недостаточностью, ГМЛЖ, при диабетической и недиабетической нефропатии. Она также очень эффективна у пожилых пациентов, больных изолированной систолической АГ (ИСАГ), при неэффективности монотерапии ИАПФ или диуретиками (табл. 2, 3).
При комбинированной АГТ с помощью ИАПФ и диуретика принципиально важным остается вопрос о безопасной дозы ТД, т. к. еще в 1959 г. появилось первое сообщение о том, что ГХТ может вызывать нарушение толерантности к глюкозе. С того времени накопилось множество свидетельств о неблагоприятном влиянии ТД на показатели углеводного обмена у больных АГ независимо от наличия или отсутствия сахарного диабета [5]. Помимо неблагоприятного влияния на углеводный обмен ТД могут негативно воздействовать на липидный обмен. Результаты ряда клинических исследований показали, что применение ТД приводит к повышению уровня общего холестерина на 5–20 % и триглицеридов на 15–30 % от исходного уровня [6]. В настоящее время доказано, что только низкие дозы ТД (не более 12,5– 25,0 мг ГХТ в сутки) могут быть использованы для постоянного лечения больных АГ – даже в сочетании с ИАПФ. Безопасность низких доз ГХТ в сочетании с ИАПФ выявлена в ряде исследований. Так, например, в многоцентровом исследовании, включившем 505 пациентов, применение 12,5 мг ГХТ в комбинации с 10 мг лизиноприла уменьшало АД так же эффективно, как и 25 мг ГХТ [7]. Но более высокая доза ТД привела к снижению уровня калия и увеличению уровня глюкозы в плазме крови. Авторы этого исследования сделали вывод, что при неэффективности монотерапии предпочтительно перевести больного на комбинированную терапию вместо увеличения дозы ТД. Еще в одном многоцентровом исследовании с участием 402 пациентов к эналаприлу (20 мг/суг) добавляли ГХТ (6,25 или 12,50 мг/сут) [8]. Присоединение обеих доз ТД привело к практически двукратному нарастанию антигипертензивного эффекта по сравнению с мо нотерапией эналаприлом, однако более высокая доза ГХТ не имела явного преимущества. Обе дозы ГХТ показали одинаковую безопасность в отношении побочных эффектов и не привели к метаболическим нарушениям [8]. C учетом имеющихся на сегодняшний день данных оптимально начинать лечение с низких доз ИАПФ (например, лизиноприла 10 мг/сут) и ТД (6,25–12,5 мг/сут ГХТ) с возможным последующим увеличением доз одного или обоих препаратов вдвое (предпочтительнее вначале увеличить вдвое дозу ИАПФ, а затем в случае недостижения целевого АД увеличить вдвое и дозу ГХТ). Особое значение это свойство комбинации ИАПФ и ГХТ в дозах не более 12,5 мг имеет в гериатрической практике, поскольку практически все больные пожилого возраста имеют сопутствующий атеросклероз коронарных, сонных и бедренных артерий.
Антигипертензивная эффективность комбинаций различных ИАПФ с диуретиками подтверждена рядом исследований, в т. ч. российских [9–13]. Так, например, одним из представителей класса ИАПФ является лизиноприл. В многоцентровом исследовании были изучены антигипертензивная эффективность, влияние на функцию почек терапии лизиноприлом и его фиксированной комбинации с диуретиком ГХТ у больных АГ [13]. В исследовании участвовали 58 пациентов (27 мужчин и 31 женщина) 33–75 лет (55,0 ± 1,5 года) со средней длительностью АГ 12,3 ± 1,4 года. У 61 % больных имела место АГ I и у 39 % II степени тяжести по классификации ВНОК 2007 г. по уровню АД. Через 2 недели “чистого фона” все больные начинали лечение лизиноприлом в дозе 10 мг/сут однократно утром. Через 2 недели у больных, не достигших целевого уровня АД (≤ 140/90 мм рт. ст., а при наличии сахарного диабета ≤ 130/80 мм рт. ст.), доза лизиноприла удваивалась (20 мг/ сут). Если монотерапия лизиноприлом не позволяла достигать целевого уровня АД, к лечению добавляли диуретик ГХТ в виде фиксированной комбинации с лизиноприлом (20 мг лизиноприла/12,5 мг ГХТ) по одной таблетке однократно утром и назначали дополнительный визит через 2 недели для оценки эффективности препарата. При недостижении целевого уровня АД на фоне комбинированной терапии доза данной фиксированной комбинации удваивалась (40 мг лизиноприла/ 25 мг ГХТ). Состояние функции почек как органа-мишени при АГ и ее динамику оценивали при помощи пробы Реберга с расчетом скорости клубочковой фильтрации (СКФ) и определения микроальбуминурии (МАУ) в суточной моче [13].
Авторы отмечают, что на фоне монотерапии лизиноприлом в дозе 10–20 мг/сут в целом по группе через 4 недели терапии происходило достоверное снижение АД со 151,2 ± 1,2/92,2 ± 1,2 до 137,2 ± /85,8 ± 1,2 мм рт. ст. (Δ -14,0 ± 1,0/-6,4 ± 0,8; p < 0,001). Целевого уровня АД достигли 37 % больных, остальных пациентов перевели на фиксированную комбинацию с 12,5 мг ГХТ. За 16 недель лечения в среднем по группе АД снизилось со 151,2 ± 1,2/92,2 ± 1,2 до 127,4 ± 1,0/79,2 ± 0,9 мм рт. ст. (Δ -23,8 ± 1,5/-13,0 ± 1,1; p < 0,001). Достоверной динамики частоты сердечных сокращений не отмечено. Целевого АД достигли 98 % пациентов [13].
Поскольку больных с почечной недостаточностью не включали в исследование, уровень креатинина крови у всех пациентов оставался в пределах 63,7–140,0 (89,2 ± 2,4) мкмоль/л. СКФ колебалась от 69,8 до 187,1 (98,7 ± 4,5) мл/мин. У 28 % больных выявлена гиперфильтрация, которая является основным неиммунным механизмом прогрессирования гипертонической нефропатии, со временем ведущей к снижению СКФ и повышению уровня азотистых шлаков крови [14], что подтверждается наличием отрицательной корреляционной зависимости уровня креатинина от СКФ. МАУ была выявлена у 72 % больных. Суточная экскреция альбумина составила 5–290 (45,3 ± 6,0) мг/сут. Выраженность МАУ нарастала с увеличением тяжести АГ (r = 0,57, p = 0,003) от 37,1 ± 4,4 мг/сут при I до 58,8 ± 13,9 мг/сут при II степени тяжести АГ (p = 0,003) [13].
Авторы также отметили, что лечение лизиноприлом в виде монотерапии и его фиксированной комбинацией с ГХТ привело к снижению уровня МАУ более чем в 2 раза (ΔМАУ -28,6 ± 3,9 мг/сут; p < 0,001), а также увеличению СКФ с 80,8 ± 2,6 до 97,7 ± 3,0 мл/мин (ΔСКФ 20,7 ± 3,4 мл/мин, р < 0,001) у больных с исходно нормальной и сниженной СКФ и уменьшению СКФ со 145,7 ± 5,1 до 120,2 ± 7,3 мл/мин (ΔСКФ -26,9 ± 7,3 мл/мин; p = 0,005) при исходной гиперфильтрации. Разнонаправленное влияние терапии на СКФ у больных с исходно нормальным и повышенным этим показателем является положительным моментом, поскольку гиперфильтрация в настоящее время рассматривается как основной неиммунный механизм развития нефросклероза, что ведет к прогрессированию АГ и развитию почечной недостаточности [2, 5, 14]. Отсутствие снижения СКФ на фоне АГТ у больных без гиперфильтрации свидетельствует об отчетливом нефропротективном эффекте терапии. Снижение уровня МАУ за 16 недель терапии произошло у всех (100 %) больных, с нормализацией – у 88 % больных с исходно повышенной МАУ [13].
По сообщению исследователей, в группе больных, оказавшихся “нечувствительными” к монотерапии лизиноприлом, имевших исходно достоверно более высокий уровень креатинина крови и более низкую СКФ, комбинированная терапия лизиноприлом с ГХТ благоприятно воздействовала на функцию почек в виде статистически значимого снижения уровня МАУ с 53,1 ± 9,2 до 20,4 ± 5,4 мг/сут (ΔМАУ -32,7 ± 5,8 мг/сут, р < 0,001) и увеличения СКФ с 87,4 ± 4,2 до 113,3 ± 3,5 мл/мин (ΔСКФ 25,9 ± 3,1 мл/мин, р < 0,001) [13].
Следует обратить внимание на тот факт, что биохимические показатели крови (калий, натрий, глюкоза, аланинаминотрансфераза, аспартатаминотрансфераза) на фоне терапии обоими препаратами достоверно не изменялись. Переносимость лизиноприла и его фиксированной комбинации с ГХТ была хорошей, различий в переносимости выявлено не было. Нежелательные явления в виде сухого кашля отмечены у одного больного, имели легкую степень выраженности и прошли самостоятельно после отмены препарата [13].
Есть также данные об эффективность и безопасности комбинаций других ИАПФ, например эналаприла, периндоприла, моэксиприла, фозиноприла, с тиазидными и тиазидоподобными диуретиками [9–12]. Однако практически все исследования с использованием ИАПФ и диуретика за редким исключением [9, 12] не ставили перед собой цель оценивать эффективность и безопасность лечения комбинацией препаратов. Как правило, речь шла либо об ИАПФ, либо о диуретике, а второй препарат присоединялся только при неэффективности первого, что диктует необходимость дальнейших исследований.
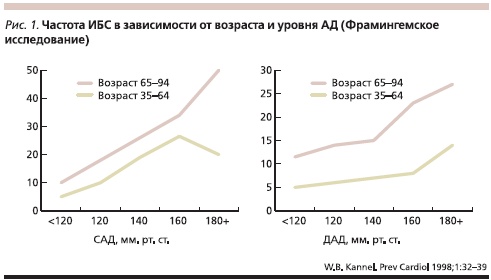
Проблема АГ особенно актуальна для пожилых больных, поскольку распространенность АГ нарастает с возрастом и после 50 лет превышает 50 %, а у лиц старше 80 лет – 80 % [15]. Кроме того, наличие АГ оказывает существенное влияние на состояние здоровья, продолжительность и качество жизни пожилых пациентов, поскольку она является самостоятельным прогностически независимым фактором риска развития таких сердечно-сосудистых заболеваний, как инсульт, ИБС, а также преждевременной смерти. Так, возраст старше 55 лет для мужчин и старше 65 лет для женщин является одним из дополнительных факторов риска при стратификации риска сердечнососудистых осложнений [16]. Другими словами, при одинаковом уровне АД, как систолического, так и диастолического, риск развития ИБС (рис. 1) и инсульта всегда выше у больного пожилого возраста по сравнению с более молодыми пациентами. Поэтому при лечении пожилых больных особенно важно достижение целевых уровней АД. В связи с этим высокая антигипертензивная эффективность комбинации ИАПФ и диуретика, в частности лизиноприла и ГХТ, имеет весьма существенное значение.
Такое выраженное увеличение частоты АГ у пожилых лиц имеет свое объяснение с точки зрения патогенеза. С возрастом (после 60 лет) даже у практически здоровых людей количество функционирующих нефронов уменьшается в 2 раза [17]. Соответственно, уменьшается площадь фильтрации и возникают объем-зависимые подъемы АД. Это создает условия для повышения эффективности диуретиков при лечении АГ у лиц данной возрастной группы. С возрастом также снижается растяжимость аорты, что в настоящее время считают основным механизмом развития ИСАГ у пожилых [18, 19], возрастает чувствительность к поваренной соли [20] и развивается дисфункция эндотелия (снижается выработка сосудорасширяющих факторов, в частности оксида азота, и повышается сосудосуживающихся) [21].
C возрастом увеличивается частота ИСАГ, превышая 40 % у больных старше 60 лет [22]. Под ИСАГ понимают повышение уровня систолического АД (САД) до 140 мм рт. ст. и выше при диастолическом АД (ДАД) менее 90 мм рт. ст. [1]. С другой стороны, среди пациентов с ИСАГ преобладают лица старше 60 лет: в данной возрастной подгруппе ИСАГ составляет 65–75 % от всех случаев АГ [22]. Это, по-видимому, связано с тем, что повышение САД происходит по меньшей мере до 80-летнего возраста, в то время как диастолического – только до 50-летнего, а затем оно либо выравнивается, либо имеет тенденцию к снижению (рис. 2) [23].

Важность выделения проблемы ИСАГ связана с тем, что повышение САД, в т. ч. изолированное (при нормальном ДАД), является важным фактором риска развития сердечнососудистых, церебральных осложнений и хронической почечной недостаточности [24, 25]. Поэтому расценивать повышение САД как проявление возрастной нормы, как это было около 10 лет назад, является серьезной ошибкой, которая имеет для больного самые серьезные последствия. Повышение САД и ДАД как факторов риска развития всех осложнений АГ минимум равнозначны, и необходимо добиваться их полной нормализации. Более того, во многих случаях повышение САД играет даже большую роль в развитии сердечно-сосудистых осложнений: у лиц всех возрастных групп риск развития всех сердечнососудистых осложнений АГ (ИБС, в т. ч. инфаркт миокарда, инсульт, сердечная недостаточность, атеросклероз периферических артерий) сильнее коррелировал с уровнем САД, а не ДАД [24, 25]. Установлено, что ИСАГ увеличивает смертность от сердечнососудистой патологии в 2–5 раз и общую смертность на 51 % по сравнению с таковой у лиц, имеющих нормальные показатели АД [24].
Средством первого выбора для лечения ИСАГ являются в т. ч. тиазидные и тиазидоподобные диуретики [1]. Их применение у больных с ИСАГ приводит не только к нормализации АД, но и к снижению смертности, риска осложнений (инфаркта, инсульта, сердечной и почечной недостаточности, деменции). Так, если снизить САД хотя бы на 12–13 мм рт. ст., это приведет к уменьшению риска развития ИБС и инсульта (на 21 и 37 % соответственно) и смертности от этих причин (на 27 и 36 % соответственно) [25]. В связи с этим применение фиксированных комбинаций, в состав которых входят диуретики, особо актуально в реальной клинической практике. Различия среди множества фиксированных комбинаций, содержащих комбинацию ИАПФ и ГХТ, базируются, конечно, на различиях в свойствах ИАПФ.
Особое внимание для лечения АГ у пожилых привлекают препараты, метаболизм которых не зависит от ряда факторов, в т. ч. функции печени. Хорошо известно, что больные старше 60 лет имеют множество сопутствующих заболеваний и одно из наиболее частых – это различная патология печени. Поэтому особое внимание при выборе ИАПФ для этой категории больных заслуживает лизиноприл. Его отличительными фармакокинетическими чертами являются очень низкая липофильность, отсутствие метаболизма в организме [26]. Прием пищи не влияет на всасывание препарата. Он единственный(!) из ИАПФ не метаболизируется в печени. Пик концентрации в крови отмечается через 7 часов после приема препарата. Период полувыведения составляет 12 часов, назначают лизиноприл 1 раз в день. Выводится почками. Данный препарат в отличие от всех других длительно действующих ИАПФ является активным действующим веществом, а не пролекарством, требующим метаболических изменений. Это большое клиническое преимущество лизиноприла, поскольку он может в той же дозе назначаться пациентам с любой сопутствующей патологией печени без потери клинического эффекта в отличие от всех других ИАПФ.
Поэтому в России распространены фиксированные комбинации, содержащие лизиноприл и ГХТ. Хотелось бы обратить внимание на препарат Литэн H, который выпускается в двух вариантах: лизиноприл 10 мг + ГХТ 12,5 и лизиноприл 20 мг + ГХТ 12,5 мг. Наличие двух дозировок позволяет врачу более индивидуально подбирать лечение для каждого больного. Так, при АГ I степени (АД 140–159 и/или 90–99 мм рт. ст.) лечение следует начинать с лизиноприла 10 мг + ГХТ 12,5 мг, а при необходимости, особенно при высоком и очень высоком риске развития осложнений, в дальнейшем переходить на вариант лизиноприл 20 мг + ГХТ 12,5 мг. При АГ II степени (АД – 160–179 и/или 100–109 мм рт. ст.) сразу рекомендуется назначать лизиноприл 20 мг + ГХТ 12,5 мг.
Таким образом, комбинированная терапия, прежде всего фиксированные комбинации АГП, является на сегодняшний день терапией первой линии в лечении АГ. В настоящее время по-прежнему самой часто назначаемой комбинацией в очень большом количестве клинических ситуаций, в т. ч. при лечении АГ у пожилых и ИСАГ, является комбинация ИАПФ и ТД ГХТ. Ее отличительными особенностями являются высокая антигипертензивная эффективность, низкая частота побочных эффектов (в т. ч. за счет нейтрализации побочных эффектов друг друга), наличие органопротективных свойств, метаболическая нейтральность (при условии дозы ГХТ не более 12,5 мг). Большое значение для клинической практики имеют и дополнительные свойства ИАПФ, в частности лизиноприла. Более широкое и рациональное использование этих фиксированных комбинаций позволит повысить эффективность лечения АГ, снизить риск сердечно-сосудистых осложнений и смерти.
Информация об авторах:
Остроумова Ольга Дмитриевна – доктор медицинских наук, профессор кафедры факультетскойтерапии и профболезней МГМСУ.
E-mail: ostroumova.olga@mail.ru;
Максимов Максим Леонидович – кандидат медицинских наук, доцент кафедры клинической фармакологиии пропедевтики внутренних болезней ГОУ ВПО “Первый МГМУ им. И.М. Сеченова”.
E-mail: maksim_maksimov@mail.ru



