Введение
Инфекции нижних дыхательных путей, среди которых внебольничная пневмония (ВП) занимает лидирующее место, являются третьей по значимости причиной смертности в мире, уступая только ишемической болезни сердца и цереброваскулярным заболеваниям, а в странах с низким уровнем доходов - первое место [1, 2].
В Европе заболеваемость ВП - 1,07-1,2 случая на 1000 человек в год, выше у мужчин. Ежегодно в США регистрируется 5,6 млн пациентов с ВП, из которых госпитализируются 1,1 млн, 10 тыс. из этих пациентов умрут во время госпитализации, а один из трех взрослых умрет в течение года после госпитализации с пневмонией. Согласно статистическому отчету о состоянии смертности в Южной Африке, грипп и ВП вместе заняли шестое место среди основных причин смерти в 2015 г. [3]. В России ВП ежегодно заболевают более 2 млн человек, что составляет 3,86 на 1000 случаев заболеваний. К группе наиболее высокого риска относят лиц моложе 5 лет и старше 75 лет [4]. Смертность от ВП составляет 5%, но среди пациентов, требующих госпитализации, доходит до 21,9%, среди пожилых - 46% [5, 11].
Существенны и экономические потери, ассоциированные с ведением больных ВП: ежегодные затраты в США составляют около 20 млрд долларов, среди которых значительная часть приходится на пациентов с ВП, требующих госпитализации [6, 12].
Вопросами диагностики и рациональной фармакотерапии ВП занимаются все ведущие медицинские сообщества [7, 11]: Американское общество по инфекционным заболеваниям (IDSA) и Американское торакальное общество (ATS), Японское респираторное общество, Российское респираторное общество и др. В связи с высокой распространенностью данной патологии, удручающими цифрами смертельного исхода, с возникающей резистентностью микроорганизмов к действию антибактериальных препаратов вопрос об актуальности исследований в данной области отпадает. В рамках оптимизации ведения пациентов с ВП исследуют вопрос компетентности практикующих врачей в фармакотерапии данного заболевания, ведь проведение фармакоэпидемиологических исследований позволяет выявлять основные ошибки фармакотерапии ВП среди врачей терапевтического профиля, повышать качество оказания медицинской помощи и оптимизировать тактику ведения больных ВП путем повышения приверженности врачей к следованию клинических рекомендаций [8].
Методы
В ходе второго этапа исследования KNOCAP (полное авторское название проекта «The assessment of students’ and physicians’ knowledge of community-acquired pneumonia basics») за 2017-2020 гг. в одной из поликлиник Белгорода было отобрано и проанализировано 242 протокола, содержащих основную информацию о пациентах, обратившихся за помощью к врачу-терапевту для лечения нетяжелой ВП в рамках амбулаторно-поликлинической помощи [12].
В вышеуказанных протоколах обследования зафиксированы необходимые данные, позволяющие в полной мере ретроспективно оценивать состояние больного, а именно пол, возраст, основные жалобы, анамнез заболевания (сроки его начала, проведенные ранее диагностические исследования до настоящего обращения и их результаты, лечебные мероприятия), наличие сопутствующей патологии и/или перенесенных инфекций, аллергических реакций; указаны информация о семейном и эпидемиологическом анамнезах, объективные дынные больного (описаны лечащим врачом, согласно принятым нормам оформления истории болезни), в качестве итога сформулирован основной диагноз, план предстоящего обследования и лечения.
Протоколы осмотра отбирались путем сплошного просмотра врачебных историй болезни в базе данных поликлиники в соответствии с критериями включения:
1. Наличие подтвержденного заключительного диагноза ВП в соответствии с Международной классификацией болезней, травм и причин смерти 10 пересмотра (МКБ-10), кодирующейся в рубриках J13-J16 и J18.
2. Амбулаторное лечение в соответствии со шкалой CURB-65/CRB-65, оценивающей риск неблагоприятного прогноза и выбора места лечения при ВП [8].
Критерии исключения из исследования: пациенты с ВП, требующие госпитализации по шкале CURB-65/CRB-65 (нарушение сознания, азот мочевины крови >7 ммоль/л (при наличии), частота дыхательных движений >30/ мин, уровень артериального давления: систолическое <90 или диастолическое <60 мм рт. ст., возраст >65 лет, отсутствие необходимой информации для адекватной ретроспективной оценки тяжести состояния пациента.
Таким образом, были рассмотрены две когорты больных: первая - пациенты с нетяжелой ВП и отсутствием факторов риска и/или сопутствующих заболевания, вторая - с наличием факторов риска и/или имеющих коморбидный фон (истощение, наркомания, хронический алкоголизм, сахарный диабет, ХОБЛ, застойная сердечная недостаточность, хроническая почечная недостаточность, цирроз печени) и/или для пациентов, принимавших за последние 3 месяца системные антимикробные препараты (АМП) два и более дней. Несмотря на то что в обоих случаях лечения вышеуказанных групп рекомендовано использование таблетированных форм АМП, тактика антимикробной терапии таких больных меняется, т.к. возрастает вероятность этиологической роли грамотрицательной флоры [8, 13], следовательно, подобное разграничение является необходимой частью фармакотерапии. В итоге количество больных в первой группе составило 138 (57%), во второй - 104 (43%). Следует акцентировать внимание на том, что основной причиной распределения пациента с ВП в группу № 2 стал самостоятельный прием больными АМП накануне - 48 человек (46,2%); хроническая сердечная недостаточность была выявлена у 26 (25%) пациентов, ХОБЛ и полиморбидность - у 13 (12,5%) и менее 5% суммарно составили пациенты с сахарным диабетом (1%) и хронической болезнью почек (2,8%). Затем был проведен анализ фармакотерапии, назначенной врачом, и сделана последующая оценка соответствия или несоответствия клиническим рекомендациям по ведению пациентов с ВП.
Следующий этапом данного исследования - проведение образовательных мероприятий, в ходе которых врачам были предложены способы оптимизации ведения пациентов с ВП:
- упор на изучение клинических рекомендаций (согласно данным настоящего исследования, лишь 31% врачей и 37% студентов используют клинические рекомендации в качестве основного руководства к выбору антимикробной терапии;
- разбор выявленных ошибочных вариантов фармакотерапии ВП с целью предупреждения назначения нерациональной антимикробной терапии;
- на основе разработанной универсальной программы поддержки решений (зарегистрирован вариант программы «Амбулаторная помощь при COVID-19» [14]) разработана и внедрена в клиническую практику подобная по концепции программа поддержки принятия врачебных решений - «Внебольничная пневмония в амбулаторной практике у взрослых», оптимизирующая выбор стартовой антибиотикотерапии ВП, для врачей первичного звена;
- внедрение в работу шкал (PSI, CURB-65) и/или алгоритмов для оценки тяжести и выбора корректной эмпирической антимикробной терапии из существующих клинических рекомендаций;
- разбор ситуационных задач для понимания практической значимости настоящего обучения и максимального вовлечения специалистов в данный процесс.
В ходе завершающего этапа настоящего исследования проведен повторный анализ фармакотерапии ВП теми же врачами, выполнена статистическая обработка и интерпретация полученных результатов.
Результаты и обсуждение
В ходе реализации первого этапа исследования (анализа многоцентрового исследования KNOCAP) рассчитаны показатели средней полноты уровня первичного ответа (СПО) по анкете [9, 10]. Медиана первичного показателя уровня СПО врачей составила 0,525, или 52,5% правильных ответов (Q1-Q3: 0,5-0,65).
Проведенный анализ структуры назначений показал, что лишь 75 (30,9%) пациентов получали лечение и диагностические обследования, соответствовавшие клиническим рекомендациям, 167 (69,1%) - не соответствовавшие в той или иной мере (табл. 1). Наиболее часто специалисты на амбулаторном этапе терапии ошибочно назначали пациентам без факторов риска и сопутствовавшей патологии цефалоспорины с парентеральным путем введения (56,8%), следующими препаратами выбора стали амоксициллин/клавуланат или амоксициллин/сульбактам (22,5%) и в 12,4% - респираторный фторхинолон, в 8,1% случаев АМП при установленном диагнозе «внебольничная пневмония» назначен не был. Структура ошибочного назначения для пациентов с наличием факторов риска (ХОБЛ, бронхиальной астмы, хронической болезни почек, сахарного диабета) либо наличием курса приема АМП за последние 3 месяца была следующей: в 80% случаев специалисты назначали цефалоспорины с парентеральным путем введения, в 8,3% антимикробная терапия назначена не была, в 6,7% - макролиды и 5,0% врачей рекомендовали прием амоксициллина.

Согласно актуальным клиническим рекомендациям [8], диагностический минимум при установленном диагнозе «внебольничная пневмония» сводится к обязательному выполнению рентгенографии органов грудной клетки в двух проекциях и назначения клинического анализа крови. В большинстве (88,4%) анализируемых проколов эти обследования были проведены, однако в 11,6% случаев общий анализ крови назначен не был.
После проведения мероприятий по оптимизации ведения пациентов с ВП группой врачей-терапевтов была повторно протестирована с помощью разработанной анкеты на основании клинических рекомендаций [8]. Повторная медиана уровня СПО выросла до 0,643 (64,3% верных ответов; Q1-Q3: 0,44-0,74). Данный показатель увеличился более чем на 10% (рис. 1), следовательно, с учетом приведенного ранее статистического анализ в рамках бинарной логистической регрессии это увеличивает шансы правильного назначения фармакотерапии ВП в 2,18 раза.
Настоящее исследование структуры назначений выявило ожидаемое улучшение фармакотерапии нетяжелой формы ВП: после обучения уже в 68,4% случаев рекомендации специалистов соответствовали клиническим рекомендациям [8] и лишь в 31,6% были обнаружены ошибки диагностического или фармакотерапевтического плана (табл. 2).
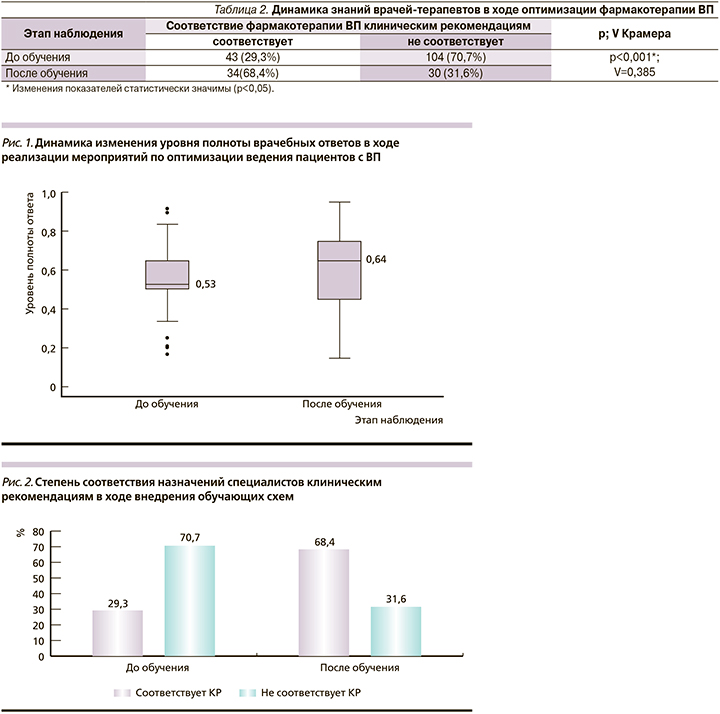
В свою очередь было установлено статистически значимое снижение частоты нерациональных назначений в результате реализации предложенных мер по оптимизации лечения ВП - с 70,7 до 31,6% (p<0,001; рис. 2). Полученная разница в значениях сопровождалась средневыраженной силой связи, согласно рекомендациям Rea & Parker (V=0,385).
Заключение
Представлен комплексный разбор тактики фармакотерапии больных ВП в условиях реальной клинической практики на амбулаторно-поликлиническом этапе оказания медицинской помощи, а также степень ее соответствия имеющимся клиническим рекомендациям.
Изучена структура назначений практикующих врачей в ходе проведения обучающих и информационно-поддерживающих мероприятий, в результате чего выявлено статистически значимое снижение частоты нерациональных назначений с 70,7 до 31,6% (p<0,001, V=0,385).
Таким образом, следует считать целесообразным проведение фармакоэпидемиологических исследований для выяснения предпочтений врачей при выборе фармакотерапии внебольничной пневмонии, выявление факторов, связанных с нерациональным назначением АМП. Оправданно внедрение в работу шкал и/или алгоритмов, программ поддержки принятия решений, соответствующих клиническим рекомендациям, для оценки тяжести состояния пациента и выбора корректной эмпирической антибактериальной пневмонии.



