Актуальность
Пролапс тазовых органов (ПТО) встречается у 50% женщин репродуктивного возраста, которые имели вагинальные роды, а среди женщин 40–49 лет его частота достигает 77,2% [1]. Исследование «Women´s Health Initiative Study» среди 16 616 женщин перименопаузального возраста показало, что частота выявления маточного пролапса составляет 14%, цистоцеле – 34%, ректоцеле – 19% (суммарно – 67%) [2].
Установлено, что основной этиологической причиной ПТО являются беременность и влагалищные роды, поэтому проявления его имеются уже в послеродовом периоде, которые с течением времени прогрессируют.
К росту заболеваемости пациенток в старшем возрасте приводят позднее обращение за медицинской помощью, отсутствие симптомов при начальных стадиях заболевания, отсутствие стандартов по диагностике и лечению, а также выжидательная тактика относительно ранних форм [3].
Исследователи сходятся во мнении, что многие женщины, страдающие ПТО, не имеют родовой травмы в анамнезе, а развитие пролапса является следствием необратимого чрезмерного травматического растяжения леваторов и других структур, формирующих тазовое дно [4, 5].
Ранее перенесенные хирургические вмешательства по поводу пролапса в настоящее время относят к факторам риска в связи с частыми рецидивами (до 50%), при этом более молодые женщины и пациентки с более выраженным пролапсом чаще испытывают рецидивы после хирургического восстановления тазового дна [6].
Клиническая картина ПТО на ранних стадиях отличается неспецифичностью симптомов и их скудностью, поэтому объективная оценка состояния тазового дна имеет принципиальное значение при обращении женщины к акушеру-гинекологу по любому поводу и в любом возрасте [3].
Применение простого Алгоритма диагностики недостаточности тазового дна (НТД) «5 STEPS» [7] позволяет своевременно выявлять неблагополучие еще до появления выраженных симптомов, предпринять необходимые меры для профилактики прогрессирования заболевания и избежать хирургического вмешательства в большинстве случаев (в отсутствие тяжелых послеродовых травматических повреждений тазовых структур). По рекомендациям FDA (Food and Drug Administration, 2016), достижение идеальной тазовой поддержки не является необходимым для большинства женщин, чтобы добиться симптоматической помощи, и не каждая женщина с выпадением половых органов нуждается в оперативном лечении. Однако травмы тазового дна при осложненных родах и оказании оперативных пособий могут приводить к сложным анатомическим и функциональным нарушениям, которые требуют хирургической коррекции.
Стратегии лечения ПТО, разработанные отечественными авторами, предполагают оперативное лечение независимо от наличия сопутствующих нарушений начиная со II степени. Напротив, за рубежом первой линией терапии считают консервативные методы, и только в отсутствие эффекта (сохранение или усиление симптомов) решается вопрос об операции. В США 95% гинекологов и 98% урологов используют в своей практике пессарии [8].
Был проведен анализ 428 анкет, заполненных российскими акушерами-гинекологами анонимно, который показал, что начало лечения с консервативных методов при пролапсе I–II степеней с наличием или без симптомов с целью лечения и профилактики более тяжелых форм заболевания поддержали лишь 13% врачей [9]. Однако и к оперативному лечению прибегли бы только 7%. Очевидно, 80% врачей предпочитают наблюдательную тактику либо затрудняются в выборе из-за недостаточной информированности об этой патологии. Акушеры-гинекологи, которые считают, что лечение НТД необходимо начинать с консервативных методов, прежде всего с тренировок мышц тазового дна – МТД (54%), с высокой долей вероятности выбирают и пессарии при I–II степенях пролапса. Частое мочеиспускание также послужило предиктором использования пессариев пациентками [9].
Многие акушеры-гинекологи сообщают о трудностях диагностики травматических повреждений фасций и леватора в отдаленном после родов периоде и выбора тактики лечения, что стало предметом рассмотрения настоящей публикации.
Мануальные приемы в диагностике повреждений структур тазового дна в родах и выбор хирургической тактики лечения
Методика пальпации m. puborectalis (медиальных отделов m. levator ani), с помощью которой диагностируют травму этой мышцы, описана H.P. Dietz (2008) [10]. Для оценки целостности/травмы m. puborectalis пальпирующий палец помещают параллельно уретре, кончик пальца фиксируют возле шейки мочевого пузыря, а его ладонную поверхность прижимают к задней/дорсальной поверхности лобкового симфиза. В норме палец располагается между уретрой медиально и m. puborectalis – латерально, а при волевом сокращении мышц таза хорошо ощущается исследователем.
Вариант, свидетельствующий о полном отрыве m. puborectalis: мышца не пальпируется на задней поверхности симфиза и нижней лобковой ветви непосредственно сбоку от пальца, расположенного параллельно уретре. При сокращении мышц таза этот палец может перемещаться латерально по нижней лобковой ветви на 2–3 см, при этом не ощущается ткань мышцы и ее сокращение (рис. 1).
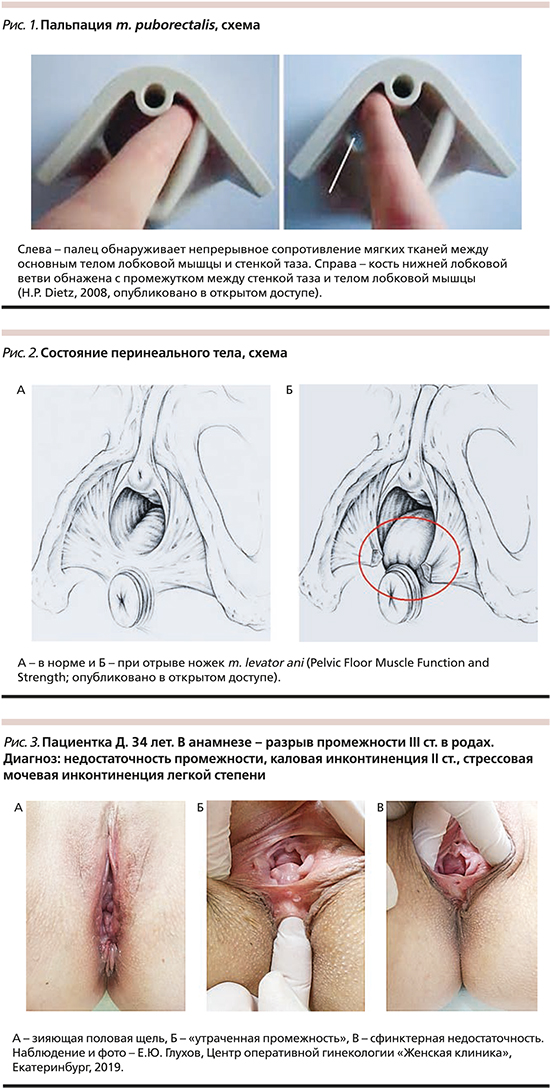
Автором было показано, что данная методика не уступает по точности (80–87%) и сравнима с 3D/4D транслабиальным ультразвуковым исследованием и может быть использована в диагностике травмы мышцы.
С помощью четырехмерной ультразвуковой визуализации H.P. Dietz определил, что расстояние леватор–уретра более 25 мм свидетельствует об отрыве m. puborectalis с чувствительностью 63% и специфичностью 94%, а согласованность между результатами, полученными разными исследователями, составляет 81%. H.P. Dietz установил, что в когорте обследованных им пациенток с пролапсом (стадия II или выше) у 23% из них обнаружен отрыв леватора и определил, что риск пролапса для таких женщин составляет 1,9 (95% доверительный интервал [ДИ]: 1,7–2,1), т.е. в 2 раза выше по сравнению с теми, у кого сохранялась целостность мышцы. Ассоциация была наиболее сильной для цистоцеле (отношение шансов [ОШ]=2,3, 95% ДИ: 2,0–2,7) и выпадения матки (ОШ=4,0, 95% ДИ: 2,5–6,5).
Основным анатомическим образованием, отвечающим за смыкание половой щели, является мышечный комплекс в виде незамкнутого овала, в который входят m. constrictor cunni (совр. назв. – m. bulbospongiosus) и поверхностная поперечная мышца промежности (m. transversus superficialis perinei) (рис. 2). Любое повреждение промежности с нарушением целостности указанных мышц приводит к разрушению этого комплекса, и если его адекватно не восстановить, то результатом будет зияние половой щели.
При разрывах промежности II и III степеней кроме m. constrictor cunni повреждаются глубокая поперечная мышца промежности и мышцы, поднимающие задний проход (лобково-копчиковая и лобково-прямокишечная), в месте перехода в наружный сфинктер ануса. Если не происходит послойного их восстановления (2–3 ряда отдельных швов) или заживление раны промежности произошло вторичным натяжением, то в дальнейшем это может клинически проявляться недержанием мочи (НМ) при напряжении и легкими формами анальной инконтиненции.
Анатомические изменения при повреждении мышечно-фасциальных структур тазового дна, описанные Е.Ю. Глуховым в руководстве «Недостаточность тазового дна. Терапия на основе достижений науки и клинической практики» (2021) [3], реализуются в следующие состояния.
Полное отсутствие мышц, а иногда и кожи промежности, когда задняя спайка имеет минимальную высоту и непосредственно переходит в анальное кольцо, получило название «утраченная промежность», предложенное Е.Ю. Глуховым (рис. 3). В большинстве случаев такое состояние промежности является исходом разрыва промежности III степени с неадекватным восстановлением целостности мышц промежности и анального сфинктера и, как правило, сопровождается сфинктерной недостаточностью (анальной инконтиненцией). При хирургической коррекции таких состояний кроме пластики промежности необходимо выполнять сфинктеропластику. В отдаленном после родов периоде частичную утрату наружного сфинктера ануса можно определить пальпаторно при ректальном исследовании (рис. 3Б), при трансперинеальном (трансректальном) ультразвуковом исследовании, а также при сфинктерометрии.
Травма мышц леваторов в родах – отрыв или неполный разрыв m. levator ani (лонно-прямокишечная и лонно-копчиковая мышцы), с учетом их анатомии и функции может приводить к формированию стрессового НМ, а также к дисхезии (запору), причиной которых является диссенергическая дефекация. Подобные состояния начинают проявляться сразу после родов или в более поздние сроки и встречаются у 8% пациенток после самостоятельных родов.
К. Van Delft обнаружил, что большинство травм леваторов, диагностированных через 3 месяца после родов, уже не были очевидными через 12 месяцев (62%; 95% ДИ: 41–79%) [11]. Из 30 разрывов леваторов 9 (30%) были стойкими. Женщины с сохраняющимися признаками разрыва чаще имели симптомы НТД и приводили к слабости силы сокращений МТД. В то время как отрыв леваторов и их чрезмерное растяжение были связаны со снижением сократительной функции мышц [12], тот факт, что женщины с дефектами леваторов по-прежнему способны сокращать МТД, может свидетельствовать о том, что, возможно, неповрежденные мышцы компенсируют функцию поврежденных [13]. В ряде случаев, когда неповрежденная мышца берет на себя функцию поврежденной, она гипертрофируется, а зачастую находится в спастическом состоянии, что в свою очередь может быть причиной синдрома хронической тазовой боли.
Повреждение m. levator ani может быть и без разрывов стенок влагалища и промежности, а являться результатом перерастяжения тканей в процессе прохождения плода через родовой канал. Это проявляется увеличением расстояния между медиальными порциями m. levator ani и разрывом ректо-вагинальной перегородки, что ведет к расширению и удлинению леваторного отверстия (расстояния между ее медиальными краями) и дальнейшему формированию ректоцеле. Отсутствие травмы (разрыва) кожи промежности и слизистой оболочки влагалища в родах не говорит об отсутствии повреждения МТД и фасций.
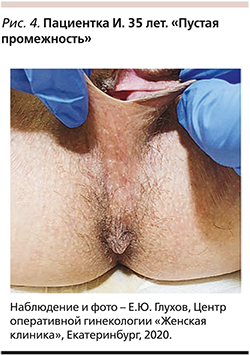 В случае, когда кожа промежности в месте разрыва восстановлена, а мышцы практически отсутствуют, названо Е.Ю. Глуховым «пустая промежность» (рис. 4). Аналогичное состояние промежности бывает после неадекватно выполненной реконструктивно-пластической операции – пластики промежности. Подобные случаи нередки и требуют определенных хирургических подходов при выполнении повторной пластической операции.
В случае, когда кожа промежности в месте разрыва восстановлена, а мышцы практически отсутствуют, названо Е.Ю. Глуховым «пустая промежность» (рис. 4). Аналогичное состояние промежности бывает после неадекватно выполненной реконструктивно-пластической операции – пластики промежности. Подобные случаи нередки и требуют определенных хирургических подходов при выполнении повторной пластической операции.
Повреждение endopelvic fascia является другим вариантом родового травматизма. Тазовая фасция представляет собой плотный волокнистый слой соединительной ткани, окружающей влагалище и прикрепляющей его к arcus tendineus тазовой фасции (fascia pelvis) латерально. Разрывы или отрывы фасций от мест их прикрепления встречаются с частотой около 30% после родов [14].
Fascia pubocervicalis может смещаться от ее боковых прикреплений к дуговидным сухожилиям (Arcus tendineus fascia pelvis) на боковых стенках таза. Это вызывает пролапс передней стенки влагалища и мочевого пузыря с клинической картиной цистоцеле за счет латерального дефекта фасции. Если дефект фасции образуется в ее средних отделах, то формируется центральное цистоцеле. Оценка наличия центрального либо латерального дефекта фасции определяет вид хирургического вмешательства, и нередко рецидив пролапса после хирургического лечения связан с недооценкой этого состояния.
Когда имеется разрыв ректовагинальной перегородки, стенка прямой кишки соприкасается с влагалищной стенкой и создает «выпуклость» на задней нижней стороне влагалища (ректоцеле) [15].
Диагностика разрывов фасции в амбулаторных условиях проста и доступна. Она описана Н.А. Нечипоренко и выполняется с использованием ложкообразных зеркал на высоте потуги (проба Вальсальвы) и визуализации «выпячивания» на соответствующей стенке влагалища [16].
Пациенток с ПТО и выявленными травматическими повреждениями необходимо направить к специалисту для дополнительного обследования и оперативного лечения.
Урогинекологические пессарии Dr. Arabin в консервативном лечении ПТО
Консервативное лечение НТД, в т.ч. ПТО, включающее модификацию образа жизни, физическую терапию (тренировки МТД и мочевого пузыря), гинекологические пессарии и лекарственную терапию (при генито-уринарном менопаузальном синдроме и тазовой боли) является эффективной стратегией и имеет низкий риск побочных эффектов. Консервативное лечение рекомендуется на уровне первичной медицинской помощи, а также пациенткам, для которых хирургические методы лечения неприемлемы.
По данным обзора R. Magali et al. (2013) по использованию пессариев, их следует рассматривать в качестве первой линии терапии для всех женщин с симптоматическим пролапсом и/или стрессовым НМ (степень доказательности – II, уровень рекомендации – 1А) [17]. В литературе есть подтверждения, что пессарии могут предотвращать прогрессирование пролапса или даже приводить к уменьшению его тяжести после 1–4 лет его использования [18]. Через 2 недели после начала использования пессария K. Jones et al. (2008) наблюдали уменьшение размера генитального перерыва с 4,8 до 4,1 см и дальнейшее уменьшение до 3,9 см через 3 месяца [19].
Эффективность применения пессариев при симптоматическом ПТО, по данным одного рандомизированного клинического исследования, составляет 60%, по данным многочисленных когортных исследований достигает 92% [3]. При сравнении результатов лечения в группе женщин, использовавших пессарии, с таковыми, полученными от прооперированных, выявлено статистически значимое снижение степени пролапса, улучшение функции мочевого пузыря, кишечника и сексуальной функции через год после проведенного лечения в обеих группах без существенной разницы между ними [20]. Аналогичное сравнение проведено А.W.M. Coolen et al. (2018), которое показало, что у женщин с пролапсом II степени и выше через 12 месяцев средний балл домена UDI-6 (симптомы НМ) по опроснику PFDI-20 составил 0 в группе как хирургического лечения, так и пессария (р<0,01). При этом 72% женщин, проходивших лечение пессарием, в дальнейшем отказались от операции [20].
По данным отдельных авторов, при использовании пессариев происходят положительные объективные изменения, сопровождающиеся снижением степени опущения у 21% женщин после 1-го года использования (по POP-Q) [18, 19]. Почти все симптомы пролапса купируются в течение до 2 месяцев использования пессария: наличие «выпуклости» в половой щели (с 90 до 3%; р<0,001), чувство давления (с 49 до 3%; р<0,001), непроизвольная потеря мочи (с 12 до 0%; р=0,003), а также запоры (с 14 до 0%; р=0,001). N. Radnia et al. (2019) сообщают, что уже через 6–8 месяцев 97% женщин, успешно использовавших индивидуально подобранный пессарий, были удовлетворены и сообщили о значительном улучшении симптомов [22]. Кроме того, показано, что использование пессариев значительно улучшает качество жизни пациентов [23].
А.А. Суханов и соавт. провели рандомизированное клиническое исследование с участием 45 женщин в послеродовом периоде с наличием факторов риска НТД, выявленных в период беременности и родов (избыточная масса тела, повторные роды, многоплодная беременность, макросомия плода, многоводие, быстрые/стремительные роды). Отмечена высокая частота пролапса I–II степеней у женщин с факторами риска – 82 против 29% в группе без факторов риска (n=45) соответственно (p<0,001, рис. 5А). Пациентки применяли кольцевидные силиконовые урогинекологические пессарии Dr. Arabin (Германия), которые вводили на 3–5-й день послеродового периода и через 6–8 недель производили замену пессария на кубический (рис. 5Б) с продолжительностью использования 12 месяцев.
Через год использования пессариев отмечено, что площадь зияния половой щели уменьшилась на 71% (р<0,01), в контроле (без лечения) – на 45% (р<0,05), степень пролапса матки уменьшилась на один пункт у 80 и 62% пациенток (р<0,001 в соответствующих группах), при этом сила сокращений МТД после родов была не выше 3 баллов до лечения и через год увеличилась до 4–5 баллов по шкале Оксфорда у 62% пациенток, использовавших пессарии (против 47% пациенток без лечения), р<0,05.
Таким образом, применение урогинекологических пессариев Dr. Arabin женщинами с факторами риска после родов позволяет снижать частоту и выраженность ПТО, повышать силу сокращений МТД [24].
Е.Ю. Глуховым и соавт. проведена оценка эффективности и общей удовлетворенности пациенток с ПТО при консервативном лечении с использованием урогинекологических пессариев Dr. Arabin. В исследовании приняли участие 95 пациенток с ПТО II–IV степеней с наличием или без ассоциированных симптомов, из которых 93,7% нуждались в оперативном лечении, которое, однако, не могло быть выполнено из-за наличия противопоказаний или отказа пациенток. Возраст участниц колебался значительно (от 34 до 87 лет), но в среднем составил 66,9 (±12,7) года. Для консервативной коррекции ПТО использовали силиконовые пессарии гинекологические кубические перфорированные Dr. Arabin.
По данным анамнеза, пациентки продемонстрировали характерную для больных пролапсом терпимость, когда ощущение инородного тела (87,4%; 83/95), затруднения при мочеиспускании и дефекации (56,8%; 54/95), необходимость вправления выпуклости перед опорожнением мочевого пузыря (18,1%; 6/95) заставили их обратиться к врачу в среднем лишь через 4,9 (±2,3) года, с максимальным сроком – через 15–20 лет.
По классификации POP-Q были очевидны увеличенные значения точек передней стенки влагалища (средние Аа+2,1 и Ва 2,04), размера gh (6,4 см) и уменьшенная длина влагалища в покое (средняя tvl 5,3). 40 (42,1%) пациенток имели полный пролапс матки, из них почти половина (42,5%; 17/40) имели декубитальные язвы (рис. 6). Этим пациенткам перед введением пессария проводили обработку язвы кавитированным раствором 0,05%-ного водного хлоргексидина (на курс 8–14 до полной эпителизации язвы), пессарии применяли только в дневное время, на ночь вводили крем, содержащий эстриол 0,5 мг ежедневно, в дальнейшем – в постоянном режиме через день.
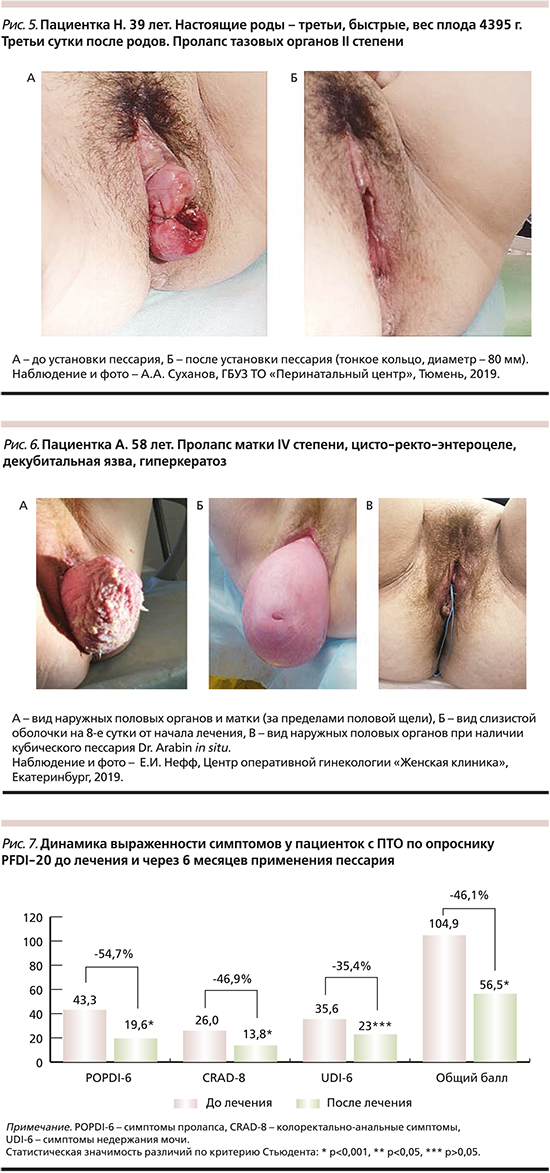
Оценка симптомов ПТО во всех трех доменах опросника PFDI-20 продемонстрировала уменьшение их частоты и выраженности через 6 месяцев применения пессариев (рис. 7).
Восстановление топографо-анатомического расположения передней стенки влагалища, а следовательно, и мочевого пузыря привело к уменьшению всех урогинекологических симптомов. Однако нами отмечено парадоксальное сохранение или даже усиление симптомов стрессовой инконтиненции у части пациенток (16,8%, 16/95), что было связано со скрытой формой НМ и обструктивным удержанием мочи на фоне перегиба шейки мочевого пузыря.
Суммарная оценка тяжести симптомов ПТО по опроснику PFDI-20 (Pelvic Floor Distress Inventory Questionnaire) при применении пессария уменьшилась на 46,1% и по домену POPDI-6 (симптомы пролапса) уменьшение было максимальным (на 54,7%). Объективное улучшение состояния пациенток подтверждает высокую эффективность данной технологии в коррекции симптоматического пролапса.
Что урогинекологический пессарий Dr. Arabin полностью удовлетворяет их потребности подтвердили 88,4% (84/95) пациенток, среди них те, кто исходно использовал его как временный вариант, и те, для которых пессарий – это вариант паллиативной помощи из-за наличия противопоказаний к хирургическому вмешательству по состоянию соматического здоровья. Причем 12,6% (12/95) женщин имели неудачный опыт ношения пессария в анамнезе, однако мы смогли подобрать им подходящий вариант: 23,2% (22/95) пациенток обратились после ранее проведенного оперативного лечения с рецидивом заболевания в период от 6 месяцев до 8 лет, и все они были удовлетворены результатом использования пессария Dr. Arabin.
Возможность замены размера изделия – условие адекватной паллиативной помощи пациенткам с ПТО. Первоначально размер пессария Dr. Arabin подбирался путем измерения расстояния gh (по POP-Q), который ориентировочно соответствует длине грани куба. Однако 13,6% (13/95) пациенток потребовалась замена на пессарий большего/меньшего размера в течение первой недели. Из них 3 пациенткам – в пользу увеличения размера в связи с указанием на выпадение изделия при нагрузке в течение дня и 10 – на меньший (из-за дискомфорта при самостоятельном введении и удалении). Смена размера пессария в течение первого месяца понадобилась еще 9 (9,5%) пациенткам, причем в сторону как уменьшения, так и увеличения размера. Дискомфорт в области заднего прохода, усиливающийся при наклонах, обычно служил симптомом, требующим пересмотра соответствия размера изделия в пользу меньшего. Одной пациентке с выраженной недостаточностью промежности и ректоцеле III степени не удалось подобрать пессарий.
Среди женщин, выразивших удовлетворенность использованием пессария Dr. Arabin, 76% (72/95) пациенток приняли решение о его применении в дальнейшем, 12,6% (12/95) пациенток, удовлетворенных эффектом от пессария Dr. Arabin, напротив, утвердились в желании оперативной коррекции в будущем, считая регулярную установку изделия неудобным для себя вариантом. Одной (1,1%) пациентке пришлось временно прекратить использование пессария в связи с развитием воспаления из-за нарушения техники использования изделия и возобновить его применение после комплексной терапии.
Таким образом, в настоящем исследовании 93,7% пациенток нуждались в хирургической коррекции, что отражает отечественный подход, однако все они либо имели противопоказания, либо отказались от операции, а использование урогинекологических пессариев Dr. Arabin позволило уменьшить частоту и тяжесть симптомов ПТО на 54,7%, удовлетворенность методом высказали 88,4% пользователей, при этом 76% отдали предпочтение его дальнейшего использования против 12,6% пациенток, запланировавших операцию [3].
Зарубежные авторы также отмечают, что улучшение показателей по опроснику PFDI-20 на 50% связано с продолжением использования пессария [6]. Показатели успешности до 62% были зарегистрированы у пациенток с пролапсом III и IV степеней, что указывает на то, что пессарии являются отличным вариантом лечения даже в популяции с тяжелыми формами ПТО [25]. В исследовании A.W.M. Coolen et al. среди женщин с ПТО II степени или выше, использовавших пессарии или перенесших хирургическое вмешательство, симптомы ПТО были нивелированы практически в равной степени. При этом 72% женщин, использовавших пессарии, отказались от операции [21], что совпадает с результатами нашего наблюдения. Результаты 10 исследований приведены в обзоре, подтверждающем улучшение симптомов ПТО и мочевого пузыря после лечения пессарием [25]. В краткосрочной перспективе через 3 или 4 месяца продолжают использовать пессарий от 50 до 80% пациенток и после 1 года использования показатели продолжения лечения остаются неизменными [25]. В связи с этим мы можем согласиться с рекомендацией Комитета по урогинекологии, изложенной в Technical update on pessary use (2013), согласно которой пессарии следует рассматривать для всех женщин с симптомами пролапса и/или стрессовым НМ [26].
За счет особой вогнутой формы кубического пессария Dr. Arabin наряду с функцией заполнения средней трети влагалища он осуществляет поддерживающую функцию, а также достаточно стабильную фиксацию в проекции урогенитальной диафрагмы и ректовагинальной перегородки. Вкупе с восстановлением нормальных топографо-анатомических взаимоотношений органов малого таза ношение пессария дает удивительный эффект уменьшения отека и восстановления тургора тканей, в отсроченном периоде у части пациенток становится очевидным возможность полноценной коррекции меньшим размером кубического пессария.
Заключение
Отмечается высокая распространенность ПТО среди женщин после родов, что диктует необходимость объективной оценки состояния тазового дна при обращении к акушеру-гинекологу по любому поводу и в любом возрасте.
Для диагностики травматических повреждений мышцы, поднимающей задний проход, и фасций могут быть использованы мануальные приемы, простые, доступные, с высокой чувствительностью и специфичностью.
Стратегии коррекции ПТО включают хирургическое лечение, целью которого является восстановление анатомических структур и функции тазового дна либо консервативное лечение в отсутствие явных травматических повреждений начиная с ранних стадий с целью профилактики прогрессирования заболевания или как симптоматическая помощь при более тяжелых клинических ситуациях.
Вагинальный урогинекологический пессарий Dr. Arabin – это не только альтернатива оперативному лечению и/или этап подготовки к нему, но и самостоятельный метод коррекции ПТО. Высокая эффективность (54,7% в снижении симптомов ПТО) и общая удовлетворенность (88,4%) пациенток при использовании пессария позволяют рассматривать эту технологию как первую ступень оказания помощи пациенткам с ПТО, в т.ч. с его тяжелыми формами (III–IV степени).
Финансирование. Исследования проведены за счет средств авторов.



