Острый панкреатит (ОП) относится к числу распространенных хирургических заболеваний и составляет в среднем от 3 до 10% случаев всех неотложных заболеваний органов брюшной полости. Возрастающий уровень заболеваемости свидетельствует об актуальности проблемы диагностики и лечения ОП в практическом здравоохранении [24].
Одним из наиболее частых причин развития ОП по праву считают злоупотребление алкоголем, алкогольные эксцессы либо прием суррогатов алкоголя. В настоящее время роль алкоголя как патогенетического фактора поражения поджелудочной железы общепризнанно [2, 4, 6, 7, 22–24, 28, 31]. Подобную причину заболевания выделяют в среднем у 35–50% больных подавляющего большинства стран [22, 24, 28].
Литературные данные и практические наблюдения свидетельствуют о том, что алкогольные панкреатиты относятся к наиболее тяжелым формам ОП [2, 4, 6, 7, 22–24, 28, 31]. ОП развивается на фоне нарушений дренажной функции панкреатических протоков. С алкоголизмом связывают токсическое повреждение поджелудочной железы, нарушение функции печени, извращение синтеза ферментов [6, 7, 22, 31]. Таким образом, прием алкоголя и его суррогатов резко усиливает секреторную активность поджелудочной железы, а длительное употребление алкогольных напитков приводит к дуодениту с отеком большого дуоденального соска, создавая затруднение оттоку панкреатического сока и желчи. Алкоголь в этих обстоятельствах оказывает токсическое действие на экзокринную активность железы, вызывая дегенеративные изменения в ацинарных клетках, способствуя развитию ОП [2, 6, 22–24].
Несмотря на многочисленные исследования, посвященные изучению больных ОП, вопросы клиники, диагностики и тактики лечения этого заболевания, связанные с употреблением алкоголя, изучены недостаточно и порой противоречивы. С одной стороны, это вызвано многосторонним действием алкоголя на организм, с другой – недостаточностью данных о структуре эндотоксикоза при этом заболевании [4, 23, 24]. В зависимости от продолжительности заболевания, времени воздействия, качества и количества принятых алкогольных напитков в паренхиме поджелудочной железы развиваются некроз, атрофия и фиброз клеток. Соответствующие изменения выявляются и в печени. Анатомическая близость печени и поджелудочной железы и тесные функциональные связи между ними создают угрозу повреждения и функциональной недостаточности печени при острых заболеваниях поджелудочной железы [22, 23].
Проблема диагностики и лечения больных ОП на фоне хронической алкогольной интоксикации и алкогольных поражений печени представляет большой интерес и относится к категории особо сложных. Хроническая алкогольная интоксикация и поражения печени значительно увеличивают риск летального исхода [2, 6, 7]. Обусловленная ОП системная воспалительная реакция ухудшает функциональные способности пораженной алкоголем печени и приводит к выраженным нарушениям портального кровотока [10, 12, 13, 15].
При лечении больных ОП и функциональных нарушений печени комплексные мероприятия направлены на коррекцию гиповолемии и электролитного дисбаланса, используют антиферментные препараты, блокаторы желудочной секреции, распираторную и инотропную поддержку, антибиотики, парэнтеральное и ранее энтеральное питание, методы экстракорпоральной детоксикации [23, 24]. Большое внимание выделяют улучшению микроциркуляторных процессов и купированию рассеянного внутрисосудистого свертывания [14, 20, 21, 23].
С этой целью используют различные препараты, включая пентоксифиллин, низкомолекулярные гепарины, а также кровозаменители – ренглюман, Реомакродекс [23]. В последнее время для коррекции патологии сосудистого русла широко используется препарат Актовегин, который обладает эндопротекторным свойством, увеличивает утилизацию кислорода, улучшает энергетический метоболизм, усиливает транспорт глюкозы в клетку за счет переносчиков благодаря наличию изонил-фосфор-олигосахаридов, улучшает метаболическую активность микрососудистого эндотелия [30, 34].
Целью настоящего исследования стало улучшение микроциркуляторных нарушений печени и портального кровотока при лечении больных ОП на фоне алкогольных поражений печени – гепатопатии.
Материал и методы
Под нашим наблюдением находились 24 больных ОП (основная группа) в возрасте 22–55 лет, из них 20 мужчин и 4 женщины. В отношении всех больных в ходе лечения с целью коррекции патологии микроциркуляторного русла и портального кровотока использовали Актовегин по 10 мл 1 раз в сутки на 0,9%-ном физиологическом растворе. Группу сравнения составили 24 больных аналогичной патологией, которым в процессе лечения с целью коррекции микроциркуляторных нарушений и портального кровообращения предлагали препарат пентоксифиллин.
Диагноз ОП устанавливался на основании клинических, лабораторных и инструментальных данных. Комплекс обследования включал клиниколабораторную диагностику с использованием клинических и биохимических методов исследования крови, ультразвукового исследования (УЗИ) органов брюшной полости, эзофагогастродуоденоскопии, лапароскопии; определение концентрации алкоголя в крови по международным стандартам, принятым по Международной классификации болезней 10-го пересмотра. Оценку состояния тяжести больных давали с применением критериев шкалы SAPS (Simplified acute physiology score). У всех больных имелся алкогольный анамнез более 5 лет. Концентрация алкоголя в крови составила при поступлении 1,5±0,3 мг/%. Состояние больных при поступлении оценивалось как тяжелое, что соответствовало по шкале SAPS 8,8±0,59 балла. По ходу хирургического лечения оценивали клинико-морфологическое состояние печени. Наиболее информативными при диагностике поражений печени считались методы УЗИ, УЗ допплерографии, компьютерная томография печени и лапароскопия.
Данные проведенных исследований сопоставлялись с результатами клинических исследований крови, биохимических показателей функционального состояния печени.
Контрольные исследования с применением клинических и биохимических анализов крови применяли ежедневно в отделении реанимации, а после стабилизации состояния больных и перевода в хирургическое отделение через каждые 3 суток.
Результаты исследования и обсуждение
Данные проведенных контрольных исследований подтвердили клиническую эффективность проводимой терапии в основной группе с применением Актовегина для коррекции микроциркуляторных нарушений печени и портального кровотока. Клинический эффект препарата оценивался по срокам разрешения пареза кишечника, сокращения размеров воспалительного инфильтрата брюшной полости при ОП, сокращения размеров печени, улучшения результатов клинико-биохимических показателей крови, лейкоцитарного индекса интоксикации, показателей воротного кровотока.
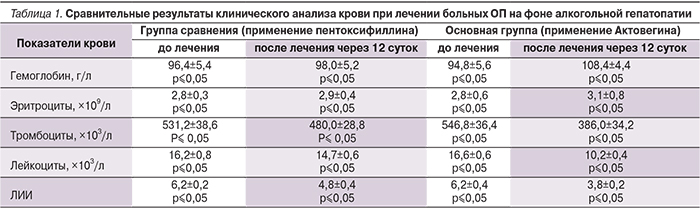
На фоне проведенной терапии в основной группе отмечали уменьшение явлений интоксикации и устранение пареза кишечника из 24 (100%) у 19 (79,1%) пациентов на третьи сутки применения Актовегина в комплексной терапии. В группе сравнения с использованием пентоксифиллина разрешение пареза кишечника наблюдалось на 5–7-е сутки. Сокращение размеров воспалительного инфильтрата брюшной полости в течение 7 суток наблюдали у 18 (75%) больных основной группы, а в группе сравнения было отмечено у 13 (54,2%) больных. Данные клинических и биохимических исследований крови свидетельствовали о повышении уровня гемоглобина, числа эритроцитов, снижении числа лейкоцитов, тромбоцитов, лейкоцитарного индекса, интоксикации у 22 (91,6%) пациентов основной группы на 12-е сутки, а в группе сравнения – у 18 (75%). Данные проведенных исследований анализов крови проведены в табл. 1.
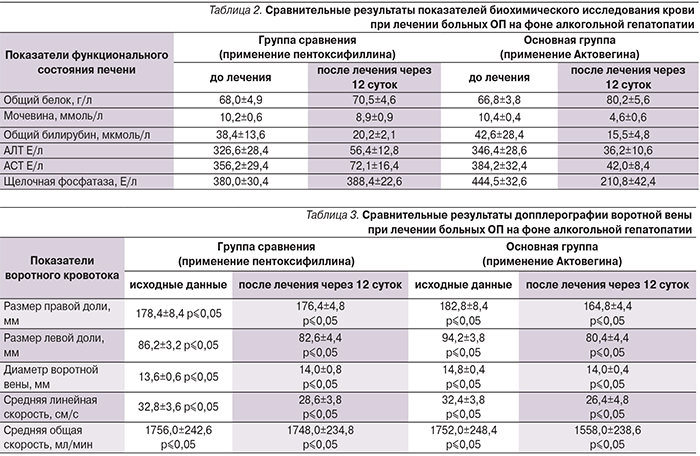
По мере улучшения показателей анализов крови на 12-е сутки проводимого лечения наблюдали сокращение размеров печени у 21(87,5%) больного основной группы наряду со снижением уровней аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы, билирубина, мочевины и улучшением показателей воротного кровообращения (табл. 2, 3).
Среди больных группы сравнения положительный результат получен в аналогичные сроки у 16 (66,7%) пациентов, у 5 (20,8%) больных анализы существенно не изменились, а у 4 (16,5%) отмечено ухудшение показателей.
Из наблюдаемых 24 (100%) больных основной группы с применением Актовегина у 1 (4,1%) пациента состояние ухудшилось в связи с прогрессированием острой печеночной и полиорганной недостаточности. На 4-е сутки от момента госпитализации больной умер от интоксикации. Среди больных группы сравнения при применении пентоксифиллина для коррекции микроциркуляторных процессов умерли 4 (16,6%) больных в связи с нарастающей смешанной интоксикацией, развитием делирия и полиорганной недостаточности.
Заключение
Проведенные исследования свидетельствуют об эффективности применения препарата Актовегин для коррекции патологии микроциркуляторного русла и функциональных нарушений пораженной алкоголем печени при комплексном лечении больных ОП. Эффект лечения достигается благодаря эндотелиопротективному действию Актовегина, способствующего увеличению скорости капиллярного кровотока, улучшению клеточного и тканевого метаболизма в печени, что сопровождается стимуляцией биоэнергетических процессов и регенераций гепатоцитов.



