Одним из наиболее распространенных в мире заболеваний является сахарный диабет 2 типа (СД2), связанный с развитием сосудистых осложнений [1–3]. Распространенность данной патологии увеличивается с возрастом. Известно, что к моменту диагностики СД2 у половины пациентов присутствуют различные осложнения заболевания, которые приводят к ухудшению качества жизни, ранней инвалидизации и преждевременной смерти. Согласно результатам исследования
CODE-2 (Cost of Diabetes in Europe – Type 2), различные осложнения имели 59 % обследованных больных СД2, причем 23 % страдали двумя, а 3 % тремя осложнениями и более [4]. Экономические последствия, обусловленные сосудистыми осложнениями диабета, чрезвычайно велики. Их развитие в среднем удорожает лечение СД2 в 3–10 раз [5]. Поэтому проблема терапии СД2 остается в центре пристального внимания врачей различных специальностей.
Результат сахароснижающей терапии – снижение уровня гликозилированного гемоглобина (HbA1c) – напрямую связан с прогнозом заболевания и является оптимальным критерием эффективности профилактики развития и прогрессирования осложнений диабета [6–8]. Фармакотерапия СД2
должна воздействовать на основные патофизиологические нарушения, присущие заболеванию: дисфункцию β-клеток и инсулинорезистентность [9]. Среди неинсулиновых сахароснижающих препаратов (ССП) производные сульфонилмочевины (ПСМ) –наиболее эффективные средства, снижающие HbA1c в среднем на 1,5–2,0 %, причем вариабельность степени снижения гликемии связана с ее исходным уровнем до инициации лечения этими препаратами [10]. Кроме того, ПСМ позволяют быстро снижать уровень гликемии (натощак и постпрандиальный) у больных СД2. Поскольку
функционирование β-клеток поджелудочной железы играет ключевую роль как в течении СД2, так и в ответе на все виды сахароснижающей терапии, наличие в островках Лангерганса достаточного количества функционально активных β-клеток является непременным условием проявления фармакологического эффекта неинсулиновых препаратов, включая ПСМ [3, 10].
Среди характеристик, которые следует учитывать при выборе ССП длительной терапии СД2, необходимо отметить эффективность в отношении снижения уровней HbA1c и глюкозы крови натощак, постпрандиальной гликемии, способность вызывать гипогликемию, влияние на отдаленный
прогноз. Важное клиническое значение имеют пути метаболизма и выведения, а также дополнительные метаболические эффекты ССП. Принято считать, что в целом механизм действия различных ПСМ одинаков [9, 10]. Между тем по своей химической структуре этот класс секретогогов неоднороден, что определяет индивидуальные терапевтические свойства отдельных его
представителей. Особенности фармакокинетического профиля, различные аффинность, селективность и обратимость связывания со специфическими белками – рецепторами β-клеток обусловливают значимые отличия в клинических свойствах различных ПСМ и, что представляется особенно важным, в их спектре безопасности [11, 12]. Применение современных ПСМ позволяет избегать побочных эффектов, традиционно свойственных этому классу CCП (гипогликемия, прибавка массы тела). В ряду ПСМ гликлазид (Диабетон МВ) наделен всеми необходимыми клинически значимыми позитивными свойствами, присущими этим противодиабетическим средствам.
Среди больных СД2 распространенность ишемической болезни в 2–4 раза, риск развития острого инфаркта миокарда (ОИМ) – в 6–10 раз, мозговых нарушений – в 4–7 раз выше, чем среди лиц без диабета [13, 14]. Иначе говоря, больным СД2 присущ высокий риск сердечно-сосудистых осложнений, что выдвигает высокие требования к кардиоваскулярной безопасности препаратов. Принимая во внимание серьезный сердечно-сосудистый риск для пациентов с СД2, уместно остановиться на данных
Датского регистра [15], включившего 107 806 больных СД2, 9607 из которых имели ОИМ в анамнезе. Анализ результатов 9-летнего наблюдения показал достоверное снижение риска общей, сердечно-сосудистой смертности, ОИМ и инсульта у пациентов как с перенесенным ОИМ, так и без него, получавших гликлазид, в отличие от тех, кто принимал другие ПСМ (рис. 1). Эти данные можно считать
важным источником информации определения эффективной стратегии сахароснижающей терапии в отношении улучшения отдаленного прогноза заболевания.

Хронические осложнения СД2 до настоящего времени остаются главной проблемой большинства пациентов. В последние годы особое внимание уделяется диагностике ранней стадии
диабетической нефропатии – стадии микроальбуминурии (МАУ), поскольку она является не только предиктором почечной патологии, но и признаком генерализованного повреждения сосу-
дов – иначе говоря, важным маркером развивающегося атеросклероза. По данным исследований, у 30–40 % больных СД2 МАУ выявляется уже в момент установления диагноза. Доказано, что наличие МАУ при диабете ассоциируется не только с более быстрыми темпами падения скорости клубочковой фильтрации, но и с более высокой сердечно-сосудистой смертностью [16, 17]. Интенсивный контроль гликемии при СД2, согласно результатам исследования ADVANCE, обеспечивает отчетливый ренопротективный эффект (рис. 2) [18]. В группе интенсивного контроля гликемии, основанного на применении гликлазида (Диабетона МВ), регресс нефропатии минимум на одну стадию (т. е. от макро- к микро- или нормоальбуминурии либо от микро- к нормоальбуминурии) отмечен у 62 % пациентов. При этом в 57 % случаев был достигнут нормальный уровень альбуминурии. Эти свойства Диабетона МВ значительно повышают возможности лечения СД2.
Итак, эффективность применения Диабетона МВ в профилактике прогрессирования альбуминурии становится дополнительным основанием его использования больными СД2 в качестве ССП. Признанием достоинств Диабетона МВ в отношении улучшения отдаленного прогноза СД2 является расширение спектра показаний к применению этого препарата, который включает профилактику сосудистых осложнений СД2. Обсуждаются дополнительные механизмы действия Диабетона МВ, связанные прежде
всего с особым строением молекулы гликлазида, содержащей азобициклооктановую группу. Этой особенностью препарата исследователи объясняют антиоксидантные и вазопротекторные свойства гликлазида, не зависящие от уровня гликемии [19, 20]. Здесь следует отметить антиатерогенный эффект Диабетона МВ: например, в терапевтических концентрациях препарат значительно повышает время задержки между воздействием прооксидантов на уровень липопротеидов низкой плотности (ЛПНП) и началом окисления. Иначе говоря, Диабетон МВ обеспечивает защиту ЛПНП от окисления. Этот эффект, как показало исследование, не воспроизводится при приеме других ПСМ.
Принято считать, что выбор наиболее безопасных режимов cахароснижающей терапии с меньшим
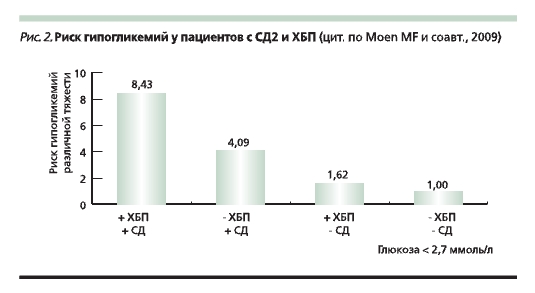
риском гипогликемий имеет определяющее значение для предупреждения сердечно-сосудистых рисков при СД2 [6, 7]. Ведь наиболее тяжелые последствия гипогликемических эпизодов напрямую связаны с сердечнососудистой заболеваемостью и смертностью. Кроме того, у пациентов с СД2 часто наблюдается хроническая болезнь почек (ХБП), которая вносит дополнительный вклад в повышение риска гипогликемий (рис. 2), что предъявляет к безопасности сахароснижающей терапии дополнительные требования [21, 22].
Применяющиеся в клинической
практике ССП эффективны в отно-
шении снижения уровня гликемии,
однако с точки зрения безопасности
они существенно различаются [3, 6,
9]. К примеру, глибенкламид – весь-
ма эффективный препарат в плане
снижения глюкозы в крови, что обу-
словлено низкой обратимостью его
связи с рецептором СМ и, соответ-
ственно, пролонгированной секре-
тогенной активностью. Однако это
может сопровождаться чрезмерной
гиперинсулинемией, чреватой высо-
ким риском развития гипогликемий,
а в прогностическом плане – быстрым
истощением функциональной актив-
ности β-клеток.
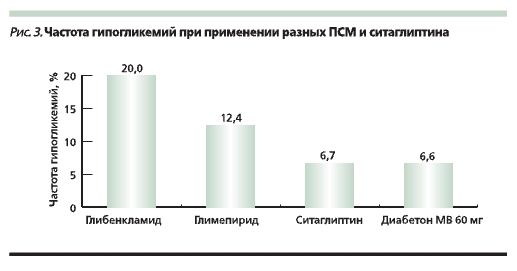
Важная информация была получена в исследовании (The Middle East Ramadan study), в котором изуча-
ли частоту симптоматической гипогликемии у постящихся мусульман с СД2, получавших лечение ситаглиптином – препаратом группы ингибиторов дипептидилпептидазы-4 (ДПП-4), или ПСМ во время Рамадана [23]. Показательно, что частота возникновения гипогликемических эпизодов была
меньше при применении гликлазида, чем других ПСМ (глибенкламид, глимепирид), и такой же, как при использовании ингибитора ДПП-4 (рис. 3). Таким образом, выбор ПСМ может влиять на риск развития гипогликемии в условиях измененного режима питания (например, нерегулярного приема
пищи). О низком риске гипогликемий на фоне применения гликлазида, сопоставимом с таковым для ситаглиптина, свидетельствуют и результаты исследования S.R. Aravind и соавт. [24]. Нельзя
не вспомнить, что стратегия достижения гликемического контроля в исследовании ADVANCE, основанная на применении Диабетона МВ, ассоциировалась с очень низким риском
эпизодов гипогликемии при одновременном обеспечении эффективного контроля гликемии у пациентов СД2, несмотря на то что 70 % больных получали препарат в дозе 120 мг/сут [18].
Причем частота гипогликемий была почти в вчетверо меньше, чем в исследовании UKPDS (0,5 против 1,8 %), несмотря на более низкий уровень HbA1c, достигнутый пациентами в ходе исследования ADVANCE.
Высокие эффективность и безопасность Диабетона МВ доказаны во многих контролируемых клини-
ческих исследованиях. Однако всегда интересны и показательны данные, полученные в условиях реальной клинической практики, а не в жестких рамках рандомизированного исследования. В этом плане заслуживают внимания новые результаты применения Диабетона МВ, полученные в исследовании DIAMOND (DIAMicrON MR in Daily practice) наблюдательной программе по оценке
эффективности и безопасности терапии этим ССП в повседневной практике [25]. Основные цели программы DIAMOND: изучение эффективности Диабетона МВ в монотерапии и/или в комбинации с другими ССП пациентов с ранее неудовлетворительным контролем СД2 и оценка безопасности стратегии увеличения дозы препарата до максимальной (120 мг/сут). В программе приняли участие 394
пациента на терапии диетой или одним пероральным ССП (метформин, глитазон, ингибитор ДПП-4,
акарбоза, глинид или ПСМ, за исключением гликлазида), которые переводились на Диабетон МВ с продолжением или отменой предшествующей терапии (если ранее больной принимал препарат группы секретагогов). При последнем варианте терапии Диабетон МВ назначался в дозе, эквивалентной таковой ранее принимаемого препарата (например, 3,5 мг глибенкламид = 60 мг Диабетона МВ, 1 или 2 мг глимепирида = 30 или 60 мг Диабетона МВ соответственно и т. д.). Средний возраст пациентов при включении в программу составил 59,0 ± 9,2 года, средний уровень HbA1c – 8,4 ± 0,9 %, средний уровень гликемии натощак – 9,0 ± 1,9 ммоль/л.
Через 6 месяцев лечения Диабетоном МВ (в монотерапии в 30 % и в комбинации в 70 % случаев) целевой уровень HbA1c < 7 % был достигнут 64,7 % больных, HbA1c < 6,5 % – каждым третьим из
них. Кроме того, отмечено достоверное снижение массы тела, уровней систолического и диастолического артериального давления. Наконец, несмотря на небольшую продолжительность исследования, имела место положительная динамика альбуминурии, о чем свидетельствовало снижение числа пациентов как с МАУ (с 29,19 до 22,59 %), так и с протеинурией (с 5,08 до 3,30 %).
Низкая частота гипогликемий отмечена при хорошем результате лечения – значимом снижении уровня HbA1c на 1,6 %. Важно отметить, что тяжелых гипогликемий не наблюдалось, а легкие гипогликемии были зарегистрированы в 2,28 % случаев.
С течением времени потребность в сахароснижающей терапии может меняться. В отношении длительного удержания контроля гликемии следует вновь обратиться к результатам ADVANCE. Значения HbA1c, достигнутые к концу первого года наблюдения группой интенсивной терапии (6,5 %),
удерживались на протяжении всего исследования – в течение 5 лет. Для достижения целевого уровня
HbA1c 70 % пациентов суточная доза Диабетона МВ была постепенно увеличена до 120 мг [18]. Эти данные демонстрируют принципиальную важность увеличения дозы Диабетона МВ с целью проявления всего спектра эффективности препарата.
Одной из сложных проблем проведения сахароснижающей терапии является несоблюдение пациентами врачебных рекомендаций. Причем низкая приверженность лечению может иметь место со стороны не только пожилого больного с когнитивными нарушениями, но и молодого пациента, ведущего активный образ жизни. Диабетон МВ назначается один раз в сутки в удобное для всех время – утром во время завтрака, что, несомненно, является фактором, улучшающим и приверженность
пациента длительному лечению, и его эффективность. Последовательной титрацией под контролем гликемии устанавливается оптимальная доза Диабетона МВ, и если она максимальная – 120 мг, то все равно полностью принимается пациентом утром, 1 раз в день.
Подводя итог, следует еще раз подчеркнуть, что СД2 представляет серьезную проблему для здоровья
населения. Достижение целевого гликемического контроля для многих пациентов с СД2 остается и сегодня нелегкой задачей, однако применение современного ССП Диабетона МВ, положительные эффекты и безопасность применения которого подтверждаются обширной доказательной базой
данных, значительно повышает возможности лечения заболевания. При этом можно добиться как непосредственного клинического результата, так и достоверного улучшения прогноза СД2 – снижения частоты тяжелых осложнений диабета, в частности нефропатии.



