Введение
Распространенность манифестного первичного гипотиреоза в популяции составляет 0,2–2,0%, субклинического (СГ) – до 10% у женщин и до 3% у мужчин. Наибольшей частоты гипотиреоз достигает среди женщин старшей возрастной группы, где его показатель распространенности доходит до 12%.
Даже начальная тиреоидная дисфункция может сопровождаться развитием негативных метаболических и функциональных эффектов, в т.ч. кардиоваскулярных [6]. В настоящее время накоплено достаточно данных в пользу того, что при СГ сердце и сосуды могут рассматриваться как потенциальные органы-мишени [5–8]. Первоначально после описания СГ в 1973 г. он рассматривался как компенсаторная реакция организма, не требующая никакой коррекции. В дальнейшем было показано, что СГ сопровождается изменением многочисленных суррогатных показателей, которые могут быть связаны с сердечно-сосудистым риском [1].
N. Rodondi и соавт. [9] приводят данные, указывающие на то, что у больных СГ с уровнем тиреотропного гормона (ТТГ) >10 мкМЕ/мл в возрасте старше 65 лет повышен риск развития сердечной недостаточности (СН).
Следует отметить, что единого мнения в отношении уровня ТТГ, характеризующего СГ, нет. В начале 2000-х гг. были опубликованы результаты американских [2] и европейских [3] эпидемиологических исследований, показавших, что референсный диапазон для ТТГ, под которым подразумевается его уровень у 95% здоровой популяции, слишком широк, поскольку у подавляющего большинства здоровых людей без признаков патологии щитовидной железы он не превышает 2–2,5 мкМЕ/мл. Были высказаны идеи о целесообразности сужения референсного диапазона для диагностики гипотиреоза, а затем и об уменьшении целевого уровня ТТГ на фоне проведения заместительной терапии.
В исследовании SHIP [4] верхний предел для уровня ТТГ в среднем составил 2,2 мкМЕ/мл.
Геометрическая модель изменений формы и гипертрофии миокарда определяется профилем хронической гемодинамической перегрузки (Филатов Н.П. и соавт., 1993; Rossi и соавт., 1991). Выделяют три основных типа изменения формы миокарда левого желудочка (ЛЖ):
- Концентрическое ремоделирование, которое не является вариантом гипертрофии миокарда ЛЖ и характеризуется увеличением толщины стенки ЛЖ без увеличения его массы: относительная толщина стенки (ОТС) ЛЖ >0,45.
- Концентрическая гипертрофия миокарда ЛЖ, характеризующаяся увеличением его массы и относительным утолщением его стенок, при этом размеры полости ЛЖ не увеличиваются (ОТС >0,45). Концентрическая гипертрофия ЛЖ наиболее часто встречается при артериальной гипертензии (АГ): до 85–90% всех случаев гипертрофии ЛЖ у больных АГ. Этот тип гипертрофии рассматривается как адаптивное изменение миокарда ЛЖ.
- Эксцентрическая гипертрофия миокарда ЛЖ, характеризующаяся увеличением массы ЛЖ и размеров его полости без относительного увеличения толщины стенок (ОТС <0,45). Этот тип гипертрофии является дезадаптивным изменением мио-карда ЛЖ.
Цель исследования состояла в выявлении взаимосвязи повышения уровня ТТГ с развитием и прогрессированием СН у больных ишемической болезнью сердца (ИБС) и АГ. При этом была поставлена задача оценить характер влияния и прогностическую значимость нарушения функции щитовидной железы на сердечно-сосудистую систему путем сопоставления уровня ТТГ и основных функциональных показателей работы сердца.
Материал и методы
Обследованы 42 пациента в возрасте от 45 до 80 лет, госпитализированных в кардиологическое отделение ГКБ № 1 г. Краснодара со стенокардией, аритмией, АГ и хронической СН (ХСН). Критерии исключения: декомпенсация других тяжелых хронических соматических заболеваний, недостаточность функции надпочечников, новообразования (опухоль гипофиза и др.), терминальная хроническая почечная недостаточность, перенесенный инфаркт миокарда, врожденные либо приобретенные пороки сердца.
Всем пациентам проведены исследование артериального давления, биохимический анализ крови с последующим расчетом скорости клубочковой фильтрации по формуле CKD-EPI, определение ТТГ, ЭКГ, ЭхоКГ на аппарате Medison Sonoace 8000. Изучены следующие структурные параметры сердца: передне-задний размер (ПЗР, мм) левого предсердия (ЛП, мм); конечный диастолический размер (КДР, мм) ЛЖ; толщина задней стенки (ТЗС, мм) ЛЖ; толщина межжелудочковой перегородки (ТМЖП, мм); масса миокарда ЛЖ (ММЛЖ, г); фракция выброса (ФВ, %) ЛЖ по методу Симпсона; определен тип ремоделирования миокарда ЛЖ.
Статистическую обработку результатов исследования провели с помощью пакета программ Statisticа 6.0 и Biostat. Корреляционный анализ был выполнен с использованием коэффициента корреляции Спирмана. Сравнение выборок проведено с помощью метода Манна–Уитни. Тип распределения в выборках проверен с использованием критерия Шапиро–Уилкса. Различия считали статистически значимыми при значениях р<0,05.
Результаты и обсуждение
Было выделено 2 группы пациентов: 21 человек с повышением уровня ТТГ от 3,4 до 10 мкМЕ/мл (группа с СГ) и 21 – с уровнем ТТГ от 0,23 и до 3,4 мкМЕ/мл (контрольная группа – КГ).
Группы достоверно не различались по половому признаку (19 женщин и 2 мужчины в группе с СГ и 21 женщина в КГ), наличию сопутствующего сахарного диабета (2 человека в КГ и 3 – в группе с СГ), частоте встречаемости АГ (по 20 человек в каждой из групп), частоте встречаемости фибрилляции предсердий (7 человек в КГ и 6 – в группе с СГ), частоте встречаемости ИБС (по 17 человек в каждой из групп), функциональному классу ХСН.
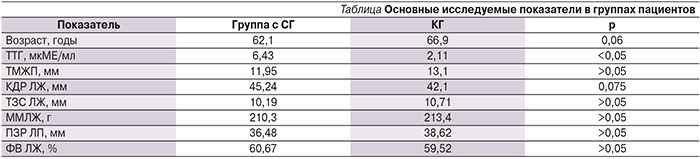
Результаты исследования представлены в таблице.
В КГ 1 (4,76%) пациент имел концентрическое ремоделирование миокарда ЛЖ, 16 (76,19%) – концентрическую гипертрофию ЛЖ, 4 (19,05%) – эксцентрическую гипертрофию ЛЖ.
В группе с СГ 1 (4,76%) пациент имел нормальное строение миокарда ЛЖ, 9 (42,86%) – концентрическую гипертрофию миокарда ЛЖ, 11 (52,38%) – эксцентрическую гипертрофию ЛЖ. Различия между группами были достоверными (р<0,05).
Несмотря на более молодой возраст пациентов в группе с СГ (выраженная тенденция; р=0,06), входящие в нее больные имели сопоставимые с КГ ФВ, частоту встречаемости фибрилляции предсердий и ПЗР ЛП. КДР ЛЖ у пациентов группы с СГ был больше, чем в КГ (выраженная тенденция; р=0,075), что говорит о серьезных дезадаптивных процессах в структуре миокарда, которые являются предпосылкой для развития и более раннего прогрессирования ХСН.
Выводы
Увеличение уровня ТТГ сопровождается дезадаптивной перестройкой структуры миокарда ЛЖ, тенденцией к его дилатации, что является предпосылкой для более раннего развития и прогрессирования ХСН у кардиологических больных.
Полученные данные позволяют предположить наличие негативного влияния СГ на дилатацию ЛП и развитие фибрилляции предсердий, что требует проведения более крупномасштабных исследований по этому вопросу.
Результаты исследования ставят на повестку дня вопрос о целесообразности скрининговой диагностики нарушений функции щитовидной железы у кардиологических больных и более раннего начала заместительной гормональной терапии при СГ для уменьшения риска возникновения и прогрессирования ХСН.



