При лечении инфекций нижних дыхательных путей у детей – бронхита и пневмонии (ПВМ), широко используются антибиотики (АБ). Особенно часто они применяются при ПВМ. При бронхите АБ используются не всегда. Например, острый простой бронхит у ребенка 7 лет не требует назначения АБ, т. к. известно, что в 80–90 %
случаев он вызывается вирусами, а вирусная инфекция не нуждается в антибактериальном лечении. Поэтому в настоящее время общепризнанно, что показаниями к назначению АБ при остром простом бронхите, остром обструктивном бронхите и рецидивирующем бронхите у детей являются указание на бактериальную природу заболевания, а также наличие у ребенка факторов, указывающих на риск неблагоприятного развития процесса. В частности, это возможность микроаспирации инфицированного содержимого носоглотки, особенно при ее массивной микробной контаминации, и развития ПВМ [1–3].
Проведенный нами анализ собственных данных и данных литературы [2, 4–6] позволил сформулировать основные показания к назначению антибактериальной терапии при острых бронхитах, острых обструктивных бронхитах и обострении рецидивирующего бронхита у детей.
Ими являются:
- наличие у ребенка выраженных симптомов интоксикации и длительной гипертермии (более 3–4 дней), особенно у грудных детей;
- затяжное течение заболевания без тенденции к его разрешению в течение 7–10 дней;
- наличие выраженного трудно поддающегося терапии бронхообструктивного синдрома;
- нарастание признаков инфекционного токсикоза и дыхательной недостаточности в динамике заболевания;
- изменения в анализах периферической крови воспалительного характера, говорящие о бактериальной этиологии бронхита (нейтрофильный лейкоцитоз, увеличенная СОЭ); наличие у ребенка неблагоприятного преморбидного фона, способного создавать реальную угрозу развития ПВМ, – т. н. модифицирующих факторов.
К модифицирующим факторам бронхита, т. е. факторам, утяжеляющим течение болезни независимо от ее этиологии и создающим риск развития ПВМ, следует отнести:
- недоношенность, особенно у детей первого полугодия жизни;
- гипотрофию 2-й и 3-й степеней;
- тяжелую энцефалопатию;
- наличие врожденных аномалий развития, в первую очередь врожденных пороков сердца и сосудов;
- другие наследственные, врожденные и приобретенные заболевания, создающие предпосылки к неблагоприятному течению болезни (например, спинальная амиотрофия Гофмана, муковисцидоз, бронхолегочная дисплазия и т. п.).
Относительными показаниями к проведению антибактериальной терапии являются развитие острого обструктивного и рецидивирующего бронхита у часто болеющих детей, у детей с хроническими заболеваниями носоглотки, при которых отмечается массивная микробная колонизация верхних дыхательных путей и создаются особо благоприятные условия для микроаспирационного проникновения инфекции в бронхиальное и альвеолярное пространства и вследствие этого – развития ПВМ.
Врач-педиатр может лечить ребенка с бронхитом в домашних условиях. Но, если появляются симптомы нарастающей интоксикации, при высокой и длительной температуре (свыше 38,5 ° при длительности 4–5 дней и более), нарастающей одышке, тогда для детей, особенно младшего возраста, а иногда и более старших детей, необходима госпитализация.
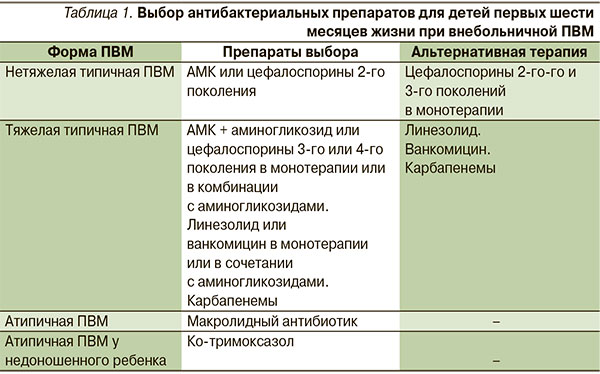
По-иному обстоит дело при типичной внебольничной ПВМ, которую диагностируют приблизительно у 15–20 на 1000 детей первого года жизни, у 36–40 на 1000 в дошкольном возрасте, а в школьном и подростковом возрастах диагноз ПВМ устанавливается примерно в 7–10 случаях на 1000 детей. Наиболее часто внебольничная типичная ПВМ вызывается бактериальными возбудителями. Это Streptococcus pneumoniae, Haemophilus influenzae, Мycoplasma pneumoniae, Chlamydia pneumoniae, Staphylococcus epidermidis, Staphylococcus aureus, Escherichia сoli, Klebsiella pneumoniae и Streptococcus pyogenes, причем самую большую роль здесь играет S. рneumoniaе. Возбудитель встречается в 40–45 % случаев [2–4, 7–9]. Однако в грудном периоде раннего детства этиологическая роль пневмококка достигает 35–45 % всех случаев ПВМ лишь к 6-месячному возрасту ребенка. До этого возраста причиной ПВМ у детей являются S. еpidermidis, S. aureus, E. сoli, K. рneumoniae, S. рyogenes и вирусы. H. influenzae, тип b, как причина ПВМ встречается начиная с 3–5-месячного возраста и отмечается приблизительно в 10 % всех случаев внебольничных ПВМ у детей до 7 лет.
ПВМ, вызванные атипичными возбудителями, или атипичные внебольничные ПВМ, у детей обусловлены в основном M. pneumoniaе, C. trachomatis и С. pneumoniae. Для микоплазменной инфекции характерны подъем температуры тела до 38–39 °С, явления интоксикации, симптомы вегетодистонии (бледность, «мраморность» кожи, потливость). Один из ведущих симптомов – сухой мучительный кашель, который может вызывать рвоту и приводит к нарушению сна ребенка. Развивается бронхообструктивный синдром со всеми присущими ему проявлениями.
При ПВМ, вызванной C. trachomatis, лихорадка встречается редко; наоборот, температура тела или субфебрильная, или нормальная. Отмечается бронхообструкция. При ПВМ, вызванной C. рneumonia, характерен упорный «стакаттоподобный» кашель.
«Золотым» стандартом диагностики ПВМ является рентгенография органов грудной клетки, это высокоинформативный и специфичный метод. Его специфичность составляет 92 %.
При диагностике используются критерии, которые к тому же свидетельствуют о тяжести заболевания и помогают в выборе антибактериальной терапии:
- размеры инфильтрации легких и ее распространенность;
- наличие или отсутствие плеврального выпота;
- наличие или отсутствие деструкции легочной паренхимы.
Лечение нетяжелой ПВМ, а это 75–80 % случаев воспаления легких у детей, проводится в домашних условиях. Тяжелую, особенно деструктивную, ПВМ, осложненную плевритом, а также внебольничную ПВМ у детей первых 3–6 месяцев жизни и у детей любого возраста, имеющих модифицирующие факторы, лечат в стационаре.
При выборе стартового(ых) антибактериального(ых) препарата(ов) при респираторной инфекции нижних дыхательных путей у детей необходимо учитывать спектр предполагаемых возбудителей и индивидуальную переносимость АБ. Наиболее принятой практикой отечественных и зарубежных пульмонологов является назначение при типичной картине острого бронхита, острого обструктивного бронхита или острого эпизода рецидивирующего бронхита, в качестве препарата выбора АБ группы пенициллинов широкого спектра действия – амоксициллина (АМ), амоксициллина клавуланата (АМК) [10].
Альтернативными препаратами (при неэффективности терапии или при непереносимости) являются цефалоспорины 2–3-го поколений или макролиды. Все эти препараты назначаются внутрь.
АМ активен в отношении грамположительных и грамотрицательных микроорганизмов. Препарат обладает бактерицидными свойствами.
В АМК клавулановая кислота ингибирует β-лактамазы II, III, IV и V типов. Благодаря высокой тропности к пенициллиназам образуется стабильный комплекс с ферментами, что предупреждает ферментативную деградацию АМ под влиянием β-лактамаз и расширяет спектр действия препарата. Так, АМК активен в отношении аэробных грамположительных бактерий: S. pyogenes, S. viridans, S. pneumoniae, S. aureus, S. epidermidis, E. faecalis, Corynebacterium spp., Bacillus anthracis, Listeria monocytogenes; анаэробных грамположительных бактерий: Clostridium spp., Peptococcus spp., Peptostreptococcus spp.; аэробных грамотрицательных бактерий: E. coli, Klebsiella spp., Proteus mirabilis, P. vulgaris, Yersinia enterocolitica, Salmonella spp., Shigella spp., Haemophilus influenzae, H. ducreyi, Neisseria gonorrhoeae, N. meningitidis, Bordetella pertussis, Gardnerella vaginalis, Brucella spp., Pasteurela multocida, Campylobacter jejuni, Vibrio cholerae, Moraxella catarrhalis, Helicobacter pylori; анаэробных грамотрицательных бактерий: Bacteroides spp., включая B. fragilis.
В настоящее время на фармацевтическом рынке России появился отечественный препарат АМК для приема внутрь – Арлет®, произведенный ОАО СИНТЕЗ (Россия). Это таблетки, содержащие 500 мг амоксициллина и 125 мг клавулановой кислоты, или 875 мг амоксициллина и 125 мг клавулановой кислоты. Взрослым и детям старше 12 лет (или c массой тела более 40 кг) при инфекции нижних дыхательных путей назначают по 1 таблетке 500/125 мг каждые 8 часов или по 1 таблетке 875/125 мг каждые 12 часов. Детям младше 12 лет с массой тела менее 40 кг доза препарата подбирается индивидуально на основании рекомендуемой схемы дозирования (для амоксициллина) – 45 мг/кг/сут в 2 приема или 40 мг/кг/сут в 3 приема. Оптимальной лекарственной формой препарата для детей от 6 до 12 лет являются таблетки 500/125 мг при назначении 2 раза/сут.
Максимальная суточная доза клавулановой кислоты (в форме калиевой соли) для детей составляет 10 мг/кг массы тела. Максимальная суточная доза амоксициллина составляет 45 мг/кг массы тела. Курс лечения – 5–14 дней. Продолжительность курса лечения определяется лечащим врачом. Лечение не должно продолжаться более 14 дней без повторного медицинского осмотра. При одновременном применении Арлета с антацидами, глюкозамином, слабительными средствами, аминогликозидами абсорбция его из желудочно-кишечного тракта замедляется, при одновременном применении Арлета с аскорбиновой кислотой его адсорбция повышается.
При одновременном применении Арлета с бактерицидными антибиотиками (в т. ч. аминогликозиды, цефалоспорины, циклосерин, ванкомицин, рифампицин) проявляется синергизм действия. С антибиотиками с бактериостатическим механизмом действия (макролиды, хлорамфеникол, линкозамиды, тетрациклины, сульфаниламиды) проявляется антагонизм действия. Диуретики, НПВС и другие лекарственные средства, блокирующие канальцевую секрецию, повышают концентрацию амоксициллина.
Побочные действия АМ и АМК – это аллергические реакции: крапивница, эритематозные высыпания; редко – мультиформная экссудативная эритема; в единичных случаях – анафилактический шок, ангионевротический отек. Со стороны пищеварительной системы у некоторых детей отмечаются тошнота, рвота, диарея, боли в животе, нарушение функции печени. Поэтому к противопоказаниям к назначению АМК относятся нарушения функции печени при приеме АМ/клавулановой кислоты в анамнезе; инфекционный мононуклеоз или лимфолейкоз (опасность появления экзантемы) и повышенная чувствительность к амоксициллину, клавулановой кислоте, другим компонентам препарата.
При бронхитах, протекающих с клиническими признаками, позволяющими заподозрить микоплазменную или хламидийную этиологию (вспышка заболеваемости в детском коллективе или в семье, длительная выраженная фебрильная лихорадка при микоплазмозе или нормальная и субфебрильная температура при хламидийной этиологии заболевания, отсутствие отчетливой интоксикации и одышки, невыразительность физикальных данных при наличии упорного, сухого или непродуктивного «стакаттоподобного» навязчивого кашля), особенно при затяжном течении, и неэффективности предшествующей терапии β-лактамными АБ-препаратами выбора являются макролиды, а для детей старше 7-летнего возраста – доксициклин.
Особенности этиологии ПВМ у детей первых 6 месяцев жизни делают препаратом выбора даже при нетяжелой форме заболевания ингибиторозащищенный АМ (АМК) или цефалоспорин 2-го поколения (цефуроксим или цефазолин), которые вводятся парентерально [11]. При ПВМ, протекающей с нормальной или субфебрильной температурой, особенно при наличии обструктивного синдрома и указаний на вагинальный хламидиоз у матери, можно думать об инфекции C. trachomatis. В этих случаях целесообразно сразу назначать макролидный АБ (азитромицин, рокситромицин или спирамицин) внутрь. В отношении недоношенных детей следует помнить о возможности ПВМ, вызванной Pneumocysticus carinii. При подозрении на пневмоцистоз детям наряду с АБ назначают ко-тримоксазол, потом при подтверждении пневмоцистной этиологии
ПВМ переходят только на ко-тримоксазол, который ребенок получает не менее 3 недель [10].
При тяжелой ПВМ с высоким риском неблагоприятного исхода препаратами выбора являются ингибиторозащищенный АМ в комбинации с аминогликозидами или цефалоспорины 3-го или 4-го поколения – цефтриаксон, цефотаксим, цефепим в монотерапии или в сочетании с аминогликозидами в зависимости от тяжести заболевания, карбапенемы (имипенем и меропенем). При подозрении или при диагностике стафилококковой этиологии заболевания показано назначение линезолида или ванкомицина в зависимости от тяжести заболевания отдельно или в комбинации с аминогликозидами (табл. 1).
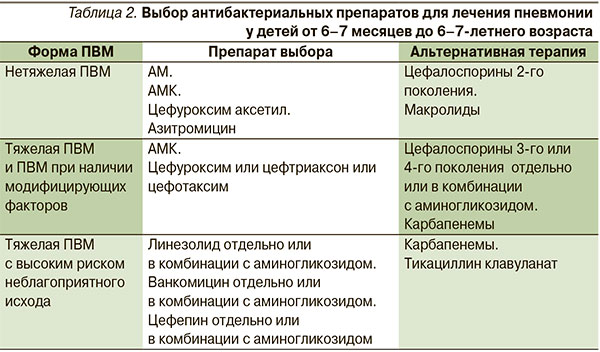
В возрасте от 6–7 месяцев до 6–7 лет при выборе стартовой антибактериальной терапии больным с нетяжелой ПВМ наиболее целесообразно назначение антибактериальных препаратов внутрь. С этой целью могут быть использованы АМ, АМК или цефалоспорин 2-го поколения – цефуроксим аксетил, цефаклор.
Но в некоторых случаях (отсутствие уверенности в выполнении назначений, достаточно тяжелое состояние ребенка при отказе родителей от госпитализации и другие подобные ситуации) оправдан ступенчатый метод проведения терапии, когда в первые 2–3 дня лечение проводится парентерально, а затем при улучшении или стабилизации состояния больного тот же АБ назначают внутрь. С этой целью может быть использован АМК, но он парентерально вводится внутривенно, что затруднительно в домашних условиях. Поэтому чаще используется цефуроксим внутримышечно и цефуроксим аксетил перорально.

Помимо ß-лактамов лечение может проводиться макролидами. Но с учетом этиологической значимости гемофильной палочки (до 7–10 %) для детей этой возрастной группы из широкого спектра макролидных АБ препаратом выбора для стартовой эмпирической терапии является азитромицин, оказывающий воздействие на H. influenzae. В случае ПВМ, вызванной атипичными возбудителями М. pneumoniae, C. pneumoniae, что в этом возрасте отмечается довольно редко, также назначаются макролиды.
Больным тяжелой ПВМ и ПВМ с наличием модифицируемых факторов показано парентеральное введение АБ или использование ступенчатого метода. Препаратами выбора в зависимости от тяжести и распространенности процесса, характера модифицируемых факторов являются АМК цефуроксим или цефтриаксон, цефотаксим. Альтернативными препаратами при неэффективности стартовой терапии являются цефалоспорины 3-го или 4-го поколения, карбапенемы (табл. 2).
Макролиды в этой группе используются редко, т. к. подавляющее большинство ПВМ, вызванных атипичными возбудителями, протекает нетяжело.
При выборе антибактериальных препаратов лечения ПВМ у детей старше 6–7 лет и подростков АБ выбором для больных нетяжелой ПВМ являются АМ и АМК перорально или макролиды. Альтернативные АБ – цефуроксим аксетил или доксициклин перорально, или макролиды, если до этого назначался АМ или АМК. Препаратами выбора для больных тяжелой ПВМ, требующей госпитализации, или с ПВМ у детей и подростков, имеющих модифицируемые факторы, являются АМК или цефалоспорины 2-го поколения (табл. 3).
В период реконвалесценции острых бронхитов широко используют методы физиотерапевтического воздействия, лечебную гимнастику, санаторно-курортное лечение. Подавляющее большинство ПВМ рассасывается бесследно, хотя процесс полного выздоровления занимает до 1–2 месяцев. При неправильном и несвоевременном лечении ПВМ в основном у детей с хроническими заболеваниями легких, такими как муковисцидоз, пороки развития и др., возможно развитие сегментарного, или долевого, пневмосклероза и деформаций бронхов в зоне поражения.



